La angioplastia primaria es el tratamiento de elección en los pacientes con infarto agudo de miocardio con elevación de ST. La fibrinolisis queda relegada a situaciones en las que no hay intervencionismo disponible o éste no puede realizarse en el tiempo adecuado. La fibrinolisis falla en un 40-50% de los casos y esto conlleva peor fracción de eyección y aumento de la mortalidad. En estos pacientes, la angioplastia de rescate ha demostrado que salva miocardio en riesgo y mejora el pronóstico. En pacientes ingresados en centros sin intervencionismo, se ha demostrado que la estrategia de trasladar al paciente, para intervencionismo precoz, en las 24 h siguientes de la fibrinolisis, conlleva mejor pronóstico, especialmente en infartos de alto riesgo. La angioplastia facilitada, con la información disponible en la actualidad, no ha demostrado ningún beneficio respecto a la angioplastia primaria y, dado que se asocia a aumento de mortalidad, reinfarto, hemorragia e ictus, debe evitarse. Un tercio de los pacientes con infarto agudo se presentan más de 12 h después del inicio de los síntomas. Los resultados de un nuevo metaanálisis indican un beneficio en términos de supervivencia en los pacientes tratados con angioplastia primaria tardía. Probablemente se beneficien más de esta estrategia los pacientes sintomáticos, con isquemia residual o con viabilidad documentada.
Palabras clave
La angioplastia primaria es el tratamiento de reperfusión de elección en el infarto agudo de miocardio (IAM) cuando ésta se realiza en el tiempo adecuado. Su superioridad con respecto a la fibrinolisis se ha demostrado en múltiples ensayos aleatorizados1,2 que ponen de manifiesto que la reperfusión mecánica, con respecto a la fibrinolisis, conlleva menor mortalidad, reinfarto, tasa de reoclusión de la arteria causal y hemorragia intracraneal, así como menor incidencia de isquemia recurrente.
El tratamiento trombolítico se reserva para los casos en que no se dispone de equipo para realizar angioplastia primaria o ésta no puede realizarse en el tiempo adecuado.
El intervencionismo percutáneo coronario (IPC) tras fibrinolisis se ha utilizado y estudiado en distintas circustancias. En unas, se realiza intervencionismo por fallo del tratamiento trombolítico: no consigue abrir la arteria (angioplastia de rescate) o la abre pero se produce su reoclusión precoz (angioplastia urgente por reoclusión). En otras situaciones, se realiza IPC como tratamiento complementario a la fibrinolisis eficaz (angioplastia sistemática electiva tras fibrinolisis), con objeto de tratar la lesión residual y, finalmente, se han utilizado los dos tratamientos asociados, con la finalidad de optimizar la reperfusión: angioplastia facilitada.
Además, algunos estudios han analizado el posible impacto de abrir la arteria en pacientes que llegan más tarde (más de 12h) del tiempo clásicamente establecido como límite para beneficiarse de la apertura de la arteria.
En este capítulo se revisan las evidencias actuales del intervencionismo tras la fibrinolisis y de la angioplastia primaria tardía.
ANGIOPLASTIA DE RESCATE¿Se realiza IPC tras el fallo de la fibrinolisis, en pacientes que continúan con isquemia miocárdica, en las primeras 12h de evolución del IAM?
De los estudios realizados para detectar la eficacia de los fibrinolíticos, mediante coronariografía, sabemos que 90min después del tratamiento un alto porcentaje de los pacientes no presentan flujo o éste está disminuido: un 27% de los pacientes presentan flujo TIMI 0/1 en la arteria causal y un 20%, flujo TIMI 23. Estos pacientes tienen riesgo aumentado de muerte con respecto a los que presentan flujo TIMI 3 y son los candidatos para la angioplastia de rescate.
El primer problema es la definición de ausencia de reperfusión tras la fibrinolisis en la práctica clínica cotidiana, ya que, obviamente, no se realiza coronariografía sistemática en ese tiempo a todos los pacientes para establecer este diagnóstico. Así pues, éste se establece como un diagnóstico de probabilidad guiado por parámetros clínicos: persistencia del ascenso de ST, persistencia del dolor, inestabilidad hemodinámica, ausencia de arritmias de reperfusión, etc. Sin embargo, la correlación entre estos parámetros y la ausencia de reperfusión falla en un número no despreciable de casos, tal y como se ha visto en algunos estudios4,5.
Con objeto de unificar criterios, las guías sobre actuación en el IAM con ascenso de ST de la ACC/ AHA de 2004 establecieron que una reducción de al menos un 50% de la elevación del segmento ST a los 60-90min es indicativa de reperfusión y una reducción de más del 70% se considera reperfusión completa6.
El primer trabajo que analizó de forma prospectiva y aleatorizada la angioplastia de rescate fue el estudio RESCUE7, que aleatorizó a 151 pacientes con IAM anterior y flujo TIMI 0/1 en la angiografía realizada 4,5h después de la fibrinolisis a angioplastia de rescate o tratamiento conservador. En ese estudio, la angioplastia de rescate se asoció a una reducción del objetivo combinado de muerte o insuficiencia cardiaca a los 30 días (el 6,4 frente al 16,6%; p = 0,05).
En 2004 se publicó el estudio MERLIN, que incluyó a 307 pacientes con IAM de cualquier localización, con fibrinolisis fallida y aleatorizados a coronariografía urgente, con o sin angioplastia de rescate, o tratamiento conservador. En ese estudio se permitía entrar a los pacientes hasta 10h después del tratamiento fibrinolítico. El diagnóstico de fibrinolisis fallida se estableció por una reducción menor del 50% de la elevación del ST a los 60min. La mortalidad a 30 días, objetivo principal, fue similar en ambos brazos: el 9,8% de angioplastia de rescate frente al 11% de tratamiento conservador (p = 0,7). Sin embargo, la tasa de eventos cardiacos mayores (ECM) fue menor en los pacientes tratados con IPC (el 37,3 frente al 50%; p = 0,02), así como la tasa de reinfarto (el 7,2 frente al 10,4%; p = 0,03) y la necesidad de nueva revascularización (el 6,5 frente al 20,1%; p = 0,01). A cambio, los pacientes tratados con IPC tuvieron una tasa mayor de accidentes cerebrovasculares (el 4,6 frente al 0,6%; p = 0,03), mayoritariamente de origen tromboembólico, no hemorrágico8. Merece la pena observar que sólo se realizó angioplastia a un 54% (el 50% con stent y el 3% con IIb/IIIa) de los pacientes asignados a coronariografía urgente, y que ésta se realizó con una media de 5,5h desde el tratamiento trombolítico.
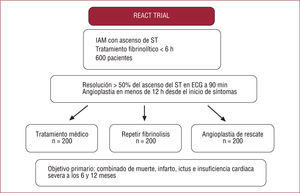
En 2005 se publicó el estudio REACT9, que incluyó a 600 pacientes con IAM de menos de 12h de evolución desde el inicio de los síntomas, con fibrinolisis fallida determinada por una reducción menor del 50% de la elevación del ST a los 90min, con o sin persistencia del dolor torácico (fig. 1). En ese estudio se limitó a 6h el tiempo de inclusión tras fibrinolisis fallida y se compararon tres estrategias: angioplastia de rescate, nueva fibrinolisis y tratamiento conservador. Los 600 pacientes previstos quedaron en 427 (el estudio se detuvo antes de tiempo por reclutamiento muy lento), de ellos, se asignó a 142 a refibrinolisis, 141 a tratamiento conservador y 144 a angioplastia de rescate. El objetivo primario, un compuesto de muerte, reinfarto, ictus e insuficiencia cardiaca severa a los 6 meses, se redujo de manera significativa en los pacientes tratados con IPC, frente a nueva administración de fibrinolisis y tratamiento conservador (el 15,3 frente al 31 y el 29,8%, respectivamente; p = 0,003). Hubo una tendencia no significativa a la reducción en la mortalidad de cualquier causa con el IPC, en comparación con las otras dos estrategias (el 6,2 frente al 12,7 y el 12,8% en nueva fibrinolisis y tratamiento conservador), y la tasa libre de nueva revascularización fue significativamente mayor con la angioplastia que con nueva fibrinolisis o tratamiento conservador (el 86,2 frente al 77,6 y el 74,4%; p = 0,05). No hubo diferencias en la incidencia de ictus entre las tres estrategias. En este estudio se realizó IPC a un 74% de los pacientes asignados a este brazo y hubo una mayor frecuencia de utilización de stent (88%) y IIb/IIIa (55%) que en el estudio MERLIN.
Diseño del estudio REACT9.
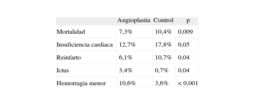
El estudio más reciente publicado es un metaanálisis que incluye 8 ensayos, entre los que están el RECUE, el MERLIN y el REACT, y compara la angioplastia de rescate con el tratamiento conservador y nueva fibrinolisis10. Entre todos suman 1.177 pacientes. Los resultados revelan que la angioplastia, en comparación con el tratamiento conservador, se asocia a una tendencia a menor mortalidad, una reducción significativa de la insuficiencia cardiaca y del reinfarto, a los 6 meses, a expensas de un incremento en la tasa de ictus y de hemorragia menor (tabla 1).
Resultados del metaanálisis de angioplastia de rescate10
| Angioplastia | Control | p | |
| Mortalidad | 7,3% | 10,4% | 0,009 |
| Insuficiencia cardiaca | 12,7% | 17,8% | 0,05 |
| Reinfarto | 6,1% | 10,7% | 0,04 |
| Ictus | 3,4% | 0,7% | 0,04 |
| Hemorragia menor | 10,6% | 3,6% | < 0,001 |
La nueva administración de fibrinolisis, frente al tratamiento conservador, no muestra reducciones significativas en mortalidad o reinfarto y conlleva un incremento de la incidencia de hemorragia menor (el 14,6 frente al 7,8%; p = 0,03).
Algunos aspectos técnicos del IPC pueden tener relevancia. Al igual que en la angioplastia primaria, el stent conlleva mejores resultados que la angioplastia con balón, tal y como se demostró en el estudio STOPAMI-411, que compara la angioplastia de rescate con stent (90 pacientes) y sólo con balón (91 pacientes) en pacientes con fibrinolisis fallida, dentro de las 24h del inicio de los síntomas del IAM, siempre que tuvieran un flujo TIMI ≤ 2. En esta ocasión el objetivo primario fue el índice de miocardio en riesgo salvado (proporción del defecto inicial de perfusión salvado por la intervención) medido por SPECT con 99mTc sestamibi basal (después de fibrinolisis fallida, pero antes de la intervención) y repetida a los 7-10 días. Se utilizaron IIb/IIIa en un 97% y la media del tiempo transcurrido desde la fibrinolisis hasta la angioplastia fue 10h en ambos brazos. El índice de miocardio salvado fue significativamente mayor en el grupo tratado con stent (0,35 [0,24, 0,56] frente a 0,25 [0,04, 0,43]; p = 0,005). La mortalidad al año fue menor en el grupo del stent, aunque sin alcanzar significación estadística. Los resultados de este estudio, aunque el número de pacientes incluidos sea pequeño, son realmente interesantes ya que demuestran que hay una cantidad importante de miocardio que se recupera con angioplastia, incluso 10h después de la fibrinolisis fallida, y el stent es superior a la angioplastia con balón. Por otro lado, a pesar de la alta utilización de IIb/IIIa, la tasa de hemorragia mayor no fue alta, el 4% en ambos brazos.
En la angioplastia primaria, el implante del stent directo, sin predilatar, se asocia a menor incidencia de fenómeno de falta de flujo y mejor resolución del segmento ST12,13, probablemente en relación con una menor incidencia de embolia distal. Este aspecto se ha estudiado también en la angioplastia de rescate14, con iguales resultados: el stent directo conlleva una mejor perfusión miocárdica, con mayor incidencia de flujo TMPG 3 (TIMI myocardial perfusión grade).
No hay datos específicos sobre la utilización de catéteres de tromboaspiración en la angioplastia de rescate, pero es razonable pensar que tengan la misma utilidad que en la angioplastia primaria.
En conclusión, aunque las recientes guías15 de la Sociedad Europea siguen siendo restrictivas en la indicación de la angioplastia de rescate (indicación IIa-A para infartos grandes siempre y cuando se realice en las 12h desde el inicio de los síntomas), cada vez hay más datos que avalan una estrategia de reperfusión mecánica precoz en pacientes con IAM tras fibrinolisis fallida, que es más eficaz si la decisión se toma precozmente (60-90min tras fibrinolisis), en pacientes con áreas importantes de miocardio en riesgo y evidencia de isquemia, especialmente si se utilizan estrategias adecuadas: stent, inhibidores de los receptores plaquetarios IIb/IIIa, stent directo, tromboaspiración, etc.
CORONARIOGRAFÍA E IPC SISTEMÁTICO TRAS FIBRINOLISISAunque está bien establecido que la angioplastia primaria es el tratamiento de elección en los pacientes con IAM, todavía hay muchos problemas de logística que la hacen difícil o no aplicable a gran parte de la población, por lo que la fibrinolisis es el tratamiento de reperfusión más utilizado todavía en muchas áreas. Si bien es cierto que la trombolisis abre la arteria en casi un 80% de los casos, sólo consigue una reperfusión eficaz (flujo TIMI 3) en un 50-60% de las arterias y deja la lesión sin tratar, con el consiguiente riesgo de reoclusión precoz. Ésta ha sido la base para la realización de estudios con estrategias de coronariografía sistemática y revascularización precoz tras fibrinolisis, con vistas a completar la reperfusión en estos pacientes.
Este tipo de estrategia se analizó en el estudio español GRACIA-116, en el que se aleatorizó a 500 pacientes con IAM tratados con trombolíticos a una estrategia invasiva habitual, con coronariografía dentro de las 24h (19,5h de media) tras fibrinolisis, seguida de revascularización con IPC o con cirugía, y a una estrategia conservadora (coronariografía y revascularización guiadas por isquemia). La tasa de ECM a 30 días fue igual con ambas estrategias; sin embargo, la estrategia invasiva se asoció a una menor necesidad de nueva revascularización (indicada por isquemia) durante el ingreso hospitalario (el 2 frente al 12%; p < 0,0001) y una estancia hospitalaria más corta, sin incremento de la tasa de hemorragia. A un año, el objetivo primario del estudio, un combinado de muerte, reinfarto o nueva revascularización a 12 meses, fue menor con la estrategia invasiva (el 9 frente al 21%; p = 0,0008).
Tres años después se publicó el GRACIA-217, que comparó la angioplastia primaria con stent dentro de las primeras 3h de aleatorización, con fibrinolisis con dosis plenas de tecnecteplasa seguido de IPC sistemático con stent entre las 3 y 12h tras aleatorización; fue un estudio de no inferioridad. Los pacientes asignados a fibrinolisis recibieron tratamiento con enoxaparina y los asignados a angiplastia primaria, abciximab antes de la inserción del introductor arterial y heparina no fraccionada durante el procedimiento. El estudio incluyó a 212 pacientes con IAM y los objetivos primarios fueron el grado de reperfusión epicárdica y miocárdica, así como la extensión del daño miocárdico determinados por el tamaño del infarto y la función del ventrículo izquierdo a las 6 semanas. La estrategia de fibrinolisis seguida de IPC sistemático con stent resultó equivalente a la angioplastia primaria en cuanto a su capacidad de limitar el tamaño del infarto y preservar la función del ventrículo izquierdo y se asoció, en este estudio, a una mayor frecuencia (el 21 frente al 6%; p = 0,003) de reperfusión completa miocárdica medida por flujo epicárdico y miocárdico TIMI 3 y resolución de la suma de la elevación del segmento ST ≥ 70%. A los 6 meses, el combinado de muerte, reinfarto, ictus y revascularización (objetivo secundario) fue igual con las dos estrategias.
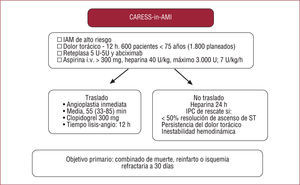
El estudio CARESS-in-AMI18 analizó una situación diferente: se trató con fibrinolisis (mitad de dosis de reteplasa más abciximab) a pacientes menores de 75 años, ingresados por IAM en hospitales sin equipo de angioplastia primaria, y después se los aleatorizó a traslado e IPC inmediato al hospital de referencia o tratamiento conservador y sólo angioplastia de rescate. Ésta solamente se indicaba si la fibrinolisis no era eficaz o aparecían datos de deterioro hemodinámico. Se incluyó a 600 pacientes con uno o más criterios de alto riesgo: elevación del segmento ST extensa, fracción de eyección < 35%, bloqueo de rama izquierda o infarto previo o Killip clase > 2. El objetivo primario fue un combinado de muerte, reinfarto o isquemia refractaria a 30 días y el análisis se realizó por intención de tratar (fig. 2).
Diseño del estudio CARESSin-AMI18.
El tiempo medio entre la fibrinolisis y la coronariografía en los pacientes asignados a estrategia invasiva fue 125min, y los pacientes asignados a esta estrategia tuvieron menos eventos cardiacos (el 4,4 frente al 10,7%; p = 0,004); las tasas de hemorragia mayor e ictus fueron iguales en los dos brazos.
Estos estudios demuestran que, en los pacientes con IAM ingresados en hospitales sin intervencionismo, una estrategia de traslado al hospital de referencia para IPC lo más precoz posible es superior a la estrategia conservadora de esperar y sólo enviar a los que no reperfundan o sufran complicaciones. Seguramente se beneficiarán más los pacientes con IAM de alto riesgo, tal y como demuestra el estudio CARESS-in-AMI.
ANGIOPLASTIA FACILITADADentro del apartado de coronariografía e IPC sistemático tras fibrinolisis está el concepto de angioplastia facilitada, que consiste en administrar fibrinolíticos (dosis plenas o menores, solos o en combinación con otros fármacos, como los inhibidores de los IIb/IIIa) poco antes del IPC, con el objetivo de lisar el trombo mientras se prepara la angioplastia primaria. Esta estrategia podría salvar miocardio en riesgo y facilitaría el procedimiento al encontrar ya la arteria abierta.
No obstante, los distintos ensayos, con distintas estrategias de tratamiento previo al IPC han fallado en demostrar beneficio. Los últimos datos vienen de 2 estudios recientes, ASSENT-419 y FINESSE20, y un metaanálisis21 recientemente publicado.
El estudio ASSENT-4 intentó demostrar que en pacientes con IAM de menos de 6h de evolución, en los que la angioplastia primaria se retrasa (1-3h), intentar abrir la arteria con dosis plenas de tecnecteplasa antes de realizar IPC obtendría beneficio en cuanto a reducción de un combinado de muerte, insuficiencia cardiaca y shock en los siguientes 90 días. Se planeó incluir a 4.000 pacientes en un diseño aleatorizado, pero se suspendió precozmente, cuando habían entrado 1.667 (838 asignados a IPC convencional y 829 asignados a IPC facilitada) por exceso de mortalidad en los pacientes con angioplastia facilitada (el 6 frente al 3%; p = 0,0105). El objetivo primario fue estadísticamente más frecuente en la IPC facilitada, así como la incidencia de ictus, reinfarto y necesidad de nueva revascularización a 90 días.
En el mismo número de la revista Lancet se publicó el metaanálisis de Keeley et al, que analizaba los resultados de 17 ensayos (incluido el ASSENT-4) que comparan IPC facilitada (2.237 pacientes) con IPC primaria convencional (2.267 pacientes). A pesar de que la fibrinolisis previa se asocia a una incidencia mayor de flujo TIMI 3 en la arteria causal (el 37 frente al 15%), esto no se traduce en un beneficio clínico y los resultados generales son superponibles a los del ASSENT-4: la IPC facilitada conlleva exceso significativo de mortalidad (el 5 frente al 35%; p = 0,04), necesidad de nueva revascularización (el 4 frente al 1%; p = 0,01), tasa de hemorragia mayor (el 7 frente al 5%; p = 0,01) e ictus (el 1,1 frente al 0,3%; p = 0,0008).
Por último, un año después se publicaron los resultados del estudio FINESSE, cuya hipótesis de trabajo fue que la angioplastia primaria precedida de tratamiento precoz con abciximab, sólo o asociado a mitad de dosis de reteplasa, sería superior a la angioplastia primaria con abciximab en la sala de hemodinámica. Se trata de un estudio aleatorizado a las tres ramas de tratamiento, a doble ciego, que incluyó a 2.452 pacientes con IAM de menos de 6h de evolución. El objetivo primario fue un compuesto de muerte de cualquier causa, fibrilación ventricular tardía (> 48h), shock cardiogénico e insuficiencia cardiaca a los 90 días. No hubo diferencias en el objetivo primario entre los tres grupos de tratamiento (el 9,8%, abciximab + reteplasa; el 10,5%, abciximab previo; el 10,7%, abciximab en sala; p = 0,55) ni en la mortalidad a 90 días (el 5,2, el 5,5 y el 4,5%, respectivamente; p = 0,49), a pesar de que la tasa de resolución de la elevación del segmento ST fue significativamente mayor en los pacientes con angioplastia facilitada combinada y sola (el 43,9, el 33,1 y el 31%; p = 0,01 y p = 0,003, respectivamente).
En conclusión, la angioplastia facilitada consigue una apertura más rápida de la arteria, pero esto no se traduce en ningún beneficio clínico y se asocia a un incremento en la mortalidad y en el resto de los eventos cardiacos mayores, por lo que en la actualidad las guías, tanto americanas como europeas, contraindican su uso6,15.
ANGIOPLASTIA PRIMARIA TARDÍACerca de un tercio de los pacientes con IAM se presentan tarde (más de 12h desde el inicio de los síntomas) al primer contacto médico, según datos del registro estadounidense de infarto agudo de miocardio NRMI22. En ese intervalo horario los fibrinolíticos no ofrecen ya beneficio en cuanto a supervivencia6; sin embargo, no parece haber una dependencia tan clara entre el beneficio clínico y el tiempo transcurrido desde el inicio de los síntomas en la angioplastia primaria. De hecho, en el NRMI-2, con 27.080 pacientes incluidos, la mortalidad no aumentó con el incremento del tiempo síntomas-balón y sí aumentó con el incremento del tiempo puerta-balón23 por encima de las 2h. Una explicación para este hecho es que el índice de miocardio en riesgo salvado es muy alto en las primeras 2h desde el inicio del IAM y mucho más bajo, aunque significativo, a partir de las 6h, y permanece estable más allá de las 12h24, según datos observados en un trabajo realizado con SPECT por Schomig et al en 2006. Esto mismo se pudo apreciar en el estudio STOPAMI11, en el que había pacientes incluidos con más de 12h de evolución del IAM. El índice de miocardio en riesgo salvado disminuyó progresivamente a medida que aumentaba el tiempo desde el inicio de los síntomas en los pacientes tratados con fibrinolíticos, pero no así en los tratados con angioplastia primaria, en los que permaneció alto y relativamente estable.
Por otro lado, es conocida la relación entre arteria abierta y mejora de la supervivencia tras un IAM25, y se han invocado otros argumentos de los posibles beneficios de mantener la arteria abierta (tabla 2). Todo esto ha dado pie a la publicación reciente de dos ensayos y un metaanálisis que estudian los posibles beneficios de abrir la arteria en pacientes con IAM con presentación tardía.
El estudio BRAVE-2 se publicó en 2005, con 365 pacientes ya asintomáticos, que se presentaron tras 12-48h (media, 22,5h) de evolución del IAM desde el comienzo de los síntomas, y aleatorizados a IPC inmediata o tratamiento conservador26. Se excluyó a los pacientes con insuficiencia cardiaca con Killip > 2. El tamaño del IAM por SPECT a 5-10 días, objetivo primario, fue significativamente menor en los pacientes tratados con IPC inmediato (el 8 frente al 13%; p < 0,001). La tasa de muerte, reinfarto e ictus (objetivo secundario) se redujo de forma no significativa en el grupo tratado con IPC (el 4,4 frente al 6,6%; p = 0,37). Más de la mitad de los pacientes conservaban algo de flujo en la arteria implicada y el 40% de los que tenían flujo TIMI 0 presentaban algún grado de circulación colateral, hechos que explican el beneficio obtenido en miocardio en riesgo salvado a pesar del tiempo de evolución del IAM.
Un año después se publicó el estudio OAT27, que intentó demostrar el beneficio de abrir la arteria todavía más tarde (3-28 días) en pacientes asintomáticos con IAM de alto riesgo, definido por fracción de eyección < 50% y oclusión (flujo TIMI 0-1) proximal de una arteria principal. Se excluyó a los pacientes con insuficiencia cardiaca importante, shock, creatinina > 2,5mg/dl, con lesión severa de tronco y/o tres vasos, con angina de reposo y con isquemia severa inducible. Se incluyó a 2.166 pacientes a quienes se aleatorizó a IPC más tratamiento médico óptimo o sólo tratamiento médico óptimo. El objetivo primario, un combinado de muerte, reinfarto o insuficiencia cardiaca clase IV de la clasificación NYHA, fue igual con ambas estrategias a los 4 años de seguimiento. Hubo una tendencia, no significativa, a aumento de reinfarto en los pacientes tratados con IPC.
Conviene decir que este estudio representa un porcentaje muy pequeño de los pacientes con IAM y no es muy representativo del «mundo real». De hecho, se suspendió antes de tiempo por reclutamiento muy lento (sólo 2 pacientes por centro y por año) debido a los criterios tan restrictivos de inclusión. No obstante, los pacientes tratados con angioplastia tuvieron menor necesidad de nueva revascularización en el seguimiento (el 18,4 frente al 22,0%; p = 0,03).
Finalmente, en 2008 se publicó un metaanálisis que recoge los datos de 10 ensayos con 3.560 pacientes con IAM de más de 12h (más de 60 días) de evolución desde el inicio de los síntomas, que comparan IPC con tratamiento conservador, en pacientes estables28.
Los resultados, con seguimiento medio de 2,8 años, demuestran una reducción significativa de la mortalidad con IPC (el 6,3 frente al 8,4%; p = 0,03) y una mejoría significativa de la fracción de eyección en el seguimiento en los pacientes tratados con IPC (p = 0,008). La tasa de reinfarto fue igual en los dos grupos de tratamiento.
En conjunto, si bien las últimas guías de la Sociedad Europea no encuentran suficiente nivel de evidencia para recomendar su uso15 (indicación clase III, nivel de evidencia B), parece que la angioplastia primaria, en pacientes con presentación tardía después de un IAM, puede asociarse a beneficios en términos de mortalidad a largo plazo, fundamentalmente a expensas de evitar remodelado ventricular y deterioro de la fracción de eyección, y mejora en la clase funcional (menos pacientes con angina en seguimiento, en el estudio OAT). Seguramente se benefician más los pacientes con angina residual o insuficiencia cardiaca, con isquemia demostrada en tests no invasivos, así como los pacientes de alto riesgo, con fracción de eyección deprimida y arterias tributarias de grandes áreas de miocardio.
CONCLUSIONESLa angioplastia de rescate es el tratamiento de elección en pacientes con IAM y fibrinolisis fallida, y es recomendable realizarla lo más precozmente posible.
En pacientes ingresados en centros sin intervencionismo, se ha demostrado que la estrategia de trasladar al paciente, para intervencionismo precoz, en las 24h siguientes de la fibrinolisis conlleva mejor pronóstico, especialmente en infartos de alto riesgo, siempre y cuando esto se haga en un tiempo adecuado.
La angioplastia facilitada se asocia a aumento de mortalidad, reinfarto, hemorragia e ictus y, por lo tanto, debe evitarse.
Las guías actuales no recomiendan la angioplastia sistemática en pacientes que se presentan con más de 24h de evolución del IAM, si bien parece que información más reciente indica que puede haber un beneficio en términos de mortalidad a largo plazo.