Recientemente se han producido numerosas novedades en el manejo de la fibrilación auricular no valvular y el tratamiento antiarrítmico, anticoagulante y no farmacológico empleado, pero su aplicación a la clínica no es inmediata. El objetivo del trabajo es conocer las características generales de manejo y tratamiento antiarrítmico de una población general de pacientes con fibrilación auricular no valvular actualmente en España.
MétodosEstudio observacional y prospectivo de 1.318 pacientes consecutivos con fibrilación auricular no valvular, anticoagulados y reclutados entre junio de 2013 y marzo de 2014. Se analizan sus características generales, el manejo y el tratamiento antiarrítmico utilizado.
ResultadosLa media de edad era 73,8±9,4 años; eran mujeres el 42,5%. La fibrilación auricular fue paroxística en el 28% de los casos, permanente en el 50%, persistente en el 17,6%, persistente de larga duración en el 4,5% y de novo en 66 pacientes (5%). Se eligió control del ritmo en el 39,4% de los casos y de frecuencia en el 60,6%. Tomaron bloqueadores beta el 60,2%, digoxina el 19,5% y antagonistas del calcio el 10,7%. Los antiarrítmicos empleados fueron amiodarona (12,6%), flecainida (8,9%), propafenona (0,4%), sotalol (0,5%) y dronedarona (2,3%). Se realizó cardioversión previa en el 41,9%, ablación en el 3,4% y cierre de orejuela en el 0,2%.
ConclusionesActualmente en nuestro país se maneja a los pacientes con fibrilación auricular no valvular preferentemente con control de frecuencia, sobre todo con bloqueadores beta, reciben pocos antiarrítmicos y se los somete en muy baja proporción a tratamientos no farmacológicos.
Palabras clave
La fibrilación auricular (FA) es la arritmia más frecuente en los países occidentales. Su prevalencia, estimada en un 1,5-2%1, aumenta con la edad y es el 1% a edades < 60 años y llega al 12% a los 75–84 años. Más de un tercio de los pacientes con FA tiene 80 o más años1,2. Recientemente, el registro OFRECE español ha estimado la prevalencia de la FA en España en el 4,4% de la población mayor de 40 años y el 17,7% de los mayores de 803. La FA se asocia frecuentemente a enfermedad cardiaca estructural y otras entidades crónicas y conlleva, además, una importante morbimortalidad (aumento de mortalidad y del riesgo de ictus, insuficiencia cardiaca [IC], demencia, etc., y aumento de ingresos y del coste sanitario)2,4–10.
Desde 2010 hemos asistido a la publicación casi anual de guías europeas y americanas para la FA, lo que traduce el cambio significativo en el manejo de esta arritmia. La sucesiva aparición de escalas de riesgo embolígeno y hemorrágico más discriminativas, el papel importante de los dispositivos de estimulación cardiaca en la detección de FA silente, los nuevos anticoagulantes orales (ACO) y antiarrítmicos y el desarrollo de la ablación han impulsado esta revolución. Recientemente se ha establecido una definición más clara de fibrilación auricular no valvular (FANV) como la que se da en ausencia de estenosis mitral reumática, prótesis valvular cardiaca o reparación valvular mitral1. También se han producido importantes cambios en el manejo general y en el tratamiento farmacológico y no farmacológico (decisión de realizar una estrategia de control de ritmo o de frecuencia en el manejo inicial de la FANV, indicaciones de los clásicos y nuevos fármacos antiarrítmicos, etc.), recogidos en las guías de práctica clínica, con ligeras diferencias entre ellas11. Sin embargo, la aplicación a la práctica clínica habitual de estas evidencias derivadas de ensayos clínicos solventes y con clase de indicación establecida en las guías de práctica clínica no es inmediata.
El objetivo de este trabajo es analizar las actuales características generales de manejo de la FANV, la estrategia de control del ritmo o de la frecuencia cardiaca y el empleo de tratamiento antiarrítmico o no farmacológico en una población general no seleccionada de pacientes con FANV en España.
MÉTODOSDatos y diseño del estudioLos datos de este estudio provienen del Registro FANTASIIA (Fibrilación Auricular: influencia del Nivel y Tipo de Anticoagulación Sobre la Incidencia de Ictus y Accidentes hemorrágicos), un estudio nacional, multicéntrico, observacional y prospectivo que recoge información general de la características y situación actual de la población española con FANV de cualquier tipo, según los criterios establecidos en la guía europea de FA1. El estudio tiene como objetivo principal evaluar la incidencia de eventos tromboembólicos y hemorrágicos en una población no seleccionada de pacientes con FANV durante 3 años de seguimiento, en relación con el tipo de agentes antitrombóticos empleados, antagonistas de la vitamina K (AVK) o ACO directos, y la adecuación de la anticoagulación (en aquellos que reciben AVK). El diseño incluye una visita inicial de inclusión y 3 visitas de seguimiento, tras 1, 2 y 3 años, en las que se recogen los datos clínicos y analíticos de los pacientes en un cuaderno de datos electrónico.
Los datos que se analizan concretamente en este trabajo forman parte de los objetivos secundarios del Registro FANTASIIA y son los relacionados con las características generales de manejo de la FANV, estrategia inicial de control de la FA, control del ritmo o de la frecuencia y tipo de tratamiento empleado, clase de antiarrítmico o tratamiento no farmacológico, utilizando los datos basales en un corte transversal en la visita de inclusión del Registro FANTASIIA.
Población del estudioSe estudia en este análisis preliminar a 1.318 pacientes consecutivos, seguidos en consultas ambulatorias, diagnosticados de FANV (excluidos aquellos con valvulopatía mitral reumática o portadores de válvulas protésicas) incluidos en el Registro FANTASIIA por 81 investigadores —de los que el 81% son cardiólogos; el 11%, médicos de atención primaria, y un 8%, internistas— desde junio de 2013 a marzo de 2014, procedentes de 50 centros repartidos por toda España, estratificados por niveles de asistencia y seleccionados aleatoriamente. Todos los pacientes eran mayores de 18 años y, por diseño del estudio, recibían tratamiento con anticoagulantes, un 80% con AVK y un 20% con ACO directos (dabigatrán, rivaroxabán y apixabán), al menos durante los 6 meses previos a la inclusión en el estudio. El manejo general de los pacientes se realizó de acuerdo con la práctica clínica habitual. El Registro FANTASIIA cumple todos los requisitos de la Declaración de Helsinki y el protocolo del estudio fue aprobado por el Comité de Ensayos Clínicos y Ético del Hospital Universitario de Alicante y por todos los comités éticos de los centros participantes. La totalidad de los pacientes participantes firmaron el consentimiento informado.
Análisis estadísticoLas variables cuantitativas se describen mediante la media±desviación estándar o mediana [intervalo intercuartílico] en función de si siguen o no una distribución normal utilizando el test de Kolmogorov-Smirnov para comprobar la distribución normal. Para las comparaciones entre grupos se utilizó el test de la t de Student en el caso de variables continuas y la de la χ2 en el caso de variables cualitativas. Se consideró significativo un valor de p<0,05. Para el análisis estadístico se utilizó el paquete estadístico SPSS versión 12.
RESULTADOSCaracterísticas basales de los pacientes del estudioSe incluyó a 1.318 pacientes que cumplían los criterios de inclusión y exclusión antes citados, durante el periodo comprendido entre junio de 2013 y marzo de 2014 en toda España. Las características basales se muestran en la tabla 1. La media de edad era 73,8±9,4 años, y 758 (57,5%) eran varones. El factor de riesgo más prevalente fue la hipertensión arterial, en 1.068 (81,0%), seguida de la hipercolesterolemia, en 711 (54,0%), y la diabetes mellitus, en 386 (29,0%). Otras comorbilidades relevantes fueron accidente cerebrovascular isquémico —210 (15,9%)— y sangrado mayor —44 (3,3%)—. En la visita de inicio, la mayoría de los pacientes, 948 (71,9%), estaban tratados con acenocumarol, 68 (5,2%) con warfarina y 303 (23,0%) con alguno de los nuevos ACO directos. Se había realizado cierre de la orejuela izquierda en 3 (0,2%). Los valores medios de los índices de riesgo trombótico y hemorrágico fueron: CHADS2, 2,32; CHA2DS2-VASc, 3,79, y HAS-BLED, 1,99. Tenía CHA2DS2-VASc=0 el 4,9% de los casos, CHA2DS2-VASc=1 el 24,1% y CHA2DS2-VASc ≥ 2 el 71%. Tenían HAS-BLED < 3 el 72,4% y ≥ 3 el 27,6%. Recibían antiagregantes 126 pacientes (9,8%): ácido acetilsalicílico solo 95 (7,4%), clopidogrel solo 21 (1,6%), prasugrel solo 1 (0,1%) y doble antiagregación 9 (0,8%).
Características basales de la población del estudio
| Pacientes | 1.318 |
| Mujeres | 560 (42,5) |
| Edad (años) | 73,8±9,4 |
| Edad ≥ 75 años | 689 (52,3) |
| Factores de riesgo cardiovascular | |
| Hipertensión | 1.068 (81,0) |
| Hipercolesterolemia | 711 (54,0) |
| Diabetes mellitus | 386 (29,3) |
| Tabaquismo | 60 (4,6) |
| Enfermedad concomitante | |
| Afección renal | 251 (19,0) |
| Insuficiencia hepática | 13 (1,0) |
| EPOC y/o apnea del sueño | 222 (16,8) |
| Enfermedad vascular periférica | 92 (7,0) |
| Ictus previo | 210 (15,9) |
| Enfermedad tiroidea | 173 (13,1) |
| Consumo de alcohol o drogas | 210 (15,9) |
| Sangrados mayores | 44 (3,3) |
| Enfermedad cardiaca previa | 629 (47,7) |
| Insuficiencia cardiaca | 376 (28,5) |
| Enfermedad coronaria | 245 (18,6) |
| CHADS2 | |
| 0 | 64 (4,9) |
| 1 | 318 (24,1) |
| ≥ 2 | 936 (71,0) |
| CHA2DS2-VASc | |
| 0 | 16 (1,2) |
| 1 | 86 (6,5) |
| ≥ 2 | 1.216 (92,3) |
| HAS-BLED ≥ 3 | 363 (27,7) |
| Tratamiento concomitante | |
| Diuréticos | 784 (59,5) |
| IECA | 411 (31,2) |
| ARA-II | 540 (41,0) |
| Estatinas | 742 (56,3) |
| Antiplaquetarios | 130 (9,9) |
| Tratamiento anticoagulante | |
| Antagonistas de la vitamina K | 1.016 (77,1) |
| Acenocoumarol | 948 (71,9) |
| Warfarina | 68 (5,2) |
| Nuevos anticoagulantes directos | 303 (23,0) |
ARA-II: antagonistas del receptor de la angiotensina II; CHADS2: insuficiencia cardiaca, hipertensión, edad ≥ 75 años, diabetes mellitus, ictus/accidente isquémico transitorio; EPOC: enfermedad pulmonar obstructiva crónica; HAS-BLED: hipertensión, insuficiencia renal/hepática, ictus, predisposición o historia de hemorragia reciente, índice internacional normalizado lábil, edad avanzada, uso de fármacos que predisponen a la hemorragia o al abuso de alcohol; IECA: inhibidores de la enzima de conversión de la angiotensina; VASc: enfermedad vascular, edad de 65 a 74 años, sexo femenino.
Los valores expresan n (%) o media±desviación estándar.
La FA era paroxística en 367 (28%) de los casos, permanente en 656 (50%), persistente en 231 (17,6%) y persistente de larga duración en 59 (4,5%). Se trataba de una FA de novo (primer episodio) en 66 pacientes (5%). El tiempo desde el diagnóstico inicial de la FA fue 3,2±1,8 años. Estaba en ritmo sinusal en la visita basal el 32,2%. Se eligió una estrategia de control del ritmo en el 39,4% de los casos (el 45,3% de los pacientes menores de 75 años y el 30,2% de los de 75 o más) y de control de frecuencia en el 60,6% (el 54,7% de los menores de 75 años y el 69,8% de los de 75 o más) (p<0,001). Se había realizado cardioversión previa en el 41,9% (eléctrica en el 19% y farmacológica en el 22,9%) y ablación de la FA en el 3,4% (el 2,2% en paroxística, el 1,3% en persistente y el 0,15% en persistente de larga evolución). En la tabla 2 se muestran las características de los pacientes para los que se optó por una estrategia de control de ritmo o control de frecuencia. Los pacientes con control de ritmo eran de menos edad, tenían en menor proporción diabetes mellitus, enfermedad pulmonar obstructiva crónica, insuficiencia renal e IC, y en mayor proporción antecedentes de enfermedad tiroidea. Su índice de Charlson resumido era más bajo. Se optó por control de ritmo en el 44,1% de los pacientes atendidos por cardiólogos y el 19,2% de los atendidos por internistas/médicos de atención primaria (p<0,001). No hubo diferencias significativas en el resto de las características analizadas (tabla 2).
Características de los pacientes para los que se eligió una estrategia de control de ritmo o control de frecuencia
| Control de ritmo | Control de frecuencia | p | |
|---|---|---|---|
| Pacientes (n=1.318) | 39,4 | 60,6 | |
| Edad (años) | 71,0±9,3 | 75,5±9,0 | < 0,001 |
| Mujeres | 44,5 | 41,2 | 0,240 |
| Comorbilidad y FRCV | |||
| Antecedentes de hipertensión arterial | 80,5 | 81,7 | 0,589 |
| Antecedentes de hiperlipemia | 55,5 | 53,0 | 0,375 |
| Diabetes mellitus | 25,3 | 31,9 | 0,011 |
| Fumador actual | 5,22 | 4,1 | 0,361 |
| EPOC/SAOS | 12,9 | 19,5 | 0,002 |
| Insuficiencia renal | 16,0 | 20,9 | 0,026 |
| Diálisis | 0,2 | 0,9 | 0,119 |
| Disfunción hepática | 0,9 | 1,0 | 0,946 |
| Cáncer | 7,2 | 9,1 | 0,198 |
| Arteriopatía aórtica o de EEII | 6,0 | 7,5 | 0,283 |
| Accidente cerebrovascular previo | 16,1 | 18,8 | 0,196 |
| Embolia no cerebral previa | 2,1 | 2,6 | 0,558 |
| Enfermedad tiroidea | 16,6 | 10,8 | 0,002 |
| Uso de fármacos que predisponen a la hemorragia o al abuso de alcohol | 2,9 | 4,6 | 0,113 |
| Índice de Charlson resumido | 0,98±1,11 | 1,27±1,20 | < 0,001 |
| Antecedentes cardiológicos | |||
| Cardiopatía previa | 45,2 | 49,5 | 0,133 |
| Insuficiencia cardiaca | 24,7 | 33,1 | 0,001 |
| Enfermedad coronaria previa | 19,3 | 18,2 | 0,609 |
| Síndrome coronario agudo previo | 15,4 | 14,1 | 0,482 |
| Revascularización coronaria previa | 10,8 | 11,1 | 0,899 |
| Miocardiopatía dilatada | 11,8 | 12,5 | 0,680 |
| Miocardiopatía hipertrófica | 2,7 | 2,7 | 0,952 |
| Enfermedad pericárdica crónica | 0,2 | 0,4 | 0,556 |
| Valvulopatía aórtica | 2,1 | 2,9 | 0,396 |
| Hipertrofia ventricular izquierda por HTA | 15,4 | 16,7 | 0,553 |
| Bradiarritmia previa | 6,3 | 6,6 | 0,844 |
| Ablación previa | 3,8 | 2,4 | 0,122 |
| Marcapasos | 6,0 | 7,7 | 0,248 |
EPOC: enfermedad pulmonar obstructiva crónica; FRCV: factores de riesgo cardiovascular; HTA: hipertensión arterial; SAOS: síndrome de apnea obstructiva del sueño.
Los valores expresan porcentaje o media±desviación estándar.
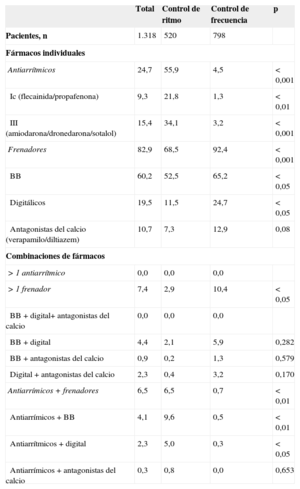
Solo se emplearon fármacos antiarrítmicos en el 24,7% de los casos. Los fármacos antiarrítmicos más empleados en el control del ritmo cardiaco fueron: amiodarona (12,6%), flecainida (8,9%), propafenona (0,4%), sotalol (0,5%) y dronedarona (2,3%). Los fármacos más frecuentemente utilizados para el control de la frecuencia cardiaca fueron los bloqueadores beta (60,2%), digoxina (19,5%) y antagonistas del calcio (verapamilo o diltiazem) (10,7%). En la tabla 3 se muestra la proporción de pacientes que recibían cada fármaco y sus combinaciones, tanto en el grupo total como en los de control de ritmo y control de frecuencia. Globalmente, ningún paciente recibió la combinación de dos o más antiarrítmicos de clase I o III, mientras que el 13,9% recibió la combinación de dos o más frenadores (6,5%) o de un antiarrítmico más un frenador (7,4%). Las combinaciones más frecuentes fueron un antiarrítmico más bloqueador beta y bloqueador beta más digitálico (tabla 3). El uso de antiarrítmicos fue más frecuente en el grupo de control de ritmo (el 55,9 frente a solo el 4,5% del grupo de control de frecuencia; p<0,001), y el uso de frenadores fue más frecuente en el de control de frecuencia (el 92,4 frente al 68,5%; p<0,001). La combinación de antiarrítmicos y frenadores fue más frecuente en el grupo de control de ritmo (el 15,4 frente al 0,7% del grupo de control de frecuencia; p<0,01) y la de varios frenadores, en el grupo de control de frecuencia (el 10,4 frente al 2,9%; p<0,05) (tabla 3).
Fármacos antiarrítmicos y frenadores y su uso combinado, en el grupo total y en los subgrupos de control de ritmo y control de frecuencia
| Total | Control de ritmo | Control de frecuencia | p | |
|---|---|---|---|---|
| Pacientes, n | 1.318 | 520 | 798 | |
| Fármacos individuales | ||||
| Antiarrítmicos | 24,7 | 55,9 | 4,5 | < 0,001 |
| Ic (flecainida/propafenona) | 9,3 | 21,8 | 1,3 | < 0,01 |
| III (amiodarona/dronedarona/sotalol) | 15,4 | 34,1 | 3,2 | < 0,001 |
| Frenadores | 82,9 | 68,5 | 92,4 | < 0,001 |
| BB | 60,2 | 52,5 | 65,2 | < 0,05 |
| Digitálicos | 19,5 | 11,5 | 24,7 | < 0,05 |
| Antagonistas del calcio (verapamilo/diltiazem) | 10,7 | 7,3 | 12,9 | 0,08 |
| Combinaciones de fármacos | ||||
| > 1 antiarrítmico | 0,0 | 0,0 | 0,0 | |
| > 1 frenador | 7,4 | 2,9 | 10,4 | < 0,05 |
| BB + digital+ antagonistas del calcio | 0,0 | 0,0 | 0,0 | |
| BB + digital | 4,4 | 2,1 | 5,9 | 0,282 |
| BB + antagonistas del calcio | 0,9 | 0,2 | 1,3 | 0,579 |
| Digital + antagonistas del calcio | 2,3 | 0,4 | 3,2 | 0,170 |
| Antiarrímicos + frenadores | 6,5 | 6,5 | 0,7 | < 0,01 |
| Antiarrímicos + BB | 4,1 | 9,6 | 0,5 | < 0,01 |
| Antiarrítmicos + digital | 2,3 | 5,0 | 0,3 | < 0,05 |
| Antiarrímicos + antagonistas del calcio | 0,3 | 0,8 | 0,0 | 0,653 |
BB: bloqueadores beta.
Salvo otra indicación, los valores expresan porcentajes.
También hubo diferencias en el tipo de fármacos utilizados en relación con la fracción de eyección del ventrículo izquierdo (FEVI) de los pacientes. La FEVI fue<45% en 206 casos (el 15,6% del total) y ≥ 45% en los restantes 1.112 (84,4%). La estrategia de control de ritmo fue menos frecuente entre los pacientes con FEVI deprimida (el 29,1 frente al 41,4%; p<0,001), al contrario que la de control de frecuencia, más frecuente en ambos grupos, pero más aún en el grupo con FEVI deprimida (el 70,9 frente al 58,6%; p<0,001). En la tabla 4 se muestra la distribución del uso de fármacos antiarrítmicos según la FEVI. Entre los pacientes con FEVI deprimida, fue más frecuente el uso de antiarrítmicos de clase III que de clase Ic (el 15,5 frente al 0,5%). Los frenadores más usados en ambos grupos fueron los bloqueadores beta. La digoxina se utilizó más en los pacientes con FEVI deprimida.
Manejo y fármacos antiarrítmicos utilizados según la fracción de eyección del ventrículo izquierdo estuviera deprimida (< 45%) o conservada (≥ 45%)
| Total | FEVI < 45% | FEVI ≥ 45% | p | |
|---|---|---|---|---|
| Pacientes, n | 1.318 | 206 | 1.112 | |
| Estrategia de control | ||||
| Control de ritmo | 39,4 | 29,1 | 41,4 | < 0,001 |
| Control de frecuencia | 60,6 | 70,9 | 58,6 | < 0,001 |
| Antiarrítmicos | 24,7 | 16,0 | 26,2 | < 0,01 |
| Ic (flecainida/propafenona) | 9,3 | 0,5 | 10,9 | < 0,05 |
| III (amiodarona/dronedarona/sotalol) | 15,4 | 15,5 | 15,3 | 0,965 |
| Frenadores | 82,9 | 67,9 | 85,7 | < 0,01 |
| Bloqueadores beta | 60,2 | 50,5 | 61,9 | < 0,05 |
| Digitálicos | 19,5 | 26,2 | 18,2 | < 0,05 |
| Antagonistas del calcio (verapamilo/diltiazem) | 10,7 | 2,9 | 12,1 | < 0,05 |
FEVI: fracción de eyección del ventrículo izquierdo.
Salvo otra indicación, los valores expresan porcentajes.
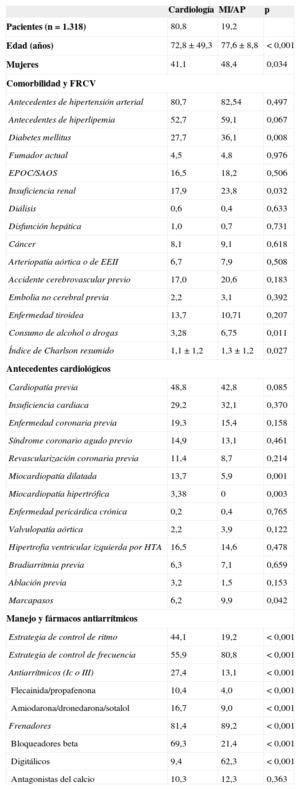
En la tabla 5 se reflejan las características y el manejo de los pacientes atendidos por cardiólogos (1.066 [80,8%]) e internistas o médicos de atención primaria (252 [19,2%]). No hubo diferencias relevantes en la mayor parte de las características de los pacientes de ambos grupos, salvo por una edad mayor, una mayor prevalencia de diabetes mellitus e insuficiencia renal y un índice de Charlson resumido algo mayor en lo atendidos por no cardiólogos, y una mayor prevalencia de miocardiopatías dilatada o hipertrófica en los atendidos por cardiólogos. La prevalencia de los demás factores de riesgo cardiovascular, comorbilidades y cardiopatías asociadas (incluidas enfermedad coronaria e IC) fue similar en ambos grupos (tabla 5). La estrategia de control de ritmo fue significativamente menos frecuente, como ya se ha comentado, entre los pacientes seguidos por internistas o médicos de atención primaria. El uso de fármacos antiarrímicos, tanto de clase Ic como de clase III, fue más frecuente entre los cardiólogos (tabla 5), mientras que la utilización de fármacos para controlar la frecuencia fue mayor entre los internistas y médicos de atención primaria. Hubo diferencias en el tipo de fármaco frenador usado, y los bloqueadores beta se utilizaron mucho más para los pacientes seguidos por cardiólogos y los digitálicos, en los seguidos por internistas o médicos de atención primaria.
Características de los pacientes atendidos por cardiólogos e internistas o médicos de atención primaria
| Cardiología | MI/AP | p | |
|---|---|---|---|
| Pacientes (n=1.318) | 80,8 | 19,2 | |
| Edad (años) | 72,8±49,3 | 77,6±8,8 | < 0,001 |
| Mujeres | 41,1 | 48,4 | 0,034 |
| Comorbilidad y FRCV | |||
| Antecedentes de hipertensión arterial | 80,7 | 82,54 | 0,497 |
| Antecedentes de hiperlipemia | 52,7 | 59,1 | 0,067 |
| Diabetes mellitus | 27,7 | 36,1 | 0,008 |
| Fumador actual | 4,5 | 4,8 | 0,976 |
| EPOC/SAOS | 16,5 | 18,2 | 0,506 |
| Insuficiencia renal | 17,9 | 23,8 | 0,032 |
| Diálisis | 0,6 | 0,4 | 0,633 |
| Disfunción hepática | 1,0 | 0,7 | 0,731 |
| Cáncer | 8,1 | 9,1 | 0,618 |
| Arteriopatía aórtica o de EEII | 6,7 | 7,9 | 0,508 |
| Accidente cerebrovascular previo | 17,0 | 20,6 | 0,183 |
| Embolia no cerebral previa | 2,2 | 3,1 | 0,392 |
| Enfermedad tiroidea | 13,7 | 10,71 | 0,207 |
| Consumo de alcohol o drogas | 3,28 | 6,75 | 0,011 |
| Índice de Charlson resumido | 1,1±1,2 | 1,3±1,2 | 0,027 |
| Antecedentes cardiológicos | |||
| Cardiopatía previa | 48,8 | 42,8 | 0,085 |
| Insuficiencia cardiaca | 29,2 | 32,1 | 0,370 |
| Enfermedad coronaria previa | 19,3 | 15,4 | 0,158 |
| Síndrome coronario agudo previo | 14,9 | 13,1 | 0,461 |
| Revascularización coronaria previa | 11,4 | 8,7 | 0,214 |
| Miocardiopatía dilatada | 13,7 | 5,9 | 0,001 |
| Miocardiopatía hipertrófica | 3,38 | 0 | 0,003 |
| Enfermedad pericárdica crónica | 0,2 | 0,4 | 0,765 |
| Valvulopatía aórtica | 2,2 | 3,9 | 0,122 |
| Hipertrofia ventricular izquierda por HTA | 16,5 | 14,6 | 0,478 |
| Bradiarritmia previa | 6,3 | 7,1 | 0,659 |
| Ablación previa | 3,2 | 1,5 | 0,153 |
| Marcapasos | 6,2 | 9,9 | 0,042 |
| Manejo y fármacos antiarrítmicos | |||
| Estrategia de control de ritmo | 44,1 | 19,2 | < 0,001 |
| Estrategia de control de frecuencia | 55,9 | 80,8 | < 0,001 |
| Antiarrítmicos (Ic o III) | 27,4 | 13,1 | < 0,001 |
| Flecainida/propafenona | 10,4 | 4,0 | < 0,001 |
| Amiodarona/dronedarona/sotalol | 16,7 | 9,0 | < 0,001 |
| Frenadores | 81,4 | 89,2 | < 0,001 |
| Bloqueadores beta | 69,3 | 21,4 | < 0,001 |
| Digitálicos | 9,4 | 62,3 | < 0,001 |
| Antagonistas del calcio | 10,3 | 12,3 | 0,363 |
AP: atención primaria; EEII: extremidades inferiores; EPOC: enfermedad pulmonar obstructiva crónica; HTA: hipertensión arterial; MI: medicina interna; SAOS: síndrome de apnea obstructiva del sueño.
Salvo otra indicación, los valores expresan porcentaje o media±desviación estándar.
El manejo de los pacientes con FANV tiene como objetivo reducir los síntomas y prevenir las complicaciones graves asociadas a ella. Se debe buscar ambos objetivos simultáneamente. La prevención de las complicaciones relacionadas con la FA se basa en el tratamiento antitrombótico, el control de la frecuencia cardiaca ventricular y el tratamiento adecuado de las enfermedades cardiacas concomitantes. Estas medidas pueden controlar los síntomas por sí solas, pero el alivio sintomático puede precisar también un tratamiento adicional de control del ritmo mediante cardioversión eléctrica o farmacológica o por ablación. En este análisis transversal de los datos basales del Registro FANTASIIA de FANV, se presentan las características del manejo de la FANV en relación con su tratamiento y el manejo antiarrítmico (estrategia elegida de control de ritmo o de frecuencia cardiaca y el tratamiento antiarrítmico empleado, fuera o no farmacológico). En nuestra serie la proporción de FANV paroxística fue del 28%, y la de FA permanente, la encontrada con mayor frecuencia, del 50%, cifras similares a lo descrito en otros trabajos recientes1,8–10. En cuanto a la estrategia de control elegida, la más frecuente fue el control de la frecuencia, que se llevó a cabo en más del 60% de los casos, frente al 39% en que se eligió control del ritmo. La estrategia de control de ritmo fue menos frecuente que la de control de frecuencia en todos los subgrupos analizados, como se muestra en la tabla 2, aunque fue significativamente menos frecuente en los pacientes de más edad, con comorbilidades como diabetes mellitus, enfermedad pulmonar obstructiva crónica e insuficiencia renal, y en aquellos con IC y FEVI deprimida (< 45%) (tabla 4). Asimismo, el control de ritmo fue menos frecuente en los pacientes atendidos por internistas/médicos de atención primaria (el 19,2 frente al 44% de los cardiólogos; p<0,001). Posiblemente, esta menor elección de la estrategia de control de ritmo se sustenta en los resultados de los estudios que han demostrado la no superioridad del control del ritmo frente al control de la frecuencia11–15.
Así, en el estudio AFFIRM11 no se objetivó superioridad de una estrategia frente a la otra en cuanto a reducción de mortalidad o ictus. Tampoco se encontraron diferencias entre ambas en el estudio RACE12 respecto a la mortalidad cardiovascular de pacientes con FA e IC, y otro tanto ocurrió en el estudio AF-CHF13 con la mortalidad cardiovascular en pacientes con FA y FEVI < 35%. Es más, tampoco se ha demostrado con el control del ritmo mayor beneficio en calidad de vida que con el control de la frecuencia cardiaca, como han demostrado estudios como el AFFIRM11 o el RACE12, pero también otros como PIAF y STAF14,15. Un estudio posterior16, que incluyó a más de 5.000 pacientes de la vida real, confirmó de nuevo los hallazgos de los estudios previos. Parece contradictorio, y esto ya ha sido señalado anteriormente17, que las guías de práctica clínica sigan insistiendo, en sus resúmenes de indicaciones, más en el control del ritmo que en el de la frecuencia sin evidencias claras al respecto1,2. En nuestro estudio, sin embargo, los hallazgos confirman la inclinación preferente en la práctica clínica de los médicos en España hacia la estrategia de control de la frecuencia, por encima de la de control del ritmo. Este hecho, además, es razonable teniendo en cuenta la elevada media de edad de la población del estudio. Esta inclinación fue significativamente más frecuente entre los médicos no cardiólogos que entre los cardiólogos (tabla 5). Es posible, no obstante, que las características de la población del FANTASIIA (edad avanzada, elevada prevalencia de comorbilidades y enfermedades cardiacas, escasa incidencia de primeros episodios de FA, indicación de anticoagulación crónica, etc.) hayan sesgado los resultados. Si se hubiera incluido a pacientes más jóvenes, con menos comorbilidades y sin indicación de anticoagulación crónica, posiblemente la elección de una estrategia de control de ritmo habría sido mayor, como se ve en estudios recientes8–10.
La utilización de fármacos antiarrítmicos (Ic y III) fue también escasa en nuestro trabajo, solo en una cuarta parte de la muestra global, quizá en concordancia también con el porcentaje de pacientes sometidos a estrategia de control del ritmo (tabla 3). Entre los empleados, el más frecuente fue la amiodarona (el 12,6% de los pacientes), seguida por flecainida (8,9%), dronedarona (2,3%), sotalol (0,5%) y propafenona (0,4%). Que la amiodarona sea el fármaco antiarrítmico más utilizado concuerda con las recomendaciones de las guías de práctica clínica1,2, que dejan claro que el antiarrítmico más eficaz y seguro para el mantenimiento del ritmo sinusal en pacientes para quienes sea imprescindible, sobre todo casos con cardiopatía estructural grave y/o IC avanzada o inestable, es la amiodarona1,17. Algunos artículos18,19, basados en la experiencia cotidiana, vienen a concluir que, si bien los efectos secundarios extracardiacos de la amiodarona son superiores a los de los demás antiarrítmicos, con las dosis utilizadas en FA y con un seguimiento estricto, se puede minimizarlos y resolverlos con la simple retirada del fármaco en la mayoría de los pacientes. Por otra parte, el bajo porcentaje de uso de dronedarona en nuestro entorno parece razonable de acuerdo con las recomendaciones actuales de la Agencia Europea del Medicamento20 y los resultados de los estudios ANDROMEDA21 y PALLAS22. Además, en el único estudio comparativo con otro fármaco, dronedarona fue inferior a amiodarona en la prevención de recurrencias de la FA23 (el 63,5 frente al 42%). La utilización de antiarrímicos de clase Ic, sobre todo flecainida, fue algo menos frecuente, y casi no se usaron en los pacientes con FEVI deprimida, tal como recomiendan las guías de práctica clínica1,2. En ningún paciente se combinaron antiarrímicos, aunque sí antiarrímicos con frenadores, sobre todo con bloqueadores beta y digoxina, en pacientes sometidos a control de ritmo (el 15,4% del total de este subgrupo) (tabla 3).
Respecto al control de la frecuencia cardiaca, los fármacos más frecuentemente utilizados en nuestro estudio fueron los bloqueadores beta (el 60,2% de los casos), seguidos por digoxina (19,5%) y antagonistas del calcio (10,7%), en concordancia con las recomendaciones de las guías de práctica clínica, que establecen el uso preferente de los bloqueadores beta con indicación de clase I y evidencia B1,2. Los bloqueadores beta fueron los fármacos frenadores predominantemente usados por los cardiólogos y la digital, por los internistas y médicos de atención primaria. El uso de bloqueadores beta y digitálicos no difirió de manera apreciable en relación con la FEVI deprimida o conservada (tabla 4). Estos datos son parecidos a los observados en otros estudios europeos recientes8,9.
En nuestro estudio se realizó cardioversión previa en el 41,9% de los casos (eléctrica en el 19% y farmacológica en el 22,9%) y ablación de la FA en solo el 3,4% de los casos, siendo el porcentaje mayor en la FA paroxística. Aunque pueda parecer, en el caso de la ablación de FA, una cifra baja, hay que recordar que las guías recomiendan una actitud prudente en este sentido1,2, y que los resultados de registros europeos recientes sobre población general con FA encuentran cifras similares, en torno al 5-7%8–10.
Limitaciones del estudioEl presente estudio es un análisis preliminar de los datos basales del Registro FANTASIIA, cuyo seguimiento está en curso. Hay que esperar a su finalización, prevista en 2016, para obtener un análisis más detallado y adecuado sobre el manejo, el tipo de estrategia empleada y los fármacos antiarrítmicos utilizados para la FANV en España, situaciones que pueden variar en función del tiempo y la evolución de cada paciente en particular. Otra limitación es que se presenta el tratamiento farmacológico en curso a la visita de inclusión, y no los posibles cambios que hubiera podido haber en el pasado, debido al diseño del estudio.
CONCLUSIONESActualmente, se tiende a manejar a los pacientes con FANV de cualquier tipo anticoagulados en nuestro país en mayor proporción con una estrategia de control de frecuencia, la mayoría son de edad avanzada, y se los trata para este objetivo sobre todo con bloqueadores beta. Reciben pocos fármacos antiarrítmicos (amiodarona es el más frecuente) y se los somete en muy baja proporción a tratamientos no farmacológicos como la ablación.
FINANCIACIÓNEl registro FANTASIIA cuenta con una beca no restrictiva de Pfizer/Bristol-Myers-Squibb.
CONFLICTO DE INTERESESNinguno.