En 1987, Cox1 definió los principios y la técnica de uno de los tratamientos más efectivos hasta la fecha para suprimir la fibrilación auricular (FA): la cirugía del laberinto (en inglés, maze). El procedimiento consistía en prevenir las reentradas auriculares y facilitar que los impulsos eléctricos sinusales activasen de forma ordenada todo el miocardio auricular. El patrón de lesiones de la técnica del Cox-maze se fundamentaba en el aislamiento o ablación de unas regiones anatómicas muy definidas que habían sido identificadas en estudios animales previos2.
La iteración del patrón de lesiones para reducir el riesgo de bloqueos condujo a las técnicas Cox-maze II y Cox-maze III. A pesar de su gran eficacia, la cirugía del lanerinto era técnicamente compleja y asociaba un riesgo hemorrágico debido a las limitaciones instrumentales que suponían cortar y suturar la pared auricular. Finalmente, el desarrollo de fuentes de energía alternativa que permitían emular el patrón de lesiones usando radiofrecuencia y/o crioablación (cirugía del Cox-maze IV3) redujo los riesgos asociados a la técnica cut and sew (cortar y coser) y generalizó su indicación.
En los años noventa, Haïsaguerre et al. detectaron que el aislamiento eléctrico por catéter de las venas pulmonares con radiofrecuencia era capaz de interrumpir la FA4, lo que propició un crecimiento exponencial de las técnicas percutáneas. Mientras, la cirugía de las arritmias auriculares, debido a su mayor agresividad, quedaba restringida a procedimientos quirúrgicos en los que, de manera concomitante, se abordaba otra enfermedad estructural o coronaria cardiaca.
En la última década, sin embargo, se ha acumulado evidencia sobre la alta recurrencia de arritmias auriculares en pacientes sometidos a ablación por catéter de FA persistente y persistente de larga duración5. En paralelo, además, la aparición de nuevas fuentes de energía y abordajes quirúrgicos de mínima invasión por toracoscopia han relanzado el interés por la cirugía aislada de las arritmias auriculares. Así, por ejemplo, en la última guía clínica europea de FA, la cirugía toracoscópica aislada de la FA se recomienda (IIa B) para pacientes con FA paroxística o persistente refractaria a antiarrítmicos con recurrencia o alto riesgo de recurrencia después de una ablación percutánea6.
La toma de decisiones en el abordaje de la FA sintomática refractaria o con alto riesgo de recurrencia tras tratamiento médico óptimo y ablación por catéter de venas pulmonares es compleja7. Los resultados de nuevas tecnologías como la ablación por campos pulsados8 son muy prometedores, y queda por dilucidar el efecto de los procedimientos dirigidos como la ablación de facilitadores de la FA o basados en aproximaciones mecanicistas9. En este contexto, la cirugía toracoscópica de la FA no debe considerarse una alternativa al tratamiento por catéter, entre otros motivos, porque la evidencia de su superioridad frente a la ablación con catéter es contradictoria10. En su lugar, se debe valorar la cirugía como tratamiento complementario que puede estar indicado en casos refractarios o complejos pero que, de cualquier forma, debe considerarse en el algoritmo de toma de decisiones en centros de alta experiencia en el tratamiento de la FA.
En un artículo publicado recientemente en Revista Española de Cardiología, Wesselink et al.11 comparan los resultados de la ablación quirúrgica con radiofrecuencia por abordaje mínimamente invasivo en pacientes sometidos o no sometidos a ablaciones percutáneas previas. Al cabo de 1 año, encuentran una mayor supervivencia libre de arritmias auriculares en pacientes sin ablación previa (el 72,5 frente al 61,7%; p <0,001). Es difícil pensar, como se argumenta en el artículo, que el procedimiento percutáneo previo per se induzca un remodelado auricular de una magnitud suficiente para influir en los resultados de una posterior cirugía. Al contrario, es muy probable que el número de procedimientos de ablación previos no sea más que un marcador de riesgo o un factor intermedio entre la duración y el grado de remodelado auricular y el fracaso del tratamiento quirúrgico. Esto es, los pacientes con FA más complejas y de más duración han sido tratados en más ocasiones antes de ser remitidos a una cirugía.
De hecho, cada vez son más frecuentes los programas o abordajes híbridos, que combinan cirugía y catéter para pacientes con FA persistente o persistente de larga duración. En estos casos, la ablación aislada de las venas pulmonares tiene un rendimiento limitado, y la combinación de los 2 abordajes puede asegurar ablaciones más extensas y efectivas de toda la pared posterior de la aurícula, el ligamento de Mashall, la orejuela, el istmo izquierdo, la vena cava superior y el istmo cavotriscúspideo, emulando un patrón clásico de lesiones de Cox12 y evitando las limitaciones de las 2 técnicas por separado.
TÉCNICA QUIRÚRGICA DE LA ABLACIÓN TORACOSCÓPICA DE LA FA AISLADALa ablación quirúrgica se realiza con un abordaje por puertos, sin esternotomía, toracotomía ni circulación extracorpórea, en un quirófano o una sala híbrida. El patrón de lesiones quirúrgicas más comúnmente realizado busca: a) aislar eléctricamente la pared posterior de la aurícula izquierda con una lesión en caja (box lession) que englobe la desembocadura de las 4 venas pulmonares; b) resecar el ligamento de Marshall, y c) excluir mecánica y eléctricamente la orejuela izquierda mediante su amputación con un clip o sutura. Recientemente se ha introducido un nuevo abordaje híbrido denominado convergencia (en inglés, convergence), en el que el abordaje quirúrgico está limitado a hacer una ablación de la pared posterior de la aurícula izquierda13.
Según la duración de la FA, el mapeo elecrofisiológico o los procedimientos previos realizados, se pueden realizar otras lesiones como ablaciones del istmo izquierdo abordando el trígono anterior (conjunto de lesiones tipo Dallas), de la vena cava superior o inferior, de la cresta terminal, de la orejuela derecha, etc.
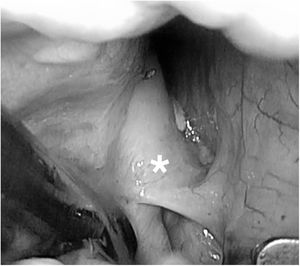
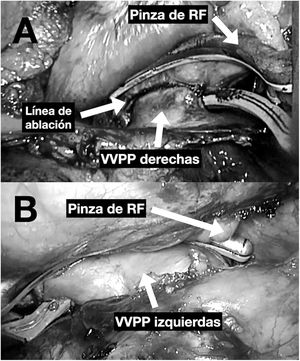
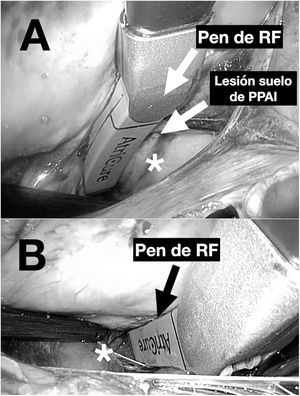
Básicamente, se utilizan 2 tipos de instrumentos: pinzas y dispositivos tipo pen de radiofrecuencia. La correcta colocación de estos dispositivos exige de una disección quirúrgica de las venas pulmonares, el ligamento de Marshall (figura 1) y los senos pericárdicos transverso y oblicuo. En general, estos procedimientos exigen un entrenamiento quirúrgico previo debido a la dificultad técnica que exige el abordaje toracoscópico. En la figura 2, se puede apreciar la ablación de las venas pulmonares derechas (figura 2A) e izquierdas (figura 2B) con unas pinzas de radiofrecuencia bipolar. En la figura 3A se observa cómo se realiza una lesión en el suelo de la pared posterior de la aurícula izquierda, conectando las venas pulmonares inferiores a través del seno transverso. En la figura 3B se muestra una lesión entre las venas pulmonares superiores a través del seno transverso. Una vez completadas las lesiones, se comprueba el bloqueo de entrada y salida de la pared posterior de la aurícula izquierda y de las venas pulmonares derechas o izquierdas.
A: lesión en el suelo de la pared posterior de la aurícula izquierda a través del seno oblicuo (*) con pen de radiofrecuencia. B: lesión en el techo de la pared posterior de la aurícula izquierda a través de seno transverso (*) con pen de radiofrecuencia. PPAI: pared posterior de la aurícula izquierda; RF: radiofrecuencia.
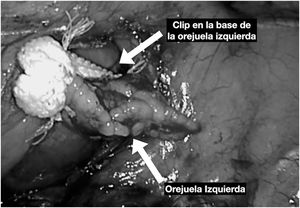
Por último, todos los procedimientos toracoscópicos de ablación de FA deben acompañarse de la exclusión de la orejuela mediante clip o sutura automática (figura 4), pues se ha demostrado que no solo produce un aislamiento mecánico de la orejuela y reduce el riesgo de fenómenos tromboembólicos14, sino también logra su exclusión eléctrica15.
La ablación toracoscópica de FA tiene demostrado un alto grado de eficacia a largo plazo, con supervivencias libres de FA a 5 años por encima del 50% y una incidencia de eventos adversos serios (conversión a esternotomía, hemorragia grave, ictus…) inferior al 1%10.
EL IMPACTO DE LAS ABLACIONES PREVIAS EN LA ABLACIÓN QUIRÚRGICA DE LA FAEn el estudio de Wesselink et al.11 publicado en Revista Española de Cardiología, los autores comparan los resultados de una ablación por toracoscopia entre pacientes con y sin ablaciones percutáneas previas. El espectro de pacientes de la serie tiene un perfil desfavorable para un abordaje percutáneo (entre 4 y 6,5 años de duración de la arritmia, el 66,6% de FA persistente o persistente de larga duración, el 41,5% mayores de 65 años, con aurículas muy dilatadas, etc.), lo que justifica la indicación de la cirugía.
Los autores detectaron una mayor supervivencia libre de ritmo sinusal al año en el grupo de pacientes sin ablaciones previas (el 72,5 frente al 61,1%; p=0,034), una vez ajustadas las diferencias por puntuación de propensión. Intuitivamente, parece evidente que los pacientes en que ya ha fracasado un procedimiento percutáneo previo tengan mayor riesgo de un nuevo fracaso independientemente de cuál sea el segundo procedimiento (quirúrgico o percutáneo). La cuestión es si es el hecho en sí de la ablación percutánea previa lo que incrementa el riesgo del segundo fracaso o es el sustrato más extenso y agresivo de estos enfermos. Es decir, ¿las ablaciones previas son un factor de riesgo per se, o más bien son un indicador de riesgo o factor intermedio de una mayor tasa de fracaso de la terapia de control de ritmo?
Los propios autores especulan sobre esta posibilidad en la discusión de sus hallazgos en este estudio, y apuntan, mediante un estudio de la composición del colágeno extracelular de las orejuelas izquierdas, a sustratos más avanzados en pacientes con procedimientos previos. Obviamente, es difícil pensar que esa alteración del colágeno se pueda explicar por una ablación previa, habida cuenta de que raramente se realiza la ablación percutánea de las orejuelas, por el riesgo embolígeno asociado.
De cualquier forma, llama la atención que un 46% de los pacientes en el grupo de ablación previa se habían sometido a 2 o más procedimientos percutáneos antes de ser remitidos a cirugía y un 14,7%, 3 o más. Cabría plantearse si no se debería haber referido a esos pacientes antes de una ablación quirúrgica o a centros de referencia expertos en abordajes de la FA más complejos.
En nuestro país, la cirugía de la FA se practica raramente en comparación con otros países europeos y Estados Unidos. Según el Registro Español de Cirugía Cardiovascular, en 2019 solo se realizaron 23 cirugías aisladas de FA por toracoscopia y cirugía concomitante de la FA solo en un 4% de los pacientes con FA intervenidos por otro motivo16. Las explicaciones de estos datos son muy especulativas: la intervención se indica en fases muy avanzadas de la historia natural de la FA, el sobrecoste económico asociado al procedimiento no es asumible, la falta de entrenamiento entre los cirujanos, el desconocimiento de la técnica por parte de la comunidad cardiológica en su conjunto, etc.
De cualquier forma, sí parece que, en España, la ablación toracoscópica de la FA está muy poco indicada y realizada, cuando existe evidencia del valor añadido que puede aportar dentro de programas de abordaje integral (clínico, intervencionista y quirúrgico) de pacientes con FA compleja en centros de excelencia.
FINANCIACIÓNNinguna.
CONFLICTO DE INTERESESM. Carnero Alcázar es proctor de AtriCure Europe, empresa dedicada a la fabricación de dispositivos para ablación quirúrgica de FA y cuyo logo aparece en alguna figura del presente artículo. L. Maroto-Castellanos y J.J. González-Ferrer declaran no tener conflictos de intereses.