La guía de práctica clínica vigente propone un tratamiento integral de la insuficiencia cardiaca con fracción de eyección reducida (IC-FEr), con la administración precoz de tratamientos de los que se ha demostrado que reducen la progresión de la enfermedad. Sin embargo, estos fármacos tienen sus particularidades, que es importante conocer, ya que pueden modificar la frecuencia cardiaca (bloqueadores beta e ivabradina), la presión arterial (los bloqueadores beta, los inhibidores del sistema renina-angiotensina-aldosterona, el sacubitrilo-valsartán y mínimamente los inhibidores del SGLT2 y el vericiguat), así como la función renal o los iones (los inhibidores del sistema renina-angiotensina y el sacubitrilo-valsartán). En consecuencia, el tratamiento de la IC-FEr se debe individualizar en función del perfil clínico del paciente, ya que según sus características clínicas se podrán emplear algunos o todos los fármacos modificadores de la enfermedad. El vericiguat es un estimulador de la guanilato ciclasa soluble que actúa en una vía no abordada antes, que es la del óxido nítrico-guanilato ciclasa soluble-GMPc y complementa las otras vías terapéuticas utilizadas en la IC-FEr, y mejora las funciones cardiaca, vascular y renal de estos pacientes. En este contexto el vericiguat, del que se ha demostrado reducción del riesgo de complicaciones en el paciente con IC-FEr, tiene un excelente perfil de seguridad y escasas interacciones, y por sus características farmacológicas (efecto mínimo en la presión arterial y ningún impacto en la función renal, los iones o la frecuencia cardiaca), es un tratamiento sencillo de emplear en todo el espectro clínico de pacientes con IC-FEr.
Palabras clave
En 2016, la guía de la Sociedad Europea de Cardiología (ESC) sobre insuficiencia cardiaca con fracción de eyección reducida (IC-FEr) planteaba una aproximación terapéutica escalonada, basada en la persistencia de los síntomas del paciente. De manera muy resumida, el tratamiento debía comenzar con un inhibidor de la enzima de conversión de la angiotensina (IECA) o un antagonista del receptor de la angiotensina II (ARA-II) en caso de intolerancia, junto con bloqueado- res beta (BB), ajustando las dosis hasta las dosis objetivo recomendadas o las máximas toleradas, y diuréticos en caso de síntomas congestivos. Si el paciente continuaba sintomático (clase funcional de la New York Heart Association [NYHA] ≥ II), se añadía un antagonista de la aldosterona. Si a pesar de esto, el paciente continuaba con síntomas, se establecía un tercer escalón, con tres alternativas terapéuticas, complementarias entre sí: sustituir el IECA o ARA-II por sacubitrilo- valsartán, terapia de resincronización cardiaca o añadir ivabradina, según los casos y las características del paciente1.
Sin embargo, desde entonces han surgido numerosas publicaciones que han ayudado a comprender que la IC-FEr es una enfermedad progresiva, en la que intervienen numerosos sistemas neurohormonales que se retroalimentan, y sobre los que hay que actuar pronto y de manera holística2,3 El tratamiento de algunos de ellos, pero no de todos, se va a traducir en una respuesta parcial e insuficiente. De hecho, en un reciente estudio que analizaba los resultados de varios ensayos clínicos, se objetivó que, en comparación con la combinación de IECA/ARA-II y BB (primer escalón del tratamiento de la guía ESC 2016), la combinación de sacubitrilo-valsartán, BB, antagonista de la aldosterona e inhibidor del SGLT2 (primer escalón del tratamiento en la actualización de la guía de IC) se traduce en reducciones muy marcadas del riesgo de complicaciones como mortalidad cardiovascular, muerte por cualquier causa y hospitalizaciones por IC4.
En este contexto, la guía ESC 2021 de IC, al igual que la canadiense de 2021 y la última actualización del American College of Cardiology3,5,6 adoptan un enfoque más general y completo, con el objetivo de intervenir precoz y globalmente en los diferentes sistemas neurohormonales que participan en la etiopatogenia de la IC (algunos por activación de vías deletéreas y otros por inhibición de vías protectoras).
Así, la guía ESC 2021 de IC propone un primer escalón con IECA (I A) o sacubitrilo-valsartán (I B), BB (I A), antagonistas de la aldosterona (I A) e inhibidores del SGLT-2 (I A) para disminuir el riesgo de hospitalización por IC y muerte3. Aunque la guía propone el tratamiento con todos estos grupos terapéuticos, es evidente que según las características del paciente (presión arterial, frecuencia cardiaca, función renal, potasio sérico, etc.), se podrá tratarlo con todos o solo algunos de ellos7. Como segundo escalón, la guía plantea los ARA-II, la ivabradina y el vericiguat. Los ARA-II están indicados en caso de que no se pueda emplear los IECA o el sacubitrilo-valsartán; la ivabradina, si el paciente persiste sintomático y se encuentra en ritmo sinusal con una frecuencia cardiaca ≥ 70 lpm a pesar del tratamiento con BB a las dosis máximas recomendadas o toleradas (o en lugar de los BB si no pueden emplearse), y el vericiguat, en caso de que el paciente permanezca sintomático y con empeoramiento clínico a pesar de los tratamientos del primer escalón (tabla 1)3. No obstante, dependiendo de las características clínicas del paciente, estos podrán emplearse antes, incluso de inicio, según los casos7. Por ello es muy importante conocer aspectos prácticos de cómo se debe emplear cada uno de estos fármacos para establecer la mejor estrategia terapéutica individualizada para cada paciente.
Indicación y recomendaciones de la guía ESC 2021 de insuficiencia cardiaca sobre los tratamientos farmacológicos modificadores del curso de la IC-FEr
| Tratamiento | Posición en el algoritmo | Recomendación | Indicación |
|---|---|---|---|
| IECAa | Primer escalón | I A | Para disminuir el riesgo de hospitalización por IC y muerte |
| Sacubitrilo-valsartánb | I B | ||
| Bloqueadores betac | I A | ||
| Antagonistas de la aldosterona | I A | ||
| iSGLT2d | I A | ||
| Vericiguat | Segundo escalónf | IIb B | Si persiste sintomático con empeoramiento de la IC, para reducir el riesgo de hospitalización por IC o muerte cardiovascular |
| Ivabradina | 1. IIa B1 | Si persiste sintomático, en ritmo sinusal con FC ≥ 70 lpm, añadido1 o no2 (intolerancia/contraindicación) a los bloqueadores beta, para reducir el riesgo de hospitalización por IC o muerte cardiovascular | |
| 2. IIa C2 | |||
| ARA-IIe | I B | Si no pueden tomar IECA o sacubitrilo-valsartán, para reducir el riesgo de hospitalización por IC o muerte cardiovascular |
Tabla elaborada con datos de McDonagh3. ARA-II: antagonistas del receptor de la angiotensina II; FC: frecuencia cardiaca; IC-FEr: insuficiencia cardiaca con fracción de eyección reducida; IECA: inhibidores de la enzima de conversión de la angiotensina; iSGLT2: inhibidores del cotransportador de sodio-glucosa tipo 2.
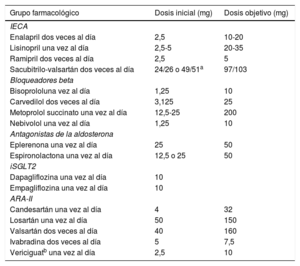
En primer lugar, es importante señalar que, en general, siempre que sea posible, hay que intentar alcanzar las dosis máximas recomendadas de cada fármaco modificador del curso de la IC-FEr (tabla 2)8, ya que son las dosis que lograron el mayor beneficio clínico demostrado en los ensayos clínicos.9,25-36
Dosis inicial y dosis objetivo de los principales tratamientos farmacológicos modificadores del curso de la IC-FEr
| Grupo farmacológico | Dosis inicial (mg) | Dosis objetivo (mg) |
|---|---|---|
| IECA | ||
| Enalapril dos veces al día | 2,5 | 10-20 |
| Lisinopril una vez al día | 2,5-5 | 20-35 |
| Ramipril dos veces al día | 2,5 | 5 |
| Sacubitrilo-valsartán dos veces al día | 24/26 o 49/51a | 97/103 |
| Bloqueadores beta | ||
| Bisoprololuna vez al día | 1,25 | 10 |
| Carvedilol dos veces al día | 3,125 | 25 |
| Metoprolol succinato una vez al día | 12,5-25 | 200 |
| Nebivolol una vez al día | 1,25 | 10 |
| Antagonistas de la aldosterona | ||
| Eplerenona una vez al día | 25 | 50 |
| Espironolactona una vez al día | 12,5 o 25 | 50 |
| iSGLT2 | ||
| Dapagliflozina una vez al día | 10 | |
| Empagliflozina una vez al día | 10 | |
| ARA-II | ||
| Candesartán una vez al día | 4 | 32 |
| Losartán una vez al día | 50 | 150 |
| Valsartán dos veces al día | 40 | 160 |
| Ivabradina dos veces al día | 5 | 7,5 |
| Vericiguatb una vez al día | 2,5 | 10 |
Tabla elaborada con datos de McDonagh3, Armstrong9 y las fichas técnicas de carvedilol10, bisoprolol11, nebivolol12, eplerenona13, espironolactona14, enalapril15, ramipril16, sacubitrilo-valsartán17, losartán18, valsartán19, candesartán20, dapagliflozina21, empagliflozina22, ivabradina23 y vericiguat24. ARA-II: antagonistas del receptor de la angiotensina II; IC-FEr: insuficiencia cardiaca con fracción de eyección reducida; IECA: inhibidores de la enzima de conversión de la angiotensina; iSGLT2: inhibidores del cotransportador de sodio-glucosa tipo 2.
Se comienza con 24/26 mg bid para los pacientes sin tratamiento previo con IECA o ARA-II o que hayan recibido dosis bajas de estos medicamentos o tengan presión arterial sistólica 100-110 mmHg, antecedentes de hipotensión ortostática, filtrado glomerular ≤ 60 ml/min/1,73 m2 o insuficiencia hepática moderada. Se recomienda aumentar la dosis lentamente, duplicando la dosis cada 3-4 semanas.
La dosis inicial recomendada de vericiguat es 2,5 mg 1 vez al día. La dosis se debe doblar aproximadamente cada 2 semanas para alcanzar la dosis objetivo de mantenimiento de 10 mg 1 vez al día, en función de la tolerancia del paciente. Si los pacientes experimentan problemas de tolerancia (hipotensión sintomática o presión arterial sistólica < 90 mmHg), se recomienda una reducción temporal de la dosis o la interrupción del vericiguat. Los pacientes con presión arterial sistólica < 100 mmHg no deben iniciar el tratamiento.
El inicio del tratamiento con los fármacos modificadores del curso de la IC-FEr debe ser precoz, en función de las características del paciente (presión arterial, frecuencia cardiaca, función renal, electrolitos). En consecuencia, es importante conocer cómo afectan a estos parámetros los diferentes fármacos modificadores del curso de la enfermedad7. Así, los BB reducen la presión arterial y la frecuencia cardiaca, pero no tienen efecto en la función renal o los electrolitos; los IECA, los ARA-II, el sacubitrilo-valsartán y los antagonistas de la aldosterona pueden reducir la presión arterial, empeorar la función renal y aumentar la potasemia; los inhibidores del SGLT2 tienen discreto efecto en la presión arterial, ninguno en la frecuencia cardiaca y, aunque puede haber un empeoramiento inicial de la función renal, son fármacos nefroprotectores; la ivabradina solo actúa en la frecuencia cardiaca del paciente en ritmo sinusal (en los pacientes en fibrilación auricular no tiene impacto y no está indicada), pero no tiene efecto en la presión arterial, la función renal o los electrolitos; por último, el vericiguat tiene un efecto mínimo en la presión arterial, pero ningún impacto en la frecuencia cardiaca, la función renal o los electrolitos10-24.
Aunque la recomendación general es seguir las indicaciones de las guías de práctica clínica, lo cierto es que no siempre se puede emplear todos los fármacos de primera línea desde el principio (p. ej., un paciente con bradicardia no puede tomar BB, y si presenta hiperpota- semia, tampoco inhibidores del sistema renina-angiotensina-aldoste- rona). En consecuencia, lo importante no es tanto la división entre fármacos de primer o segundo escalón, sino administrar los fármacos modificadores del curso de la enfermedad (que reducen las hospitalizaciones por IC y la mortalidad cardiovascular) en función de las características del paciente, con el objetivo de restablecer la mayoría de los sistemas neurohormonales implicados en la génesis y la evolución de la IC2.
Con respecto al entorno donde iniciar los fármacos para la IC, el paciente estable puede comenzar todos ellos en contexto ambulatorio (consultas externas, unidades de IC). En el caso de que el paciente esté ingresado, los BB se iniciarán tras estabilizar y aliviar/eliminar la congestión, idealmente antes del alta hospitalaria. Si el paciente ya los tomaba antes del ingreso, se intentará mantenerlos (o disminuir la dosis, en su caso), salvo que el paciente se encuentre muy congestivo, hipotenso o en shock37. Durante el ingreso se puede comenzar con los inhibidores del sistema renina-angiotensina-aldosterona siempre que la función renal, las cifras de potasio y la presión arterial lo permitan. En el caso de los inhibidores del SGLT2, salvo hipotensión o deterioro grave de la función renal, también se pueden iniciar antes del alta hospitalaria. Con respecto al vericiguat, antes de comenzar el tratamiento con este fármaco se deberá optimizar el estado volémico del paciente y ajustar el tratamiento diurético para estabilizarlo después del episodio de descompensación, especialmente si hay cifras de pép- tidos natriuréticos muy elevadas (tabla 3)3,9-24.
Inicio, ajuste de dosis, contraindicaciones e interacciones de los principales tratamientos farmacológicos modificadores del curso de la IC-FEr
| Bloqueadores beta | Antagonistas de la aldosterona | IECA/ARA-II | INRA | iSGLT2 | Ivabradina | Vericiguat | |
|---|---|---|---|---|---|---|---|
| Inicio | Para pacientes estables, inicio ambulatorio; los pacientes hospitalizados o con IC progresiva deben iniciarlo tras estabilizar y aliviar/eliminar la congestión, idealmente antes del alta hospitalaria | Dependiendo de las características del paciente, se pautará ambulatorio o en el hospital | Dependiendo de las características del paciente, se pautará ambulatorio o en el hospital | Dependiendo de las características del paciente, se pautará ambulatorio o en el hospital | Dependiendo de las características del paciente, se pautará ambulatorio o en el hospital | Para pacientes estables, ambulatorio | Se pautará en el hospital, al alta hospitalaria o en las visitas sucesivas de control |
| Ajuste de dosis | Comenzar a dosis bajas y doblar la dosis al menos cada 2 semanas hasta la dosis máxima objetivo/ tolerada Se debe monitorizar FC, PA, estado clínico (signos/síntomas de congestión, astenia, etc.) y peso | Antes de iniciarlos se comprobará la función renal y los iones (potasio) Comenzar a dosis bajas y se valora ajustar la dosis a las 4-8 semanas Monitorizar PA Bioquímica tras 1 y 4 semanas de iniciar el tratamiento o aumentar la dosis, y a las 8 y 12 semanas, y a los 6, 9 y 12 meses y cada 4 meses a partir de entonces | Antes de iniciar/ajustar estos fármacos, se debe comprobar la función renal y los electrolitos Comenzar con dosis bajas, y duplicar la dosis en intervalos superiores a 2 semanas en la consulta, valorando la PA y la bioquímica de control (función renal y potasio) a las 1-2 semanas tras el inicio y 1-2 semanas tras alcanzar el fin del ajuste de dosis Después, monitorización analítica periódica (4 meses) o en caso de descompensación | Antes de iniciarlos se comprobará la función renal y los iones (potasio). Si el paciente estaba tomando IECA, se requiere un periodo de aclaramien- to de 36 h antes de iniciar sacubitrilo-valsartán (no hace falta si tomaba ARA-II) Comenzar a dosis bajas y se valorará ajustar en periodos no inferiores a 2 semanas, valorando tolerancia y PA, y repetir la bioquímica (función renal, potasio) 1-2 semanas tras el inicio, 1-2 semanas tras cada ajuste de dosis, y después cada 4 meses | Antes de iniciarlo se comprobará la función renal No se requiere ajuste de dosis | Comenzar con 5 mg bid (mayores de 75 años, plantear 2,5 mg bid) Tras un periodo no inferior a 2 semanas, subir a 7,5 mg bid (o reducir a 2,5 mg bid) según FC No modificar dosis si FC en reposo 50-60 lpm | Comenzar con dosis bajas (2,5 mg) y doblar la dosis aproximada-mente cada 2 semanas en función de la tolerancia, hasta alcanzar la dosis objetivo de 10 mg/día |
| Contraindica-ciones | Bloqueo auriculoventricular avanzado (segundo o tercer grado), sin marcapasos, isquemia crítica en extremidades (en situaciones menos graves se pueden administrar), asma (contraindicación relativa; EPOC no es contraindicación) o alergia | Reacción alérgica conocida relacionada con el fármaco | Antecedentes de angioe- dema, estenosis bilateral de las arterias renales (unilateral en caso de riñón único), embarazo o riesgo de embarazo, o en caso de reacción alérgica conocida relacionada con el fármaco | Antecedentes de angioedema, estenosis arteria renal bilateral, embarazo, alto riesgo de embarazo o lactancia, reacción alérgica, TFGe < 30 ml/min/1,73 m2, síntomas de hipotensión, o PA sistólica < 90 mmHg | Reacciones alérgicas o efectos secundarios graves, embarazo, alto riesgo de embarazo, lactancia, TFGe < 20 ml/min/1,73 m2 (en DAPA CKD se incluyeron a partir de 25 ml/ min/1,73 m2) o síntomas de hipotensión o PA sistólica < 95 mmHg | Situaciones cardiovasculares inestables, fibrilación auricular, enfermedad renal o hepática grave, embarazo o lactancia, reacción alérgica conocida al fármaco | Reacción alérgica, toma concomitante de otros estimuladores de la guanilato ciclasa soluble, como el riociguat |
| Interacciones farmacológicas farmacocinéti- cas y farmacodiná- micas | Antiarrítmicos, nitratos, antagonistas del calcio no dihidropiridínicos, antihipertensivos, ciclosporina, bloqueadores beta tópicos, anestésicos, digoxina, AINE, corticoides, simpaticomiméti- cos, antidiabéticos, inhibidores/ inductores CYP P450 | Fármacos que aumenten el potasio (diuréticos ahorradores de potasio, suplemen-tos de potasio, INRA/IECA/ARAII), antihipertensivos, litio, ciclosporina, tacrolimus, AINE, trimetoprim, bloqueadores alfa, antidepresivos tricíclicos, neurolépticos, baclofeno, corticoides, inhibidores/ inductores CYP 3A4, digoxina | Inhibición doble del sistema renina-angiotensina, diuréticos ahorradores de potasio, suplementos de potasio, sales de potasio, ciclosporina, heparina, fármacos antihipertensivos, litio, antidepresivos tricíclicos, antipsicóticos, anestésicos, nitratos, AINE, AAS, simpaticomiméticos, alopurinol, inmunosupreso- res, corticoides, procainamida, citostáticos, alcohol, trombolíticos, biguanidas, sulfonilureas, insulina | Diuréticos, insulina, secretagogos | Fármacos que prolongan el intervalo QT, inhibidores/ inductores del CYP3A4, fármacos bradicardizan- tes | Ninguna (no se recomienda tratamiento concomitante con inhibidores de la fosfodieste- rasa 5) | |
Tabla elaborada con datos de McDonagh3, Armstrong9, las fichas técnicas de carvedilol10, bisoprolol11, nebivolol12, eplerenona13, espironolactona14, enalapril15, ramipril16, sacubitrilo-valsartán17, losartán18, valsartán19, candesartán20, dapagliflozina21, empagliflozina22, ivabradina23, vericiguat24 e Ibáñez38 AAS: ácido acetilsalicílico; AINE: antiinflamatorios no esteroideos; ARA-II: antagonistas del receptor de la angiotensina II; EPOC: enfermedad pulmonar obstructiva crónica; IECA: inhibidores de la enzima de conversión de la angiotensina; INRA: inhibidores de la neprilisina y el receptor de la angiotensina; iSGLT2: inhibidores del cotransportador de sodio-glucosa tipo 2; FC: frecuencia cardiaca; IC-FEr: insuficiencia cardiaca con fracción de eyección reducida; PA: presión arterial; TFGe: tasa de filtrado glomerular estimada.
Con respecto al ajuste de dosis, excepto en el caso de los inhibidores del SGLT2, que no requieren ajuste (dosis única diaria), y los antagonistas de la aldosterona, que hay que ajustar pasadas al menos 4 semanas, en el resto de los casos (BB, IECA, ARA-II, sacubitrilo-valsar- tán, ivabradina y vericiguat), se realizará al menos cada 2 semanas (tabla 3)3,9-24.
Los pacientes con IC tienen numerosas comorbilidades, lo que implica que están polimedicados39,40. Por lo tanto, es muy importante considerar las posibles interacciones farmacológicas para disminuir el riesgo de posibles efectos adversos o que la eficacia de los fármacos para la IC disminuya9,24,38. En la tabla 3 se resumen las principales interacciones farmacocinéticas y farmacodinámicas con los fármacos modificadores del curso de la enfermedad, así como sus contraindicaciones. A diferencia de otros fármacos para la IC, el vericiguat prácticamente no tiene interacciones con otros fármacos ni contraindicaciones, lo que facilita su empleo en la práctica clínica diaria3,9-24,38.
El seguimiento adecuado de los pacientes con IC-FEr permite optimizar el tratamiento farmacológico. Para ello es imprescindible monitorizar la función renal, los electrolitos, la presión arterial y la frecuencia cardiaca durante el tratamiento. En el caso de los BB, se monitoriza la presión arterial y la frecuencia cardiaca; con los inhibidores del sistema renina-angiotensina-aldosterona y el sacubitrilo- valsartán, la función renal, los iones y la presión arterial; con los inhibidores del SGLT2 y el vericiguat, el estado volémico y la presión arterial, y con la ivabradina, la frecuencia cardiaca (tabla 4)3,9-24.
Monitorización de los principales tratamientos farmacológicos modificadores del curso de la IC-FEr
| Bloqueadores beta | Antagonistas de la aldosterona | INRA/IECA/ARA-II | iSGLT2 | Ivabradina | Vericiguat | |
|---|---|---|---|---|---|---|
| Electrolitos; función renal | Ninguna | Monitorización durante el ajuste de dosis y luego de manera periódica | Monitorización durante el ajuste de dosis y luego de manera periódica | Ninguna | Ninguna | Ninguna |
| Presión arterial | Monitorización durante el ajuste de dosis y luego de manera periódica | Pequeña reducción de la presión arterial | Monitorización durante el ajuste de dosis y luego de manera periódica | Pequeña reducción de la presión arterial | Ninguna | Efecto mínimo en la presión arterial |
| Frecuencia cardiaca | Monitorización durante el ajuste de dosis y luego de manera periódica | Ninguna | Ninguna | Ninguna | Monitorización durante el ajuste de dosis y luego de manera periódica | Ninguna |
Tabla elaborada con datos de McDonagh3, Armstrong9 y las fichas técnicas de carvedilol10, bisoprolol11, nebivolol12, eplerenona13, espironolactona14, enalapril15, ramipril16, sacubitrilo-valsartán17, losartán18, valsartán19, candesartán20, dapagliflozina21, empagliflozina22, ivabradina23 y vericiguat24. ARA-II: antagonistas del receptor de la angiotensina II; INRA: inhibidores de la neprilisina y el receptor de la angiotensina; IC-FEr: insuficiencia cardiaca con fracción de eyección reducida; IECA: inhibidores de la enzima de conversión de la angiotensina; iSGLT2: inhibidores del cotransportador de sodio-glucosa tipo 2.
Aunque los fármacos para la IC son seguros, durante el seguimiento pueden surgir diferentes problemas con uno o más de ellos, de distinta intensidad, por lo que es importante conocerlos y saber cómo actuar de manera correcta, con el objetivo de minimizar los riesgos y maximizar el beneficio clínico. En la tabla 5 se resumen los problemas más relevantes de los principales tratamientos farmacológicos modificadores del curso de la IC-FEr, así como la actuación más adecuada9-24.
Problemas más relevantes y actuación con los principales tratamientos farmacológicos modificadores del curso de la IC-FEr
| Bloqueadores beta | Antagonistas de la aldosterona | IECA/ARA-II | INRA | iSGLT2 | Ivabradina | Vericiguat | |
|---|---|---|---|---|---|---|---|
| Hipotensión | Si asintomático, vigile Si sintomático, valore reducir/suspender otros fármacos que disminuyan la PA y no tengan demostrado beneficio pronóstico, así como el estado volémico/diuréticos | Obtenga un balance volémico adecuado, ajustando los diuréticos en caso necesario | NA | Si los pacientes sufren problemas de tolerancia (hipotensión sintomática o PA sistólica < 90 mmHg), se recomienda una reducción temporal de la dosis o la interrupción de vericiguat | |||
| Tos | NA | NA | Si se confirma que es por IECA (no por descompensación de IC o por enfermedad pulmonar), se puede plantear el cambio a ARA-II | Puede ser síntoma de enfermedad pulmonar o de descompensación de IC. Si hay tos persistente, considere sustituir por ARA-II | NA | NA | NA |
| Empeoramiento de la función renal e hiperpotasemia | NA | Puede haber un empeoramiento inicial, generalmente leve, para el que no hay que tomar medidas concretas Considere suspender/reducir fármacos que puedan interferir, como AINE o suplementos de potasio | Al inicio del tratamiento, puede haber una caída ligera del filtrado | NA | NA | ||
| Empeoramiento clínico (astenia, disnea, fatiga, descompensación de la IC) | Si aumenta la congestión, incremente la dosis de diurético o reduzca a la mitad la dosis de bloqueador beta Si aumenta la fatiga (o bradicardia), reduzca a la mitad y revise en 1-2 semanas Si hay deterioro clínico grave, reduzca a la mitad o suspenda el bloqueador beta | NA | NA | NA | NA | NA | NA |
| Bradicardia | Si FC < 50 lpm y empeoramiento de síntomas, ajuste/ suspenda tratamiento bradicardi- zante concomitante, y reduzca/ suspenda bloqueadores beta, según la gravedad | NA | NA | NA | NA | Si FC < 50 lpm o bradicardia sintomática, reduzca la dosis o suspenda | NA |
| Glucemia | NA | NA | NA | NA | Monitorice la glucemia, sobre todo de los pacientes diabéticos y en particular si toman insulina o sulfonilureas, ajustando la medicación concomitante en caso necesario | NA | NA |
| Infecciones genitourinarias | NA | NA | NA | NA | Profilaxis higiénica adecuada, y pautar antibiótico en su caso | NA | NA |
Tabla elaborada con datos de McDonagh3, Armstrong9 y las fichas técnicas de carvedilol10, bisoprolol11, nebivolol12, eplerenona13, espironolactona14, enalapril15, ramipril16, sacubitrilo-valsartán17, losartán18, valsartán19, candesartán20, dapagliflozina21, empagliflozina22, ivabradina23 y vericiguat24. ARA-II: antagonistas del receptor de la angiotensina II; INRA: inhibidores de la neprilisina y el receptor de la angiotensina; IC-FEr: insuficiencia cardiaca con fracción de eyección reducida; IECA: inhibidores de la enzima de conversión de la angiotensina; iSGLT2: inhibidores del cotransportador de sodio-glucosa tipo 2.
Con respecto al vericiguat, el estudio VICTORIA objetivó en pacientes con IC-FEr una reducción significativa de la variable primaria combinada muerte cardiovascular o primera hospitalización por IC, hospitalizaciones totales por IC y la variable combinada muerte por cualquier causa o primera hospitalización por IC con el vericiguat añadido al tratamiento estándar de la IC en comparación con el pla cebo, con un excelente perfil de seguridad9. Dado que el vericiguat solo tiene un efecto ligero en la presión arterial, ningún impacto en la función renal, los iones o la frecuencia cardiaca y un escaso riesgo de interacciones farmacológicas9,24, su empleo en la práctica clínica y su seguimiento son sencillos, por lo cual pueden aplicarse a todo el espectro de pacientes con IC-FEr.
ConclusionesEn los últimos años, el tratamiento de la IC-FEr ha evolucionado desde un abordaje escalonado a un tratamiento transversal, más integrador, que proporciona un mayor beneficio clínico, al actuar sobre los diferentes sistemas neurohormonales implicados en la génesis de la IC-FEr. Sin embargo, cada uno de estos fármacos tiene sus peculiaridades, que es necesario conocer para iniciar y ajustar la dosis de manera adecuada, darles un seguimiento correcto y actuar frente a las posibles complicaciones que pueden ir surgiendo. El vericiguat es un estimulador de la guanilato ciclasa soluble que actúa por una vía no abordada previamente, que es la del óxido nítrico-guanilato ciclasa soluble-guanosina monofosfato cíclico, y complementa las otras vías terapéuticas utilizadas en la IC-FEr mejorando las funciones cardiaca, vascular y renal de estos pacientes. En este contexto el vericiguat, del que se ha demostrado que reduce el riesgo de complicaciones del paciente con IC-FEr, con un excelente perfil de seguridad y escasas interacciones farmacológicas, por sus características (efecto mínimo en la presión arterial y ninguno en la función renal, los iones o la frecuencia cardiaca), es un fármaco sencillo de emplear en todo el espectro clínico de los pacientes con IC-FEr.
Contribución de los autoresTodos los autores han contribuido significativamente al trabajo presentado en este artículo en la concepción, el diseño o la adquisición de información o en el análisis y la interpretación de datos. Todos los autores han participado en la redacción o revisión del manuscrito y aceptan su publicación.
Conflicto de interesesJ.M. Cepeda-Rodrigo no declara ningún conflicto de intereses en relación con este artículo. J. Comín-Colet ha recibido honorarios como ponente de Bayer, no relacionado con el presente artículo. A. García- Quintana ha recibido financiación por servicios de consultoría y conferencias de Bayer, Daiichi- Sankyo, Pfizer, Astra Zeneca, Boehringer Ingelheim, Novartis y Rovi. M. Anguita Sánchez ha recibido compensaciones por asesoría y ponencias de Bayer, Daiichi- Sankyo y Pfizer. J.L. Zamorano ha recibido honorarios por ponencias de Bayer y Daii- chi-Sankyo. J.R. González-Juanatey ha recibido compensaciones por asesoría y ponencias de: Amgen, AstraZeneca, Bayer, Boehringer- Ingelheim, MSD, Daichii-Sankyo, Ferrer International, Novartis, Lilly, Sanofi y Servier.
AgradecimientosContent Ed Net (Madrid) proporcionó asistencia editorial en la redacción de este manuscrito con financiación de Bayer Hispania.