A pesar de la existencia de estrategias de prevención primaria y secundaria1,2, los tratamientos antitrombóticos con un mecanismo de acción inmediato3,4 y las estrategias de reperfusión coronaria rápida5,6, sigue habiendo un número considerable de pacientes con un síndrome coronario agudo (SCA) que se presentan con inestabilidad hemodinámica (clase Killip avanzada) o eléctrica (parada cardiaca extrahospitalaria)7. Estos pacientes con SCA que sufren estas temibles complicaciones pueden agruparse bajo la definición genérica de «pacientes vulnerables» (PV). Algunos datos recientes indican que la incidencia de PV oscila entre el 3 y el 13% del total de pacientes con SCA, con una prevalencia que es de 2 a 3 veces superior en los individuos con un infarto agudo de miocardio con elevación del segmento ST que en aquellos con infarto de miocardio sin elevación del segmento ST7. Es importante señalar que los PV se caracterizan por unas tasas de mortalidad muy altas, lo cual subraya la necesidad de estrategias para mejorar su pronóstico7. Lamentablemente, con frecuencia se excluye a los PV de los ensayos controlados y aleatorizados (ECA), lo cual impide determinar el mejor enfoque basado en la evidencia para tratarlos. Esto incluye la vía de acceso vascular y el tratamiento antitrombótico óptimo, aspectos que forman parte de la asistencia de esta población de gran complejidad cuando se someten a intervenciones coronarias percutáneas (ICP).
Actualmente se acepta de manera universal el uso de la vía radial como método de acceso vascular más seguro y preferido para los pacientes que se someen a una ICP5,6. Sin embargo, en los PV se usa con más frecuencia la vía femoral que la radial8. Esto puede atribuirse a la percepción de que la vía de acceso femoral puede resultar más fácil en este contexto (p. ej., porque el pulso femoral es más fácil de palpar que el radial si la presión arterial es baja) o que estos pacientes pueden requerir una intervención coronaria más compleja que posiblemente requiera un acceso vascular de mayor calibre9. No obstante, el acceso por la vía radial y la capacidad de realizar intervenciones coronarias complejas a través de ella dependen en gran manera de la experiencia del operador. Se debe señalar que el acceso femoral en los PV, en los que a menudo no se usa una guía mediante ecografía, se asocia a con mayor riesgo de complicaciones locales en la zona del acceso vascular, hemorragias y muerte8,9.
La reciente guía sobre el SCA5,6 recomienda el uso de heparina no fraccionada (HNF) como método estándar para la anticoagulación intraintervención, si bien esta recomendación está respaldada por un nivel de evidencia bajo (clase de recomendación I, nivel de evidencia C). Las ventajas farmacodinámicas y farmacocinéticas de la bivalirudina respecto a la HNF, que se han traducido en una reducción de las complicaciones hemorrágicas, han permitido que ese fármaco pase a ser una opción de tratamiento razonable para los pacientes con SCA que se someten a una ICP10. Sin embargo, todavía no se conocen las consecuencias clínicas asociadas con el uso de la bivalirudina en una cohorte de PV como los que están en una clase Killip avanzada o inestabilidad eléctrica, que tienen mayor riesgo de complicaciones hemorrágicas11.
En un artículo publicado recientemente en Revista Española de Cardiología, Gargiulo et al.12 describen los resultados de un análisis post hoc de PV del programa MATRIX (Minimizing Adverse Haemorrhagic Events by Transradial Access Site and Systemic Implementation of Angiox, NCT01433627), en el que se comparó el acceso radial con el femoral y el uso de bivalirudina con el de la HNF. En resumen, el estudio MATRIX es un ensayo clínico multicéntrico prospectivo y de diseño abierto, en el que se aleatorizó con un diseño factorial 2 × 2 a los pacientes con SCA a intervención con acceso transradial (n = 4.197) o transfemoral (n = 4.207) (MATRIX-Acceso) y a la administración peroperatoria de bivalirudina (n = 3.610) o HNF (n = 3.603) junto con uso provisional de inhibidores de la glucoproteína IIb/IIIa (MATRIX-Antitrombina). Se realizó también una tercera aleatorización de los pacientes tratados con bivalirudina para comparar la infusión de este fármaco tras la intervención (n = 1.799) con la ausencia de infusión tras la intervención (n = 1.811) (MATRIX-Duración del tratamiento). Sin embargo, los resultados de esta última comparación no se incluyeron en este análisis post hoc. Los objetivos principales del MATRIX-Acceso y el MATRIX-Antitrombina fueron los eventos adversos cardiovasculares mayores (MACE), definidos como la combinación de muerte por cualquier causa, infarto de miocardio o ictus a los 30 días, y los eventos adversos clínicos netos (NACE), definidos como la combinación de la revascularización arterial no coronaria, la hemorragia mayor asociada con el injerto (Bleeding Academic Research Consortium [BARC] tipo 3 o 5) o los MACE a 30 días. Se han publicado ya los resultados del ensayo a 30 días y a 1 año13-15. Tanto en el MATRIX-Acceso como en el MATRIX-Antitrombina, no se observaron diferencias en los 2 objetivos combinados principales de MACE y NACE14, excepto porque los NACE fueron significativamente menos frecuentes con el acceso radial que con el femoral. Esto se debe a una menor frecuencia de hemorragias mayores según criterios BARC y las muertes por cualquier causa13, aunque sin alcanzar la significación estadística. Aunque no hubo diferencias en los diversos objetivos secundarios de hemorragia mayor BARC y la hemorragia de cualquier grado BARC, la mortalidad por cualquier causa o de causa cardiovascular en relación con la vía de acceso vascular, sí hubo una disminución estadísticamente significativa de esos parámetros con la bivalirudina en comparación con la HNF. Sin embargo, la utilización de bivalirudina se asoció con un aumento significativo de la tasa de trombosis del stent definitiva.
Se clasificó como PV a un total de 934 pacientes del MATRIX-Acceso y el MATRIX-Antitrombina, que suponen aproximadamente el 11,1% de la población del ensayo, y se los incluyó en este análisis post hoc. Concretamente, 472 (5,5%) fueron asignados al acceso radial y 472 (5,6%) al femoral y 397 (5,5%), a bivalirudina y 422 (5,0%), a HNF. Hasta donde sabemos, esta cohorte de PV constituye la evaluación más amplia y más reciente de los resultados en función de la vía de acceso vascular y de la pauta de tratamiento antitrombótico16. Debe felicitarse a los autores por incluir en su ensayo a estos pacientes que se encuentran en un estado más crítico, puesto que ello permite obtener una perspectiva respecto al mejor tratamiento para este tipo de pacientes que a menudo son excluidos de los ECA. La inclusión de estos pacientes también pone de relieve el carácter de estudio de la práctica clínica real que tiene la experiencia del ensayo MATRIX, y muestra unas tasas de PV que reflejan las de dicha práctica clínica. A pesar de las limitaciones inherentes a los análisis post hoc similares, que los autores reconocen adecuadamente, los realizados en los PV son, de hecho, muy informativos y tienen utilidad clínica.
Tal como cabía prever, la población de PV estaba en un estado mucho más grave y tenía mayor riesgo que la población de pacientes no vulnerables. Los inhibidores de la glucoproteína IIb/IIIa, el balón de contrapulsación intraaórtico, la afección de la principal izquierda o la enfermedad multivaso y la necesidad de cirugía de revascularización aortocoronaria fueron más frecuentes en los PV. A los 30 días, los PV presentaron unas tasas significativamente superiores de casi todos los criterios de valoración isquémicos (MACE, NACE, mortalidad por cualquier causa y de causa cardiovascular, ictus, trombosis del stent, revascularización urgente del vaso diana) y hemorrágicos (hemorragias de cualquier grado y hemorragias mayores según diversas clasificaciones), en comparación con los pacientes no vulnerables. Aunque las características basales y de la intervención estuvieron generalmente bien igualadas en los subgrupos de PV y no vulnerables asignados a la vía radial o a la femoral y al tratamiento con bivalirudina o con HNF, los PV tenían una edad significativamente superior según el tipo de tratamiento antitrombótico asignado aleatoriamente y mostraban una forma de presentación con infarto agudo de miocardio con elevación del segmento ST con una frecuencia significativamente superior según la vía de acceso asignada en la aleatorización.
En este análisis, no se observaron interacciones significativas en cuanto a los objetivos principales o secundarios entre las 2 vías de acceso vascular (radial y femoral) ni en cuanto a la anticoagulación intraintervención (bivalirudina y HNF) con los criterios de PV, con la única excepción de la hemorragia BARC 3a favorable a la bivalirudina en los PV. En la cohorte de PV, en comparación con la vía de acceso vascular femoral, la vía radial conllevó una reducción significativa de las hemorragias de cualquier grado BARC (riesgo relativo [RR] = 0,64; intervalo de confianza del 95% [IC95%], 0,44-0,90) y de la hemorragia mayor BARC (RR = 0,47; IC95%, 0,24-0-95), junto con una tendencia a la reducción de los MACE (RR = 0,89; IC95%, 0,64-1,25), los NACE (RR = 0,82; IC95%, 0,59-1,13), la mortalidad por cualquier causa (RR = 0,80; IC95%, 0,51-1,25) y la mortalidad de causa cardiovascular (RR = 0,81; IC95%, 0,51-1,28). Tiene interés señalar que los beneficios aportados por el acceso radial quedaban notablemente atenuados tanto en la cohorte de PV como en la de no vulnerables cuando se incluían los centros con un porcentaje bajo o medio de ICP realizadas por vía radial. En la cohorte de PV, en comparación con la HNF, la bivalirudina implicó una reducción significativa de la hemorragia mayor BARC (RR = 0,30; IC95%, 0,13-0,63), la mortalidad por cualquier causa (RR = 0,51; IC95%, 0,31-0,84) y la mortalidad de causa cardiovascular (RR = 0,50; IC95%, 0,30-0,53), junto con una tendencia a la reducción de los MACE (RR = 0,84; IC95%, 0,59-1,19), los NACE (RR = 0,73; IC95%, 0,52-1,02) y las hemorragias de cualquier grado BARC (RR = 0,72; IC95%, 0,50-1,02). Sin embargo, la bivalirudina se asoció con un aumento del número de infartos de miocardio (RR = 1,46; IC95%, 0,88-2,41) y trombosis del stent definitivas (RR = 1,54; IC95%, 0,55-4,35) en los PV.
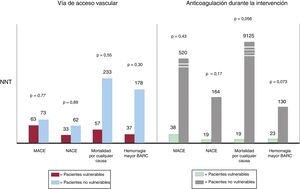
La principal limitación de este estudio es su baja potencia estadística para investigar los efectos de las estrategias de tratamiento experimentales en los PV. De hecho, aunque la cohorte de PV se encuentra, en general, entre las más grandes identificadas en un ensayo del SCA, en términos absolutos continúa siendo demasiado pequeña para que se pueda llegar a ninguna conclusión definitiva, por lo que los resultados deben considerarse generadores de hipótesis, en especial teniendo en cuenta que el análisis fue también post-hoc y que la aleatorización no se estratificó en función de que se tratara de PV o no. Además, a la vista de las diferencias antes mencionadas en las características basales y de la intervención entre los PV y los no vulnerables asignados a la vía femoral o a la radial y al tratamiento con bivalirudina o con HNF, la falta de un análisis de regresión multivariante no permite descartar la existencia de factores predictivos independientes en los resultados incluidos. A pesar de estas limitaciones y de la baja probabilidad de que se realice un ECA grande diseñado para identificar la vía de acceso vascular óptima y la mejor pauta de tratamiento antitrombótico seleccionado para los PV, se debe aprovechar lo mejor posible los datos aportados, que constituyen el conjunto más amplio, actual e indicativo de la situación de los pacientes en la práctica clínica real. Concretamente, estos resultados respaldan en general, y especialmente en manos de operadores experimentados, la elección de la arteria radial con preferencia a la femoral para la vía de acceso vascular, así como el uso de bivalirudina en vez de HNF como pauta de tratamiento antitrombótico. Las altas tasas de eventos en los PV contribuyen a un mayor impacto en la reducción del riesgo absoluto con la vía de acceso radial o con el tratamiento de bivalirudina en comparación con lo que ocurre en los pacientes no vulnerables, como pone de manifiesto el número de pacientes que es necesario tratar para los parámetros de valoración clave, incluidos los objetivos combinados principales de MACE y NACE, la mortalidad por cualquier causa y la hemorragia mayor BARC (figura 1).
Número de pacientes que es necesario tratar (NNT) según la vía de acceso vascular (radial frente a femoral) o según la anticoagulación durante la intervención (bivalirudina frente a heparina no fraccionada) en pacientes vulnerables en comparación con los no vulnerables. BARC: Bleeding Academic Research Consortium; MACE: eventos adversos cardiovasculares mayores; NACE: eventos adversos clínicos netos.
En conclusión, se dispone de muy pocos datos en el ámbito de los pacientes con un SCA que se presentan con inestabilidad hemodinámica o eléctrica y es improbable que se realicen ECA para determinar cuál es la vía de acceso óptima y la mejor anticoagulación durante la intervención para estos pacientes. Aunque parece recomendable un mayor esfuerzo por incluir a los PV en los estudios prospectivos o los estudios retrospectivos de casos y controles emparejados, este amplio análisis post-hoc de un ECA pertinente respecto a esta cuestión respalda las posibles ventajas de la arteria radial frente a la femoral para el acceso vascular, siempre y cuando el centro tenga un gran volumen de ICP por vía radial, así como el uso de bivalirudina en comparación con la HNF, que fueron uniformes en los PV y no vulnerables, con una mayor reducción del riesgo absoluto en los segundos debido a sus mayores riesgos isquémico y hemorrágico basales.
CONFLICTO DE INTERESESD.J. Angiolillo declara que ha recibido pagos por consultoría u honorarios de Abbott, Amgen, Aralez, AstraZeneca, Bayer, Biosensors, Boehringer Ingelheim, Bristol-Myers Squibb, Chiesi, Daiichi-Sankyo, Eli Lilly, Haemonetics, Janssen, Merck, PhaseBio, PLx Pharma, Pfizer, Sanofi y The Medicines Company y ha recibido pagos por su participación en actividades de revisión de CeloNova y St. Jude Medical. D.J. Angiolillo declara también que su centro ha recibido subvenciones de investigación de Amgen, AstraZeneca, Bayer, Biosensors, CeloNova, CSL Behring, Daiichi-Sankyo, Eisai, Eli Lilly, Gilead, Janssen, Matsutani Chemical Industry Co., Merck, Novartis, Osprey Medical, Renal Guard Solutions y Scott R. MacKenzie Foundation. M. Galli no tiene nada que declarar.