Este artículo presenta una revisión de las publicaciones y los estudios más relevantes en el ámbito de la cardiología intervencionista en el año 2014. Dentro del intervencionismo coronario, el tratamiento integral del síndrome coronario agudo sigue siendo objeto de múltiples estudios que evalúan diferentes dispositivos y estrategias farmacológicas y mecánicas sin incrementar el riesgo de hemorragia ni la necesidad de reintervención. Algunos sustratos anatómicos particulares siguen generando un importante número de publicaciones, tanto por los resultados de diferentes stents como por el uso de técnicas específicas. Los stents farmacoactivos bioabsorbibles se emplean en lesiones cada vez más complejas con resultados prometedores. El intervencionismo cardiaco estructural avanza en su desarrollo: nuevas evidencias con las prótesis aórticas percutáneas, resultados de la reparación mitral percutánea o seguridad y eficacia de la oclusión de la orejuela izquierda. Finalmente, la denervación renal ha generado uno de los grandes debates del año.
Palabras clave
El estudio ATLANTIC (Administration of Ticagrelor in the cath Lab or in the Ambulance for New ST elevation myocardial Infarction to open the Coronary artery), internacional, multicéntrico y aleatorizado, incluyó a 1.862 pacientes con infarto agudo de miocardio con elevación del segmento ST (IAMCEST) de menos de 6h, y comparó el tratamiento con ticagrelor prehospitalario (en la ambulancia) con el hospitalario (en la sala de hemodinámica)1–5. Los objetivos primarios fueron la resolución de la elevación del segmento ST antes de la intervención coronaria percutánea (ICP) ≥ 70% y la proporción de pacientes que no tenían flujo TIMI (Thrombolysis In Myocardial Infarction) de grado 3 en la arteria responsable del infarto. Los objetivos secundarios fueron las tasas de eventos adversos cardiovasculares mayores y trombosis de stent definitiva a los 30 días. La mediana de tiempo desde la aleatorización hasta la angiografía fue de 48min y la diferencia de tiempo medio entre las 2 estrategias de tratamiento fue de 31min. Los 2 objetivos primarios no difirieron significativamente entre el tratamiento prehospitalario e intrahospitalario. Las trombosis definitivas de stent fueron inferiores en el grupo prehospitalario que en el grupo en hospital (0,0 y 0,8% en las primeras 24h, 0,2 y 1,2% a los 30 días; p=0,02). Las tasas de hemorragia mayor fueron bajas y prácticamente idénticas en ambos grupos. La administración prehospitalaria de ticagrelor en pacientes con IAMCEST parece segura, pero no mejora la reperfusión coronaria pre-ICP.
El CVLPRIT es un ensayo prospectivo, aleatorizado, multicéntrico, en pacientes con IAMCEST6, cuyo objetivo es determinar el tratamiento óptimo de las lesiones no responsables detectadas durante la ICP primaria2,6. Se incluyó a los pacientes cuando se detectó enfermedad multivaso y se aleatorizaron a tratar solo la arteria responsable (n=146) o a revascularización completa (n=150). El objetivo principal fue el combinado de mortalidad por cualquier causa, infarto recurrente, insuficiencia cardiaca o necesidad de revascularización a los 12 meses. La revascularización completa (en el mismo procedimiento en el 59% de los pacientes y durante el ingreso en el resto) se asoció con un mejor resultado primario (el 10,0 frente al 21,3%; p=0,009).
El estudio NOMI7 evalúa la hipótesis de que el óxido nítrico inhalado puede reducir el daño miocárdico durante la reperfusión en el IAMCEST mediante ICP primaria1,7. Se incluyó a 250 pacientes (< 12h desde el comienzo de los síntomas) y se les aleatorizó a recibir oxígeno a través de mascarilla facial, con o sin óxido nítrico (a una concentración de 80 partes por millón). La administración de gas comenzó en la sala de cateterismo antes de la ICP y continuó hasta 4h después de la reperfusión. Se evaluó mediante resonancia magnética cardiaca el tamaño del infarto y el remodelado del ventrículo izquierdo, y a las 48-72h después del procedimiento no hubo diferencias en el tamaño del infarto entre los grupos con y sin óxido nítrico (el 18,0 frente al 19,4%; p=0,44).
Infarto agudo de miocardio sin elevación del segmento STEl estudio FAMOUS-NSTEMI8 comparó la reserva fraccional de flujo (RFF) con la angiografía para guiar la decisión de manejo y optimizar el pronóstico en el infarto de miocardio sin elevación del segmento ST. Se incluyó prospectivamente a 350 pacientes, aleatorizados 1:1, con ≥ 1 estenosis coronarias ≥ 30% según estimación visual en 6 hospitales de Reino Unido. El operador en el grupo guiado por RFF (n=176) conocía la RFF, que se midió pero no se comunicó al operador en el grupo guiado por angiografía (n=174). Para el objetivo principal, la proporción de pacientes tratados inicialmente con tratamiento médico fue superior en el grupo guiado por RFF que en el guiado por angiografía (el 22,7 frente al 13,2%; p=0,022). A los 12 meses, la revascularización continuó siendo más baja en el grupo guiado por RFF. No hubo diferencias en la evolución clínica y calidad de vida entre los grupos.
Acceso vascularEl estudio ISAR CLOSURE9 comparó de forma aleatorizada la hemostasia femoral manual frente a 2 dispositivos (uno intravascular y otro extravascular) en más de 4.500 pacientes tras coronariografía con un introductor de 6 Fr. El objetivo primario fue el compuesto de complicaciones vasculares de cualquier tipo en los 30 días tras el procedimiento, que se produjo en el 6,9% de los pacientes del grupo de dispositivos frente al 7,9% del grupo de compresión manual (p=no significativa). El tiempo de compresión fue significativamente menor en el grupo de dispositivos y, entre ellos, el fracaso fue menor en el dispositivo intravascular frente al extravascular (5,3 y 12,2%: p<0,001).
Enfermedad coronaria: lesiones específicasTronco izquierdoUn metanálisis que incluyó a más de 2.300 pacientes (obtenidos de ensayos aleatorizados y registros clínicos) a los que se realizó ICP electiva con stent farmacoactivo (SFA) sobre lesiones graves distales del tronco izquierdo no protegido evaluó los resultados de una estrategia de stent único frente a doble stent10. Tras un seguimiento medio de más de 32 meses, la incidencia combinada de eventos cardiacos adversos fue significativamente menor en la estrategia de stent único (el 20,4 frente al 32,8%; p<0,001), al igual que la necesidad de nueva revascularización (el 10,1 frente al 24,3%; p<0,001).
RestenosisEl estudio RIBS IV11 comparó el tratamiento con balón de paclitaxel (SeQuent® Please, B. Braun Surgical) con el SFA de everolimus (Xience PrimeTM, Abbott Vascular) en pacientes con restenosis de un SFA. Se incluyó a 309 pacientes con restenosis de un SFA, aleatorizados a ambas estrategias. Al 90% de los pacientes se le realizó seguimiento angiográfico. A los 9 meses, el grupo de SFA de everolimus tenía un diámetro luminal mínimo mayor que el grupo de balón de paclitaxel (2,03 y 1,80mm, respectivamente; p=0,004) y al año, la ausencia de reintervención fue superior en el grupo de SFA (el 96 comparado con 87%; p=0,008), así como la ausencia de eventos cardiacos mayores —combinado de muerte cardiaca, infarto y revascularización del vaso responsable— (el 90 frente al 82%; p=0,044).
Oclusiones crónicasEl estudio prospectivo CTO-IVUS12 aleatorizó a 402 pacientes con oclusión coronaria crónica a estrategia de ICP guiada por ecografía intravascular o guiada por angiografía tras el cruce con éxito de la guía. Además se aleatorizó adicionalmente a los pacientes a recibir SFA liberadores de zotarolimus o de biolimus. El objetivo primario fue el combinado de muerte cardiaca, infarto y revascularización del vaso a los 12 meses, que ocurrió menos frecuentemente en el grupo guiado por ecografía intravascular que en el guiado por angiografía (2,6 y 7,1%, respectivamente; p=0,035). La tasa de cruce entre grupos fue significativamente más alta desde el grupo de angiografía hacia el de ecografía intravascular que al contrario (17,4 y 2,5%, respectivamente; p<0,001). El análisis por protocolo mostró un objetivo primario menor en el grupo de ecografía intravascular que en el de angiografía (2,2 y 8,4%; p=0,005).
BifurcacionesEl estudio prospectivo y aleatorizado BABILON13 comparó los resultados clínicos y angiográficos del tratamiento de lesiones en bifurcación con balón de paclitaxel más stent convencional frente al implante de SFA de everolimus. El objetivo primario fue la pérdida angiográfica a los 9 meses en la rama principal, que resultó ser 0,31±0,48mm en el grupo de balón de paclitaxel y 0,16±0,38mm en el grupo de SFA (p=0,15). No hubo diferencias significativas en la rama secundaria. Sin embargo, el objetivo secundario combinado (muerte cardiaca, infarto o necesidad de revascularización) fue significativamente más alto en el grupo de balón de paclitaxel a expensas de una mayor restenosis (13,5 y 1,8%, respectivamente; p=0,027) y necesidad de nueva revascularización (15,4 y 3,6%; p=0,045).
Stents farmacoactivosEl estudio prospectivo y aleatorizado CENTURY II14 comparó la no inferioridad del SFA Ultimaster (Terumo, Tokio, Japón) con sirolimus y polímero bioabsorbible, con el SFA Xience (Abbott Vascular) con everolimus y polímero permanente. Se incluyó a más de 1.100 pacientes; para el objetivo primario (combinado de muerte cardiaca, infarto o revascularización del vaso tratado), el SFA Ultimaster fue no inferior al SFA Xience (4,36 y 5,27%; p<0,0001) a los 9 meses. El compuesto de muerte cardiaca e infarto fue del 2,9 y el 3,8%, respectivamente (p=0,40), y la necesidad de revascularización del 4,5 y 4,2% (p=0,77). La tasa de trombosis fue del 0,9% en ambos grupos.
El estudio BIOSCIENCE15 buscó comparar la seguridad y eficacia de un nuevo SFA de cromo-cobalto ultrafino (Orsiro, Biotronik), liberador de sirolimus a través de un polímero biodegradable con el SFA de everolimus (Xience, Abbott Vascular) con estructura fina y polímero de larga duración. Se incluyó a 2.119 pacientes con 3.139 lesiones asignados a stent de sirolimus (1.063 pacientes, 1.594 lesiones) o stent de everolimus (1.056 pacientes, 1.545 lesiones). En el 19% de los pacientes, el primer síntoma fue un IAMCEST. El objetivo principal (definido como fracaso en la lesión tratada) fue el compuesto de muerte cardiaca, infarto relacionado con el vaso tratado y revascularización del vaso tratado, a los 12 meses, y no hubo diferencias significativas en ambos grupos (6,5 y 6,6%; p<0,0004 para no inferioridad). Tampoco hubo diferencias en trombosis definitivas (0,9 y 0,4%; p=0,16). En el subgrupo de pacientes con IAMCEST, el SFA de sirolimus se asoció a una mejor evolución (el 3,3 frente al 8,7%; p=0,024).
Stents bioabsorbiblesEl registro GHOST-EU16 incluyó a 1.189 pacientes que han recibido 1 o más stents bioabsorbibles —bioabsorbable vascular scaffold— (Absorb BVS, Abbott Vascular). El objetivo primario fue el fracaso de la lesión, definido como el combinado de muerte cardiaca, infarto o necesidad de revascularización de la lesión. Se implantó un total de 1.731 Absorb (presión media 12,3±3,4 atmósferas), con éxito en el 99,7% de los casos. El objetivo primario ocurrió en el 4,4% de los pacientes a los 6 meses (mediana de 109 días) y la tasa anualizada del objetivo primario alcanzó el 10,1%. La diabetes mellitus fue el único predictor independiente del objetivo primario (p=0,006). La incidencia de trombosis definitiva o probable alcanzó el 2,1% a los 6 meses, con una mediana de 6,5 días.
El estudio multicéntrico y aleatorizado ABSORB II17 incluyó a 501 pacientes con 1 o 2 lesiones en arterias coronarias nativas, asignados a recibir un stent bioabsorbible (Absorb BVS, Abbott Vascular) o un SFA de everolimus (Xience, Abbott Vascular) en un diseño 2:1. La ganancia luminal aguda fue menor en el grupo de Absorb con angiografía coronaria cuantitativa (1,15 frente a 1,46mm; p<0,0001) y con ecografía intravascular (2,85 y 3,6mm2, respectivamente; p<0,0001) y resultó en un menor diámetro y área luminal tras el procedimiento. Sin embargo, al año, las tasas de angina fueron menores en el grupo de Absorb (el 22 frente al 30%; p=0,04), aunque este fue un hallazo post-hoc, pues no estaba definido previamente. El objetivo combinado al año fue similar entre ambos stents (el 4,8 frente al 3,0%; p=0,35) y el combinado global (muerte, infarto o cualquier revascularización) tampoco fue significativamente diferente (7,3 y 9,1%; p=0,47).
Intervencionismo percutáneo en enfermedad coronaria: antiagregación y anticoagulaciónEl estudio ISAR TRIPLE18,19 ha aleatorizado a 614 pacientes a recibir ácido acetilsalicílico y un antagonista de la vitamina K más de 6 semanas (n=307) o a 6 meses de clopidogrel (n=307) tras una ICP con SFA. A los 9 meses de seguimiento no hubo diferencias significativas entre ambos grupos (el 9,8 frente al 8,8%; p=0,63) con respecto al objetivo combinado primario (muerte, infarto, trombosis de stent, ictus o hemorragia TIMI mayor). Tampoco hubo diferencias significativas en el objetivo secundario de hemorragia TIMI mayor (5,3 y 4%; p=0,44).
El estudio SECURITY20 ha evaluado la no inferioridad del tratamiento antiagregante doble durante 6 o 12 meses en pacientes tratados con ICP y SFA de segunda generación. El objetivo primario fue un combinado de muerte cardiaca, infarto, ictus, trombosis de stent o hemorragias mayores a los 12 meses. Se aleatorizó a 1.399 pacientes a recibir doble antiagregación durante 6 meses (n=682) o 12 meses (n=717). El objetivo primario ocurrió en el 4,5 y el 3,7%, respectivamente (p=0,47), a los 12 meses, confirmando la hipótesis de no inferioridad. Tampoco hubo diferencias en la aparición de trombosis de stents a los 12 meses (0,3 y 0,4%; p=0,69) o a los 24 meses (0,0,1 y 0%; p=0,31).
El estudio español ESTROFA DAPT incluyó de forma prospectiva a pacientes consecutivos tratados con SFA de nueva generación y que al alta recibieron doble antiagregación durante 6 meses. Los criterios de selección de los pacientes fueron isquemia silente, angina estable, síndrome coronario agudo de bajo riesgo o síndrome coronario agudo con alto riesgo de hemorragia. Se realizó un análisis de propensión con la cohorte de pacientes del estudio ESTROFA-2 (4.354 pacientes tratados con SFA de segunda generación y al menos 12 meses de doble antiagregación), para comparar los resultados con una estrategia de 12 meses21,22. Finalmente se incluyó a 2.572 pacientes emparejados (1.286 en cada grupo) con características bien equilibradas. La incidencia de trombosis de stent definitiva tras 12 meses fue del 0,4% en el grupo de 6 meses y del 0,6% en el grupo de 12 meses (p=0,4) y la incidencia de trombosis definitiva o probable fue del 0,7 y el 1,5%, respectivamente (p=0,09).
El estudio BRIGHT23 evaluó la hipótesis de que la bivalirudina es superior a la heparina en monoterapia o a heparina más tirofibán en el objetivo compuesto de eventos isquémicos y hemorrágicos en pacientes sometidos a ICP urgente por síndrome coronario agudo. Se aleatorizó a 2.194 pacientes en los 3 grupos (1:1:1). La mayoría de ellos (89%) se presentó como IAMCEST, el acceso fue radial en casi el 80% y la perfusión de bivalirudina se continuó tras la ICP (media 234min) en el grupo correspondiente. El objetivo combinado a 30 días (eventos mayores cardiacos y cerebrovasculares y hemorragias) fue significativamente menor en el grupo de bivalirudina comparado con la monoterapia de heparina y con heparina más tirofibán (el 8,8 frente al 13,2 frente al 17,0%; p<0,001). Esto se debe, predominantemente, a la reducción de hemorragias en el grupo de bivalirudina, ya que los eventos isquémicos mayores no fueron diferentes entre los 3 grupos al año (6,7, 7,3 y 6,8%; p=0,9).
El estudio HEAT-PPCI24 aleatorizó a 1.829 pacientes con IAMCEST, a los que se realizó coronariografía urgente, en tratamiento con bivalirudina o con heparina. Se realizó ICP primaria en el 83 y el 82% de los pacientes, respectivamente. No hubo diferencias significativas en el uso de inhibidores de la glucoproteína IIb/IIIa (13 y 15%). El objetivo primario de eficacia (eventos cardiacos adversos mayores) a las 4 semanas ocurrió en el 8,7% del grupo de bivalirudina frente al 5,7% en el grupo de heparina (p=0,01), sobre todo por el incremento de trombosis de stent (3,4 frente a 0,9%, p=0,001), la mayoría de ellas agudas. El objetivo primario de seguridad (hemorragias mayores) ocurrió en el 3,5 y el 3,1%, respectivamente (p=0,59).
El estudio DAPT25 incluyó a 9.961 pacientes con implante de, al menos, un SFA que, tras 12 meses de tratamiento con ácido acetilsalicílico y una tienopiridina (clopidogrel o prasugrel), se asignaron aleatoriamente a recibir tratamiento tienopiridínico o placebo durante 18 meses adicionales. Todos los pacientes siguieron con ácido acetilsalicílico. El objetivo coprimario del estudio fue la trombosis del stent y los eventos combinados de muerte, infarto o ictus durante el periodo comprendido entre los 12 y los 30 meses. El objetivo primario de seguridad fue la hemorragia moderada o grave. Comparado con placebo, el tratamiento continuado con tienopiridinas redujo la incidencia de trombosis del stent (el 0,4 frente al 1,4%; p<0,001) y de eventos cardiovasculares y cerebrovasculares mayores (el 4,3 frente al 5,9%; p<0,001). La incidencia de infarto de miocardio fue también inferior con tratamiento tienopiridínico que con placebo (2,1 y 4,1%, respectivamente; p<0,001). La incidencia de muerte por cualquier causa fue del 2,0% en el grupo que siguió tratamiento tienopiridínico y del 1,5% en el grupo placebo (p=0,052), pero la muerte de origen cardiaco no fue diferente (0,9 y 1,0%; p=0,98). La incidencia de hemorragia moderada o grave fue mayor en el grupo con tratamiento tienopiridínico (el 2,5 frente al 1,6%; p=0,001).
Técnicas de diagnóstico intracoronarioEl estudio FAME 226 incluyó a 1.220 pacientes con enfermedad coronaria estable, en los que se evaluaron todas las estenosis angiográficas con RFF. La hipótesis era que la ICP guiada por RFF sería superior al tratamiento médico. Los pacientes con al menos una estenosis con RFF ≤ 0,80 fueron aleatorizados a ICP guiada por RFF más tratamiento médico o a tratamiento médico exclusivo. Se trató médicamente a los pacientes con RFF>0,80 en todas las lesiones y se les incluyó en un registro. El objetivo primario fue un compuesto de muerte, infarto o revascularización urgente en los 2 años posteriores a la aleatorización, y fue significativamente inferior en el grupo de ICP que en el de tratamiento médico (el 8,1 frente al 19,5%; p<0,001). Este resultado se debió a una reducción en la necesidad de revascularización urgente en el grupo de ICP (el 4,0 frente al 16,3%; p<0,001), sin diferencias significativas entre grupos en las tasas de muerte o infarto. En un análisis específico, la tasa de muerte o infarto entre los 8 días y 2 años fue menor en el grupo de ICP que en el de tratamiento médico (el 4,6 frente al 8,0%; p=0,04). Finalmente, entre los pacientes del registro, la tasa del objetivo primario a 2 años fue del 9%.
El estudio OCT-STEMI27 incluyó a 201 pacientes con IAMCEST, a los que se realizó coronariografía urgente y después se les aleatorizó a ICP primaria, guiada o no por tomografía de coherencia óptica. Tras analizar los datos de la tomografía, los pacientes de este grupo recibieron más stents, pero la tasa de eventos cardiacos adversos mayores fue similar entre ambos grupos, con una tasa baja de restenosis binaria en los 2 grupos (el 2 frente al 3%; p=no significativa) a los 9 meses.
Intervencionismo cardiaco estructuralImplante percutáneo de válvula aórticaEl estudio US CoreValve28 comparó el implante percutáneo de válvula aórtica (TAVI) utilizando una bioprótesis autoexpandible con la sustitución valvular aórtica quirúrgica en pacientes con estenosis aórtica grave y elevado riesgo operatorio (según la puntuación de la Society of Thoracic Surgeons)28. Tras aleatorizar a 795 pacientes, el objetivo principal fue la mortalidad por cualquier causa a 1 año, que resultó significativamente menor en el grupo percutáneo frente al quirúrgico (14,2 y 19,3%; p=0,04). Aunque la necesidad de marcapasos permanente fue mayor en el grupo percutáneo (el 22,3 frente al 11,3% al año; p<0,001), hubo una incidencia significativamente superior de hemorragias mayores, fracaso renal y aparición de fibrilación auricular en el grupo quirúrgico.
El estudio CHOICE29, que comparó Sapien-XT con CoreValve, es un ensayo clínico cuyo objetivo es determinar si la válvula expandible con balón se asocia a un porcentaje de éxitos superior al de la válvula autoexpandible29,30. Se aleatorizó a 241 pacientes y se alcanzó el éxito del dispositivo en el 95,9% del grupo de válvula expandible con balón y en el 77,5% del grupo de válvula autoexpandible (p<0,001) debido a una menor insuficiencia aórtica residual (el 4,1 frente al 18,3%; p<0,001) y la necesidad menos frecuente de implantar más de una válvula (el 0,8 frente al 5,8%; p=0,03) en el grupo de válvula expandible con balón. La mortalidad cardiovascular a 30 días fue similar (4,1 y 4,3%; p=no significativa), al igual que las complicaciones hemorrágicas y vasculares, pero se precisó implantar un marcapasos permanente con mayor frecuencia en el grupo de válvula autoexpandible (el 17,3 frente al 37,6%; p=0,001).
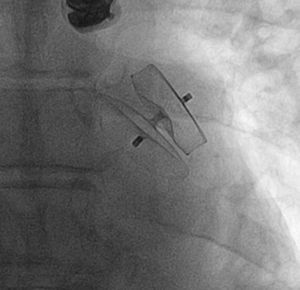
Cierre percutáneo de la orejuela izquierdaEl registro IBERIAN31 recogió de forma retrospectiva a 167 pacientes con fibrilación auricular no valvular y contraindicación para anticoagulación tratados con implante de un dispositivo en la orejuela izquierda. La edad media era de 75 años y se obtuvo éxito del procedimiento en el 95% de los pacientes (figura 1). En el seguimiento a los 2 años, el 19% sufrió algún evento, con una reducción del 75% en la incidencia de ictus frente al esperado por la escala de riesgo (el 2,4 frente al 9,6%). La mortalidad global fue del 11% y las hemorragias mayores del 6%.
Reparación mitral percutáneaEl tratamiento percutáneo de la regurgitación mitral con MitraClip® añadido al tratamiento médico se ha demostrado seguro y eficaz. Un estudio observacional retrospectivo incluyó a todos los pacientes tratados con MitraClip® en España desde noviembre de 2011 hasta julio de 2013 en los 4 hospitales españoles con mayor número de implantes32. Se incluyó a 62 pacientes, con fracción de eyección media del 36±14%, clase funcional III (37%) o IV (63%) y elevado riesgo quirúrgico (EuroSCORE, 17±11). Se implantó con éxito el dispositivo en el 98% (en el 61% un solo clip y en el 39%, 2 o más clips) (figura 2). En el seguimiento al año, el 91% de los pacientes se encontraba en clase funcional ≤ II y la insuficiencia mitral era ≤ 2 en el 81%. La mortalidad al año fue del 6,5%.
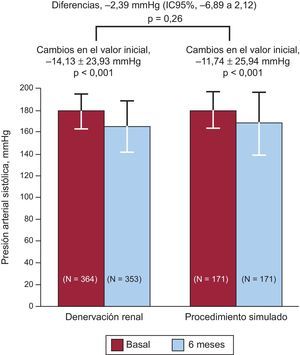
Denervación renalEl estudio SIMPLICITY HTN-333, prospectivo, aleatorizado y controlado con un procedimiento simulado, evaluó la eficacia de la denervación renal en pacientes con hipertensión arterial resistente. El criterio de valoración principal de eficacia fue el cambio en la presión arterial sistólica a los 6 meses y el secundario, el cambio en la presión arterial sistólica media ambulatoria de 24h. El objetivo primario de seguridad fue un combinado de muerte, insuficiencia renal, embolias, crisis hipertensiva o nueva estenosis de la arteria renal a los 6 meses. Se aleatorizó 2:1 a 535 pacientes y el descenso de presión arterial sistólica a los 6 meses fue de 14,1±23,9mmHg en el grupo de denervación y de 11,7±25,9mmHg en el grupo de procedimiento simulado (p<0,001 para ambos respecto a la basal, y p=0,26 para la superioridad de la denervación) (figura 3). El cambio en la presión arterial sistólica media ambulatoria de 24h fue de 6,8±15,1mmHg en el grupo de denervación y de 4,8±17,3mmHg en el grupo de procedimiento simulado (p=0,98 para la superioridad). No hubo diferencias significativas en la seguridad entre los 2 grupos.
Resultados del objetivo primario (reducción de la presión arterial sistólica media a los 6 meses) en el estudio SYMPLICITY HTN-3, que compara denervación renal frente a procedimiento simulado. IC95%: intervalo de confianza del 95%. Reproducido con permiso de Bhatt et al.33.
El tratamiento de los ancianos con síndrome coronario agudo los convierte en una población de elevado riesgo, por la dificultad para predecir su riesgo de hemorragia y por el impacto que la fragilidad y el estado funcional pueden tener en el pronóstico34,35. El registro sueco SCAAR36 confirma la seguridad y la eficacia de la ICP primaria en mayores de 80 años y demuestra que los pacientes que sobreviven a la fase temprana postinfarto tienen un pronóstico incluso ligeramente mejor que la población general. Los avances en el tratamiento médico y el aumento en el uso del abordaje radial, posiblemente contribuyan a esta mejoría de los resultados. En lo que respecta al tratamiento del infarto de miocardio sin elevación del segmento ST, la aportación de Angeli et al37 demuestra que los ancianos, a los que con más frecuencia se trata de forma conservadora o con estrategia invasiva selectiva, se benefician incluso más que los pacientes de menor edad de un manejo invasivo precoz.
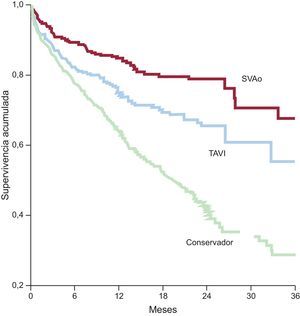
Estenosis aórticaEl registro PEGASO38 ha mostrado que, aunque a la mayoría de octogenarios con estenosis aórtica grave sintomática se les trata de forma conservadora en España, su supervivencia aumenta si se realiza una intervención, ya sea percutánea o quirúrgica (figura 4). Los resultados del estudio US CoreValve28, realizado en una población con una media de edad de 83 años, sugieren que el implante de TAVI se asocia incluso con una mejoría de la supervivencia respecto a la sustitución valvular aórtica quirúrgica. Es importante señalar que esta mejoría fue similar en los pacientes mayores y menores de 85 años. Esto quiere decir que, aunque la tasa de algunas complicaciones post-TAVI, como las vasculares o los trastornos de conducción, sean más frecuentes en ancianos, la TAVI va camino de convertirse, si no lo es ya, en el tratamiento de elección para octogenarios con estenosis aórtica grave sintomática39,40.
Supervivencia acumulada en el registro Pronóstico de la Estenosis Grave Aórtica Sintomática del Octogenario. SVAo: sustitución valvular aórtica; TAVI: implante percutáneo de válvula aórtica. Adaptado con permiso de Martínez-Sellés et al38.
Por otro lado, es clave que en todo octogenario en que se plantee la implantación de una TAVI se realice una valoración geriátrica integral, ya que varios índices sencillos de dependencia o fragilidad han demostrado su utilidad pronóstica en estos pacientes. Actualmente está en marcha un registro europeo que precisamente trata de valorar la utilidad de varios de estos parámetros en la predicción del pronóstico post-TAVI41. La idea es cambiar el actual concepto de heart team a uno de patient team que no solo valore las características cardiovasculares, sino que permita una evaluación integral del paciente.
CONFLICTO DE INTERESESNinguno.