Palabras clave
INTRODUCCIÓN
El campo de la cardiología pediátrica y las cardiopatías congénitas (CC) está en continuo progreso no sólo en aspectos clínicos, sino también terapéuticos, con nuevos tratamientos como las intervenciones percutáneas y la cirugía cardiaca, en creciente expansión. Ya no hablamos de cardiología pediátrica porque no sólo afecta al niño, abarca al paciente afecto de cardiopatía congénita que incluye al feto, el niño y el adulto, por lo que es una entidad multidisciplinaria. Cada vez más profesionales se ven involucrados, y se precisa mayor implicación entre obstetras, pediatras, cardiólogos pediátricos y cardiólogos de adultos, entre otros.
Es imposible tratar todos los temas que incluye esta disciplina, por lo que esta actualización se centra en algunos campos e intenta resaltar las publicaciones más interesantes desde septiembre de 2009 a agosto de 2010.
TÉCNICAS DE IMAGEN
El diagnóstico en cardiología pediátrica y de las CC ha avanzado espectacularmente en los últimos años, sobre todo conforme han ido progresando los avances en las nuevas técnicas de imagen.
Ecocardiografía fetal
En el diagnóstico de las CC en vida fetal, la ecocardiografía ha avanzado espectacularmente y permite, con la ecocardiografía fetal precoz, detectar las anomalías cardiacas antes de la semana 16 de gestación. En el primer trimestre, la traslucencia nucal aumentada, el flujo anormal del ductus venoso y la arteria umbilical única eran los únicos datos de cardiopatías; ahora siguen siendo una señal de alerta, pero no siempre de CC. La visión de un plano de cuatro cámaras correcto en las semanas 11-13 mejora el cribado de cardiopatía1-3. Sin embargo, la sospecha de CC recae todavía en los obstetras, por lo que un entrenamiento adecuado aumenta el diagnóstico. Así, McBrien et al4 publican un aumento del 28 al 43% de diagnóstico de CC al año tras un curso de formación específico.
Para la monitorización del crecimiento de las estructuras cardiacas fetales, Lee et al5 han realizado un estudio mediante z-score de referencia en una población de 2.735 fetos, interesante para el seguimiento en las asimetrías de cavidades o de vasos. Los autores aportan su propio calculador de z-score online, disponible en la web www. obsono.org.
La ecocardiografía tridimensional (eco-3D) fetal a tiempo real (4D) también se aplica para afinar en el diagnóstico de cardiopatías complejas y puede aportar datos anatómicos mejores que la 2D en la interrupción del arco aórtico6 o en el truncus arterioso7.
Ecocardiografía
La ecocardiografía sigue siendo la referencia para el diagnóstico morfológico y funcional8. Inicialmente, el diagnóstico morfológico de las anomalías estructurales era la base de las CC. Sin embargo, en los últimos años, el estudio de la función de los corazones estructuralmente diferentes del normal es cada vez más importante. Dentro del estudio ecocardiográfico normal en el niño, la inclusión del estudio por Doppler tisular se ha convertido en una parte importante del estudio. La Sociedad Americana de Ecocardiografía (López et al9) ha publicado uno de los artículos más interesantes de este año, las guías para la realización correcta de las mediciones de todas las estructuras cardiacas pediátricas.
Las nuevas aplicaciones del estudio funcional cardiaco (la deformación del corazón o strain) en 2D o speckle-tracking son técnicas en desarrollo10. El interés suscitado por el papel del ventrículo derecho (VD) en la circulación normal y su importancia también en el seguimiento de las cardiopatías en los adultos11 ha hecho que estas nuevas técnicas diagnósticas se apliquen para su estudio funcional y en la evolución postoperatoria (sobre todo tras cirugía de Fallot12), así como para el estudio del ventrículo único13. Sin embargo, uno de los principales problemas de estas técnicas es la variabilidad elevada entre las diferentes marcas de ecógrafos, que impide la homogeneidad de los resultados y su aplicación práctica generalizada y real14,15.
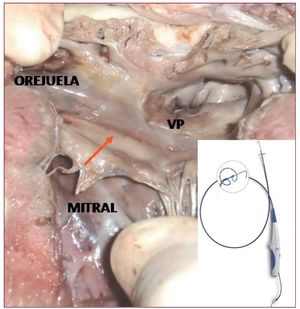
La eco-3D tiene cada vez más importancia en la visualización de las estructuras cardiacas (fig. 1), sobre todo en la valoración de las válvulas auriculoventriculares16. Se emplea, además, para el estudio funcional cardiaco. Van de Zwaan et al17 publican la utilidad de la eco-3D para el seguimiento y la determinación de la función del VD en CC. Comparada con la resonancia magnética (RMC), la eco-3D tiene una sensibilidad del 95%, una especificidad del 89% y un valor predictivo negativo del 99% para el diagnóstico de disfunción del VD con valores telediastólicos > 105 ml/m2, telesistólicos > 54 ml/m2 y fracción de eyección < 43%.
Figura 1. Imagen de ecocardiografía tridimensional transesofágica en paciente con comunicación interauricular multiperforada. AO: aorta; VCI: vena cava inferior; VCS: vena cava superior.
Hay cada vez más comunicaciones sobre la utilidad de la eco-3D transesofágica en las reparaciones quirúrgicas y en el intervencionismo cardiaco de las CC18-20.
Tomografía computarizada cardiaca (cardio-TC) y RMC en cardiopatías congénitas
La cardio-TC, a pesar de la exposición a radiación que implica, cada vez se emplea más como estudio complementario a la ecocardiografía en CC, por su alta resolución espacial, porque no requiere sedación y por su rapidez en el diagnóstico de CC complejas, sobre todo para la visualización completa de los grandes vasos y las ramas pulmonares distales21. Sin embargo, en la valoración funcional cardiaca, en múltiples cardiopatías y en la valoración del ventrículo único y del VD, la RMC sigue siendo la técnica de referencia22.
HIPERTENSIÓN ARTERIAL PULMONAR EN PEDIATRÍA
En el último año se han publicado documentos muy relevantes en el campo de la hipertensión arterial pulmonar (HAP): las nuevas guías clínicas americanas23 sobre el diagnóstico y manejo de la HAP en los adultos, incluida la actualización de la clasificación (Dana Point), las guías europeas24 (publicadas en español en REVISTA ESPAÑOLA DE CARDIOLOGÍA25), así como revisiones y puestas al día sobre los mecanismos celulares y moleculares implicados en la patogenia de la enfermedad26, la importancia de la función ventricular derecha en su evolución y su pronóstico27 o las nuevas terapias en experimentación28. Asimismo, REVISTA ESPAÑOLA DE CARDIOLOGÍA ha publicado durante 2010 excelentes revisiones sobre el tema29-34. Pero como las propias guías americanas23 reconocen, carecemos de clasificaciones, documentos de consenso y protocolos diagnósticos y terapéuticos específicos para la HAP pediátrica, a la que se aplican por defecto los protocolos creados para la enfermedad del adulto.
Sin embargo, en los últimos años, y muy especialmente durante 2009 y 2010, ha comenzado la publicación de trabajos y series sobre HAP pediátrica que han puesto de manifiesto que el espectro de la HAP en el niño es mucho más complejo y heterogéneo que en el adulto. La forma más frecuente de HAP en el niño es la asociada a cardiopatía congénita (tanto reparada como no reparada), que supone más del 50% de todas las series. También se pone de manifiesto la relativa frecuencia de etiologías multifactoriales34 y la frecuente asociación de síndromes polimalformativos o cromosomopatías en los enfermos pediátricos con HAP.
Asimismo, y a falta de una clasificación especifica de la HAP pediátrica, se han publicado propuestas para la mejora de la clasificación de la HAP asociada a la cardiopatía congénita35 que ilustran claramente la complejidad y la variedad de cuadros clínicos (con muy distintos pronósticos y manejos) englobados dentro de la llamada «HAP asociada a cardiopatía congénita».
También se han publicado interesantes revisiones sobre el diagnóstico36-38 (incidiendo en la necesidad de equipos multidisciplinarios para el estudio de estos pacientes), sobre los valores normales para el test de los 6 min de marcha en niños, y marcadores biológicos, como el ácido úrico o el BNP39, que han facilitado la estratificación del riesgo de los pacientes pediátricos con HAP.
Sobre las peculiaridades del cateterismo en la HAP pediátrica, se han publicado recomendaciones especiales para reducir el riesgo de la anestesia en estos niños40, así como series pediátricas que analizan el riesgo y la influencia de la anestesia general en los resultados de las determinaciones de presiones y resistencias pulmonares41 o la eficacia en el test de vasorreactividad de distintos fármacos, como el óxido nítrico42, el sildenafilo43 o el iloprost44. Destaca la excelente revisión publicada por Giglia et al45 sobre las cifras de resistencias pulmonares que pueden contraindicar la cirugía cardiaca, tanto en el cierre de defectos septales como en las cardiopatías subsidiarias de corrección univentricular o en los candidatos a trasplante cardiaco.
También se ha avanzado mucho en el conocimiento de la epidemiología, la evolución y la respuesta al tratamiento de entidades específicas dentro de la HAP pediátrica, como la información aportada por el registro británico sobre la HAP idiopática en niños46, la HAP asociada a causas distintas de la CC47, la asociada a enfermedad del corazón izquierdo48, la HAP neonatal49, la HAP en la displasia broncopulmonar50-52 o la hernia diafragmática congénita53. También se describen casos de HAP en pacientes con D-trasposición de grandes arterias corregida precozmente54, de patogenia aún poco clara. Respecto al tratamiento, se han publicado revisiones tanto sobre el tratamiento de la HAP aguda (en las unidades de cuidados intensivos55-58) como sobre la HAP crónica58. También se ha profundizado en el conocimiento de la farmacocinética en niños de algunos de los fármacos más empleados, como el bosentán (en el estudio FUTURE-159 se describen las dosis idóneas en niños, así como la seguridad de la nueva presentación pediátrica) o el sildenafilo43, y se han publicado series sobre el uso crónico en niños del epoprostenol intravenoso o el iloprost inhalado60. Otro de los aspectos más novedosos es la publicación sobre el efecto de los nuevos vasodilatadores pulmonares en pacientes con fisiología univentricular, tanto en el postoperatorio inmediato de Glenn o Fontan61 como en el Fontan fallido62, aunque se trata aún de estudios no controlados y con escaso número de pacientes.
CARDIOLOGÍA INTERVENCIONISTA
El tratamiento mediante cateterismo de los defectos cardiacos congénitos y estructurales ha experimentando un desarrollo espectacular en las últimas tres décadas. El cateterismo terapéutico constituye en la actualidad la primera opción terapéutica para muchas de estas enfermedades y una opción de relevancia en combinación con la cirugía en otras63. Aunque se han publicado estudios multicéntricos que analizaban y comparaban los resultados de los primeros procedimientos de dilatación u oclusión, estos son obsoletos o han tenido un alcance limitado. Con el ánimo de racionalizar el análisis de los datos, conocer los resultados inmediatos y de su seguimiento, unificar los documentos de consenso elaborados por los expertos y mejorar la calidad de los procedimientos de intervencionismo, se han creado varios proyectos de bases de datos: el IMPACT Registry (Improving Pediatric and Adult Congenital Treatments) del National Cardiovascular Data Registry de la American College of Cardiology Foundation y la Society for Cardiovascular Angiography and Interventions (SCAI), el Mid-Atlantic Group of Interventional Cardiology (MAGIC), el Congenital Cardiac Catheterization Project on Outcomes (C3PO), el Congenital Cardiovascular Interventional Study Consortium (CCISC) y el Joint Council on Congenital Heart Disease (JCCHD) National Quality Improvement Initiative64,65. Estas bases de datos proveerán en los próximos años los datos para la realización de estudios multicéntricos y de colaboración, lo que demuestra el gran progreso en este campo en los últimos años en conseguir una mejora de la calidad y la coherencia de la información sobre los procedimientos terapéuticos no quirúrgicos en los defectos cardiacos congénitos.
Se ha evaluado en varias publicaciones la seguridad y la eficacia en el cierre percutáneo de la comunicación interauricular ostium secundum de un nuevo dispositivo (bioSTAR, NMT Medical)66. Se trata de un dispositivo biodegradable que aporta un nuevo concepto en los oclusores: tras el implante, se produce la reabsorción progresiva del dispositivo y se mantiene la oclusión completa del defecto. Morgan et al67 publican la primera experiencia en niños, con unos resultados similares a los de otros dispositivos (Amplatzer Septal Occluder) para el cierre de comunicación interauricular (CIA) de tamaño < 16 mm.
Se ha generalizado el uso de los dispositivos de segunda generación de Amplatzer para el cierre del ductus (ADO II). El menor perfil del catéter de liberación y sus discos de retención simétricos puede ofrecer ciertos beneficios clínicos adicionales comparado con otros dispositivos. El dispositivo se puede liberar desde ambos accesos, venoso o arterial, se puede utilizar en ductus de menor tamaño y en pacientes más pequeños, y es especialmente útil en ductus de forma tubular. Queda por determinar en nuevos estudios la anatomía ductal a la que se adapta mejor cada dispositivo y la mejor estrategia técnica68-70.
En los últimos años han cobrado especial relevancia procedimientos que precisan de la estrecha colaboración entre el cirujano cardiovascular y el cardiólogo intervencionista para el implante de dispositivos o la realización de angioplastias (procedimientos híbridos). Este tipo de actuaciones terapéuticas puede realizarse en quirófano o en el laboratorio de hemodinámica, de forma combinada o secuencial. En un estudio multicéntrico prospectivo con datos de siete centros de Estados Unidos, se evaluó la frecuencia de eventos adversos en relación con las características de los procedimientos. Se realizaron 128 procedimientos desde febrero de 2007 a diciembre de 2008: implante de stent ductal (n = 55), rehabilitación vascular (n = 25), cierre periventricular de comunicación interventricular (CIV) con dispositivo (n = 7), valvulotomía (n = 3) y procedimientos diagnósticos híbridos (n = 38). La frecuencia de eventos adversos fue de 16 de los 128 procedimientos, de los que sólo 2 fueron mayores/fatales71.
En el síndrome de hipoplasia de las cavidades izquierdas (SHCI) cobra especial interés el enfoque híbrido. Venugopal et al72 analizan sus resultados en 21 neonatos con esta entidad o sus variantes (5 de los neonatos presentaban estenosis aórticas críticas con ventrículos izquierdos borderline o con función sistólica pobre). La técnica consistía en realizar un banding quirúrgico de ambas arterias pulmonares y el implante de un stent en el ductus; 4 neonatos nacieron con el septo interauricular prácticamente íntegro; hubo 6 muertes en el postoperatorio tras la paliación I (< 30 días) y otro antes del estadio combinado I-II de Norwood. De los 12 que accedieron a la siguiente intervención, a 9 se les practicó la intervención del estadio combinado I-II y a 3, corrección biventricular. De estos 12, 2 fallecieron tras la intervención del estadio combinado I-II. Los autores concluyen que el enfoque híbrido es una alternativa válida en el manejo de neonatos con alto riesgo (bajo peso < 2,5 kg, atresia aórtica, septo interauricular integro o restrictivo, presencia de anomalías cardiacas asociadas, prematuridad, alteraciones extracardiacas genéticas graves y colapso posnatal con pH < 7) con síndrome de hipoplasia de cavidades izquierdas (SHCI) o sus variantes.
Honjo et al73 publican el seguimiento clínico de 58 pacientes sometidos a paliación univentricular usando estrategias híbridas (n = 19) o paliación tipo Norwood I con shunt tipo Blalock-Taussig. En la evaluación previa al estadio II, no hubo diferencias significativas en la presión telediastólica ni en la presión media en arteria pulmonar, con tendencia a menor mezcla venosa en los Norwood y mayor índice de Nakata en los híbridos. Se trasplantó a 4 pacientes del grupo Norwood antes del estadio II; 42 pacientes se sometieron a paliación estadio II o estadio II del procedimiento híbrido. La paliación híbrida no tuvo un efecto significativamente adverso en el desarrollo de las arterias pulmonares, que mostraban desarrollo y hemodinámica similares. Los autores concluyen que la estrategia de paliación híbrida en el SHCI constituye una clara alternativa al Norwood I. Una ventaja, intuitiva pero probada, de esta estrategia es que evita el bypass cardiopulmonar y la reconstrucción del arco en el periodo neonatal, y se difiere hasta el estadio II a los 4-6 meses. Hay pacientes para los que este enfoque híbrido no es aceptable, particularmente aquellos con estenosis del arco preductal, ya que se puede producir isquemia coronaria tras el implante del stent ductal.
Se han utilizado procedimientos híbridos en otras situaciones, como en el cierre preauricular de defectos interauriculares ostium secundum en pacientes en elevado riesgo74, el cierre periventricular de defectos interventriculares de difícil acceso al cirujano o en pacientes muy pequeños o con riesgo75,76 y también en la rehabilitación de arterias pulmonares77 o el rescate de válvulas percutáneas tras un implante fallido78, entre otras situaciones.
CIRUGÍA DE CARDIOPATÍAS CONGÉNITAS
Dada la extensión que ocuparía abordar todos los temas novedosos en el último año de una especialidad pujante como es la cirugía de las CC, resaltaremos una serie de temas elegidos de manera subjetiva, dejando muchos interesantes sin comentar. Además de los artículos relevantes del último año de Journal of Thoracic Cardiovascular Surgery, European Journal of Cardiothoracic Surgery y Annals of Thoracic Surgery, entre otras, se realizó un examen de los tópicos principales en congresos, revisiones, investigación y nuevas guías de práctica clínica. En último lugar, es importante reseñar la publicación de la última Conferencia de Consenso en Toronto sobre el manejo de la Cardiopatía Congénita del Adulto79, disponible en www.cachnet.org, y una puesta al día de temas y controversias entre las que destaca el estado actual de la asistencia circulatoria pediátrica en nuestro país.
Bases de datos, riesgos y registros
Actualmente está claro que son necesarias, pero ¿cómo organizarlas? Es interesante el artículo de revisión multicéntrico de Jacobs et al80 donde se plantea la necesidad de una base de datos mundial. La respuesta es sí y no. Sí se necesita, pero lo lógico es tener una plataforma que permita la unificación de las existentes.
De otra manera, pero igualmente significativa, es la magnitud de la diferencia entre datos de patología que recogen estas herramientas y lo que en realidad sucede con los pacientes. En la revisión de Karamlou et al81, con todas las limitaciones que pueda tener, se desprende que actualmente no se trata a más del 50% de los niños que nacen con SHCI en Estados Unidos y, sin embargo, este hecho se ha debatido poco en nuestro medio. En la discusión de este artículo se cita una frase impactante: «In 1977, the late great Helen Taussig shocked an audience at the Los Angeles Heart Association when somebody asked her about the future of congenital heart disease. She responded amniocentesis and abortion». ¿Estamos hoy en el futuro?
Y en cuanto a riesgos, conviene revisar la nueva y moderna estratificación en 148 procedimientos de O'Brien et al82, que comparan los resultados con escalas previas, como Aristóteles y RACHS-1.
Por último, Karamlou et al83 realizan una revisión sobre el riesgo quirúrgico en cuatro grupos específicos de enfermedad neonatal83: Norwood, transposición, atresia pulmonar con septo íntegro e interrupción de arco aórtico. El artículo concluye que los resultados dependen más del paciente o de factores de manejo que de la experiencia del equipo quirúrgico.
Controversias
¿Conducto VD-AP (Sano) o fístula BT (FBT) en el procedimiento de Norwood?
Como alternativa a la técnica original de Norwood descrita en 1981 para garantizar una fuente estable de flujo pulmonar, se ha pasado a la técnica descrita por Sano en 2001. Dicha novedad ha demostrado buenos resultados en equipos quirúrgicos más modestos, debido a su menor complejidad de manejo postoperatorio. La cuestión es si existe alguna diferencia en la evolución de los pacientes. Ballweg et al84 recogen 176 casos retrospectivos no aleatorizados en Filadelfia y concluyen que la técnica de Sano lleva a mayor disfunción ventricular y mayor regurgitación valvular auriculoventricular. La supervivencia es similar y en el análisis de regresión logística, el tipo de conducto no es factor de riesgo de muerte o trasplante cardiaco. Sí lo son el bajo peso y la asociación a otras anomalías. Hay que notar que en el grupo con FBT hay un 15% de ventrículos únicos izquierdos (factor protector en el análisis de regresión) contra 0 en el de Sano, y que hay un 89% de VI hipoplásicos en el de Sano contra el 58% en el grupo FBT.
Graham et al85 recogen 76 SCHI sin aleatorizar y observan menor mortalidad inicial en el de Sano, pero mayor tendencia a disfunción ventricular y trasplante tardío. Con ello se iguala la supervivencia final. Y finalmente Raja et al86, en una revisión de siete series, concluyen que no está clara la disfunción ventricular asociada al Sano. Habrá que esperar los resultados de estudios aleatorizados ya diseñados.
Barron et al87 estudian la posición del conducto en el Sano, derecho o izquierdo, y concluyen que probablemente sobreviven más los que lo colocan por la derecha, aunque tampoco es un estudio aleatorizado.
NIRS (Near Infrared Spectroscopy): ¿necesidad o prudencia?
Uno de los objetivos de la medicina intensiva perioperatoria siempre ha sido conseguir información por métodos poco invasivos. En este sentido, el síndrome de bajo gasto cardiaco, que se da en 1/4 de pacientes operados de CC, es una entidad de difícil diagnóstico que supone un reto terapéutico. La oximetría medida por luz infrarroja supone una determinación cada día más conocida y refinada para estimar el gasto cardiaco. De esta manera surge la controversia de si debemos realmente contar con esta determinación como estándar o todavía debemos esperar.
Tweddell et al88 opinan que es necesaria, ya que es muy difícil estimar el gasto en circulaciones en serie (cardiopatía univentricular) incluso con los procedimientos invasivos actuales. La relación entre oximetría somática y cerebral está consiguiendo niveles de ajuste de riesgos muy significativos. Por otro lado, podría evitar la monitorización invasiva con catéteres y su riesgo de trombosis, todo ello con un nivel de evidencia de al menos B, cuando más del 50% de los estándares de manejo tienen una evidencia de nivel C.
Hirsch et al89, tras una revisión de la literatura publicada, apuntan que todavía falta evidencia científica que lo defina claramente como estándar.
Cirugía tipo Fontan
Uno de los aspectos más debatidos acerca de este tipo de paliación es si se debe fenestrar o no. De hecho, ha sido tema de debate en el último congreso nacional de la especialidad (Toledo, 2010). Son interesantes dos artículos que reflejan los pros y los contras de mantener la estrategia de la fenestración sistemática o, por el contrario, usarla sólo en casos elegidos.
Bradley et al90 defienden la estrategia sistemática basándose fundamentalmente en la disminución del tiempo de estancia hospitalaria, motivada por el mayor tiempo con drenaje torácico. Dan poca importancia a la cianosis, por ser ligera (90-92%), y al riesgo de embolia paradójica, porque es pequeño. Mencionan asimismo que predecir preoperatoriamente qué Fontan necesitará fenestración no es fácil y que incluso estrategias más modernas como el Fontan off-pump no han resultado en una mejora de los tiempos de drenaje y estancia.
Por el contrario, otros autores91 prefieren utilizarla sólo en casos muy seleccionados, con resultados muy buenos, y evitar así los riesgos que supone un cortocircuito crónico o los dispositivos en lechos de baja velocidad sanguínea.
Una controversia más personal es considerar si realmente es beneficioso instaurar una circulación tipo Fontan en un estadio II, en los casos de alto riesgo. Claro está, y muy bien descrito por Rychik92 en una excelente revisión del Fontan en los últimos 40 años, que esta circulación fisiológicamente es deficitaria. En palabras textuales, este autor concluye: «Innovaciones técnicas quirúrgicas de la cirugía de Fontan pueden mejorar los resultados a corto plazo y quizá reduzcan ligeramente la morbilidad tardía, pero no cambiarán de manera fundamental la fisiopatología inherente. Es hora de admitir que la operación de Fontan es una medida temporal». Actualmente están en marcha ensayos importantes, como el SAFO (Sildenafil After Fontan Operation). Como meta futura, ese autor comenta que, después de 50 años del primer Fontan, se necesita un sistema de asistencia circulatoria derecha de apoyo en este tipo de cardiopatía, afirmación que suscribimos. Nuestros pacientes están esperando...
Ya se investigan posibles innovaciones de aspecto futurista, que pueden ser más sencillas de lo esperado, como demuestra el estudio experimental con bombas de tipo rotacional93.
De cualquier manera, Jonas94 describe las situaciones en que no es necesario obstinarse en mantener una fisiología biventricular, pasando por múltiples cirugías y estados de insuficiencia cardiaca, y optar por un «buen» Fontan.
Tópicos
Reemplazo valvular pulmonar
Es necesario prestar más atención a los pacientes operados de Fallot en la infancia cuando llegan a edades adultas. Adamson et al95 revisan el reemplazo valvular pulmonar (RVP) en 730 artículos y seleccionan 19 de ellos como mejor evidencia científica. Concluyen que, efectivamente, estos pacientes mejoran clínicamente y mejora su función ventricular derecha, y ello con baja morbimortalidad.
El grupo holandés96, pionero en este tema, repasa en su revisión sobre las oportunidades en el RVP, tipos de prótesis, tipos de accesos, resultados clínicos y pruebas de imagen, para finalmente centrarse en la cuestión controvertida del momento óptimo para realizar algún tratamiento.
Antifibrinolíticos en cirugía cardiaca pediátrica
Desde 2007, los equipos quirúrgicos pediátricos hemos trabajado sin la posibilidad de usar aprotinina, ya que se retiró del mercado por sus posibles efectos perniciosos. La argumentación se basó exclusivamente en resultados publicados en cirugía de adultos, en particular coronaria, pero nunca se demostraron efectos secundarios significativos en niños. De esta manera, Pasquali et al97 revisan un total de 30.372 pacientes de 35 instituciones para concluir que este efecto sobre la mortalidad y el fallo renal no existe en niños, e incluso puede haber un efecto beneficioso, sobre todo en las reoperaciones, en forma de menor estancia hospitalaria.
Sin embargo, todos los equipos quirúrgicos consideran el uso de ácido tranexámico, a pesar de que no existen estudios tan minuciosos sobre la dosificación y los efectos secundarios. Ngaage et al98 revisan este tema en cirugía de adulto nuevamente, y concluyen que, efectivamente, el tranexámico funciona como antifibrinolítico, aunque de menor efectividad que la aprotinina, sin efectos en la mortalidad pero con una inquietante tendencia a producir más alteraciones neurológicas.
La controversia está servida: hemos defenestrado la aprotinina cuando en niños funcionaba mejor que otros antifibrinolíticos y sin demostrar efectos deletéreos y hemos asumido el tranexámico, con menos información.
Asistencia ventricular en España
Es hora de comentar nuestra experiencia en este campo de actuación emergente. En los últimos 5 años se han implantado 20 dispositivos en nuestro país y los resultados han sido esperanzadores. De hecho, 15 dispositivos se han implantado en los últimos 2 años, se ha trasplantado a 9 pacientes y con 2 todavía en soporte. Esto implica una supervivencia mayor del 70% en nuestro país en este periodo, comparable con series internacionales con mayor experiencia. Hay que recordar que la supervivencia del grupo pionero alemán en los primeros 15 años de implante en esta población joven era alrededor del 62%. En revisiones más recientes, como la de Imamura et al en 200999 que comparan esta terapia con ECMO, la supervivencia ya llega a cifras del 86%. No obstante, hay que constatar que en pacientes pequeños, de menos de 10 kg100, esta terapia todavía es un reto, con supervivencias que rondan un 50-60%.
Procedimiento de Ross
Por último, citaremos una revisión del año 2010 de la serie combinada de procedimientos de Ross en Alemania y Países Bajos101, países con gran actividad en este registro, que nos han ido ofreciendo sus conclusiones estos últimos años. En esta revisión, los autores llaman la atención sobre un problema que surge pasada la primera década tras el procedimiento. Así como la tasa de reintervención en el homoinjerto está más categorizada y sus causas se conocen mejor, la incidencia de reintervenciones por fallo del autoinjerto aumentará tras esta primera década. Esto es lo que nos tocará en España en los próximos años, y como primera estrategia para controlar este «efecto», dichos grupos ya proponen actitudes estandarizadas de fijación del complejo anillo/unión sinotubular en la cirugía inicial, o incluso el uso de la técnica inicial de implante subcoronariano, todo ello, por supuesto, en los niños más desarrollados o adolescentes.
CONFLICTO DE INTERESES
Los autores declaran no tener ningún conflicto de intereses.
Abreviaturas
cardio-TC: tomografía computarizada cardiaca.
CC: cardiopatías congénitas.
ECMO: oxigenación con membrana extracorpórea.
eco-3D: ecocardiografía tridimensional.
FBT: fístula sistemicopulmonar de Blalock-Taussig.
HAP: hipertensión arterial pulmonar.
RMC: resonancia magnética cardiaca.
RVP: reemplazo valvular pulmonar.
SHCI: síndrome de hipoplasia de cavidades izquierdas.
VD: ventrículo derecho.
VI: ventrículo izquierdo.
*Autor para correspondencia:
Córcega, 203-205, 08036 Barcelona, España.
Correo electrónico:dcalbert@vhebron.net (D.C. Albert).