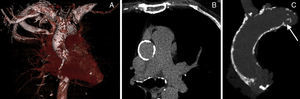
La calcificación de la aorta torácica se asocia a la calcificación coronaria y valvular y a un aumento del riesgo de eventos cardiovasculares y cerebrovasculares1. La aorta de porcelana es una calcificación excesiva de la aorta ascendente torácica (figura), un sustrato que plantea dificultades a los cirujanos cardiacos, ya que el pinzamiento aórtico y la aortotomía pueden causar una lesión aórtica excesiva o la liberación de material tromboembólico que podría producir un ictus periintervención2. La sustitución de la válvula aórtica de pacientes con aorta de porcelana puede exigir técnicas quirúrgicas avanzadas, como la sustitución de la aorta ascendente, en parada circulatoria hipotérmica profunda, la endarterectomía o el pinzamiento endovascular asistido con balón para minimizar la manipulación de la aorta intensamente calcificada.
El conducto apicoaórtico es una técnica empleada como bypass de una aorta torácica ascendente excesivamente calcificada, pero puede verse dificultada por una insuficiencia aórtica simultánea y por unas calcificaciones más generalizadas que compliquen la anastomosis distal del conducto3. El implante percutáneo de válvula aórtica (TAVI) es una alternativa muy atractiva para tratar «sin contacto» a los pacientes con estenosis aórtica grave y aorta de porcelana. La introducción del TAVI ha revolucionado el tratamiento de la estenosis aórtica en los pacientes con un riesgo (muy) alto de mortalidad operatoria. Para los pacientes realmente inoperables, el TAVI es la única opción de tratamiento que prolonga la vida, con una sorprendente reducción absoluta del 25% en la mortalidad a 2 años respecto al tratamiento médico y la valvuloplastia con balón4. A la vista de los datos favorables de las cohortes A y B del estudio PARTNER (Placement of Aortic Transcatheter Valves), las guías recientemente actualizadas de la Sociedad Europea de Cardiología y la European Association for Cardio-Thoracic Surgery para el tratamiento de las valvulopatías cardiacas recomiendan claramente el TAVI como la opción de tratamiento de elección para pacientes con estenosis aórtica inoperable cuya esperanza de vida sea aceptable, e indican que el TAVI es una alternativa razonable para la sustitución quirúrgica de la válvula aórtica en pacientes con estenosis aórtica con elevado riesgo operatorio5,6. Con la ampliación del arsenal terapéutico, resulta esencial una estratificación meticulosa del riesgo para elegir la mejor modalidad de tratamiento para cada paciente con estenosis aórtica. La Society of Thoracic Surgeons y el EuroSCORE logístico se validaron y calibraron en bases de datos quirúrgicas relativamente amplias, pero tienden a perder exactitud en las cohortes de mayor riesgo7. No resulta extraño que estos modelos de riesgo quirúrgico establecidos den malos resultados en poblaciones actuales de pacientes con TAVI, formadas por personas de más edad que a menudo presentan múltiples comorbilidades. Además, han surgido variables de riesgo específicas, como la fragilidad, la deformidad torácica y la aorta de porcelana, que no se tiene en cuenta en los modelos citados.
En un artículo publicado en Revista Española de Cardiología, Pascual et al8 presentan los resultados a corto y a largo plazo tras el TAVI con el Medtronic CoreValve System en pacientes con aorta de porcelana. Se incluyó a un total de 449 pacientes de tres centros académicos. La prevalencia de la aorta de porcelana fue del 8%. Teniendo en cuenta la falta de uniformidad en las definiciones empleadas, la aterosclerosis de la aorta se describe en hasta una tercera parte de los octogenarios a los que se practican intervenciones de cirugía cardiaca, y la frecuencia de la aorta de porcelana verdadera es de un 1-5%9–11. La incidencia de la aorta de porcelana en los grandes registros nacionales de TAVI es diversa, con valores del 5% en el registro FRANCE-2 y del 11% en el registro alemán12–14.
En la población de pacientes con aorta de porcelana estudiados, abundaban la prevalencia de factores de riesgo de enfermedad aterosclerótica típicos, los antecedentes de enfermedad arterial periférica y la revascularización coronaria. El EuroSCORE logístico calculado general no fue diferente del observado en los pacientes sin aorta de porcelana. Por consiguiente, la cohorte de pacientes con aorta de porcelana puede haber tenido un riesgo operatorio incluso mayor, dado que la aorta de porcelana en sí no se tiene en cuenta en el EuroSCORE logístico. Habría sido interesante conocer cuántos pacientes con aorta de porcelana tenían un EuroSCORE logístico calculado bajo y, no obstante, se consideró que presentaban un riesgo operatorio alto. Además, cabe preguntarse si la aorta de porcelana de por sí indica un riesgo operatorio alto, independientemente de la presencia de comorbilidades significativas, y si podría influir solamente en el resultado de la intervención y no en los resultados a largo plazo. A este respecto, resulta sorprendente que la aorta de porcelana por sí sola no comportara unas dificultades operatorias/técnicas insuperables para estos equipos con experiencia en TAVI. Es de destacar que, proporcionalmente, hubo más pacientes de la cohorte de aorta de porcelana tratados por vía de acceso axilar/subclavia. Dado que se aplicó la estrategia «primero transfemoral», esto ilustra que la aorta de porcelana se asoció a trayectos iliofemorales menos favorables debido a tamaño pequeño, tortuosidad, calcificación o enfermedad aterosclerótica. El objetivo primario de mortalidad por cualquier causa a los 2 años no mostró diferencias entre los pacientes con y sin aorta de porcelana.
La aorta de porcelana es una entidad genérica con una calcificación generalizada y circular de la aorta ascendente torácica, por lo que se la debe considerar por separado de otras variables de riesgo o comorbilidades. Se caracteriza habitualmente por un exceso de calcio en la pared aórtica, que puede asociarse, aunque no de manera exclusiva, a placas ateroscleróticas adluminales. La calcificación aórtica puede estar situada en el interior de la capa íntima, ser excéntrica e iniciarse en la base de placas fibroadiposas necróticas (tipo aterosclerótico) o puede estar situada en la capa media (no aterosclerótica). Este matiz es importante, ya que la ausencia de una aterosclerosis protruyente descarta un origen importante de embolizaciones cerebrales. La observación de que el TAVI con una aorta de porcelana no se asoció a un aumento de la frecuencia de ictus en el estudio de Pascual et al8 puede indicar, de hecho, que la aorta de porcelana y la ateromatosis protruyente no están interrelacionadas. En consecuencia, las estrategias de acceso alternativas no parecen aportar una especial ventaja respecto a la vía (ordinaria) transfemoral en los pacientes con aorta de porcelana mientras el árbol arterial iliofemoral sea accesible.
La aorta de porcelana no tiene necesariamente los mismos mecanismos fisiopatológicos que tiene la aterosclerosis. Puede manifestarse con fenotipos diferentes con mecanismos subyacentes distintos. Los conceptos básicos en cuanto a edad avanzada, radiación y enfermedad renal crónica pueden plantearse de la siguiente forma: a) la edad avanzada activa señales osteogénicas paracrinas que la expansión fibroadiposa regula a través de vesículas apoptósicas que surgen de las células del músculo liso vascular muertas y en proceso de muerte; este proceso fomenta el depósito de calcio aórtico, incluidos los cambios específicos de la pared vascular de las grandes arterias, como son el depósito de colágeno y calcio y la pérdida de fibras elásticas de la capa media, lo que da lugar a un endurecimiento del árbol arterial15; b) la radiación mediastínica puede causar una aortitis, que genera depósitos de sales de calcio como secuela de la cicatrización de la íntima o la media16, y c) los pacientes con enfermedad renal crónica muestran no solo una aterosclerosis acelerada, sino también una calcificación difusa de la media de las grandes arterias (lo que se denomina también esclerosis de Monckeberg); la calcificación excesiva de la media es el resultado de la transformación osteoblástica de las células de músculo liso vascular, y da lugar a la formación de hidroxiapatita en un medio en el que hay un exceso de calcio y fosfato17.
Por el momento no hay una definición uniformemente aceptada de la aorta de porcelana. En el estudio de Pascual et al8, el diagnóstico de la aorta de porcelana se estableció cuando dos cirujanos cardiacos coincidían en que el paciente no era un candidato adecuado para la sustitución quirúrgica de la válvula aórtica por haberse identificado una calcificación aórtica desfavorable en la tomografía computarizada o la angiografía invasiva convencional. Parece claro que la ausencia de información de tomografía computarizada de todos los pacientes es una limitación de este estudio y puede llevar a subestimación o sobrestimación de la prevalencia real. Esto se ve resaltado, además, por el hecho de que 2 pacientes del estudio pasaron finalmente del grupo de tratamiento con sustitución quirúrgica de la válvula aórtica al de TAVI debido a que la aorta de porcelana solamente se identificó después de la esternotomía. El Valve Academic Research Consortium es una colaboración internacional de representantes de organizaciones de investigación clínica, centros académicos y autoridades competentes que ha hecho público recientemente su segundo documento de consenso sobre las definiciones de variables de valoración en el TAVI18. Ese documento define la aorta de porcelana como «una calcificación circular intensa o la presencia de placas ateromatosas intensas en toda la aorta ascendente, que se extienden hasta el cayado aórtico, de tal manera que hacen que el pinzamiento aórtico no sea posible». Además, el Valve Academic Research Consortium propone el empleo de la tomografía computarizada axial sin contraste como técnica de imagen de primera elección para evaluar la calcificación a nivel de la unión sinotubular, la aorta torácica ascendente, el tronco innominado y el arco transversal. En esta línea, a todos los pacientes considerados aptos para los ensayos actualmente en marcha en los que se asigna aleatoriamente el tratamiento con sustitución quirúrgica de la válvula aórtica o TAVI, se los examina con una tomografía computarizada multicorte para valorar la aorta y los vasos arteriales periféricos. La incorporación de la tomografía computarizada multicorte y esta definición uniforme en el estudio diagnóstico ordinario de todos los pacientes permitirá esclarecer mejor la frecuencia real y las implicaciones de la aorta de porcelana.
No todas las calcificaciones de la aorta torácica tienen la misma importancia ni es probable que dificulten el pinzamiento aórtico. El Leipzig Heart Center ha propuesto una clasificación perfeccionada de la aorta de porcelana basada en el grado y la localización del calcio en la aorta torácica que podría constituir una guía uniforme en el análisis del equipo cardiaco (local), formado por cirujanos cardiacos, cardiólogos, especialistas en diagnóstico por imagen y anestesiólogos19. Además, Bapat et al20 evaluaron una serie de aortas ascendentes calcificadas, y señalaron que, en la mayoría de los pacientes, el cuadrante superior externo de la aorta ascendente distal, la denominada zona de acceso transaórtico, siguió siendo accesible a la instrumentación y el abordaje de TAVI aórtico directo (o transaórtico), lo cual aporta claramente una perspectiva diferente sobre el tema de la aorta de porcelana. No es que no se debería tocar toda aorta de porcelana.
Con la mejora de la esperanza de vida en general y como resultado del envejecimiento de las sociedades occidentales, cabe prever una epidemia de pacientes con valvulopatía aórtica degenerativa calcificada y una aorta de porcelana acompañante en un futuro próximo. El estudio de Pascual et al8 pone de manifiesto que la aorta de porcelana no afecta al resultado de la intervención con TAVI, a diferencia de lo que sucede con sus repercusiones técnicas notables en la sustitución quirúrgica de la válvula aórtica. Una conclusión lógica es que el TAVI se está convirtiendo en el tratamiento estándar para los pacientes con estenosis aórtica y aorta de porcelana.
CONFLICTO DE INTERESESNinguno.