Las guías sobre síndrome coronario agudo (SCA) recomiendan el uso de los nuevos inhibidores del P2Y12 (prasugrel y ticagrelor) antes que el clopidogrel para los pacientes con riesgo isquémico moderado-alto, siempre que no tengan un riesgo hemorrágico elevado. El objetivo de nuestro estudio es evaluar la escala de riesgo isquémico GRACE y la de riesgo hemorrágico CRUSADE en relación con la prescripción de los nuevos inhibidores del P2Y12 al alta en pacientes con SCA.
MétodosAnálisis retrospectivo de un registro multicéntrico de SCA. Se incluyó a 3.515 pacientes consecutivos. La asociación entre las escalas de riesgo y la prescripción de los nuevos inhibidores del P2Y12 se evaluó mediante análisis de regresión logística binaria.
ResultadosSe trató con prasugrel o ticagrelor a 1.021 pacientes (29%). En el análisis multivariable, tanto la escala GRACE (cada 10 puntos, OR = 0,89; IC95%, 0,86-0,92; p < 0,001) como la escala CRUSADE (cada 10 puntos, OR = 0,96; IC95%, 0,94-0,98; p < 0,001) se asociaron inversamente con el uso de los nuevos inhibidores del P2Y12. Además, otros factores no incluidos en estas escalas (tipo de revascularización, trombosis del stent hospitalaria, hemorragia mayor e indicación concomitante de terapia anticoagulante) también fueron predictores del uso de los nuevos inhibidores del P2Y12.
ConclusionesLos nuevos inhibidores del P2Y12 se prescribieron con mayor frecuencia a los pacientes con SCA con menor riesgo hemorrágico CRUSADE. Sin embargo, se encontró una paradoja en cuanto al riesgo isquémico, con mayor uso de estos agentes para pacientes con menor riesgo estimado con la escala GRACE. Estos resultados subrayan la importancia de la estratificación de riesgos para prescribir con seguridad las terapias óptimas.
Palabras clave
El tratamiento antiagregante plaquetario doble con ácido acetilsalicílico y clopidogrel se ha considerado la piedra angular del tratamiento en el contexto del síndrome coronario agudo (SCA)1. Sin embargo, a pesar de los beneficios de esta combinación, los pacientes continúan teniendo riesgo de presentar nuevos eventos cardiovasculares2–4, lo que en cierta medida puede estar relacionado con cierto déficit del efecto antiagregante plaquetario del clopidogrel5,6. Esto ha estimulado la búsqueda de fármacos antiagregantes plaquetarios más eficaces. El prasugrel y el ticagrelor son los nuevos y más potentes inhibidores del P2Y12, con los que se ha demostrado una reducción de la recurrencia de eventos isquémicos, aunque a costa de un aumento de las hemorragias, en comparación con el clopidogrel7,8. Las guías actuales para el tratamiento del SCA9,10 recomiendan el uso de estos nuevos inhibidores del P2Y12 con preferencia al clopidogrel, sobre todo en los pacientes con un riesgo isquémico moderado o alto, a menos que presenten un aumento del riesgo de hemorragia. En consecuencia, los clínicos deben buscar un equilibrio entre riesgos y beneficios para obtener el máximo beneficio clínico neto del tratamiento antiagregante plaquetario prescrito.
Una de las opciones para evaluar tanto el riesgo clínico como el potencial de sangrado es el uso de escalas de riesgo. En los pacientes con SCA, la escala GRACE es la que aporta una estratificación más exacta del riesgo de muerte mediante puntuaciones obtenidas tanto al ingreso como al alta11, y las guías actuales de SCA recomiendan su uso9,10. Por lo que respecta a la evaluación del riesgo hemorrágico, la escala CRUSADE es la que ha mostrado mayor capacidad de discriminación para evaluar el riesgo de sangrado mayor hospitalario, sobre todo en pacientes sometidos a una angiografía coronaria12. Hasta la fecha no se dispone de ningún modelo de riesgo validado para estimar el riesgo hemorrágico tras el alta de los pacientes con SCA. Sin embargo, dado que la escala de riesgo CRUSADE obtuvo buenos resultados entre los pacientes en tratamiento antiagregante plaquetario doble, este modelo de riesgo puede usarse para la estratificación del riesgo hemorrágico de los pacientes con SCA tras el alta hospitalaria13. Sin embargo, no se sabe cuál de estos riesgos es el que tiene más repercusión o si existen otros factores que influyan en el patrón de los facultativos en la selección del tratamiento antiagregante. Así pues, los objetivos de este estudio son evaluar la escala de riesgo GRACE y la escala de riesgo hemorrágico CRUSADE en relación con la prescripción de los nuevos inhibidores del P2Y12 (prasugrel y ticagrelor) en pacientes con SCA.
MÉTODOSEl presente estudio se llevó a cabo cumpliendo lo establecido en la Declaración de Helsinki y fue aprobado por el comité de ética de investigación local. Los datos analizados en este estudio se obtuvieron a partir de un registro clínico retrospectivo combinado que incluía a todos los pacientes consecutivos con diagnóstico final de SCA establecido a los que se había practicado una angiografía coronaria en 2 hospitales terciarios entre el 1 de enero de 2011 y el 31 de diciembre de 2015. Sin embargo, para este análisis, la población del estudio se limitó a los pacientes ingresados entre el 1 de noviembre de 2012 y el 31 de diciembre de 2015. Este fue el periodo en que se dispuso ampliamente de los 2 nuevos inhibidores del P2Y12 (prasugrel y ticagrelor) en los 2 hospitales participantes y cuando la frecuencia de prescripción de estos fármacos alcanzó cierta estabilidad alrededor del 30%. Se excluyó de este análisis a los primeros pacientes tratados con ticagrelor o prasugrel, ya que pueden diferir de los que iniciaron esta medicación posteriormente (p. ej., en el deseo de adoptar nuevos tratamientos o pacientes con un riesgo basal anormal). Se reclutó en total a 4.653 pacientes con SCA. De ellos, se excluyó a 1.138 (755 ingresados antes del 1 de noviembre de 2012, 142 que fallecieron antes del alta hospitalaria, y 132 y 109 pacientes [2,8%] de los que no se dispuso de las puntuaciones de las escalas de riesgo GRACE o CRUSADE o del tratamiento antiagregante plaquetario al alta). En consecuencia, formaron la población final del estudio 3.515 pacientes hospitalizados por un SCA.
Cardiólogos bien preparados recogieron detalladamente los datos relativos a las características demográficas y clínicas, los resultados de las exploraciones complementarias, los parámetros angiográficos y los eventos registrados en el hospital, así como los del tratamiento al alta. Para cada paciente, se calculó retrospectivamente la puntuación de riesgo de mortalidad a 6 meses en la escala GRACE14 y la puntuación de riesgo hemorrágico en la escala CRUSADE15. Se clasificó a los pacientes en 3 categorías en función de la puntuación de la escala de riesgo GRACE (para el SCA con elevación del segmento ST: riesgo bajo, < 100 puntos; riesgo intermedio, 100-127, y riesgo elevado, > 127; para el SCA sin elevación del segmento ST: riesgo bajo, < 89; riesgo intermedio, 89-118 y riesgo elevado > 118) y en 5 categorías según la escala de riesgo CRUSADE (riesgo muy bajo, < 21; riesgo bajo, 21-30; riesgo moderado, 31-40; riesgo elevado, 41-50 y riesgo muy alto, > 50). La hemorragia mayor se definió según los criterios del Bleeding Academic Research Consortium como los tipos de hemorragia 3 a 516. La trombosis del stent se definió siguiendo las recomendaciones del Academic Research Consortium, y solamente se consideraron para el análisis las trombosis definitivas17. El cardiólogo encargado del tratamiento tomó las decisiones de tratamiento clínico para cada paciente y no se siguió ningún protocolo para orientar la elección del tratamiento antiagregante plaquetario doble.
Las variables discretas se presentan mediante los valores de frecuencia y las variables continuas, con la media ± desviación estándar. Se llevaron a cabo análisis por categorías según la prescripción de nuevos inhibidores del P2Y12 al alta. Las diferencias en las características basales se compararon con la prueba de la t de Student para las variables continuas y con la de la χ2 para las discretas. Para evaluar la asociación independiente de las escalas de riesgo GRACE y CRUSADE con la prescripción de los nuevos inhibidores del P2Y12 al alta, se calcularon los valores de odds ratio (OR) y los intervalos de confianza del 95% (IC95%) mediante modelos de regresión logística binarios multivariables, con ajuste por otros factores predictivos de la prescripción de los nuevos inhibidores de P2Y12 al alta. Con objeto de identificar las variables asociadas con la prescripción de los nuevos inhibidores de P2Y12 al alta, se realizaron primero análisis de regresión logística binaria univariable para todas las variables que se indican en la . A continuación se realizó un análisis de regresión logística binaria con selección escalonada retrógrada para identificar los factores independientes que predecían la prescripción de los nuevos inhibidores del P2Y12 al alta. Las covariables con p < 0,05 en el análisis univariable y las que el investigador consideró de interés clínico (diabetes mellitus) se incluyeron en los modelos multivariables. El criterio de entrada se fijó en p < 0,05 y el de salida, en p = 0,10. Para investigar la influencia de los datos individuales de las escalas de riesgo CRUSADE y GRACE en la prescripción de los nuevos inhibidores del P2Y12, se elaboraron otros modelos de regresión logística binaria multivariable adicionales. Todos los valores de p < 0,05 se aceptaron como estadísticamente significativos. El análisis estadístico se realizó con el programa SPSS versión 18,0 (SPSS, Inc.; Chicago, Illinois, Estados Unidos) y el programa STATA versión 13.0 (Stata Corp. LP; Texas, Estados Unidos) (tabla 1).
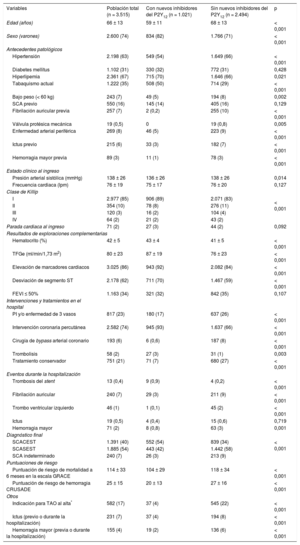
Características clínicas de la población total del estudio y en función de la prescripción de los nuevos inhibidores del P2Y12 al alta
| Variables | Población total (n = 3.515) | Con nuevos inhibidores del P2Y12 (n = 1.021) | Sin nuevos inhibidores del P2Y12 (n = 2.494) | p |
|---|---|---|---|---|
| Edad (años) | 66 ± 13 | 59 ± 11 | 68 ± 13 | < 0,001 |
| Sexo (varones) | 2.600 (74) | 834 (82) | 1.766 (71) | < 0,001 |
| Antecedentes patológicos | ||||
| Hipertensión | 2.198 (63) | 549 (54) | 1.649 (66) | < 0,001 |
| Diabetes mellitus | 1.102 (31) | 330 (32) | 772 (31) | 0,428 |
| Hiperlipemia | 2.361 (67) | 715 (70) | 1.646 (66) | 0,021 |
| Tabaquismo actual | 1.222 (35) | 508 (50) | 714 (29) | < 0,001 |
| Bajo peso (< 60 kg) | 243 (7) | 49 (5) | 194 (8) | 0,002 |
| SCA previo | 550 (16) | 145 (14) | 405 (16) | 0,129 |
| Fibrilación auricular previa | 257 (7) | 2 (0,2) | 255 (10) | < 0,001 |
| Válvula protésica mecánica | 19 (0,5) | 0 | 19 (0,8) | 0,005 |
| Enfermedad arterial periférica | 269 (8) | 46 (5) | 223 (9) | < 0,001 |
| Ictus previo | 215 (6) | 33 (3) | 182 (7) | < 0,001 |
| Hemorragia mayor previa | 89 (3) | 11 (1) | 78 (3) | < 0,001 |
| Estado clínico al ingreso | ||||
| Presión arterial sistólica (mmHg) | 138 ± 26 | 136 ± 26 | 138 ± 26 | 0,014 |
| Frecuencia cardiaca (lpm) | 76 ± 19 | 75 ± 17 | 76 ± 20 | 0,127 |
| Clase de Killip | < 0,001 | |||
| I | 2.977 (85) | 906 (89) | 2.071 (83) | |
| II | 354 (10) | 78 (8) | 276 (11) | |
| III | 120 (3) | 16 (2) | 104 (4) | |
| IV | 64 (2) | 21 (2) | 43 (2) | |
| Parada cardiaca al ingreso | 71 (2) | 27 (3) | 44 (2) | 0,092 |
| Resultados de exploraciones complementarias | ||||
| Hematocrito (%) | 42 ± 5 | 43 ± 4 | 41 ± 5 | < 0,001 |
| TFGe (ml/min/1,73 m2) | 80 ± 23 | 87 ± 19 | 76 ± 23 | < 0,001 |
| Elevación de marcadores cardiacos | 3.025 (86) | 943 (92) | 2.082 (84) | < 0,001 |
| Desviación de segmento ST | 2.178 (62) | 711 (70) | 1.467 (59) | < 0,001 |
| FEVI ≤ 50% | 1.163 (34) | 321 (32) | 842 (35) | 0,107 |
| Intervenciones y tratamientos en el hospital | ||||
| PI y/o enfermedad de 3 vasos | 817 (23) | 180 (17) | 637 (26) | < 0,001 |
| Intervención coronaria percutánea | 2.582 (74) | 945 (93) | 1.637 (66) | < 0,001 |
| Cirugía de bypass arterial coronario | 193 (6) | 6 (0,6) | 187 (8) | < 0,001 |
| Trombolisis | 58 (2) | 27 (3) | 31 (1) | 0,003 |
| Tratamiento conservador | 751 (21) | 71 (7) | 680 (27) | < 0,001 |
| Eventos durante la hospitalización | ||||
| Trombosis del stent | 13 (0,4) | 9 (0,9) | 4 (0,2) | < 0,001 |
| Fibrilación auricular | 240 (7) | 29 (3) | 211 (9) | < 0,001 |
| Trombo ventricular izquierdo | 46 (1) | 1 (0,1) | 45 (2) | < 0,001 |
| Ictus | 19 (0,5) | 4 (0,4) | 15 (0,6) | 0,719 |
| Hemorragia mayor | 71 (2) | 8 (0,8) | 63 (3) | 0,001 |
| Diagnóstico final | < 0,001 | |||
| SCACEST | 1.391 (40) | 552 (54) | 839 (34) | |
| SCASEST | 1.885 (54) | 443 (42) | 1.442 (58) | |
| SCA indeterminado | 240 (7) | 26 (3) | 213 (9) | |
| Puntuaciones de riesgo | ||||
| Puntuación de riesgo de mortalidad a 6 meses en la escala GRACE | 114 ± 33 | 104 ± 29 | 118 ± 34 | < 0,001 |
| Puntuación de riesgo de hemorragia CRUSADE | 25 ± 15 | 20 ± 13 | 27 ± 16 | < 0,001 |
| Otros | ||||
| Indicación para TAO al alta* | 582 (17) | 37 (4) | 545 (22) | < 0,001 |
| Ictus (previo o durante la hospitalización) | 231 (7) | 37 (4) | 194 (8) | < 0,001 |
| Hemorragia mayor (previa o durante la hospitalización) | 155 (4) | 19 (2) | 136 (6) | < 0,001 |
FEVI: fracción de eyección del ventrículo izquierdo; PI: arteria principal izquierda; SCA: síndrome coronario agudo; SCACEST: síndrome coronario agudo con elevación del segmento ST; SCASEST: síndrome coronario agudo sin elevación del segmento ST; TAO: tratamiento anticoagulante oral; TFGe: tasa de filtrado glomerular estimada.
Los valores expresan media ± desviación estándar o n (%).
Formaron la población del estudio 3.515 pacientes hospitalizados por SCA. Un total de 1.021 pacientes (29%) estaban en tratamiento con los nuevos inhibidores del P2Y12 al alta, prasugrel en 346 (9,8%) y ticagrelor en 675 (19,2%).
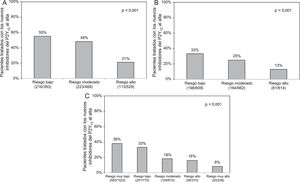
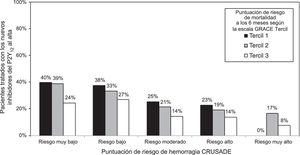
En la tabla 1 se muestran las características de la población del estudio según la prescripción de nuevos inhibidores del P2Y12 al alta. Los pacientes tratados con los nuevos inhibidores del P2Y12 presentaron inferiores puntuaciones en las escalas GRACE (104 ± 29 frente a 118 ± 34; p < 0,001) y CRUSADE (20 ± 13 frente a 27 ± 16; p < 0,001). Se observó una reducción gradual en la proporción de pacientes tratados con los nuevos inhibidores del P2Y12 según aumentaba la categoría de riesgo hemorrágico e isquémico (figura 1). Esta infrautilización de los nuevos inhibidores del P2Y12 según aumenta el riesgo isquémico se observó en todas las categorías de riesgo hemorrágico (figura 2). Así pues, cuanto mayor fuera el riesgo isquémico o hemorrágico, menor era la frecuencia de prescripción de los nuevos inhibidores del P2Y12.
Frecuencia de prescripción de los nuevos inhibidores del P2Y12 al alta, según las categorías de riesgo de mortalidad a 6 meses de la escala GRACE en pacientes con SCACEST (A) o SCASEST (B) y según las categorías de riesgo hemorrágico de la escala CRUSADE (C). SCACEST: síndrome coronario agudo con elevación del segmento ST; SCASEST: síndrome coronario agudo sin elevación del segmento ST.
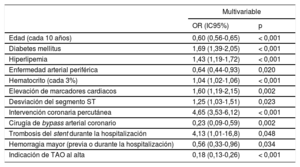
En los análisis de regresión logística binaria multivariable, se observó que las puntuaciones de riesgo tanto de la escala GRACE (cada 10 puntos, OR = 0,89; IC95%, 0,86-0,92; p < 0,001) como de la CRUSADE (cada 10 puntos, OR = 0,96; IC95%, 0,94-0,98; p < 0,001) se asociaban con la prescripción de los nuevos inhibidores del P2Y12 al alta (figura 3). Esta asociación inversa con las puntuaciones en las escalas de riesgo GRACE y CRUSADE persistió al analizar por separado la prescripción de prasugrel y la de ticagrelor (prasugrel: OR cada 10 puntos en la escala de riesgo GRACE = 0,86; IC95%, 0,82-0,90; p < 0,001; OR cada 10 puntos en la escala de riesgo CRUSADE = 0,95; IC95%, 0,92-0,99; p = 0,009; ticagrelor: OR cada 10 puntos en la escala de riesgo GRACE = 0,91; IC95%, 0,88-0,94; p < 0,001; OR cada 10 puntos en la escala de riesgo CRUSADE = 0,96; IC95%, 0,94-0,99; p = 0,003). Se presentan los datos detallados de estos análisis multivariables en la y la . Tal como se muestra en la tabla 2, cuando se incluyeron los datos individuales de ambas poblaciones de riesgo en un mismo modelo multivariable, la edad (cada 10 años, OR = 0,60; IC95%, 0,56-0,65; p < 0,001), la diabetes mellitus (OR = 1,69; IC95%, 1,39-2,05; p < 0,001), la enfermedad arterial periférica (OR = 0,64; IC95%, 0,44-0,93; p < 0,020), el hematocrito (cada 3%, OR = 1,04; IC95%, 1,02-1,06; p < 0,001), la elevación de los marcadores cardiacos (OR = 1,60; IC95%, 1,19-2,15; p = 0,002) y la desviación del segmento ST (OR = 1,25; IC95%, 1,03-1,51; p = 0,023) continuaron teniendo valor predictivo respecto a la prescripción de los nuevos inhibidores del P2Y12 al alta. Otros factores predictivos independientes, no incluidos en las escalas de riesgo GRACE o CRUSADE, fueron los siguientes: hiperlipemia, intervención coronaria percutánea, cirugía de bypass arterial coronario, trombosis del stent durante la hospitalización, hemorragia mayor (previa o durante la hospitalización) e indicación de tratamiento antiacoagulante oral al alta (tabla 2).
Valores de odds ratio multivariable para la asociación entre las escalas de riesgo GRACE y CRUSADE y la prescripción de los nuevos inhibidores del P2Y12 al alta. IC95%: intervalo de confianza del 95%; OR: odds ratio. Las variables incluidas en los modelos multivariables se presentan en la y la .
Análisis de regresión logística multivariable que incluye los datos individuales de las escalas de riesgo GRACE y CRUSADE para la predicción de la prescripción de los nuevos inhibidores de P2Y12 al alta
| Multivariable | ||
|---|---|---|
| OR (IC95%) | p | |
| Edad (cada 10 años) | 0,60 (0,56-0,65) | < 0,001 |
| Diabetes mellitus | 1,69 (1,39-2,05) | < 0,001 |
| Hiperlipemia | 1,43 (1,19-1,72) | < 0,001 |
| Enfermedad arterial periférica | 0,64 (0,44-0,93) | 0,020 |
| Hematocrito (cada 3%) | 1,04 (1,02-1,06) | < 0,001 |
| Elevación de marcadores cardiacos | 1,60 (1,19-2,15) | 0,002 |
| Desviación del segmento ST | 1,25 (1,03-1,51) | 0,023 |
| Intervención coronaria percutánea | 4,65 (3,53-6,12) | < 0,001 |
| Cirugía de bypass arterial coronario | 0,23 (0,09-0,59) | 0,002 |
| Trombosis del stent durante la hospitalización | 4,13 (1,01-16,8) | 0,048 |
| Hemorragia mayor (previa o durante la hospitalización) | 0,56 (0,33-0,96) | 0,034 |
| Indicación de TAO al alta | 0,18 (0,13-0,26) | < 0,001 |
FEVI: fracción de eyección del ventrículo izquierdo; IC95%: intervalo de confianza del 95%; OR: odds ratio; PI: arteria principal izquierda; SCA: síndrome coronario agudo; TAO: tratamiento anticoagulante oral.
El modelo multivariable incluye los parámetros individuales de las escalas de riesgo GRACE y CRUSADE; hipertensión, hiperlipemia, tabaquismo actual, bajo peso < 60 kg, SCA previo, FEVI ≤ 50%, PI y/o enfermedad de 3 vasos, intervención coronaria percutánea, cirugía de bypass arterial coronario, tratamiento conservador, trombosis del stent durante la hospitalización, diagnóstico final de SCA, indicaciones terapéuticas de TAO al alta (fibrilación auricular [previa o durante la hospitalización], válvula protésica mecánica, trombo ventricular izquierdo y otros), ictus (previo o durante la hospitalización) y hemorragia mayor (previa o durante la hospitalización).
En este estudio se evaluó la prescripción al alta de los nuevos y más potentes inhibidores del P2Y12 en relación con el riesgo clínico y hemorrágico de los pacientes con SCA. Se observó que la percepción de un riesgo hemorrágico elevado conllevaba menos prescripción de estos fármacos, a pesar del riesgo generalmente superior de estos pacientes. Esta observación es coherente con lo indicado por las guías actuales que no respaldan el uso de prasugrel o ticagrelor para pacientes con alto riesgo hemorrágico9,10. En cambio, las guías actuales recomiendan también el uso de prasugrel o ticagrelor para pacientes con un riesgo moderado o alto de eventos isquémicos9,10, debido a la reducción de dichos eventos con los 2 nuevos inhibidores del P2Y127,8. Además, algunos autores han propuesto protocolos específicos para la elección del tratamiento antiagregante plaquetario de los pacientes con SCA, cuyo primer criterio de discriminación es la escala de riesgo GRACE (clopidogrel si el valor de GRACE es < 109 y prasugrel o ticagrelor si el valor de GRACE es ≥ 109 y no hay contraindicaciones ni alto riesgo hemorrágico)18. Sin embargo, en este estudio, se observó que un mayor riesgo isquémico según la escala de riesgo GRACE no se asociaba con la prescripción de estos fármacos. De hecho, cuanto mayor era el riesgo isquémico estimado, menor era la frecuencia de prescripción de los nuevos inhibidores del P2Y12 al alta. Concretamente, la edad más avanzada fue el único factor de riesgo isquémico incluido en la escala de riesgo GRACE que mostró una asociación independiente con una menor prescripción de los nuevos inhibidores del P2Y12. Esto no resulta extraño, teniendo en cuenta que la edad avanzada es un conocido factor de riesgo hemorrágico19. Nuestras observaciones son coherentes con las de otros estudios previos que han descrito infrautilización de prasugrel o ticagrelor en los pacientes de mayor edad20. Aunque no se incluye en la escala de riesgo CRUSADE, otras muchas escalas del riesgo hemorrágico desarrolladas para los pacientes con SCA incluyen la edad en la estimación del riesgo hemorrágico21–23. Es de destacar que se observara que los pacientes con diabetes tenían mayor probabilidad de recibir los nuevos inhibidores del P2Y12 a pesar de que la diabetes tienda a asociarse con una mayor incidencia de episodios hemorrágicos24. Esta conducta de prescripción puede explicarse por la evidencia cada vez más amplia que indica un beneficio clínico neto con el empleo de los nuevos inhibidores del P2Y12 en los pacientes diabéticos tras un SCA25. Este mayor efecto beneficioso en los pacientes diabéticos puede deberse a la respuesta disminuida al clopidogrel26 junto con el elevado riesgo de eventos isquémicos de dichos pacientes27. Además, se observaron también otros factores predictivos de la prescripción de los nuevos inhibidores del P2Y12 que no se incluyen en las escalas mencionadas. Todos ellos eran predecibles, como el antecedente de intervención coronaria percutánea y la trombosis del stent (en ambos casos, actualmente se acepta el uso de los inhibidores de P2Y12 más potentes) o la indicación simultánea para un tratamiento de anticoagulación oral al alta (en esta situación, las guías actuales no recomiendan el uso de los nuevos inhibidores del P2Y129,10). En el caso de la dislipemia, no se halló una explicación obvia, más allá de su papel como factor de riesgo cardiovascular, y podría tratarse de una asociación debida al azar.
Proponemos diversos motivos para la menor prescripción de los nuevos inhibidores del P2Y12 a los pacientes con puntuaciones más altas de la escala de riesgo GRACE: a) el temor a las complicaciones hemorrágicas a causa de la dificultad de separar los riesgos isquémico y hemorrágico de los pacientes con SCA debido a la alta correlación existente entre las 2 escalas28, y en este sentido, nuestro grupo ha observado anteriormente que la escala de riesgo GRACE es no inferior a la escala de riesgo CRUSADE para predecir la hemorragia mayor durante la hospitalización29; b) el fenómeno conocido como la paradoja riesgo-tratamiento, que plantea que los clínicos tienen mayor probabilidad de tratar el SCA según lo establecido en las guías en caso de pacientes con bajo riesgo30; c) la percepción de un riesgo hemorrágico alto en los pacientes de más edad y la fuerte influencia de la edad en la escala de riesgo GRACE, y d) la existencia de otros factores no incluidos en la escala de riesgo GRACE que influyan en los patrones de los facultativos en la elección del tratamiento antiagregante plaquetario.
La principal consecuencia de nuestro estudio es que respalda la importancia de una evaluación adecuada del riesgo, que es una cuestión importante para la toma de decisiones terapéuticas. Hay clara evidencia de que un abordaje terapéutico agresivo tiene la posibilidad de modificar el pronóstico de los pacientes con SCA, aunque este efecto frecuentemente dependa del riesgo31,32. Hoy se acepta que los pacientes isquémicos de alto riesgo con un SCA requieren un tratamiento más agresivo, lo que incluye el uso de un tratamiento antitrombótico más potente y una estrategia invasiva rápida, mientras que los pacientes con menos riesgo pueden evolucionar bien con un tratamiento antitrombótico menos potente y una estrategia invasiva más selectiva9,10. La evidencia acumulada respalda que los fármacos antitrombóticos más potentes y las intervenciones invasivas pueden reducir el número de eventos isquémicos en los pacientes con SCA, pero estos tratamientos suelen aumentar el riesgo hemorrágico33. En consecuencia, las escalas de riesgo isquémico y hemorrágico han pasado a ser necesarias en la evaluación del riesgo de SCA con objeto de calcular las compensaciones entre la reducción del riesgo isquémico y el peligro de hemorragias espontáneas y relacionadas con el tratamiento. La paradoja del riesgo que hemos identificado (según la cual se trata a los pacientes con menos riesgo de manera más agresiva que a los pacientes con riesgo alto) puede deberse en parte a la percepción del riesgo hemorrágico. La forma de equilibrar los 2 riesgos puede facilitarse empleando instrumentos que tengan aún mejor capacidad de discriminar entre complicaciones hemorrágicas e isquémicas. Para resolver esta importante cuestión, serán necesarios nuevos estudios que investiguen la repercusión que la integración de los 2 riesgos tiene en la evolución de los pacientes.
LimitacionesEl presente estudio tiene las limitaciones inherentes de ser un estudio retrospectivo que incluyó a pacientes con SCA a los que se practicó una angiografía coronaria durante la hospitalización índice en 2 hospitales terciarios de España. En consecuencia, la aplicabilidad de estos resultados debe interpretarse con precaución en centros que atiendan a otros tipos de pacientes y que cuenten con otras instalaciones, y deben considerarse generadores de hipótesis. La inclusión de los pacientes con SCA a los que se practica una angiografía coronaria puede causar un sesgo de selección y favorecer un alto porcentaje de pacientes con SCA con elevación de segmento ST, en los que es más frecuente el tratamiento invasivo. Además, no se dispuso de datos sobre la posición socioeconómica, el nivel de estudios, la situación laboral o la nacionalidad, que son factores que pueden influir en la prescripción de los nuevos antiagregantes plaquetarios. Por último, aunque se analizaron las repercusiones de los eventos ocurridos durante la hospitalización en el tratamiento prescrito al alta, no se dispuso de información sobre la relación entre esos eventos y el tratamiento antitrombótico previo o sus modificaciones.
CONCLUSIONESLos resultados de este estudio indican que hay varios factores que influyen en los clínicos a la hora de prescribir los nuevos inhibidores del P2Y12 al alta a los pacientes con SCA, y que hay una infrautilización apropiada de estos fármacos en los pacientes con alto riesgo hemorrágico. Sin embargo, esto da lugar a una paradoja del riesgo isquémico, lo cual ilustra la complejidad de aplicar las guías clínicas en el contexto de la práctica clínica real. Conocer el comportamiento de prescripción de los nuevos antiagregantes plaquetarios en estas situaciones es crucial para la adecuada interpretación de los nuevos estudios que exploran las ventajas de los nuevos antiagregantes plaquetarios en el SCA y para identificar oportunidades para esfuerzos futuros para mejorar la calidad de las prescripciones.
CONFLICTO DE INTERESESE. Abu-Assi es Editor Asociado de Revista Española de Cardiología.
- –
Las guías actuales sobre el SCA recomiendan los nuevos inhibidores del P2Y12 (prasugrel y ticagrelor) para pacientes con un riesgo isquémico moderado o alto, a menos que haya un aumento del riesgo hemorrágico. Estas guías recomiendan también el uso de las escalas de riesgo GRACE y CRUSADE para la evaluación de los riesgos isquémico y hemorrágico respectivamente. Sin embargo, no se sabe cuál de los 2 riesgos es el que tiene mayor repercusión o si hay otros factores que influyan en los patrones de los facultativos en la elección del tratamiento antiagregante plaquetario.
- –
En este estudio se observa un uso apropiado de los nuevos inhibidores del P2Y12 en los pacientes con alto riesgo hemorrágico. Sin embargo, se observó una paradoja de riesgo isquémico, de manera que hubo más uso de estos fármacos en los pacientes con menos riesgo isquémico según la puntuación de riesgo GRACE. Además, se observó que otros factores, aparte de estas puntuaciones, influían en los patrones de prescripción de los clínicos. Esto ilustra la complejidad de aplicar las guías clínicas en el contexto de la práctica clínica real y resalta la importancia de una evaluación apropiada del riesgo para la toma de decisiones terapéuticas.