En España hay más de 40 millones de personas vacunadas contra la COVID-191. Las reacciones adversas a la vacuna suelen ser intrascendentes y no contrarrestan los beneficios que aporta. Por lo que respecta a los efectos adversos cardiacos, el bloqueo cardiaco completo (BCC) no se ha descrito en los ensayos clínicos de las vacunas contra la COVID-192.
Presentamos un caso de BCC con una asociación en el tiempo con la administración de la vacuna contra la COVID-19, que mostró una recuperación con tratamiento con corticoides. Se obtuvo el consentimiento informado por escrito del paciente para la publicación.
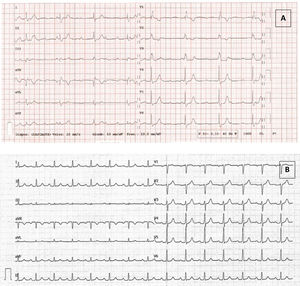
Seis días después de la primera dosis de la vacuna de ARNm contra el SARS-CoV-2 (Pfizer-BioNtech, Estados Unidos), un varón de 49 años acudió al servicio de urgencias por mareo y disnea, que se habían iniciado 3 días antes. A la exploración física se observó la presencia de bradicardia. La presión arterial era de 136/60mmHg, la frecuencia cardiaca de 40 latidos/min, la saturación de oxígeno del 100% y el paciente no tenía fiebre. El electrocardiograma (ECG) mostró un BCC con bloqueo de rama derecha del haz de His (figura 1A). Un análisis de sangre mostró unos resultados normales de función renal, electrolitos y hemograma. La proteína C reactiva (PCR) era de 15,7mg/l (< 5), la troponina T de alta sensibilidad de 17 ng/l (< 13), la creatina-cinasa de 57 U/l (< 189) y el propéptido natriurético de tipo B aminoterminal (NT-proBNP) de 307 ng/l (< 300). La ecocardiografía transtorácica mostró una fracción de eyección normal sin presencia de cardiopatía estructural.
El paciente había presentado un tumor de células germinales no seminomatoso en 2003 con metástasis pulmonares. Se le trató con orquidectomía y quimioterapia con una remisión completa. El ECG previo era normal.
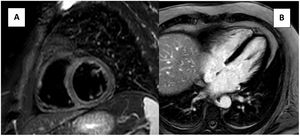
Durante la hospitalización, un análisis de sangre mostró una concentración de electrolitos normal y una elevación de la PCR de carácter menor (15,7 → 11,7mg/l). La presencia de una troponina negativa (17 → 17 → 12 ng/l) y la ausencia de anomalías de movilidad de la pared ventricular descartaron un bloqueo cardiaco (BC) isquémico. La ecocardiografía transtorácica y la resonancia magnética cardiaca (RMC), con un protocolo que incluía secuencias de cine, recuperación de inversión tau corta (STIR), mapeo T1 y T2, y realce tardío de gadolinio, revelaron una función y estructura cardiacas normales y una ausencia de edema, y descartaron la presencia de miocardiopatías o miocarditis (figura 2). La negatividad del estudio inmunológico (ANA, ENA) y las serologías (Borrelia burgdorferi, citomegalovirus, virus de Epstein-Barr, hepatitis A, B, C, herpes simple, sarampión, Treponema pallidum, Toxoplasma gondii, virus varicela-zóster, VIH, rubéola y parotiditis) descartaron las enfermedades autoinmunitarias e infecciosas. El ECG previo normal descartó un BC congénito.
El paciente ingresó con un diagnóstico de BCC. Se llevó a cabo un estudio etiológico exhaustivo en el que no se observaron anomalías. Dado que había sido vacunado recientemente, se sospechó un BCC causado por una inflamación local del sistema de conducción asociada a la vacuna. Se inició un tratamiento con corticoides mediante prednisona en dosis de 1mg/kg al día, y después de 2 dosis el paciente presentó una resolución del BCC. Posteriormente mostró una mejora progresiva de la conducción, con acortamiento progresivo del intervalo PR y del complejo QRS hasta una normalización completa (figura 1B).
Se dio de alta al paciente al cabo de 16 días. Después de un mes, el ECG continuó siendo normal y se redujo lentamente la administración de prednisona hasta suspenderla. La serología del SARS-CoV-2 mostró la presencia de inmunidad tras la vacunación contra la COVID-19.
Describimos a un paciente que presentó un BCC tras la vacunación contra la COVID-19 con la vacuna de ARNm de Pfizer/BioNTech. La conducción auriculoventricular (AV) previa había sido normal. Los trastornos cardiacos fueron sumamente infrecuentes en los ensayos clínicos de la vacuna contra la COVID-19. Con la vacuna de ARNm de Pfizer/BioNTech contra la COVID-19, menos del 0,1% de los participantes presentaron algún evento cardiaco2. No se notificaron casos de BCC en ninguno de los ensayos clínicos de las vacunas contra la COVID-19.
En un estudio reciente de una serie de casos, se observó un aumento del riesgo de arritmias cardiacas, incluido el BC, después de una segunda dosis de la vacuna de ARNm contra la COVID-19 y en los primeros 28 días después de un resultado positivo de la prueba de SARS-CoV-2 3.
El diagnóstico diferencial incluyó la miocarditis, ya que hay una relación causal plausible entre la miocarditis y las vacunas de ARNm4. Sin embargo, en las series de casos que han descrito la miocarditis después de la vacunación contra la COVID-1, todos los pacientes presentaron un dolor torácico agudo, una elevación importante de las concentraciones de troponinas y unos signos compatibles en la RMC.
La inflamación y la fibrosis pueden desempeñar un papel importante en los trastornos de la conducción. Cuando la inflamación se extiende al nódulo AV, puede causar un BCC8. La tomografía de emisión de positrones con F-fluoro-desoxi-glucosa/tomografía computarizada (PET/TC) puede desempeñar un papel en esta situación5. Se sabe que el tratamiento con corticoides mejora la conducción AV en determinadas situaciones, como el BC de la sarcoidosis cardiaca. Los pacientes en los que se obtiene un beneficio con el tratamiento con corticoides son los que tienen una inflamación del tabique que afecta a la conducción AV, pero con una fibrosis mínima o nula.
Aunque no pudimos demostrar la presencia de inflamación, planteamos la hipótesis de que una inflamación localizada del sistema de conducción asociada a una respuesta inflamatoria a la vacunación causara el BCC e iniciamos un tratamiento empírico con corticoides (1mg/kg/d), con lo que se produjo una mejora rápida de la conducción cardiaca. No se observó fibrosis en la RMC, y ello podría explicar la recuperación. Se aplicó una reducción progresiva estándar de la prednisona hasta su suspensión (reducción de 10mg cada 5 días).
Hasta el momento, tan solo hay casos clínicos aislados en los que se ha descrito una asociación entre el BC y la vacunación contra el SARS-CoV-2, en su mayor parte en pacientes de edad avanzada con trastornos de la conducción subyacentes. Nasab et al.6 publicaron la presentación de un caso de un paciente de 65 años sin cardiopatía previa que presentó un bloqueo AV 2:1 pocos días después de la vacunación contra la COVID-19 y necesitó el implante de un marcapasos permanente.
Nuestro caso es el primero en el que se presenta un BC en un paciente joven sin trastornos de la conducción preexistentes y con evidencia de resolución del trastorno de la conducción con tratamiento con corticoides. Continúa sin haberse determinado si el BC estuvo relacionado con una respuesta inflamatoria excesiva a la vacuna, y serán necesarias nuevas investigaciones sobre el uso de tratamientos inflamatorios alternativos.
En este caso, presentamos un paciente con un BCC y una asociación en el tiempo que coincidió con la administración de la vacuna contra la COVID-19, y que recuperó una conducción AV normal tras 4 semanas de tratamiento con corticoides. Aunque no se conoce la etiología del BC, el curso clínico y el efecto de los corticoesteroides sugieren una inflamación del sistema de conducción debida a una respuesta inflamatoria a la vacunación. El BCC como posible acontecimiento adverso relacionado con la vacuna es una observación que requiere un mayor estudio.
FINANCIACIÓNLos autores no recibieron ninguna ayuda económica para la investigación, autoría o publicación de este artículo.
CONTRIBUCIÓN DE LOS AUTORESConceptualización: P. Mañas; redacción versión inicial: A. Pons-Riverola; redacción, revisión y corrección: A. Pons-Riverola, P. Mañas, E. Claver, O. Meroño, J. Comín-Colet, I. Anguera; supervisión: P. Mañas, J. Comín-Colet e I. Anguera.
CONFLICTO DE INTERESESLos autores declaran no tener ningún conflicto de intereses.