La incorporación precoz del enfermo al que se ha realizado una angioplastia con stent a su vida habitual, por ausencia de impedimentos propios de la técnica, ha permitido incluir más pronto a estos pacientes en la fase II de la rehabilitación cardiaca. Aunque la rehabilitación del paciente coronario sigue para todos los pacientes unas pautas generales que pretenden abordar desde un punto de vista de prevención secundaria la aterosclerosis coronaria, las circunstancias de cada enfermo, entre las que se incluye la técnica con que ha sido revascularizado, determinan aspectos individuales de la rehabilitación del enfermo con cardiopatía isquémica. El ejercicio físico continuado (entrenamiento físico) produce, por sí mismo, grandes beneficios cardiovasculares para la prevención cardiovascular primaria y secundaria. En pacientes con infarto disminuye la mortalidad y mejora la capacidad funcional, la función ventricular y el remodelado ventricular, y hay esperanzas de que pueda mejorar la circulación colateral. También mejora la función endotelial y estimula la circulación de células madre. Se ha demostrado que el entrenamiento físico tras revascularización percutánea disminuye el número de eventos y que en pacientes con angina estable el entrenamiento físico produce menos eventos que la revascularización percutánea.
Palabras clave
En línea con la política sobre guías de práctica clínica de la Sociedad Española de Cardiología (SEC)1, se presentan en este artículo los aspectos novedosos, relevantes o conflictivos de la actualización de 2018 sobre el tratamiento de las enfermedades cardiovasculares durante el embarazo de la Sociedad Europea de Cardiología (ESC) en conjunto con la International Society of Gender Medicine (IGM), la German Institute of Gender in Medicine (DGesGM), la European Society of Anaesthesiology (ESA), y la European Society of Gynecology (ESG)2.
A propuesta del Comité de Guías de la SEC y de los coordinadores asignados a esta guía, se seleccionó un grupo de cardiólogos y ginecólogos expertos para revisar la guía. El objetivo es comentar la naturaleza y la oportunidad de esta guía, analizar la metodología y destacar las novedades (tabla) y los aspectos positivos, cuestionables o no comentados. Con dichas valoraciones, se ha elaborado un documento conjunto, revisado por los cardiólogos designados por las secciones de Cardiología Clínica, Riesgo Cardiovascular y Rehabilitación Cardiaca y Cardiología Pediátrica de la SEC y por la Sociedad Española de Ginecología y Obstetricia (SEGO).
Novedades destacables de la guía de 2018
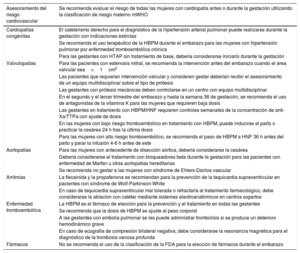
| Asesoramiento del riesgo cardiovascular | Se recomienda evaluar el riesgo de todas las mujeres con cardiopatía antes o durante la gestación utilizando la clasificación de riesgo materno mWHO |
|---|---|
| Cardiopatías congénitas | El cateterismo derecho para el diagnóstico de la hipertensión arterial pulmonar puede realizarse durante la gestación con indicaciones estrictas |
| Se recomienda el uso terapéutico de la HBPM durante el embarazo para las mujeres con hipertensión pulmonar por enfermedad tromboembólica crónica | |
| Para las gestantes con HTAP sin tratamiento de base, debería considerarse iniciarlo durante la gestación | |
| Valvulopatías | Para las pacientes con estenosis mitral, se recomienda la intervención antes del embarazo cuando el área valvular sea<1cm2 |
| Las pacientes que requieran intervención valvular y consideren gestar deberían recibir el asesoramiento de un equipo multidisciplinar sobre el tipo de prótesis | |
| Las gestantes con prótesis mecánicas deben controlarse en un centro con equipo multidisciplinar | |
| En el segundo y el tercer trimestre del embarazo y hasta la semana 36 de gestación, se recomienda el uso de antagonistas de la vitamina K para las mujeres que requieren baja dosis | |
| Las gestantes en tratamiento con HBPM/HNF requieren controles semanales de la concentración de anti-Xa/TTPa con ajuste de dosis | |
| En las mujeres con bajo riesgo tromboembólico en tratamiento con HBPM, puede inducirse el parto o practicar la cesárea 24 h tras la última dosis | |
| Para las mujeres con alto riesgo tromboembólico, se recomienda el paso de HBPM a HNF 36 h antes del parto y parar la infusión 4-6 h antes de este | |
| Aortopatías | Para las mujeres con antecedente de disección aórtica, debería considerarse la cesárea |
| Debería considerarse el tratamiento con bloqueadores beta durante la gestación para las pacientes con enfermedad de Marfan u otras aortopatías hereditarias | |
| Se recomienda no gestar a las mujeres con síndrome de Ehlers-Danlos vascular | |
| Arritmias | La flecainida y la propafenona se recomiendan para la prevención de la taquicardia supraventricular en pacientes con síndrome de Wolf-Parkinson-White |
| En caso de taquicardia supraventricular mal tolerada o refractaria al tratamiento farmacológico, debe considerarse la ablación con catéter mediante sistemas electroanatómicos en centros expertos | |
| Enfermedad tromboembólica | La HBPM es el fármaco de elección para la prevención y el tratamiento en todas las gestantes |
| Se recomienda que la dosis de HBPM se ajuste al peso corporal | |
| A las gestantes con embolia pulmonar se les puede administrar trombolisis si se produce un deterioro hemodinámico grave | |
| En caso de ecografía de compresión bilateral negativa, debe considerarse la resonancia magnética para el diagnóstico de la trombosis venosa profunda | |
| Fármacos | No se recomienda el uso de la clasificación de la FDA para la elección de fármacos durante el embarazo |
anti-Xa/TTPa: antagonistas del factor Xa/tiempo de tromboplastina parcial activado; equipo multidisciplinar: equipo multidisciplinar de atención a las cardiópatas en el embarazo; FDA: Food and Drug Administration; HBPM: heparina de bajo peso molecular; HNF: heparina no fraccionada; HTAP: hipertensión arterial pulmonar; mWHO: clasificadión modificada de la Organización Mundial de la Salud.
La nueva versión de la guía de la ESC es el resultado de una revisión sistemática de la literatura publicada entre 2011 y 2016 y se erige en una herramienta actualizada que asiste a los profesionales en la atención de las gestantes con cardiopatía. En el preámbulo se hace hincapié en que son recomendaciones de apoyo a los profesionales sanitarios, que son los responsables últimos de la toma de decisiones clínicas y quienes deben gestionar el complejo equilibrio entre 2 estrategias terapéuticas que frecuentemente presentan direcciones opuestas: por un lado, optimizar los resultados en términos de salud materna y, por el otro, permitir que el feto tenga un desarrollo adecuado minimizando los riesgos derivados de los posibles tratamientos maternos, incluidas las secuelas de la prematuridad.
Como novedad, el formato es más funcional y se estructuran nuevos apartados, como las tablas de recomendaciones en las que se recogen los aspectos fundamentales y novedosos respecto a ediciones anteriores, ordenados en función del nivel de evidencia que las sustenta. Se utilizan los niveles de evidencia (A, B y C) y de recomendación (clases I, IIa, IIb y III) conocidos.
CONSIDERACIONES GENERALESAdaptaciones fisiológicas en el embarazoEl apartado sobre la adaptación materna al embarazo se ha reducido respecto a versiones anteriores y, a pesar de que no se menciona explícitamente, cabe recordar que el puerperio es un periodo de especial vulnerabilidad para esta población.
Asesoramiento previo al embarazoEn esta nueva versión se enfatiza, incluso más que en la versión previa, la importancia de la consulta preconcepcional de toda paciente con cardiopatía antes de que se plantee el embarazo (I C)3. Como aspecto novedoso y relevante, se considera que dicho asesoramiento debe realizarse mediante abordaje multidisciplinario, y se introduce el concepto del equipo multidisciplinar especializado de atención a las cardiópatas en el embarazo, el pregnancy heart team (I C), como grupo de expertos constituido al menos por un cardiólogo, un obstetra y un anestesiólogo, que realizan conjuntamente el consejo pregestacional, supervisan la evolución del embarazo y orientan en la toma de decisiones sobre el parto y el puerperio.
Las ediciones previas recogían las distintas escalas que permiten estimar el riesgo de complicaciones maternas y ofrecer consejo pregestacional, poniendo el énfasis en la clasificación modificada de la Organización Mundial de la Salud (mWHO). Como novedad de esta versión, la mWHO se considera la escala de riesgo de elección (I C), dado que predice mejor el riesgo materno que otras escalas, tanto en registros4 como en nuestro medio5. La guía incluye una estimación, en cada una de las cinco categorías, de la probabilidad de sufrir un evento adverso de origen cardiaco, y propone la frecuencia de controles durante el embarazo y el tipo de centro en el que deberían realizarse dichos controles o atenderse el parto según la categoría (véase la figura 3 de la guía). Como resumen del resto de escalas de riesgo publicadas, para estimar el riesgo tanto materno como fetal, la nueva guía también recoge una tabla con un conjunto de variables que pueden ayudar a predecir eventos, como el antecedente de tabaquismo o la elevación de péptidos natriuréticos (NT-proBNP) por encima de 128 pg/ml en la semana 20 de gestación.
Diagnóstico cardiovascular en el embarazoLa guía sigue enfatizando que es más difícil interpretar los signos clínicos que en las pacientes no gestantes y continúa basándose en las mismas pruebas diagnósticas (electrocardiograma, ecocardiografía y prueba de esfuerzo) para evaluar el riesgo de las mujeres con cardiopatía que desean concebir. En cuanto a las radiaciones ionizantes, se mantiene el principio de «usar la menor dosis de radiación posible» y se prefiere el abordaje radial con protección abdominal en caso de requerirse un cateterismo cardiaco.
Evaluación fetalEn cuanto a la valoración fetal, la guía se hace eco de la importancia creciente de la ecografía obstétrica a las 12 semanas, cuyas sensibilidad y especificidad para las cardiopatías congénitas mayores alcanzan el 85 y el 99% respectivamente. De hecho, un feto con una medida normal de translucencia nucal tiene un riesgo bajo de cardiopatía congénita (alrededor de 1/1.000). La guía incide en la recomendación de que esta exploración ha de hacerse (o corroborarse si ya se ha explorado) idealmente entre semanas 19 y 22 (I C), momento de máxima rentabilidad diagnóstica.
Intervenciones en la madre durante el embarazoLas consideraciones generales también incluyen las indicaciones de cirugía cardiaca o tratamiento percutáneo durante la gestación cuando sean necesarios por fracaso del tratamiento médico o porque la vida de la madre esté en peligro (IIb C). Tanto para tratamientos percutáneos como para la cirugía cardiaca, se aconseja esperar al segundo trimestre de gestación y, dada la gran mortalidad fetal, se aconseja realizar una cesárea antes de la cirugía después de la semana 26 (IIa C).
Momento y modo de partoSe reconoce el beneficio del parto vaginal (I C) y se considera la posibilidad de asistirlo mediante fórceps o ventosa para evitar los pujos maternos y acortar el periodo expulsivo. Se mantiene la indicación de cesárea electiva por motivos cardiacos de la versión anterior (IIa C) para las pacientes en situación de insuficiencia cardiaca grave, en tratamiento anticoagulante oral en el momento del parto, con dilatación significativa de la aorta ascendente, en presencia de estenosis aórtica grave o en el síndrome de Eisenmenger.
Una novedad de esta guía es que, basándose en el metanálisis de Mishanina6, se considera la inducción del parto de las gestantes cardiópatas después de la semana 40 (IIa C), cuya práctica no es habitual en nuestro medio. Dicho metanálisis incluye datos sobre más de 31.000 mujeres de la población general, y se pone de manifiesto una reducción de la mortalidad fetal del 50% entre las gestantes con parto inducido frente al parto espontáneo, y una reducción del 12% en la tasa de cesáreas urgentes, aunque no se estratifican los beneficios por edad gestacional. Sin embargo, en la literatura no se ha descrito mayor evidencia que apoye la inducción sistemática del parto de las gestantes cardiópatas con buena función cardiaca, sobre todo cuando haya expectativas de un parto de inicio espontáneo y este sea posible. Por ello, para estas gestantes, una vez informadas de las ventajas y los inconvenientes de la inducción del parto, podría considerarse el abordaje estándar con inducción una vez cumplida la semana 41. La guía actual se muestra menos explícita que en ediciones previas a la hora de señalar el momento necesario de finalizar el embarazo en los casos en que se produce un retraso del crecimiento fetal, dado que cada día que se prolonga la gestación entre las semanas 24 y 28 añade un 1% a la probabilidad de supervivencia fetal sin secuelas, que aumenta al 2% entre las semanas 29 y 32.
Otra novedad es la referente a los fármacos utilizados para la inducción del parto. Aunque no desaparece la referencia al riesgo teórico de vasoespasmo coronario, se considera que tanto el misoprostol como la dinoprostona son fármacos claramente seguros a las dosis habituales. Se sigue recomendando la infusión de 2 UI de oxitocina después del alumbramiento, seguida de una perfusión de 12 MUI/min durante 4h para disminuir el riesgo de hemorragia puerperal, evitando siempre la ergometrina y la prostaglandina F2alfa. No se aconseja la profilaxis antibiótica de la endocarditis en partos ni cesáreas.
Métodos anticonceptivos, interrupción del embarazo y fertilización in vitroEl consejo anticonceptivo ocupa un lugar relevante en esta nueva guía. Dado a las mujeres cardiópatas desde que alcanzan la menarquia por cardiólogos entrenados o ginecólogos, tiene como objetivo evitar los riesgos derivados de un embarazo no planificado. Los preparados con «solo progestágenos» aparecen como alternativas seguras a los anticonceptivos orales combinados, preparados estos que aumentan el riesgo de enfermedad tromboembólica. La anticoncepción de emergencia es segura en cualquier tipo de cardiopatía y los nuevos dispositivos intrauterinos con levonorgestrel, de menor tamaño y más fácil inserción, tienen indicación para mujeres con menstruaciones abundantes. La guía recoge cierto beneficio de la esterilización tubárica histeroscópica sobre la laparoscópica, si bien hoy no está exenta de cierta controversia, dada la posible asociación no confirmada con dolor pelviano crónico.
Finalmente, se añaden al texto consideraciones generales respecto a la reproducción asistida para pacientes con cardiopatía, y se destaca la necesidad de utilizar tratamientos de estimulación ovárica de baja dosis y, sobre todo, transfiriendo un solo embrión. Los tratamientos de fertilidad están contraindicados para las mujeres con mWHO clase IV y deberían considerarse con cautela para las mujeres con mWHO III o tratamiento anticoagulante.
CARDIOPATÍAS CONGÉNITAS E HIPERTENSIÓN PULMONARHipertensión pulmonar y síndrome de EisenmengerSe sigue desaconsejando la gestación a este grupo de pacientes (III), esta es la única recomendación con evidencia b. La estratificación de riesgo es igual a la de pacientes no gestantes y se propone que las pacientes sin tratamiento previo inicien terapias combinadas (IIa C), comenzando con sildenafilo oral; los antagonistas de la endotelina están contraindicados. Debería valorarse con cautela el uso de sildenafilo para pacientes con insuficiencia placentaria, dados los resultados de un estudio reciente en fetos con retraso del crecimiento fetal, en los que se objetivó un aumento de mortalidad intrauterina7.
En pacientes con tratamiento previo, se recomienda mantener los tratamientos endovenosos, y considerar la retirada de fármacos embriotóxicos (IIa C). Se debe considerar la anticoagulación con heparinas de bajo peso, especialmente en caso de enfermedad tromboembólica crónica (I C). El seguimiento debe ser muy estrecho y en centros especializados, incluso semanal en las últimas semanas de gestación, con valoración de la saturación y la función ventricular derecha en cada visita. Se recomienda la anestesia regional sobre la general y detallar un plan de parto con mantenimiento de las terapias en el puerperio. En caso de síndrome de Eisenmenger, la anticoagulación debe usarse con cautela por alteración en factores de la coagulación o trombocitopenia.
Cardiopatías congénitasExisten pocos cambios en las recomendaciones, que siguen basándose en opiniones de expertos. La indicación de intervención previa a la gestación en general no es diferente para las mujeres que consideran gestar que para las demás pacientes y se sigue recomendando que un cardiólogo fetal experto realice un ecocardiograma fetal en las semanas 19-22 (I C).
Comunicación interauricular: sigue sin recomendarse el cierre para prevenir la embolia paradójica, y se aconsejan prevención no farmacológica de la estasis venosa y el uso de filtros de aire.
Comunicación interventricular: se recomienda 1 o 2 evaluaciones durante la gestación para descartar hipertensión pulmonar.
Canal auriculoventricular: en esta guía se lo considera como mWHO II-III por el riesgo de arritmias y aumento de la insuficiencia de válvula auriculoventricular o aparición de insuficiencia cardiaca.
Coartación aórtica: se desaconseja la gestación en la recoartación grave y se recomienda tratar con stent recubierto solo si hay hipertensión refractaria o riesgo materno o fetal.
Defectos de la válvula pulmonar y tracto de salida derecho: en estas guías no se considera que haya un incremento del riesgo obstétrico, a diferencia de las previas. Para las estenosis graves sintomáticas pese al tratamiento, se debe considerar una valvuloplastia percutánea.
Tetralogía de Fallot: se recomienda el cribado materno de 22q11 para consejo genético (como debería realizarse en todas las cardiopatías troncoconales que afecten a la gestante). Si está bien reparada, se considera mWHO II y precisa seguimiento trimestral o más frecuente en caso de IP grave. Podría considerarse el parto precoz o valvular percutáneamente si no responden a tratamiento conservador.
Enfermedad de Ebstein: solo se desaconseja la gestación a las mujeres sintomáticas con cianosis con SatO2<85% o insuficiencia cardiaca (IIa C). Se debe vigilar la posible aparición de cianosis progresiva o embolia paradójica en mujeres con cortocircuito interauricular.
Transposición de grandes arterias: en caso de switch arterial, el riesgo parece bajo, con vigilancia de la neoaorta en caso de dilatación. A las pacientes con Mustard, Senning o transposición congénitamente corregida, se las considera en mWHO III y se debe vigilar la función ventricular, los síntomas y el ritmo cada 4-8 semanas. Se desaconseja la gestación en caso de insuficiencia tricuspídea sistémica grave, clase funcional de la New York Heart Association avanzada o disfunción del ventrículo sistémico<40% (IIa C).
Circulación de Fontan: alto riesgo (mWHO III o IV) por aparición de arritmias y deterioro de la clase funcional; gran incidencia de abortos, complicaciones fetales y sangrados periparto. Se recomienda el seguimiento mensual y, como novedad, valorar el tratamiento anticoagulante a dosis terapéuticas (IIa C), tras sopesar el riesgo hemorrágico. Se desaconseja la gestación en caso de SatO2<85%, disfunción ventricular, insuficiencia moderada o grave de válvula auriculoventricular, arritmias refractarias o enteropatía pierdeproteínas (III C).
Enfermedades aórticasEsta guía no introduce ninguna novedad relevante en el abordaje o el nivel de evidencia, si bien persevera en fomentar el tratamiento óptimo de estas pacientes.
Se recomienda un estudio completo de la aorta y el consejo pregestacional multidisciplinario para las mujeres con aortopatía o válvula bicúspide. Se desaconseja la gestación en casos de Ehlers-Danlos vascular, aortopatías hereditarias con diámetro>45mm, válvulas bicúspides>50mm (> 27mm/m2), en el síndrome de Turner con>25mm/m2 y en caso de antecedentes de disección (III C). Sin embargo, se echa en falta un aspecto tan relevante como las recomendaciones de cirugía profiláctica pregestacional según el diámetro aórtico, y se deduce que deben aplicarse las guías generales para la enfermedad aórtica.
Durante el embarazo se recomienda seguimiento ecográfico cada 4-12 semanas hasta los 6 meses posparto (I C). Se mantiene la indicación de cesárea cuando el diámetro aórtico sea>45mm o haya antecedente de disección (IIa C) y se desaconseja la ergometrina (III C). Un aspecto más controvertido por la falta de nueva evidencia al respecto es la reducción del diámetro aórtico a>45mm (anteriormente>50mm) para indicar cirugía profiláctica durante el embarazo cuando el diámetro aumente rápidamente (IIa C) y además esta velocidad de progresión no se defina. En caso de una cirugía necesaria, si el feto es viable, debería considerarse el parto previo a ella (IIa C). El tratamiento con bloqueadores beta se generaliza en las aortopatías hereditarias (IIa C) y, concretamente, en el síndrome de Ehlers-Danlos vascular (I C) se recomienda específicamente celiprolol.
VALVULOPATÍASSobre las pacientes con estenosis mitral, se recuerda que la gestación puede desencadenar inestabilidad hemodinámica a pacientes previamente asintomáticas8. Asimismo, se especifica la recomendación de intervención para pacientes con área valvular mitral<1cm2 antes de la gestación (I C), y debería considerarse cuando el área sea<1,5cm2 (IIa C), preferentemente mediante intervencionismo percutáneo si es posible.
En la estenosis aórtica muy sintomática sin posibilidad de valvuloplastia con balón, se cita la alternativa novedosa, aunque con poca experiencia, de implante percutáneo de prótesis aórtica.
En la insuficiencia mitral, el problema se centra en las gestantes con insuficiencia moderada o grave, que constituyen el grupo de riesgo de aparición de insuficiencia cardiaca durante el embarazo. Las mujeres con insuficiencia mitral grave con síntomas o disfunción del ventrículo izquierdo constituyen el grupo de alto riesgo.
FIBRILACIÓN AURICULAR VALVULAR (VÁLVULAS NATIVAS)Dado el alto riesgo tromboembólico asociado con la gestación, se recomienda el inicio inmediato de anticoagulación con heparina de bajo peso molecular (HBPM) a dosis terapéuticas, sin empezar con heparina no fraccionada como se mencionaba en la guía previa, y cambiar en el segundo trimestre a anticoagulante oral, manteniendo la INR en los intervalos habituales. Se recalca la contraindicación de usar los nuevos anticoagulantes orales (ACO) no dependientes de la vitamina K durante la gestación.
PRÓTESIS VALVULARESEste apartado ha ganado protagonismo, la tabla de recomendaciones se amplía y se añaden diagramas de flujo para ayudar a la comprensión del tratamiento anticoagulante durante la gestación.
Se enfatiza de nuevo la importancia del equipo multidisciplinar, en la elección del tipo de prótesis valvular para las mujeres que desean gestar (I C). La recomendación de elección de prótesis biológica ante el deseo de gestar cambia a clase IIa C.
El embarazo de portadoras de prótesis mecánica se sigue considerando de alto riesgo para la gestante y el feto debido al tratamiento anticoagulante9, y se precisa una estrecha monitorización de la INR, el TTPa o los anti-Xa. Se insiste en que el tratamiento con heparina implica mayor riesgo de trombosis protésica.
En cuanto al tratamiento con HBPM, están por resolver las concentraciones de anti-Xa óptimas en esta población, así como la importancia del valor pico frente a otros. Una nueva recomendación IIb indica la posibilidad de monitorizar la concentración de anti-Xa antes de administrar HBPM, además de las 4-6h tras el tratamiento. Cabe resaltar la recomendación de distintos objetivos de anticoagulación para la HBPM y para los ACO en función de la localización y el tipo de prótesis o la existencia de factores de riesgo de trombosis añadidos.
Las distintas pautas terapéuticas se describen en forma de diagramas de flujo que facilitan su comprensión, según se precise una dosis baja o alta de ACO para la INR objetivo, y se insiste en que los cambios en el régimen de anticoagulación deberían realizarse en un medio hospitalario (I C).
Se remarca que es necesario planificar el parto de estas pacientes, e incluso se recomienda anticipar el momento del parto para asegurar un régimen seguro de anticoagulación periparto (I C). El parto vaginal es posible siempre y cuando se realice previamente el cambio a heparina endovenosa y se considera la cesárea como una buena opción, especialmente para las pacientes con alto riesgo de trombosis protésica, para minimizar el tiempo sin ACO. Se recomienda también si el parto ocurre cuando la paciente está en tratamiento con ACO o hayan pasado menos de 2 semanas desde su interrupción (I C).
ENFEMEDAD CORONARIAEl espacio dedicado a la enfermedad coronaria (EC) es mucho mayor que en la guía previa, y se indica que más del 20% de las muertes cardiacas maternas obedecen a EC9. Para el infarto se aconseja un abordaje multidisciplinario con intensivistas, obstetras y cardiólogos. En el infarto agudo con elevación del segmento ST, se recomienda angioplastia primaria con la posibilidad de utilizar stents farmacoactivos. Se añade a las recomendaciones la posibilidad del abordaje invasivo en el infarto agudo sin elevación del segmento ST con criterios de alto riesgo (IIa C). Pueden usarse ácido acetilsalicílico y clopidogrel (este último, el menor tiempo posible). No se recomienda el uso de antiagregantes de mayor potencia (prasugrel y ticagrelor).
MIOCARDIOPATÍAS E INSUFICENCIA CARDIACANo hay modificaciones en el tratamiento de pacientes con miocardiopatía dilatada o hipertrófica respecto a guías previas. Únicamente cabe destacar el tratamiento con bromocriptina en la miocardiopatía periparto, que se recomienda de al menos 1 semana o más si la fracción de eyección es<25% (IIb B)9. Se desaconseja un nuevo embarazo si la fracción de eyección no se recupera. El tratamiento de la insuficiencia cardiaca debe mantenerse al menos 6 meses aunque la función ventricular se recupere.
INSUFICIENCIA CARDIACA DURANTE Y DESPUÉS DEL EMBARAZOEste apartado también ha ganado relevancia en esta guía. El texto es más extenso, se amplían aspectos relativos al tratamiento, los dispositivos y el trasplante cardiaco. Asimismo se añaden diagramas de flujo sobre el tratamiento de la insuficiencia cardiaca aguda en el embarazo y el posparto para una mejor comprensión.
Destaca que, en caso de inestabilidad hemodinámica o shock, se recomienda el traslado urgente a una unidad especializada en cuidados agudos cardiológicos con posibilidad de asistencia circulatoria mecánica (IIa C). En estos casos se recomienda considerar la cesárea. En el caso específico de la miocardiopatía periparto, es preferible usar levosimendán como inotrópico por la mayor toxicidad de los agonistas beta.
En caso de insuficiencia cardiaca aguda o subaguda, se recuerda evitar los fármacos fetotóxicos (inhibidores de la enzima de conversión de la angiotensina [IECA], antagonistas del receptor de la angiotensina II [ARA-II], inhibidores de la neprilisina o antagonistas del receptor de mineralocorticoides), y se recomienda usar hidralazina y nitratos; se debe restringir el empleo de diuréticos a casos con congestión pulmonar y usar bloqueadores selectivos ↓1, iniciándolos con precaución. Las indicaciones de anticoagulación son similares que fuera del embarazo (disfunción grave, fibrilación auricular, etc.). Se sigue desaconsejando la lactancia en la insuficiencia cardiaca grave (IIb B).
ARRITMIASEn este apartado, es novedoso el cuadro de recomendaciones sobre el nivel de vigilancia y las acciones necesarias durante el parto en función del riesgo de deterioro hemodinámico. No existen novedades en el tratamiento farmacológico. Se sigue considerando que la cardioversión eléctrica es una técnica segura en caso de inestabilidad hemodinámica (I C). La ablación con catéter de las arritmias supraventriculares pasa a ser una recomendación IIa C9, preferiblemente tras el segundo trimestre. El implante de marcapasos o desfibrilador puede realizarse con seguridad a partir de la octava semana (I C).
TRASTORNOS HIPERTENSIVOSLos trastornos hipertensivos siguen ocasionando los problemas médicos más frecuentes en madre y feto (un 5-10% de las gestaciones). La definición de hipertensión arterial (HTA) en la gestación sigue siendo una presión arterial sistólica (PAS) ≥ 140 o diastólica (PAD) ≥ 90mmHg y, a pesar de la falta de evidencia, se mantienen las indicaciones de tratamiento farmacológico si la presión arterial es ≥ 150/95mmHg o ≥ 140/90mmHg si se presenta con factores de riesgo asociados. El riesgo-beneficio del tratamiento de la hipertensión10 está relacionado con una menor incidencia de HTA grave materna, preeclampsia y eventos fetales, pero sigue sin haber evidencia sobre cuáles son la cifras objetivo del tratamiento.
En cuanto a los test de laboratorio habituales relacionados con la HTA (hemoglobina, plaquetas, transaminasas, función renal y proteinuria), se cita por primera vez el test predictivo del cociente sFlt1:PIGF (factor de crecimiento placentario) ≤ 38, que excluye el diagnóstico de sospecha de preeclampsia11, aunque todavía tiene escasa difusión clínica.
Respecto a la prevención farmacológica de la preeclampsia, se tratan varios aspectos controvertidos:
- •
El ácido acetilsalicílico (100-150mg/día) desde la semana 12 a la 36-37ha pasado a recomendarse sistemáticamente para las mujeres con un criterio de riesgo alto (HTA previa, enfermedad renal o autoinmunitaria, diabetes mellitus tipos 1 y 2) o al menos 2 criterios de riesgo moderado (primer embarazo, embarazo múltiple, edad>40 años, gestación previa más de 10 años antes, índice de masa corporal>35, antecedente familiar de preeclampsia)12.
- •
En cuanto al suplemento de calcio (1,5-2g/día), se recomienda únicamente si la ingesta habitual es baja (< 600mg/día) desde la visita antenatal. Sin embargo, las vitaminas C y D no solo no la previenen, sino que aumentan el riesgo de bajo peso fetal y problemas perinatales.
- •
No hay evidencia de que los tratamientos de fertilidad aumenten el riesgo.
En el tratamiento no farmacológico de la HTA, se sigue considerando de escasa eficacia la dieta pobre en sal y se sigue recomendando limitar la ganancia de peso de las mujeres obesas a 6,8kg. Respecto al tratamiento farmacológico, siguen siendo de elección los bloqueadores beta (labetalol y metoprolol), el alfa-metildopa y los antagonistas del calcio (nifedipino) para la HTA moderada. No hay novedades en el tratamiento de la HTA grave definida empíricamente por cifras ≥ 170/110mmHg, para la que siguen estando indicados el labetalol endovenoso, el alfa-metildopa y los antagonistas del calcio orales, y puede emplearse el urapidilo endovenoso. En las crisis hipertensivas con edema pulmonar, se mantiene de elección la nitroglicerina endovenosa y, en caso de convulsiones, el sulfato de magnesio.
TROMBOEMBOLIA VENOSA DURANTE EL EMBARAZO Y EL PUERPERIOSe produce tromboembolia venosa en estos periodos hasta en el 0,2% de las gestaciones. La tromboembolia pulmonar sigue siendo una de las principales causas de morbimortalidad, con una elevada recurrencia asociada con diversos factores de riesgo identificables. La prevención se extiende a los periodos antenatal, gestacional y posparto, e informar a la paciente en riesgo es una recomendación de clase I. En esta guía no hay modificaciones respecto a la prevención o el tratamiento de los eventos tromboembólicos.
En la prevención, el fármaco de elección es la HBPM en dosis guiadas por el peso corporal (enoxaparina 0,5 UI/kg/día o dosis equivalentes de dalteparina o fondaparinux), que permiten alcanzar mejor la concentración de inhibidores del factor Xa adecuada, especialmente a las mujeres obesas. La farmacocinética varía considerablemente durante la gestación y puede requerirse aumentar la dosis hasta un 50%. Debe continuarse el tratamiento profiláctico en el periodo puerperal, 6h si el parto es vaginal y 12h tras una cesárea.
Para el diagnóstico de trombosis venosa profunda en la gestante, la técnica de elección es la ecografía de compresión bilateral. Si se realiza en series a mujeres con diagnóstico de sospecha, tiene un elevado valor predictivo negativo13, aunque es más eficaz en la trombosis proximal que en la distal y la pelviana. El dímero D no es específico, ya aumenta progresivamente durante la gestación. El diagnóstico clínico de tromboembolia pulmonar es difícil, y más en este contexto, por lo que debe confirmarse con las pruebas de imagen que sean necesarias. Respecto al tratamiento de la trombosis venosa profunda o la tromboembolia pulmonar, también es de elección la HBPM a dosis terapéuticas (enoxaparina 1mg/kg/12h o equivalentes).
Para la gestante con tratamiento anticoagulante, el parto debe planearse próximo a la semana 39 para hacer posible una reversión parcial con sulfato de protamina o la sustitución por heparina no fraccionada endovenosa. Si el riesgo hemorrágico es alto, la adición de oxitocina en el tercer estadio del parto se asocia con una menor pérdida hemática sin ocasionar deterioro hemodinámico14.
MEDICACIÓN DURANTE EL EMBARAZO Y LA LACTANCIADestaca la ausencia de recomendaciones uniformes en este apartado. Antes de comenzar un tratamiento farmacológico durante el embarazo, la guía remite a una tabla con datos sobre la seguridad clínica de la administración de fármacos o a verificarlo a través de entornos web bien establecidos. En caso de que no haya información adecuada sobre la seguridad de la administración a humanos, la decisión debe tomarse valorando el perfil de seguridad y eficacia del fármaco, todo ello consensuado con la paciente (IIa C). La guía no recomienda las decisiones basadas en las categorías de la FDA (III C).
No deja de ser llamativo que los fármacos más empleados habitualmente en cardiología estén totalmente contraindicados (estatinas, IECA/ARA-II, inhibidores de la aldosterona) o desaconsejados (atenolol) en el embarazo.
CONCLUSIONESLa nueva guía enfatiza el beneficio de estratificar el riesgo de las gestantes con cardiopatía según la clasificación mWHO. Las mujeres con riesgo de complicaciones moderado o alto durante el embarazo (mWHO II-III, III y IV) deberían recibir consejo pregestacional y tratamiento durante la gestación por un equipo multidisciplinar. El abordaje durante la gestación debe individualizarse en función del riesgo materno y en centros expertos cuando así lo requieran. Asimismo se insiste en el parto vaginal siempre que no haya una contraindicación formal cardiológica. El tratamiento médico siempre deberá valorarse en función de los datos actuales de seguridad preclínica, y no se recomienda el uso de la clasificación de la FDA.
CONFLICTO DE INTERESESNo se declara ninguno.
Grupo de Trabajo de la SEC para la guía ESC 2018 sobre el tratamiento de las enfermedades cardiovasculares durante el embarazo: Manuel Jiménez Navarro (coordinador), Laura Galian-Gay (coordinadora), Pablo Avanzas, Sara Ballesteros, Ana González García, Ernesto González Mesa, Isaac Martínez Bendayán, Antonia Pijuan Domenech, Raquel Prieto y M. Teresa Subirana.
Revisores expertos para la guía ESC 2018 sobre el tratamiento de las enfermedades cardiovasculares durante el embarazo: José Luis Bartha, Juan Caro, Juan Luis Delgado, Begoña Manso, Sandra Rosillo y J. Ignacio Zabala.
Comité de Guías de la SEC: Fernando Alfonso, Borja Ibáñez, Fernando Arribas, Gemma Berga Congost, Héctor Bueno, Arturo Evangelista, Ignacio Ferreira-González, Manuel Jiménez Navarro, Francisco Marín, Leopoldo Pérez de Isla, Antonia Sambola, Rafael Vázquez y Ana Viana-Tejedor.