En el presente artículo se comenta la guía sobre el tratamiento de las dislipemias recientemente publicada por la Sociedad Europea de Cardiología en conjunto con la European Atherosclerosis Society1. El Comité de Guías de la Sociedad Española de Cardiología (SEC) formó un grupo de trabajo compuesto por miembros de la SEC para realizar este comentario, con el objetivo de resaltar los aspectos más importantes y adaptarla a nuestra realidad. A continuación, y siguiendo el mismo orden de apartados que ofrece la guía, se comentarán sus aspectos más importantes.
PREVENCIÓN CARDIOVASCULAREn esta nueva guía existen pocas novedades con respecto a la prevención cardiovascular. Se mantiene el interés por la prevención de la enfermedad cardiovascular ateroesclerótica tanto poblacional, mediante la promoción de hábitos de vida saludables, como individual, mediante el control de los factores de riesgo cardiovascular y, muy especialmente, del colesterol unido a lipoproteínas de baja densidad (cLDL).
RIESGO CARDIOVASCULARLa herramienta SCORE sigue siendo el sistema recomendado para evaluar el riesgo cardiovascular, aun con sus limitaciones (p. ej., no es aplicable a menores de 40 años y está muy influida por la edad, aunque sube hasta los 70 años). En esta edición se recalculan al alza los riesgos y se plantea el riesgo relativo y el riesgo estimado por edad como herramientas para intensificar recomendaciones sobre hábitos de vida para personas jóvenes. Como novedad, una llamada al juicio clínico para evitar el sobretratamiento de personas de edad avanzada. Se destacan nuevos aspectos referidos a los factores modificadores del riesgo estimado: primero, la advertencia de no usar cifras de colesterol unido a lipoproteínas de alta densidad (cHDL)> 90mg/dl en el cálculo del riesgo por SCORE, puesto que parece que incrementan (y no disminuyen) el riesgo de eventos cardiovasculares agudos. Segundo, la inclusión del hígado graso no alcohólico como modificador al alza del riesgo. Finalmente, la reivindicación de las pruebas de imagen cardiovasculares no invasivas (calcio coronario2, ultrasonografía carotídea o femoral y angiografía mediante tomografía computarizada) como herramientas para la reclasificación de personas con riesgo bajo o medio e indicación IIa B.
Las categorías de riesgo cardiovascular incluyen novedades que afectan a la población con diabetes mellitus (DM) e hipercolesterolemia familiar (HF): mientras que en ediciones anteriores se consideraba a los diabéticos (de tipos 1 y 2) en riesgo alto o muy alto, en la presente se ha producido una reclasificación «a la baja» que se comenta en apartados posteriores. La lesión de órgano diana se especifica como la existencia de microalbuminuria, retinopatía o neuropatía. Esta reclasificación, orientada hacia objetivos terapéuticos de cLDL, no está comentada ni referenciada por los autores y tampoco está justificada por cambios en la evidencia, por lo que creemos que se basa en la presunción de que los diabéticos con un riesgo elevado son equivalentes de enfermedad cardiovascular establecida. Por otra parte, por primera vez se ha incluido a pacientes con HF en las categorías de riesgo muy alto (HF con enfermedad cardiovascular ateroesclerótica u otro factor de riesgo) y alto (HF sin otros factores de riesgo). Se debe decir que esta categorización, sin considerarla desacertada, tampoco tiene referencias en la guía. Por último, se destaca la importancia que este documento da a la determinación de la lipoproteína (a), al menos una vez en la vida, en pacientes con historia familiar de enfermedad cardiovascular prematura y para reclasificación al alza de pacientes con riesgo moderado. Una vez más, sorprende que en el apartado que hace referencia a la edad vascular se expliquen métodos rudimentarios para su uso cuando Cuende et al.3 ya publicaron el método científico para estimarla.
LÍPIDOS Y LIPOPROTEÍNASLa nueva guía defiende el papel causal de las lipoproteínas que contienen alipoproteína B (apoB) (LDL, lipoproteínas de muy baja densidad [VLDL] y sus remanentes) en el desarrollo y la progresión de la enfermedad cardiovascular4, y que debe concretarse en la medición del cLDL, ya sea en ayunas o no. Se considera habitual la medición en plasma del colesterol total y el cHDL (ambos valores necesarios para calcular el SCORE), así como de triglicéridos. No hay comentarios respecto a la utilidad de los cocientes lipoproteicos y se mantienen las recomendaciones sobre el valor del colesterol no-HDL y la apoB (gana relevancia) para la evaluación de riesgo, particularmente en población con hipertrigliceridemia, DM, obesidad y cLDL muy bajo. Llama la atención que, aunque se reconozca implícitamente la importancia de las partículas lipoproteicas, no se mencione la determinación del número de partículas como parámetro adicional5. También se comenta la polémica de la determinación en ayunas o no. En principio, las muestras no en ayunas pueden tener el mismo valor pronóstico que las muestras en ayunas, teniendo en cuenta la elevación de los triglicéridos en 27mg/dl de media.
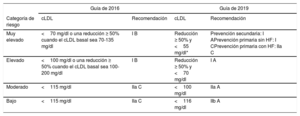
OBJETIVOS TERAPÉUTICOSUna de las principales novedades de la guía son los cambios en los objetivos terapéuticos. Salvo para los pacientes con un riesgo cardiovascular bajo, en el resto de las categorías de riesgo los objetivos de cLDL, que sigue siendo el objetivo principal en el tratamiento de los pacientes con dislipemia, se han vuelto más estrictos (tabla 1)6. Es interesante destacar que en esta guía se han establecido diferentes objetivos de LDL para el riesgo moderado y el riesgo bajo, a diferencia de guías previas en las se recomendaban los mismos objetivos de LDL para ambos niveles de riesgo. Para hacer estas recomendaciones, los autores no solo se han basado en los resultados de los ensayos clínicos, sino también en otro tipo de estudios. Reconocen como limitación que la mayoría de estos estudios no tenían un objetivo concreto de cLDL, sino que la reducción del cLDL obtenida con el tratamiento hipolipemiante (no solo con las estatinas) se asociaba con una reducción de los eventos. Ahora bien, las evidencias son lo suficientemente robustas para afirmar que el cLDL es un factor causal; que cuanto más bajo, mejor; que cuanto antes se consiga, mucho mejor, y que los objetivos propuestos son seguros. La guía también propone como objetivos secundarios el colesterol no-HDL y la apoB.
| Guía de 2016 | Guía de 2019 | |||
|---|---|---|---|---|
| Categoría de riesgo | cLDL | Recomendación | cLDL | Recomendación |
| Muy elevado | <70 mg/dl o una reducción ≥ 50% cuando el cLDL basal sea 70-135 mg/dl | I B | Reducción ≥ 50% y <55 mg/dl* | Prevención secundaria: I APrevención primaria sin HF: I CPrevención primaria con HF: IIa C |
| Elevado | <100 mg/dl o una reducción ≥ 50% cuando el cLDL basal sea 100-200 mg/dl | I B | Reducción ≥ 50% y <70 mg/dl | I A |
| Moderado | <115 mg/dl | IIa C | <100 mg/dl | IIa A |
| Bajo | <115 mg/dl | IIa C | <116 mg/dl | IIb A |
cLDL: colesterol unido a lipoproteínas de baja densidad, HF: hipercolesterolemia familiar.
Lógicamente, estos objetivos terapéuticos más estrictos implicarán la necesidad de intensificar el tratamiento hipolipemiante. Para facilitar la consecución de los objetivos en prevención secundaria, la SEC ha propuesto recientemente unos algoritmos prácticos en los que se indican los cambios terapéuticos que realizar según las características clínicas del paciente, el tratamiento hipolipemiante que esté tomando y el cLDL del paciente en el momento de ser atendido7. Es importante destacar que la guía no ha incluido la categoría denominada «de riesgo extremo», a diferencia de otras guías recientes, sino que mantienen la «de muy alto riesgo», aunque recomienda alcanzar los valores de LDL de la categoría de riesgo extremo. Esta categoría no distingue, por ejemplo, a un paciente con un síndrome coronario agudo y enfermedad arterial periférica del que solo haya presentado un síndrome coronario agudo o que tenga afectación de varios territorios vasculares. Tampoco se ha incluido en alto riesgo a los pacientes con eventos antes de los 55 (varones) y los 65 años (mujeres), sino que lo consideran solo modificador de riesgo. Por otra parte, la nueva guía establece los mismos objetivos de control lipídico para mujeres y varones, a pesar de que las cifras generales de mortalidad cardiovascular son mayores en las mujeres.
ESTILOS DE VIDA PARA MODIFICAR LOS LÍPIDOSLa guía remarca la necesidad de políticas preventivas sociales y de hábitos de vida8. La evidencia indica que una dieta de tipo mediterránea se asocia con una menor incidencia de eventos cardiovasculares. Se sigue haciendo hincapié en el estudio PREDIMED9, que señala la efectividad de la dieta mediterránea, suplementada con aceite de oliva virgen extra o nueces, para reducir los eventos cardiovasculares. Si bien se sigue enfatizando que evitar el consumo de grasas trans es una medida clave en la prevención dietética de las enfermedades cardiovasculares, la magnitud del efecto de esta intervención desciende ligeramente de> 10% (+++) a un 5-10% (++) tanto para bajar las cifras de colesterol total y cLDL como para aumentar las de cHDL. Lo mismo ocurre con el consumo de grasas saturadas: se insiste en su papel fundamental para disminuir los valores de cLDL, pero la magnitud de su impacto también desciende en la misma medida10. La mayor diferencia se encuentra en los cambios en el estilo de vida para disminuir los triglicéridos, al reducirse el efecto de la reducción del exceso de peso de> 10% (+++) a <5% (+)11 y mantenerse el del ejercicio físico (++). Se aboga por recomendar patrones nutricionales (dieta DASH, mediterránea), en contraposición con ediciones previas en las que se hacía hincapié en los porcentajes de nutrientes.
FÁRMACOS PARA EL TRATAMIENTO DE LA HIPERCOLESTEROLEMIAUna de las principales novedades respecto a guías previas es que agrupa todos los fármacos para el tratamiento de las dislipemias bajo un único epígrafe, sin separarlos por sus efectos más relevantes (hipercolesterolemia, hipertrigliceridemia o efecto en el cHDL).
EstatinasEn este apartado se enfatiza que las estatinas son capaces de producir una reducción de hasta un 50% en las cifras de cLDL y que pueden combinarse con otros hipolipemiantes. Las estatinas reducen la morbimortalidad. La reducción del cLDL en 1 mmol/l (40 mg/dl) conlleva una reducción del 22% en los eventos cardiovasculares mayores, del 23% en los eventos coronarios, del 20% en la muerte coronaria, del 17% en los ictus y del 10% en la mortalidad total a 5 años. Los beneficios más relevantes se producen durante el primer año de tratamiento. Como limitaciones, destaca la falta de demostración de un claro beneficio en pacientes en hemodiálisis o con insuficiencia cardiaca. Las estatinas poseen un efecto de clase. La elección de una u otra depende del riesgo basal y de los objetivos que deban alcanzarse en un determinado paciente, siempre teniendo en cuenta que la respuesta a las estatinas varía entre individuos, además de las comorbilidades y el uso de otros fármacos.
En cuanto a sus efectos secundarios, la miopatía es el efecto clínico más relevante y la rabdomiolisis es el más grave. Siguiendo las recomendaciones de la guía, si la creatincinasa (CK) se sitúa por debajo de 10 veces el límite superior de la normalidad y el paciente no tiene síntomas, se puede seguir usando estatinas. Si es inferior a 10 veces pero el paciente tiene síntomas, se deben interrumpir o bajar la dosis, y por encima de 10 se deben interrumpir y medir la CK cada 2 semanas. La guía distingue por primera vez la miopatía de síntomas musculares asociados con estatinas y se refieren al efecto «nocebo» de las estatinas en estudios observacionales. Por otra parte, de nuevo defiende que el beneficio en reducción de riesgo compensaría el posible efecto diabetogénico, con un aumento de nuevos casos de diabetes.
Inhibidores de la absorción de colesterolEste apartado repasa los mecanismos de acción, eficacia, efecto en la morbimortalidad y efectos adversos de la ezetimiba. Se destaca la eficacia sinérgica con las estatinas, con los secuestradores biliares y, lo más reciente, con los inhibidores de la proproteína convertasa subtilisina/kexina tipo 9 (iPCSK9). En cuanto a sus indicaciones, la ezetimiba escala posiciones, en muchas ocasiones está indicada como clase I cuando con estatinas a dosis máxima tolerada no se alcanza el objetivo, a diferencia de ediciones anteriores, en que la recomendación era IIa. Quizá, y después de tantos años sin moléculas nuevas ni futuras, el apartado se debería llamar «ezetimiba», más que «inhibidores de la absorción», ya que es el único representante de su grupo.
Inhibidores de la proproteína convertasa subtilisina/kesina tipo 9Se ha demostrado que los iPCSK9 reducen los eventos cardiovasculares en pacientes con riesgo alto/muy alto12,13. Son fármacos muy efectivos reduciendo el cLDL (60%) y se han mostrado capaces de modificar también la lipoproteína (a), aunque se desconoce el mecanismo y el efecto de su reducción. En prevención secundaria o HF de muy alto riesgo que no alcanza los objetivos tras estatinas a altas dosis y ezetimiba, han pasado a tener nivel de recomendación I A. Este es el aspecto más positivo, que en la guía previa aparecía como IIb. Actualmente en España solo se financia para pacientes con cLDL> 100mg/dl. A raíz de esta guía, la financiación debería ampliarse, ya que los pacientes con muy alto riesgo y cLDL 55-100mg/dl presentan un riesgo residual muy elevado14,15. Por lo tanto, los iPCSK9 son unos de los fármacos que más han aportado desde las guías previas y pasan a tener un nivel de recomendación I para los pacientes con muy alto riesgo tras tratamiento con estatinas y ezetimiba. Es importante destacar las limitaciones existentes en nuestro sistema público de salud para la financiación de este grupo terapéutico.
FibratosEn la dislipemia diabética con pemafibrato, un nuevo modulador selectivo de los PPAR-α, la guía hace referencia al estudio PROMINENT16. Por otra parte, sigue poniendo en cuestión el beneficio cardiovascular de los fibratos a pesar de que los 6 estudios ya publicados reflejaran una reducción del riesgo cardiovascular proporcional a la del colesterol no-HDL. Sin embargo, resta importancia a los efectos secundarios de los fibratos destacando el riesgo de miopatía y dedicando menos espacio a la relevancia del incremento de la creatinina sérica y la homocisteína. Los fibratos, especialmente el fenofibrato, siguen siendo fármacos ampliamente utilizados en España en la dislipemia mixta, en combinación con estatinas.
Ácidos grasos n–3En este apartado destaca un comentario sobre la eficacia de los ácidos grasos n-3 en la reducción de la concentración de triglicéridos como resultado del estudio EVOLVE II17. Respecto al efecto en la mortalidad y la morbilidad cardiovascular, se detallan los resultados de un metanálisis Cochrane que muestra efecto nulo, excepto para la enfermedad coronaria18, resultados similares a los de otros estudios publicados. Los efectos beneficiosos de los n-3 parecen depender de la dosis utilizada. El estudio REDUCE-IT sí que evidenció una reducción del riesgo relativo en los pacientes de alto riesgo con triglicéridos elevados y en tratamiento con estatinas, pero empleando 2g 2 veces al día19.
Estrategias terapéuticasEl documento sigue abogando por una estrategia terapéutica secuencial para el control del cLDL: estatinas de alta intensidad, ezetimiba y finalmente iPCSK9, a partir de la evidencia científica. Considerando los numerosos datos que establecen la causalidad de las LDL y que el beneficio terapéutico está asociado con la reducción del cLDL, se debería haber propuesto estrategias más novedosas, como las combinaciones terapéuticas orientadas a alcanzar los objetivos20. Aunque se menciona esta posibilidad indicando la reducción de riesgo según la eficacia hipolipemiante de tratamientos diversos, creemos que se ha perdido una buena oportunidad para cambiar el paradigma terapéutico. En este punto es importante dar a conocer que la SEC ha elaborado un consenso para, de una manera práctica, favorecer la consecución de los objetivos terapéuticos en prevención secundaria7.
Perspectivas futurasAunque la respuesta a las estatinas es individual, se pueden clasificar en función de su capacidad para reducir el cLDL (alta intensidad, reducción ≥ 50%; intensidad moderada, 30-50%). Si bien se han descrito efectos pleotrópicos, el beneficio en la prevención de los eventos cardiovasculares depende fundamentalmente de su capacidad para reducir el cLDL. Los efectos en el cHDL es discreto (elevaciones de un 1-10%), algo mayor en los triglicéridos (descenso del 10-20%, sobre todo con las estatinas más potentes) y marginal en la lipoproteína (a).
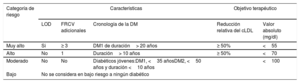
TRATAMIENTO DE LAS DISLIPEMIAS EN DIFERENTES SITUACIONES CLÍNICASPaciente diabéticoLa guía propone una reclasificación del riesgo en DM y unos objetivos diferentes de los recomendados en 2016. La nueva clasificación se muestra en la tabla 2. Los objetivos de cLDL son más estrictos que en guías anteriores. Por otra parte, el colesterol no-HDL y la apoB son marcadores de las lipoproteínas aterógenas y se consideran objetivos secundarios importantes: objetivo de colesterol no-HDL <2,6 mmol/l (< 100mg/dl) y apoB <80mg/dl en individuos con alto riesgo; colesterol no-HDL <2,2 mmol/l (< 85mg/dl) y apoB <65mg/dl en individuos con muy alto riesgo. El primer escalón terapéutico debe ser las estatinas. La ezetimiba es especialmente eficaz en la población diabética, con una reducción relativa de riesgo del 15% y absoluta del 5,5%. Los iPCSK9 son al menos igual de eficaces en diabéticos, incluso se ha demostrado que proporcionan una disminución del 2,7% del riesgo absoluto de eventos mayores a 3 años frente a población no diabética. En cuanto a los pacientes con DM1, las guías indican que el perfil aterogénico de la DM1 presenta triglicéridos y cLDL bajos, pero con el colesterol no-HDL en el límite superior o elevado. Se debe a que la insulina subcutánea acelera en el tejido adiposo el recambio de VLDL. Las estatinas están recomendadas para toda DM1 de riesgo alto o muy alto. Es decir, solo se dejaría de recomendar las estatinas para pacientes con DM1 jóvenes (< 35 años) y con menos de 10 años de duración de la enfermedad y sin otros factores de riesgo cardiovascular. No hay diferencias por sexo y el beneficio cardiovascular es similar al obtenido en pacientes con DM2.
Estratificación del riesgo cardiovascular y objetivos terapéuticos para pacientes diabéticos
| Categoría de riesgo | Características | Objetivo terapéutico | |||
|---|---|---|---|---|---|
| LOD | FRCV adicionales | Cronología de la DM | Reducción relativa del cLDL | Valor absoluto (mg/dl) | |
| Muy alto | Si | ≥ 3 | DM1 de duración> 20 años | ≥ 50% | <55 |
| Alto | No | 1 | Duración> 10 años | ≥ 50% | <70 |
| Moderado | No | No | Diabéticos jóvenes:DM1, <35 añosDM2, <50 años y duración <10 años | <100 | |
| Bajo | No se considera en bajo riesgo a ningún diabético | ||||
cLDL: colesterol unido a lipoproteínas de baja densidad; DM1: diabetes mellitus tipo 1; DM2: diabetes mellitus tipo 2; FRCV: factores de riesgo cardiovascular; LOD: lesión de órgano diana.
Se resalta la necesidad de un tratamiento intensivo, precoz y prolongado con estatinas de alta intensidad. Se debe realizar un perfil lipídico basal lo antes posible (no es necesario que sea en ayunas). Tras un síndrome coronario agudo, debe alcanzarse tanto una reducción del 50% del cLDL como un objetivo <55mg/dl, es decir, ambos objetivos de reducción relativa y absoluta. En caso de recurrencia de eventos antes de los 2 años de tratamiento con estatinas, el objetivo debe ser <40mg/dl. Estos valores se basan en la seguridad que han demostrado los estudios con iPCSK912,13, con cifras muy bajas de cLDL sin complicaciones, y en la hipótesis de que cuanto más bajo, mejor. Es necesario lograr los objetivos lo más precozmente posible (4-6 semanas), incluso iniciar el tratamiento con iPCSK9 antes del alta si el cLDL antes del síndrome coronario agudo no estaba en objetivo con dosis de estatinas/ezetimiba máximas.
Es esencial incluir a los pacientes en un programa de rehabilitación cardiaca en el que se utilice un abordaje completo del riesgo vascular mediante ejercicio, formación, dieta, cambio de estilo de vida y todas las herramientas farmacológicas disponibles, incluidos los iPCSK9. Por lo tanto, tras un síndrome coronario agudo se insiste más en la reducción de cLDL absoluta y relativa lo más precozmente posible, iniciando el tratamiento durante el ingreso.
Accidente cerebrovascularLa prevención secundaria con estatinas reduce las recurrencias de eventos neurológicos un 12% por cada 1 mmol/l que se reducen las cifras de cLDL. Por lo tanto, debe considerarse en muy alto riesgo al paciente con un accidente cerebrovascular, con los mismos objetivos terapéuticos.
Hipercolesterolemia familiarLa guía reconoce la importancia de la HF heterocigota como causa frecuente de enfermedad cardiovascular prematura debido al aumento del cLDL desde el nacimiento. Sin embargo, sigue habiendo un vacío en su detección y su tratamiento. Por lo tanto, es crucial que los médicos tomen conciencia de la importancia de una detección y un tratamiento precoces. La guía describe los criterios clínicos para su diagnóstico, fundamentalmente basados en cifras de cLDL elevadas en el paciente adulto y sus familiares y enfermedad coronaria prematura en el paciente o en un familiar. Destaca la detección precoz en niños a partir de los 5 años. El diagnóstico se debe confirmar con la detección genética de la mutación causal si está disponible. Además, la confirmación genética del caso índice es fundamental para la detección de nuevos casos en la familia mediante el cribado en cascada, que se ha demostrado coste-eficaz.
También define a la población con HF como en riesgo elevado o muy elevado de enfermedad cardiovascular ateroesclerótica, si además el paciente presenta enfermedad cardiovascular ateroesclerótica previa u otro factor de riesgo mayor. Sin embargo, en la nueva guía sorprende la falta de información sobre una ecuación basada en el estudio prospectivo español de HF (SAFEHEART) que predice con elevado valor discriminativo tanto un primer evento como las recurrencias, lo cual mejora la estratificación del riesgo21. Otra nueva recomendación es el uso de la imagen cardiovascular para valorar el riesgo de eventos22.
Con las recomendaciones de unos objetivos de cLDL más bajos, la guía enfatiza la importancia del tratamiento combinado con estatinas, primero con ezetimiba y, si no se consiguen los objetivos de cLDL, con los iPCSK9. Una predicción del riesgo de eventos cardiovasculares ateroescleróticos en los pacientes con HF puede definir mejor qué pacientes con HF se beneficiarían de los nuevos fármacos. Es preciso tener en mente que la HF cursa con valores basales de cLDL muy elevados, por lo que, según las nuevas recomendaciones, la mayoría de los pacientes serían susceptibles de recibir estos fármacos, con la consiguiente repercusión en la práctica clínica. Por lo tanto, se necesita un análisis de coste-eficacia de estos fármacos para evaluar su viabilidad en nuestro sistema sanitario.
En la guía se hace referencia al tratamiento de la HF homocigota, una forma rara y muy grave de HF. La disponibilidad de lomitapida (no comercializada en España) como tratamiento adicional a las estatinas y la aféresis de LDL reduce el cLDL hasta un 50% y puede disminuir la frecuencia de la aféresis o incluso evitarla, con la consiguiente mejora en la calidad y la cantidad de vida de estos pacientes.
Enfermedad arterial periféricaEl estudio FOURIER12, con una reducción de eventos cardiovasculares en pacientes con enfermedad arterial periférica con evolocumab, ha introducido la indicación de iPCSK9 para estos pacientes, que en ediciones previas no se incluía. El número de pacientes subsidiarios de tratamiento con iPCSK9 aumenta, y queda por definir si es coste-eficaz. De manera muy somera, se menciona el papel del fenofibrato en la reducción de amputaciones en la enfermedad arterial periférica y en la progresión de la retinopatía diabética, con un papel aún desconocido en la enfermedad de pequeños vasos. Por lo tanto, la mayor aportación en la enfermedad arterial periférica es la nueva indicación de iPCSK9 para casos seleccionados.
Otras poblaciones especialesEn pacientes con enfermedad inflamatoria crónica, infección por el virus de la inmunodeficiencia humana o enfermedad mental grave, tanto la enfermedad en sí como los tratamientos que aumentan los lípidos pueden conferir mayor riesgo, por lo que se los considera modificadores del riesgo. La guía nueva no aporta novedades en estas poblaciones. No hay nuevas evidencias para el tratamiento con estatinas en la insuficiencia cardiaca que no sea de origen isquémico o en valvulopatías, ni siquiera en la estenosis aórtica degenerativa. Desaparece la recomendación IIb de las guías anteriores de considerar los n-3 añadidos al tratamiento óptimo en insuficiencia cardiaca.
INFLAMACIÓNEste es un nuevo apartado que, como el documento de consenso de expertos de American Heart Association/American College of Cardiology de 201823, describe la evidencia de la relación de la inflamación con la arterioesclerosis. Repasa someramente los mediadores de inflamación y su modificación con los distintos tratamientos para el colesterol: estatinas, ezetimiba e iPCSK9. También hace un repaso del tratamiento específico de la inflamación con las recientes evidencias del canakinumab u otros más antiguos y menos eficaces con metotrexato.
MONITORIZACIÓN DE LÍPIDOS Y ENZIMAS DE PACIENTES EN TRATAMIENTO HIPOLIPEMIANTEEn este apartado, complementado con la tabla 13 de la guía1, se detalla con precisión la determinación sistemática de los lípidos para valorar la eficacia del tratamiento y de las enzimas para la monitorización de su seguridad. No hay ningún cambio respecto a guías previas, excepto que en el último párrafo se recomienda que se considere realizar regularmente análisis de glucohemoglobina a todos los diabéticos y a aquellos con riesgo de serlo.
COSTE-EFECTIVIDAD DE LA PREVENCIÓN DE ENFERMEDADES CARDIOVASCULARES POR MODIFICACIÓN DE LA CONCENTRACIÓN DE LÍPIDOSEn este apartado completamente nuevo, la guía hace referencia a que la enfermedad cardiovascular supone en la Unión Europea unos 210.000 millones de euros (aproximadamente el 8% de gasto total sanitario). Las estrategias de reducción de lípidos que propone esta guía conllevan un coste elevado, por lo que los análisis de coste-efectividad pueden ayudar a concentrar los recursos en intervenciones cuya ganancia neta en salud sea mayor en relación con los recursos. Respecto a las estatinas y la ezetimiba (actualmente disponible como genérico en toda Europa), es una estrategia coste-efectiva en todos los ámbitos (prevención secundaria o primaria hasta un riesgo SCORE> 1%). No obstante, es fundamental conseguir una adherencia óptima. Con los estudios de coste-efectividad publicados a mitad de 2018, los iPCSK9 solo eran rentables en pacientes en alto riesgo seleccionados. Sin embargo, a precios más bajos, serían rentables en un subgrupo más amplio de pacientes con alto riesgo. Además, en la figura 6 de la guía1 se representa en una gráfica la magnitud de la reducción del riesgo según los grupos de riesgo con los distintos grados de reducción del cLDL.
ESTRATEGIAS PARA FAVORECER UN ESTILO DE VIDA SALUDABLE Y LA ADHERENCIA AL TRATAMIENTO HIPOLIPEMIANTEEste apartado destaca que la adherencia a los cambios en el estilo de vida y a los regímenes terapéuticos es un reto tanto para los profesionales como para los pacientes. Sin cambios con respecto a la guía anterior, se insiste en que la forma más eficaz de conseguir este objetivo es utilizar programas formales de prevención y formación del paciente, ya que permiten un seguimiento más intensivo a través de equipos interdisciplinarios. Se recomienda un enfoque integral centrado en el paciente y la familia y se señalan herramientas que favorecen la adopción de estilos de vida saludables y estrategias de comunicación que mejoran la adherencia al tratamiento.
CONFLICTO DE INTERESESNo se declara ningún conflicto relacionado con el presente trabajo.
Grupo de Trabajo de la SEC para la guía ESC 2019 sobre el tratamiento de las dislipemias: Leopoldo Pérez de Isla (coordinador), Lluís Masana (coordinador), Rosa Argüeso, Raquel Campuzano, Isabel Egocheaga, Carlos Escobar, Lorenzo Fácila, Pedro Mata López, Miriam Rossi y Carmen Rus Mansilla.
Revisores expertos para la guía ESC 2019 sobre el tratamiento de las dislipemias: José Antonio Alarcón Duque, Vicente Arrarte, Gonzalo Barón, Vivencio Barrios, Amelia Carro, Almudena Castro, Juan Cosin-Sales, Rosa Fernández Olmo, José Gámez Martínez, Ana Huelmos, Miriam Sandín, Adriana Saltijeral y Alfonso Valle.
Comité de Guías de la SEC: Fernando Arribas, Gemma Berga Congost, Héctor Bueno, Arturo Evangelista, Ignacio Ferreira-González, Manuel Jiménez Navarro, Francisco Marín, Leopoldo Pérez de Isla, Antonia Sambola, Rafael Vázquez, Ana Viana-Tejedor, Borja Ibáñez y Fernando Alfonso.