Palabras clave
INTRODUCCIÓN
El objetivo principal en el tratamiento del infarto agudo de miocardio (IAM) es restaurar la permeabilidad de la arteria coronaria epicárdica; la teoría de la «arteria abierta» se basa en 2 factores fundamentales: la variable temporal («cuanto antes») y la variable de magnitud («cuanto más flujo»). Sea cual fuere el método de reperfusión empleado, el objetivo final se considera el parámetro angiográfico de «flujo epicárdico normal», como se ha demostrado en múltiples estudios1-6. Tras la evolución alcanzada en los últimos tiempos, que permite restaurar flujos epicárdicos «normales» en más del 90% de los pacientes, y el hecho de comprobar que aun en presencia de un flujo epicárdico normal hay una proporción importante de pacientes en los que no se normaliza el segmento ST y no se restaura la perfusión miocárdica evaluada mediante ecocardiografía de contraste miocárdica (ECM), el interés se ha desplazado más allá de las arterias epicárdicas, hacia la perfusión miocárdica. Son múltiples los métodos que valoran el estado de la microcirculación coronaria y la perfusión miocárdica: desde los más simples, como el análisis en el electrocardiograma (ECG) de la resolución del segmento ST previamente elevado7-19, hasta los más complejos, como la tomografía por emisión de positrones (PET)20-22. El objetivo de este artículo es revisar los hallazgos que obtenemos con la angiografía coronaria18,23-29 para el análisis de la calidad de la reperfusión, tanto en su vertiente epicárdica como en la microvascular.
TRASCENDENCIA Y LIMITACIONES DE LA VALORACION DEL FLUJO EPICÁRDICO
Arteria epicárdica abierta: graduación. Flujo TIMI
La valoración del flujo en la arteria coronaria epicárdica se sistematizó hace 20 años por el grupo de investigación TIMI (Thrombolysis In Myocardial Infarction) en los denominados grados de flujo TIMI1. En la tabla 1 se describen las características de cada uno de los grados.
Son múltiples los estudios que han demostrado la correlación de este parámetro con los eventos posteriores: reinfarto30-32, mortalidad2-6,33,34, rotura de pared libre35, desarrollo de aneurisma ventricular36 o aparición de arritmias37-40. Esta correlación con el pronóstico, que inicialmente se describió para el tratamiento trombolítico en el infarto agudo de miocardio (IAM), se ha extendido también a la terapia mediante intervencionismo coronario percutáneo (ICP)39-44. Tan sólida se ha demostrado esta relación que habitualmente se utiliza la obtención de flujo TIMI 3 como parámetro para evaluar la eficacia de distintos tratamientos, en subrogación de los eventos clínicos relevantes43-52.
Esta clasificación permite establecer la superioridad del flujo TIMI 3 sobre el resto de situaciones, incluso sobre el grado TIMI 2: la mortalidad precoz encontrada en 2 metaanálisis33,34 era significativamente inferior entre los pacientes con flujo TIMI 3 a los 90 min de la fibrinólisis que la del grupo con flujo TIMI 2 (el 3,7 frente al 6,6%; odds ratio [OR] = 0,55; intervalo de confianza [IC] del 95%, 0,4-0,76) y la del grupo con flujos TIMI 0 o 1 (9,2%; OR = 0,38; IC del 95%, 0,29-0,5). Con el desarrollo de la terapia de repermeabilización mediante ICP, el empleo de estos predictores ha seguido demostrando su validez41, aunque algunos estudios señalan que la diferencia de mortalidad entre los grados TIMI 2 y 3 podría no ser tan marcada en la época actual con el uso de terapias agresivas que combinen fármacos fibrinolíticos e ICP23. Por otra parte, los avances técnicos en el campo intervencionista (implante de stents coronarios53,54, dispositivos de trombectomía55,56, sistemas de protección distal57-60) no se han asociado de forma universal con una mejoría en las tasas de flujo TIMI 3.
No obstante, este sistema de graduación adolece de ciertas limitaciones:
1. La limitación más relevante es la subjetividad que conduce a importantes discrepancias61, incluso cuando los análisis son realizados por laboratorios centralizados con amplia experiencia62,63.
2. El tiempo de relleno de la descendente anterior (DA) es superior al de las otras arterias, al ser esta arteria normalmente más larga. Dado que el relleno de esta arteria puede compararse simultáneamente con el de la circunfleja, la tendencia a otorgar un grado de flujo TIMI 2 es mucho mayor que en el caso de la coronaria derecha64.
3. El propio grupo TIMI ha modificado (sin mucha aceptación posterior) el sistema de clasificación, distinguiendo en el grado TIMI 2 hasta 3 subgrupos distintos65 (tabla 1). En esta modificación se incluyen aspectos como la velocidad de lavado que se discutirán posteriormente.
4. En último lugar, no se puede descartar la presencia de factores que podrían modificar de manera significativa la graduación, como la presión y el momento del ciclo cardiaco en que se realiza la inyección del contraste, la frecuencia cardiaca y la presión arterial del paciente, el uso de vasodilatadores, etc. La influencia de estos factores se discute en el siguiente apartado.
Arteria epicárdica abierta: cuantificación. Corrected TIMI frame count
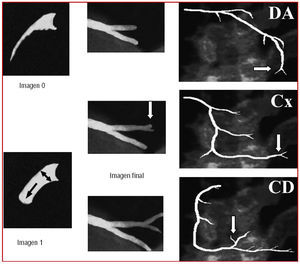
A la luz de las posibles limitaciones del sistema de graduación de flujo TIMI se han desarrollado nuevos sistemas de evaluación que profundizan en la caracterización del flujo y mejoran la reproducibilidad de los resultados: el más validado es el sistema desarrollado por Gibson et al64 denominado corrected TIMI frame count (cTFC), es decir, la cuenta de imágenes TIMI corregida. En esencia «cuantifica» el grado de flujo TIMI mediante la medición del tiempo que tarda el contraste en rellenar la arteria epicárdica en toda su longitud. Para uniformizar los criterios se definió una serie de bifurcaciones distales que sirvieran como «marca final»: la «cola de ballena» apical de la DA, la última bifurcación de la arteria obtusa marginal más distal en el territorio de la circunfleja y la primera rama que sale del tronco posterolateral en el territorio de la coronaria derecha (fig. 1). La diferencia en número de imágenes entre esta última y la primera (aquella en la que el contraste ocupa al menos el 70% del ostium arterial y comienza a desplazarse anterógradamente) constituye el TIMI frame count.
Fig. 1. Cálculo de la cuenta de imágenes TIMI. La imagen a partir de la que se comienza a contar (imagen 1) es aquella en la que el contraste avanza y rellena al menos el 70% del diámetro del ostium arterial. La última imagen (imagen final) es aquella en la que el contraste comienza a rellenar la marca final. Se representan las bifurcaciones distales de las 3 arterias epicárdicas. CD: coronaria derecha; Cx: arteria circunfleja; DA: descendente anterior.
Conviene reseñar una serie de aspectos metodológicos de este sistema:
1. Como ya se ha descrito64, la longitud de la DA es 1,7 veces superior que la de las otras 2 arterias. Por ello, se introduce en este sistema una factor de corrección (como su nombre indica) en el caso del análisis de la DA: el corrected TIMI frame count es el resultado de la diferencia absoluta dividido por el factor de corrección, 1,7.
2. Todos los valores inicialmente publicados en «cuenta de imágenes» se refieren al estándar de vídeo en Estados Unidos, NTSC: 30 imágenes/s. Para adecuar estos valores al sistema europeo (PAL) se deben convertir estos valores o bien emplear una unidad de medida uniforme: el tiempo en segundos. En la tabla 2 se detallan los valores más relevantes y sus equivalencias.
3. La definición original de este parámetro incluye la imputación del valor de cTFC = 100 en aquellos casos en los que la arteria coronaria está completamente ocluida. Esto conduce a una distribución de los valores que no sigue la ley normal, lo que implica la necesidad de usar pruebas estadísticas no paramétricas en sus análisis.
4. La implementación de este método en la práctica es más compleja que la simple valoración subjetiva del flujo, ya que consume más tiempo, limitación especialmente relevante en el contexto del paciente agudo.
Este parámetro se ha correlacionado con la aparición de eventos graves, como la mortalidad precoz tras la fibrinólisis23,66,67. Esta relación se mantiene incluso cuando el análisis se circunscribe sólo a los pacientes con flujo TIMI 3: los pacientes con valores de cTFC menores de 14 imágenes (lo que se definió como «flujo TIMI 4»64,66) presentaban una tasa de mortalidad hospitalaria del 0%, frente al 2,7% del grupo con cTFC entre 14 y 40 (flujo TIMI 3) o al 6,4% en aquellos con cTFC > 40 imágenes (p = 0,003)66. La relación del cTFC con el pronóstico posterior se ha demostrado en otras situaciones, como la angioplastia primaria en el infarto68-72 o en el seno del síndrome coronario agudo sin elevación del segmento ST (SCASEST)73.
También se ha demostrado su correlación con métodos independientes de valoración funcional coronaria, como la reserva coronaria valorada por guía Doppler74,75 o la reserva fraccional de flujo (FFR)76. En absoluta contradicción con lo descrito, también se han publicado estudios que no demuestran correlación entre el cTFC y los parámetros de reserva coronaria por guía Doppler77,78 o incluso con la mortalidad precoz79, aunque estos estudios valoraron el flujo en un número limitado de pacientes tras ICP y no de forma basal; resulta razonable no hallar correlación entre el flujo basal valorado por este método y el flujo hiperémico analizado mediante guía Doppler.
El método presenta evidentes ventajas sobre la valoración del flujo epicárdico de forma cualitativa:
1. Dado el carácter cuantitativo del parámetro, se ha demostrado62,63,80 una elevada reproducibilidad.
2. Se trata de un método de simple realización, que no requiere un equipamiento especial y que se puede realizar sobre las imágenes angiográficas recién adquiridas.
3. La descripción de puntos de corte (tabla 2) permite clasificar flujos epicárdicos dudosos.
No obstante, el método presenta ciertas limitaciones; se ha descrito una serie de factores que pueden alterar de forma significativa los valores calculados:
1. Frecuencia cardiaca: un aumento de 20 lat/min acorta la cuenta en 5 imágenes80.
2. Empleo de nitratos: aumenta la cuenta en 6 imágenes80.
3. Una inyección en el período protodiastólico: reduce la cuenta en 3-6 imágenes80.
4. DA como arteria causante del infarto: en estos casos la cuenta es superior a la de las otras arterias en 8 imágenes, incluso tras corregir con la longitud y ajustar con otras variables81.
No se ha demostrado que el cálculo se vea afectado por factores dependientes del paciente (edad, sexo, tamaño corporal, presión arterial o factores de riesgo cardiovascular82) o del procedimiento (presión de inyección83 o tipo de contraste84).
Tomando como base este método, se han desarrollado sistemas de valoración no sólo del flujo epicárdico, sino también de la microcirculación: la valoración de la reserva de flujo coronario analizando la relación de cTFC basal y cTFC tras la administración de adenosina intracoronaria74,85 o intravenosa86. Este parámetro se ha correlacionado con el análisis mediante guía Doppler74,86, aunque otros estudios no lo confirman77.
VALORACION DE LA PERFUSION Y MICROCIRCULACION MIOCARDICA
Microvasculatura abierta: valoración. Opacificación miocárdica
Desde las clásicas descripciones del «daño por reperfusión» y los fenómenos de «no reflujo»87 se han multiplicado los intentos de valorar el estado de la perfusión miocárdica tras el infarto. El más sencillo y reproducible es el análisis de la resolución del segmento ST7-19; otro de los métodos más empleados ha sido la ECM88-93, que añade a su carácter no invasivo la posibilidad de ser cuantificada. En ambos casos, se han correlacionado sus resultados con la aparición de eventos posteriores7-10,14,16,26,88-90,93-98.
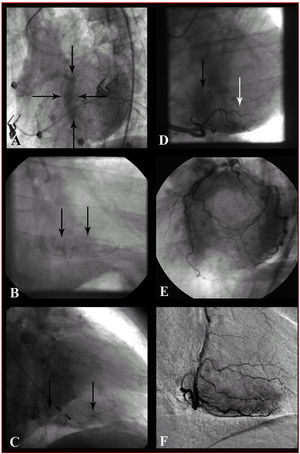
Con la creciente implantación de la ICP como tratamiento de elección en el IAM, la disponibilidad de una angiografía precoz se ha hecho muy frecuente y ha permitido el desarrollo del concepto de blush miocárdico, que podemos traducir como rubor, tinción o tatuaje miocárdico: la penetración del contraste yodado en los capilares ofrece una imagen angiográfica de «vidrio deslustrado» del territorio miocárdico irrigado. Se han propuesto 2 sistemas distintos de valoración de la tinción miocárdica: un sistema videodensitométrico que analiza la intensidad del contraste regional (myocardial blush grade [MBG]) en comparación con el del territorio contralateral o ipsolateral no afectado, propuesto por Van't Hof et al25, y un sistema de análisis dinámico que valora la intensidad del contraste mioc&aacu te;rdico y su velocidad de aparición y desaparición (TIMI myocardial perfusion grade [TMPG]), propuesto por Gibson et al24. En la tabla 1 se detallan los 4 grados de cada una de las clasificaciones. La perfusión normal se gradúa de forma idéntica en ambos sistemas: grado 3. Los casos de peor perfusión miocárdica corresponden a los grados 0 de ambas clasificaciones; los casos de importante daño por reperfusión (transformación hemorrágica o extravasación persistente) se incluyen en el TMPG 1 y MBG 0, respectivamente. Los casos de MBG 1 y 2 tienen difícil extrapolación a la clasificación TMPG, por lo que se ha propuesto una subclasificación para estos casos: el TMPG 0,599; así, los 2 sistemas no son tan diferentes como podría parecer. En la figura 2 se muestran ejemplos del análisis de perfusión miocárdica.
Fig. 2. Ejemplos de análisis de la perfusión miocárdica. A: tinción persistente del septo (delimitado por flechas): grado de perfusión miocárdica (TMPG) 1, grado de blush miocárdico (MBG) 0 en DA. B: tinción miocárdica persistente en territorio diafragmático: grados TMPG 1, MBG 0 en CD. C: tinción persistente capilar (se visualizan pequeños vasos) en CD. D: tinción de menor intensidad que en coronaria izquierda en territorio diafragmático (flecha negra, grados TMPG y MBG 2) y apenas presente en posterolateral (flecha blanca, grados TMPG 0,5 y MBG 1). E: tinción miocárdica normal (grados TMPG y MBG 3) de coronaria izquierda: se observa la imagen de «rosquilla» en proyección OAI craneal. F: tinción miocárdica normal (grados TMPG y MBG 3) de CD; ejemplo de sustracción digital (DSA).
Aunque la existencia de estos 2 sistemas puede cuestionar la validez del método, la realidad es que se ha correlacionado con la mortalidad, tanto el sistema TMPG23,24 como el MBG25,100,101 (fig. 3), incluso cuando sólo se considera a los pacientes con flujo TIMI 3. La influencia de estos parámetros también se ha demostrado en el porcentaje de miocardio salvado respecto al área en riesgo102 y la mortalidad en los pacientes en shock103 o sobre la relación de la mortalidad con el tiempo de evolución del IAM104-106. Por otra parte, también se ha demostrado la correlación de estos sistemas con otros parámetros, independientemente relacionados con el pronóstico tras el infarto, como el análisis de la reserva coronaria con guía Doppler107,108, la ECM26,95,96, el análisis mediante tomografía por emisión de fotón único (SPECT) del tamaño del infarto18 o la resolución de la elevación del segmento ST18,28,101,108.
Fig. 3. Mortalidad tras IAM y grados de opacificación miocárdica. A: tasa de mortalidad en función del grado de opacificación miocárdica: al mes (Gibson et al24), a más largo plazo (seguimiento 1,9 ± 1,7 años [Van't Hof et al25] y al año [Stone et al29]). B: tasa de mortalidad en función del grado de opacificación miocárdica en los pacientes con flujo TIMI 3 en la arteria causante: al mes (Gibson et al24) y al año (Stone et al29). TMPG: grado de perfusión miocárdica TIMI; MBG: grado de opacificación (blush) miocárdica.
La valoración de la opacificación miocárdica también tiene sus limitaciones:
1. El carácter cualitativo del parámetro es inherente a la subjetividad en su valoración. Así, la concordancia intraobservador e interobservador es limitada, como describe uno de los grupos de mayor experiencia25. En la mayoría de las publicaciones, el análisis del MBG o del TMPG se realiza en laboratorios centrales: la concordancia con la valoración llevada a cabo por otros observadores podría no ser adecuada.
2. En muchos de los estudios realizados se tiende a agrupar a los pacientes con MBG 2 y 3 o TMPG 2 y 3 en un grupo único de perfusión adecuada. Del mismo modo que se ha demostrado que no es equivalente el pronóstico de los pacientes con flujo TIMI 2 y TIMI 3, probablemente esta simplificación del sistema puede ser errónea.
3. No obstante, la limitación fundamental no es metodológica, sino el reto aún no resuelto del tratamiento de la perfusión miocárdica subóptima tras la repermeabilización coronaria. En la tabla 3 se resumen las evidencias publicadas en este terreno.
La correlación entre el análisis de la resolución del segmento ST y la opacificación miocárdica es controvertida pues, aunque ambos se han relacionado con los eventos clínicos, no siempre aparecen de forma concordante en cada paciente. Lo que pudiera interpretarse como una limitación tiende a valorarse como otro de los fenómenos de disociación, nada infrecuentes en cardiología: la recuperación «eléctrica» que demuestra el ECG no siempre se asocia con la integridad del endotelio microvascular y la recuperación de la perfusión, y viceversa. De hecho, los 2 métodos son complementarios cuando se analiza el tamaño del infarto18, o como demuestra el hecho de que el grupo de mejor pronóstico tras un infarto es el de los pacientes con ambos marcadores positivos133-135. Se dispone de amplia documentación sobre la correlación entre ECM y angiografía26,95-98,136 y no siempre se halla una correlación perfecta a pesar de que, al menos teóricamente, ambos métodos analizan la perfusión miocárdica. Sin olvidar que éste es un fenómeno dinámico (tras algunos días del infarto, muchos pacientes que inicialmente no presentaban una opacificación miocárdica adecuada pueden mostrar un grado mucho mejor135), la base de las discordancias puede estar en el distinto comportamiento de los contrastes empleados: el contraste ecográfico (microburbujas) siempre permanece en el espacio intravascular, mientras que el contraste radiológico (y también el paramagnético de la resonancia magnética) a menudo tiene paso extravascular, regresando posteriormente al torrente circulatorio. Así, algunos autores137 defienden que la perfusión miocárdica no es exactamente lo que se valora con la angiografía o la resonancia magnética, sino la permeabilidad capilar, el estado del endotelio y el edema y la hemorragia intersticiales: el daño por reperfusión.
Microvasculatura abierta: cuantificación. Desarrollos futuros
En el análisis de la perfusión miocárdica por angiografía se desarrollan varios métodos cuantitativos:
1. Los métodos basados en la sustracción digital (DSA)85,138,139, muy empleada en la radiología vascular pero poco en la angiografía coronaria, pueden facilitar la cuantificación del área de opacificación (teóricamente «equivalente» a las áreas cuantificadas en la ECM), de la intensidad de la opacificación («cuantificación del MBG»)107,140 o de la velocidad con la que la opacificación aparece o desaparece («cuantificación del TMPG»)138. Para que la DSA sea más aplicable se estudian desarrollos, como la técnica de máscara en movimiento que pretende neutralizar los movimientos inherentes al corazón.
2. Se ha propuesto un sistema de cuantificación, derivado del cTFC, en el que se cuantifican el número de imágenes que transcurren entre la entrada del contraste al miocardio y el pico de intensidad de la opacificación: el TIMI myocardial frame count. Esta cuenta es significativamente mayor en los pacientes con IAM con elevación del segmento ST que en pacientes con SCASEST141.
3. Nuestro grupo ha desarrollado un sistema de cuantificación denominado Coronary Clearance Frame Count (CCFC) con una buena correlación con los grados TMPG142. Definido como «el reverso del cTFC», cuenta la diferencia de imágenes entre el momento en el que el contraste desaparece del ostium arterial y en el que comienza a desaparecer de la bifurcación distal que se describe en el sistema del cTFC. Aunque aún no se ha establecido su potencial significación clínica, sí que se ha demostrado su correlación con los grados de perfusión miocárdica TMPG 2 o 3, estableciendo un punto de corte (45 imágenes) que permite discriminar los grados de mejor perfusión.
Análisis del cTFC y de la opacificación miocárdica. Consideraciones prácticas
Tanto el análisis cuantitativo del flujo epicárdico (cTFC) como el de la microvasculatura pueden realizarse on-line con los equipos digitales actuales u off-line con algunos de los programas de revisión de imágenes. No obstante, si las condiciones de filmación no son óptimas, la interpretación y el análisis posterior pueden verse sesgados. Por ello, se realizan una serie de recomendaciones uniformes:
1. Campo de filmación: 23 cm. La no magnificación de la imagen permite la grabación de toda la longitud de la arteria sin necesidad de desplazamientos (panning/travelling). Es de particular importancia para el correcto análisis de la opacificación miocárdica, especialmente si se realiza DSA. La calidad de las imágenes de DSA actuales (máscara fija) también se supedita de forma importante a mantener la apnea durante la grabación.
2. Velocidad de filmación: idealmente, 25 imágenes/s. No obstante, el cálculo del cTFC puede realizarse sobre cualquier velocidad de registro y posteriormente expresarlo en segundos o ajustarlo a la velocidad citada.
3. Tiempo de grabación: hasta la aparición de contraste en fase venosa. Muy relevante para el sistema de análisis TMPG. En este caso, también es particularmente importante separar al menos 30 s una inyección de la siguiente y no grabar inmediatamente tras la realización de «tests» de contraste (puede asignar valores de TMPG 1 incorrectamente).
4. Proyecciones seleccionadas:
a) Análisis de cTFC: se recomienda grabar imágenes en PA u OAD (0-30°) con angulación caudal (20-30°) para la coronaria izquierda y en OAI (45-60°) para la coronaria derecha.
b) Análisis de la opacificación: las proyecciones recomendadas difieren de las anteriores pues, especialmente en la coronaria izquierda, los territorios de perfusión pueden verse solapados. Así, se recomienda realizar OAI (45-60°) con angulación craneal (20-30°), que permite ver una imagen en «rosquilla», o lateral izquierda (90°) en el caso de la coronaria izquierda; para la coronaria derecha, se recomienda la OAI (45-60°) con o sin angulación craneal o la OAD (30°).
Desde el punto de vista práctico, en nuestro centro se analizan los datos de perfusión miocárdica derivados de la angiografía (tanto según el sistema TMPG como MBG) en todos los casos de angioplastia en el seno del IAM de forma sistemática y en otros casos de intervencionismo con fenómenos de no reflow o flujo final enlentecido, reservando la cuantificación del cTFC y del CCFC para los casos con flujo epicárdico o perfusión difíciles de catalogar. En todos estos casos, la información obtenida se complementa siempre con el análisis electrocardiográfico de la resolución del segmento ST.
CONCLUSIONES
La angiografía coronaria ofrece una información relevante, de simple adquisición e interpretación, no sólo sobre el estado de la circulación coronaria epicárdica (flujo TIMI de la arteria epicárdica y su cuantificación, la cuenta de imágenes TIMI) sino también sobre el estado de la circulación microvascular (grados de opacificación miocárdica: TIMI myocardial perfusion y myocardial blush grades). Estos datos permiten valorar de forma certera el pronóstico del paciente. El desarrollo de estas técnicas en su variante cuantitativa podría mejorar su poder predictivo.
Correspondencia: Dr. A. Pérez de Prado.
Sección de Cardiología Intervencionista. Servicio de Cardiología.
Hospital de León.
Altos de Nava, s/n. 24008 León. España.
Correo electrónico: aperez@secardiologia.es