La insuficiencia cardiaca es una entidad compleja, que conlleva elevada morbilidad y mortalidad y cuyo curso y evolución son inciertos y difíciles de predecir. Este trabajo, impulsado por las Secciones de Insuficiencia Cardiaca y Cardiología Geriátrica de la Sociedad Española de Cardiología, aborda los diferentes aspectos relacionados con los cuidados paliativos en el campo de la insuficiencia cardiaca, vía final común de la mayoría de las enfermedades cardiovasculares. También establece un consenso y una serie de recomendaciones con el objetivo de reconocer y comprender la necesidad de implementar y aplicar, de modo progresivo, este tipo de cuidados a lo largo del curso de la enfermedad, y no únicamente en sus estadios avanzados, para mejorar la atención que reciben los pacientes y su calidad de vida. La finalidad es mejorar y adecuar los tratamientos a las necesidades y los deseos de cada paciente, que debe contar con información adecuada y ser partícipe de la toma de decisiones.
Palabras clave
Las enfermedades cardiovasculares son la principal causa de mortalidad en los países occidentales1. La insuficiencia cardiaca (IC) constituye la vía final común de la mayoría de ellas y se caracteriza por un deterioro progresivo de la situación funcional del paciente hasta su muerte, que puede ocurrir también de manera súbita2,3. Es una entidad grave con elevada morbimortalidad, cuyo pronóstico es difícil de predecir, y con frecuencia no se abordan cuestiones referentes a las etapas finales de la vida hasta situaciones avanzadas de la enfermedad, cuando ya es demasiado tarde4. Además, la IC afecta fundamentalmente a pacientes ancianos, un grupo en el que las comorbilidades son frecuentes y graves3,5. Uno de los retos a los que se enfrenta el clínico es el de proporcionar una adecuada información que permita al paciente y su entorno comprender la evolución y el pronóstico de la enfermedad6.
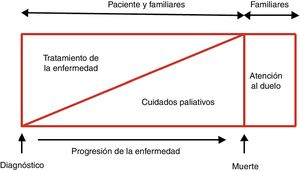
Según la Organización Mundial de la Salud, «Los cuidados paliativos constituyen un método de atención que mejora la calidad de vida de pacientes y familias cuando afrontan problemas inherentes a una enfermedad potencialmente mortal. Previenen y alivian el sufrimiento a través de la identificación temprana, la evaluación y el tratamiento correctos del dolor y otros problemas, sean estos de orden físico, psicosocial o espiritual»7. Los cuidados paliativos (CP) se desarrollaron inicialmente en pacientes oncológicos, si bien se han ido reconociendo e implementando para otras enfermedades de mal pronóstico, y hasta en el 39% de las personas que precisan actualmente CP es por causa cardiovascular7. Estos cuidados se deben iniciar desde el momento del diagnóstico, al ser una enfermedad de mal pronóstico y potencialmente mortal que adquiere mayor peso e importancia conforme avanza2,8 (figura 1). Además, no acaban con la muerte del paciente, pues se debe reconocer también la atención al duelo de familiares y cuidadores. Los CP se deben centrar en la persona, reconociendo y respetando sus necesidades y preferencias, buscando mejorar y asegurar el acceso a los cuidados que se precisen, y pueden y deben proporcionarse en distintos niveles asistenciales y también en el domicilio. En este documento, impulsado por las Secciones de Insuficiencia Cardiaca y Cardiología Geriátrica de la Sociedad Española de Cardiología, se abordan los aspectos más importantes relacionados con los CP en el campo de la IC.
Objetivos terapéuticos en pacientes con insuficiencia cardiaca. Modificado con permiso de Martínez-Sellés et al.2.
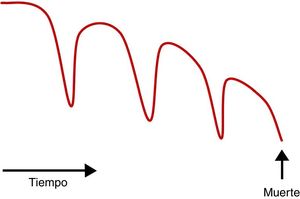
La IC repercute en la calidad de vida de los pacientes, a quienes causa sufrimiento5,6. El riesgo de muerte es elevado, y aumenta con la edad, las comorbilidades y las hospitalizaciones9. Su evolución responde a un modelo de insuficiencia orgánica (figura 2), en el que el paciente puede encontrarse inicialmente asintomático o «paucisintomático», y tras un evento agudo (descompensación) se produce un deterioro de su situación funcional2. Después, no son infrecuentes los múltiples reingresos y que el paciente presente un deterioro funcional progresivo, hasta que finalmente fallece en situación de refractariedad y/o en relación con las comorbilidades10. Este deterioro puede ocurrir también abruptamente, si bien el uso cada vez más generalizado de bloqueadores beta, antagonistas del receptor de mineralocorticoides, sacubitrilo-valsartán y desfibriladores automáticos implantables (DAI) ha reducido el porcentaje de pacientes con muerte súbita3. Es muy difícil predecir el pronóstico de la enfermedad y las calculadoras de riesgo siguen siendo imperfectas, al no incorporar condiciones prevalentes y con impacto pronóstico11, por lo que en general no son de gran ayuda en la toma de decisiones para cambiar el enfoque terapéutico (pasar de un tratamiento «curativo» a uno «paliativo»)12. Todos estos aspectos contribuyen a que los CP no se incorporen de manera sistemática en el continuo asistencial, que solo un pequeño porcentaje de pacientes los reciban adecuadamente y que a menudo se realicen tarde13,14. Además, es habitual que el curso del último año de vida en un paciente con IC sea tórpido, con descompensaciones que motivan múltiples visitas al hospital. El fallecimiento a menudo ocurre en el hospital por diversas causas que dificultan que pueda ser en su domicilio, incluyendo el entorno familiar y la falta de una cobertura asistencial que asegure el correcto control de síntomas15. Deliberar con los pacientes y familiares el pronóstico y la posible evolución de la enfermedad y planificar los cuidados en los diversos estadios deben ser pilares básicos. Por lo tanto, es necesario conocer las preferencias del paciente respecto al proceso de atención al final de la vida, como el lugar donde quiere ser atendido o el lugar preferido para fallecer. Estas preferencias pueden cambiar en el tiempo y, junto con las directrices avanzadas y los planes de decisiones avanzadas, son de ayuda en la toma decisiones16. Ensayos clínicos, como el PAL-HF, han demostrado que una intervención interdisciplinaria de CP en pacientes con IC avanzada consigue mayores beneficios en calidad de vida, ansiedad, depresión y bienestar espiritual en comparación con el tratamiento convencional17. Recientes metanálisis confirman la utilidad de incorporar los CP para mejorar la atención y calidad de vida de los pacientes con IC18. Aún son muchas las preguntas y los aspectos que mejorar en cuanto a los CP en este contexto, algunos de los cuales se recogen en la .
TRATAMIENTO MÉDICO. CONTROL DE SÍNTOMASEn pacientes con IC avanzada conviene revaluar la indicación de los distintos fármacos, centrándose especialmente en el control sintomático, evitando efectos secundarios19 y teniendo en cuenta que una misma manifestación clínica puede ser consecuencia de la IC o sus complicaciones o de comorbilidades. La retirada de medicación es una decisión individualizada que debe compartirse con el paciente y su familia.
Los signos y síntomas más frecuentes en pacientes con IC avanzada son la disnea y la congestión sistémica, el dolor, la depresión y la astenia.
DisneaSe halla disnea en más del 60% de los pacientes y es generalmente muy incapacitante20. Puede llevar asociada taquipnea y trabajo respiratorio. La causa fundamental es la congestión pulmonar, pero hay que descartar la presencia de derrame pleural, procesos intercurrentes (infecciones respiratorias, etc.) o descompensación de comorbilidades, que requerirían un tratamiento específico. Su abordaje incluye: oxigenoterapia, optimización del tratamiento diurético y vasodilatador, el uso de inotrópicos ambulatorios, opiáceos y, en ciertas situaciones, toracocentesis evacuadora.
OxigenoterapiaLa oxigenoterapia es importante en pacientes hipoxémicos, pero puede también mejorar la disnea incluso cuando el paciente no está desaturado. También son eficaces medidas sencillas como el aire fresco (corriente o de ventiladores) dirigido a la cara del paciente21.
DiuréticosLos diuréticos son la base del tratamiento y su objetivo es la descongestión pulmonar. La vía de administración y las dosis deben ser acordes con la situación clínica y el grado de congestión, con un seguimiento estrecho de la respuesta para su titulación. Una alternativa en fases muy avanzadas es la administración de furosemida subcutánea (s.c.), que puede usarse en el ámbito hospitalario o ambulatorio22, lo que reduce los ingresos23. La furosemida convencional es alcalina (pH 8,5-9) y puede causar irritación en la piel, por lo que se ha desarrollado una furosemida isotónica (pH 7-7,8) para su administración s.c., aún no comercializada, con respuesta diurética similar a la intravenosa (i.v.)24.
VasodilatadoresLos vasodilatadores se pueden usar como apoyo en el tratamiento sintomático de la disnea siguiendo las recomendaciones habituales para su empleo en IC, para evitar la hipotensión sintomática3.
Inotrópicos ambulatoriosEl levosimendán tiene ventajas demostradas por sus efectos sostenidos tras la infusión inicial, permite su uso en pacientes tratados con bloqueadores beta y no aumenta el consumo de oxígeno, entre otros. Se utiliza en pacientes con IC avanzada muy sintomáticos a pesar del tratamiento médico óptimo, con el objetivo de aliviar los síntomas, mejorar la calidad de vida y reducir los reingresos25,26.
OpiáceosLos opiáceos están indicados para el tratamiento de la disnea persistente, y actúan en receptores centrales y periféricos disminuyendo el impulso respiratorio y favoreciendo el confort del paciente. Su uso es seguro, sin impacto negativo en el pronóstico y con un riesgo bajo de depresión respiratoria si se evitan dosis altas27. El sulfato de morfina o el clorhidrato de morfina se pueden administrar por vía oral y existen formulaciones de liberación prolongada.
Toracocentesis evacuadoraLa toracocentesis evacuadora se plantea en caso de que haya derrame pleural significativo.
Congestión sistémicaLos edemas periféricos son uno de los signos más frecuentes en pacientes con IC avanzada. El tratamiento de la congestión se basa en el uso de diuréticos, y pueden requerirse dosis altas y/o la administración combinada de varios de ellos; también es seguro y eficaz en la IC con congestión refractaria el uso de suero salino hipertónico con dosis altas de furosemida i.v.28. Los edemas en las extremidades inferiores pueden ser especialmente rebeldes al tratamiento; se debe favorecer la deambulación tanto como sea posible, medidas posturales y el adecuado tratamiento del dolor y de las úlceras e infecciones que se asocian con frecuencia19.
DolorEl dolor es habitual en fases avanzadas y se subestima frecuentemente21. Su causa no está bien definida; se puede deber a la propia IC (hipoperfusión e isquemia, congestión), comorbilidades (artrosis, neuropatía diabética, etc.) o procesos intercurrentes. Independientemente de la causa, se debe evaluar, no minimizarlo y tratarlo correctamente. Los analgésicos de primera línea incluyen el paracetamol y el metamizol; deben evitarse los antiinflamatorios no esteroideos por su impacto negativo en la función renal y la retención hidrosalina. En ciertos casos, la colchicina se puede utilizar también como antiinflamatorio. Como tratamientos coadyuvantes, pueden añadirse antidepresivos, anticomiciales, benzodiacepinas o esteroides (estos últimos con especial cuidado por su potencial retención hídrica). En un segundo escalón se mantienen los tratamientos de primera línea y los coadyuvantes, se añaden opiáceos débiles (codeína, dihidrocodeína, tramadol) y se llega, en un tercer escalón, al uso de opiáceos potentes si fuera necesario (morfina, fentanilo, buprenorfina, oxicodona, tapentadol).
DepresiónSe debe distinguir la depresión de la tristeza o el dolor anticipado de la fatiga, el insomnio y otros síntomas que la IC puede ocasionar29. La depresión puede responder a los inhibidores selectivos de la recaptación de serotonina, si bien estos se han asociado con hiponatremia y retención hídrica, probablemente debido al aumento de vasopresina30. Deben evitarse los antidepresivos tricíclicos por sus efectos anticolinérgicos, hipotensión ortostática y prolongación del intervalo QTc, entre otros31. El tratamiento se debe complementar con medidas de apoyo y no farmacológicas2. Las benzodiacepinas resultan eficaces en caso de ansiedad, aunque pueden contribuir a la astenia19.
AsteniaLa IC avanzada se asocia con atrofia y debilidad osteomuscular, que intensifican la fatiga y la disnea32. Hay que identificar y tratar causas secundarias, como la anemia y la ferropenia, las infecciones o los trastornos del sueño. El entrenamiento físico puede ser beneficioso, pero es difícilmente aplicable en este contexto; es recomendable mantener la movilidad y disminuir el encamamiento en la medida de lo posible21,32.
Otros síntomasSe debe evaluar y tratar el insomnio, el síndrome confusional, las náuseas, los vómitos, la anorexia, las úlceras por presión o las úlceras en las extremidades inferiores, las alteraciones del hábito intestinal, etc. Son de aplicación las medicaciones y medidas habituales para estos síntomas en cualquier contexto. Es importante no minimizarlos, pues contribuyen a que las últimas etapas de la vida sean más desagradables y empeoran la percepción de calidad de vida del paciente19,21.
PACIENTES CON DISPOSITIVOSMarcapasos y desfibriladoresLa posibilidad de tener que desactivar un dispositivo implantado a lo largo de la enfermedad se debe discutir con el paciente y su familia desde el momento del implante4,33-35 y posteriormente, sobre todo cuando haya cambios significativos en el curso de la enfermedad (reingresos, tratamientos del DAI, etc.), y evitar hacerlo en los últimos días de vida4,36. Es fundamental explicar las ventajas y los inconvenientes de cada decisión, que se deben recoger en la historia clínica, y que la decisión sea consensuada entre todos los profesionales que tratan al paciente34.
En el caso de los marcapasos, se recomienda mantener su normal funcionamiento, ya que no modifica el curso de la enfermedad y su desactivación puede producir un empeoramiento de los síntomas e incluso el fallecimiento de pacientes dependientes sin ritmo propio33. En pacientes con tratamiento de resincronización cardiaca, se aconseja mantener la estimulación biventricular por el riesgo de empeorar los síntomas35. Se debe evitar el implante o recambio de estos dispositivos en fases avanzadas de la enfermedad.
Respecto al DAI, un tercio de los pacientes con IC avanzada recibe un tratamiento (apropiado o inapropiado) en las fases finales de la enfermedad, especialmente en los últimos días de vida, lo que causa dolor, supone una situación desagradable para el paciente y su familia y alarga la vida innecesariamente35. Es amplio el consenso sobre la conveniencia de desactivar estos tratamientos33,34,36. Se pueden desactivar las terapias antitaquicardia, manteniendo el modo de «solo monitorización», y las antibradicardia, especialmente en pacientes dependientes de la estimulación4. En caso de que no se disponga de programador, se puede realizar colocando un imán.
En el caso de otros dispositivos, como los registradores s.c. de eventos o los neuroestimuladores, también se recomienda su desactivación35.
Dispositivos de asistencia ventricularLos dispositivos de asistencia ventricular izquierda han demostrado mejorar tanto el pronóstico como la calidad de vida de los pacientes con IC avanzada, por lo que su uso como terapia de destino es cada vez más frecuente. Se recomienda que la consulta con especialistas en CP se incluya sistemáticamente en la valoración del paciente antes del implante de estos dispositivos y que los cuidados que se precisen estén disponibles en todo momento37. Sin embargo, menos de la mitad de los pacientes tienen una consulta con especialistas en CP en el mes previo a su muerte y la gran mayoría fallecen en el hospital, dentro de la unidad de cuidados intensivos, con terapias avanzadas como ventilación mecánica o tratamiento de sustitución renal38. Por otro lado, la decisión de desactivar una asistencia ventricular es una cuestión que debe ser consensuada y sobrepasa lo estrictamente médico.
ORDEN DE NO REANIMARLa orden de no reanimar (ONR) debería ofrecer a los pacientes, adecuadamente informados, la posibilidad de expresar su renuncia, voluntaria y anticipada, a recibir una reanimación cardiopulmonar (RCP) en caso de tener una parada cardiorrespiratoria (PCR). A pesar del pronóstico que tiene la IC, el uso de estas ONR está menos extendido que en otras especialidades, con una utilización menor, más tardía, menos convincente y peor interpretada39.
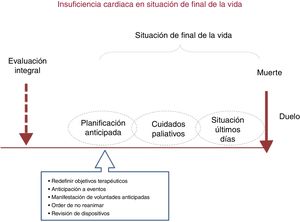
El desarrollo de una ONR forma parte de la planificación general y anticipada de los cuidados al final de la vida (figura 3). Esta planificación permite al paciente registrar sus deseos de atención sanitaria y participar en la toma de decisiones relevantes en esta fase de la enfermedad. Las conversaciones sobre las preferencias relativas a estos cuidados deben realizarse con suficiente antelación al estadio terminal, coincidiendo con revisiones ambulatorias, donde es esperable una mayor estabilidad clínica que facilite su participación activa en la toma de decisiones, o con episodios de descompensación o incluso descargas del DAI36.
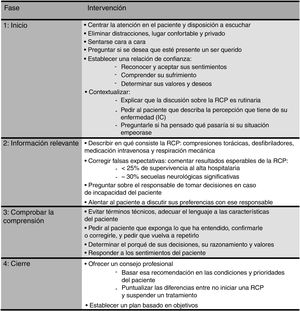
Todo esto implica y favorece que los pacientes estén correctamente informados de la situación y pronóstico de la IC desde el momento del diagnóstico. La figura 4 resume las recomendaciones básicas sobre el contenido y las características de las conversaciones sobre ONR: se debe favorecer el diálogo mediante preguntas sobre la comprensión de la enfermedad y el significado de la PCR y la RCP, evitando términos técnicos40.
Recomendaciones básicas sobre el contenido y las características de las conversaciones sobre las órdenes de no reanimar: guía de desarrollo de una conversación. IC: insuficiencia cardiaca; RCP: reanimación cardiopulmonar. Modificada con permiso de Ruiz García et al.40.
Los pacientes suelen solicitar que el médico les dé su consejo profesional, por lo que se debe estar preparado para responder adecuadamente basándose en la evidencia médica y las preferencias expuestas por el paciente. Las conversaciones sobre el final de la vida deben concluir con una decisión y una invitación a nuevas discusiones en el futuro para asegurarse de que la planificación del paciente sigue siendo acorde con sus deseos41.
A pesar del beneficio que tendría la introducción temprana de estas conversaciones en su abordaje, la inmensa mayoría de los pacientes con IC reconocen no haber tenido una conversación con sus médicos sobre el final de la vida ni sobre sus preferencias de reanimación16,39. De hecho, solo un 12% de los médicos implicados en el tratamiento de estos pacientes reconocen mantener periódicamente discusiones sobre el final de la vida42. Entre las razones están la falta de experiencia y formación, la falta de habilidades para la comunicación que dificulta encontrar el vocabulario adecuado para explicar la situación y el pronóstico de modo comprensible, la incertidumbre sobre la evolución de la IC, el miedo a causar una preocupación innecesaria o desesperanza en etapas tempranas de la enfermedad e incluso la falta de tiempo42.
Un problema que puede entorpecer el desarrollo y la implementación de estas ONR en los pacientes es su excesivo optimismo. La percepción que los pacientes cardiológicos tienen sobre el pronóstico de la IC43 y las maniobras de RCP44 se aleja significativamente de la realidad. Es habitual que estos pacientes rechacen o no soliciten este tipo de información para mantenerse en una aparente ignorancia esperanzadora, en lugar de afrontar un mal pronóstico que no les aporta ningún beneficio. Esta sobrestimación de las oportunidades de supervivencia y recuperación tras una PCR podría condicionar sus deseos y preferencias respecto al plan de tratamiento44. Por ello se hace preciso que el paciente tenga acceso temprano a toda la información pronóstica actualizada y comprensible, que le permita en cada estadio de la cardiopatía adecuar la estrategia de tratamiento a sus verdaderos deseos.
Por todo lo anterior, hay que insistir en la necesidad de establecer de forma temprana estas conversaciones y reflejar de manera clara y rápidamente accesible en la historia clínica de los pacientes sus voluntades sobre la RCP. En la ONR debe figurar el nombre del médico responsable, la fecha en que se toma la decisión y un breve resumen clínico en el que se razone la decisión. Esta orden, revisable en el tiempo, debe figurar en un lugar visible de la historia clínica del paciente, de manera que todo el personal sanitario tenga rápido acceso a la información en caso de PCR. Se recomienda que la decisión de la ONR sea compartida en sesión clínica con el resto del equipo multidisciplinario que está en contacto directo con el paciente, así como con su equipo de atención primaria.
Por último, es necesario precisar que la ONR solo se debe aplicar en el momento único de la PCR, para no iniciar la RCP o para suspenderla, pero en ningún caso debe afectar a otros cuidados39,41. Así, son poco explicables las infrautilizaciones de tratamientos farmacológicos, medios diagnósticos y medidas no farmacológicas en los grupos de pacientes con IC y una ONR en su historia frente a aquellos que no la poseían45.
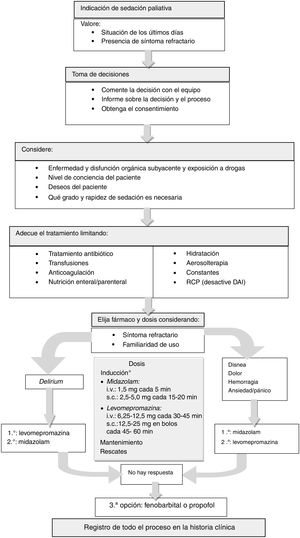
SEDACIÓN PALIATIVALa sedación paliativa se debe considerar como una herramienta terapéutica para el control de un síntoma refractario para el que los demás tratamientos no han conseguido ser eficaces y que provoca un malestar o un sufrimiento intenso en el paciente en situación de final de la vida46. Consiste en la administración de fármacos, solo en la dosis necesaria, para causar la disminución del nivel de conciencia hasta un punto en el que el paciente ya no pueda percibir el síntoma47, y para realizarla se debe contar con el consentimiento del paciente. Se trata de un proceso que incluye la toma de decisión, su registro, el procedimiento y el seguimiento del paciente sedado (figura 5).
Proceso de la sedación paliativa. DAI: desfibrilador automático implantable; i.v.: por vía intravenosa; RCP: reanimación cardiopulmonar; s.c.: por vía subcutánea. *Hasta alcanzar el nivel de sedación requerido. Puede elegirse el fármaco en función del síntoma: en caso de disnea, dolor o hemorragia, se propone elegir midazolam; en caso de delirio refractario, se recomienda utilizar inicialmente levomepromazina, aunque en muchas ocasiones también se utiliza el midazolam; el midazolam puede producir agitación paradójica y tiene una dosis techo (alrededor de 160 mg/24 h), como también la tiene la levomepromazina (200-300 mg/24 h). Si se alcanza la dosis máxima recomendada y no se ha logrado la sedación deseada con midazolam o levomepromazina, se puede combinar el primer fármaco utilizado con el otro, dejando como última opción el propofol o el fenobarbital (estos últimos se usarán solos, sin agregarlos a midazolam o levomepromazina).
La sedación paliativa debe plantearse si:
- •
El paciente está en situación de últimos días.
- •
Existe un síntoma refractario.
- •
El objetivo es reducir el sufrimiento provocado por ese síntoma.
- •
El paciente la desea, debidamente informado, y tras obtener su consentimiento o el de la persona en quien haya delegado. Cuando el paciente no puede participar en la decisión, será necesario consultar el registro de instrucciones previas.
Dado que puede resultar una decisión compleja, cuando se pueda, se deberá tomar de forma colegiada por todos los profesionales implicados en la atención del paciente.
RegistroTodo el proceso de toma de decisiones y el procedimiento quedará registrado en la historia clínica.
Procedimiento- •
Se debe realizar una adecuación del esfuerzo terapéutico. En ese momento ya no estarán indicados, y se deben suspender, algunos tratamientos (anticoagulantes, transfusiones, nutrición enteral o parenteral). Asimismo, se debe hacer constar la ONR y haberse desactivado el DAI si fuera el caso.
- •
Se debe buscar un lugar adecuado para el paciente y su familia y proporcionarles la atención que necesiten.
- •
Elección del fármaco. No hay evidencia de superioridad de un fármaco respecto a otros, pero debería cumplir los siguientes requisitos: rápido inicio, fácil ajuste de dosis, mínimos efectos secundarios y uso familiar. Los opiáceos no están indicados para la sedación paliativa47, pero se emplearán de manera concomitante si el síntoma refractario es dolor o disnea, o si los tuviera pautados previamente. Los grupos de fármacos (y prototipo) más utilizados en sedación paliativa son:
- –
Benzodiacepinas: midazolam (el más utilizado48).
- –
Neurolépticos: levomepromazina.
- –
Barbitúricos: fenobarbital.
- –
Anestésicos: propofol.
- •
Cálculo de la dosis necesaria. Se determinará la dosis de inducción, aquella necesaria para alcanzar, en ese momento, el nivel deseado de sedación desde el nivel de alerta inicial (figura 5).
- •
Dosis de mantenimiento. Si se desea mantener continuamente el nivel de sedación alcanzado con la dosis de inducción, se administrará la dosis necesaria en forma de infusión continua. Se puede calcular multiplicando la dosis de inducción por el número de dosis necesarias que habría que administrar en 24 h según la vida media del fármaco.
- •
Dosis de rescate. Cuando el paciente pierde temporalmente el nivel de sedación deseado será necesario utilizar una dosis de rescate, que será la misma que se ha requerido para inducir la sedación, salvo en el caso del propofol, que será el 50% de dicha dosis.
Se deberá realizar una evaluación sistemática del nivel de sedación (puede utilizarse la escala de Ramsay49, ), la respuesta a la estimulación, la temperatura, las secreciones bronquiales o los movimientos musculares espontáneos, y registrarlo en la historia clínica.
El adecuado control de síntomas durante la sedación puede requerir mantener o añadir otros fármacos.
CONSIDERACIONES ÉTICASComunicación y toma de decisionesLa atención de los pacientes con IC avanzada debe respetar los 4 principios de la bioética4, salvo en las situaciones en que sea imposible cumplirlos porque 2 o más entren en conflicto, en cuyo caso hay que individualizar cada caso. Se debe alentar a los pacientes a expresar y documentar sus valores, objetivos y preferencias, en particular en lo que respecta a la toma de decisiones al final de la vida4. En situaciones complejas, se debe considerar una consulta con el comité de ética asistencial o con la unidad de CP36.
La comunicación y la planificación anticipada de cuidados frecuentemente son mejorables. Las preferencias respecto a tratamientos de soporte vital a menudo no se discuten y las que se refieren a ONR muchas veces no se documentan o difieren de las preferencias de los pacientes50. Para mejorar esta situación es fundamental una comunicación abierta desde el diagnóstico, que se debe intensificar en puntos de inflexión como ingresos, deterioro funcional o agotamiento de opciones de tratamiento curativo. La comunicación se debe adaptar a la disposición del paciente para participar y debe versar sobre la posibilidad de reanimación y los tratamientos de soporte vital51, pero también sobre los objetivos y las inquietudes del paciente y sus familiares. Estos objetivos y preferencias deben actualizarse periódicamente. Los aspectos específicos de la enfermedad se deben abordar cuando sea apropiado, como el miedo a la disnea y los protocolos que se usarán para evitarla52, la reprogramación de un DAI34 o la desconexión de la asistencia ventricular.
Apoyo psicosocial y espiritual a pacientes y familias. Atención al dueloLa IC avanzada genera malestar físico, psíquico, emocional y social, con repercusión en la vida de la persona, su familia y entorno2. Es necesario explorar el sufrimiento y las reacciones ante la enfermedad, el duelo, la tristeza, la desmoralización y la depresión del paciente y su entorno sociofamiliar. El concepto de «atención centrada en la persona» se basa en tratar al paciente como un ser humano integral que consiste en cuerpo, mente y espíritu inseparables. Este concepto reconoce la importancia de la espiritualidad en la vida de una persona (además de las dimensiones físicas y mentales), frecuentemente infravalorada, y cuya naturaleza es multidimensional y abarca cuestiones, valores, creencias sobre agonía y muerte, asuntos religiosos y existenciales53. El acompañamiento espiritual debe entenderse como un acercamiento profesional y ético. Se establece un vínculo terapéutico a través de la relación de ayuda y la escucha activa para encaminar hacia la muerte en paz, dejando un legado de sabiduría y ternura a sus allegados. La intervención consiste en aliviar y controlar los síntomas y también en solucionar problemas psicosociales con el fin de conocer necesidades, abordar sus dudas, facilitar la aceptación de su enfermedad (afrontamiento), ayudar a finalizar las actividades y procesos emocionales no resueltos, sus relaciones sociales, familiares y afectivas, incluyendo la preparación para la muerte. En la IC avanzada, el bienestar espiritual permanece estable y, aunque no existe una clara equivalencia con la situación sintomática, experimentar la paz espiritual predice mejor la mortalidad que el estado funcional y la comorbilidad, y un mayor bienestar espiritual se asocia con menor incidencia de depresión, por lo que el asesoramiento espiritual tiene un impacto positivo en la calidad de vida54. La atención espiritual debe integrarse desde un ámbito multidisciplinario que debe incluir, si el paciente lo desea, a capellanes, pastores o guías espirituales de la confesión correspondiente. Por otro lado, para una correcta intervención con la familia, se debe identificar al cuidador principal, valorar las necesidades del paciente, conocer las limitaciones o sobrecarga del cuidador, proporcionar apoyo, capacitarlo para el cuidado del paciente y, en situaciones avanzadas, prepararlo para la pérdida. El duelo, con sus diferentes fases, tiene importantes consecuencias psicoafectivas, que frecuentemente necesitarán un acompañamiento. La atención al duelo se centra en ayudar a los familiares y el entorno social a expresar el dolor y la aflicción ante la pérdida. En esta fase, el médico y la enfermera de atención primaria, así como los equipos de profesionales de CP, tienen un papel destacado.
CONCLUSIONESLa IC es un síndrome clínico complejo que conduce a un deterioro funcional progresivo e inexorable en la mayor parte de los casos y condiciona la calidad de vida de los pacientes. Los CP mejoran la calidad de vida de estos pacientes y sus familias, y se deben considerar desde el momento del diagnóstico y no solo en las fases finales de la enfermedad, informando de manera activa al paciente y primando también su protagonismo en la toma de decisiones. Es fundamental controlar síntomas y mejorar la calidad de vida, lo cual se consigue con un adecuado abordaje terapéutico, la utilización escalonada de fármacos y primando la comodidad del paciente en cuanto a posología, vía de administración y dosis, así como un correcto apoyo psicosocial. Estos cuidados deben extenderse a los familiares durante la fase de duelo. Es fundamental la implicación de las autoridades sanitarias, que hagan llegar la disponibilidad de los CP al paciente con IC.
CONFLICTO DE INTERESESNo se declara ninguno.