Las indicaciones para los dispositivos cardiacos implantables (DCI), tales como el desfibrilador automático implantable (DAI) y la terapia de resincronización cardiaca (TRC), se establecieron antes de que se aprobaran los nuevos tratamientos médicos para la insuficiencia cardiaca (IC) con fracción de eyección reducida (IC-FEr)1. Los nuevos tratamientos, como la combinación de sacubitrilo y valsartán (SV) y los inhibidores del cotransportador de sodio y glucosa se han relacionado con el remodelado inverso del ventrículo izquierdo (RIVI) y la mejora de la clase funcional2, por lo que no está claro cuál es el mejor momento para implantar un DCI, ya que una mejora de la función del ventrículo izquierdo o de la clase funcional con los nuevos tratamientos de la IC-FEr podría significar que dejara de estar indicado.
El objetivo de este estudio es analizar los efectos del tratamiento con SV a la hora de modificar la indicación del DCI en una población no seleccionada con IC-FEr crónica y hallar posibles factores predictores basales relacionados con pérdida de indicación para DCI.
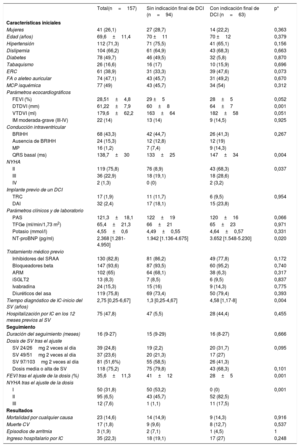
Se hizo el análisis retrospectivo de los pacientes con IC crónica sintomática y fracción de eyección del ventrículo izquierdo < 40% que iniciaron el tratamiento con SV entre septiembre de 2016 y diciembre de 2020. Los pacientes recibieron tratamiento médico según las guías de práctica clínica (tabla 1)1. Antes de iniciar el tratamiento con SV, se definió a los pacientes con indicación de DCI (DAI/TRC) según la guía europea vigente1. En la figura 1 se muestra el esquema del estudio. Se analizaron las características basales, la existencia de cambio en cuanto a la indicación de dispositivo tras ajustar la dosis de SV y los posibles factores clínicos predisponentes. Al cabo de al menos 6 meses, una vez alcanzada la dosis máxima tolerada de SV, se revaluó la indicación de DCI. Tras el análisis univariante, se incluyeron en el modelo de regresión logística los factores basales asociados con pérdida de indicación de DCI tras iniciar el tratamiento con SV. El modelo se ajustó por posibles factores de confusión. En el análisis multivariante se incluyeron la enfermedad renal crónica, la etiología de la IC, el tiempo entre el diagnóstico de la IC y el inicio del tratamiento con SV, cifras basales de la fracción aminoterminal del propéptido natriurético cerebral (NT-proBNP), el diámetro telediastólico del ventrículo izquierdo (DTDVI), la clase funcional de la New York Heart Association (NYHA) y la fracción de eyección del ventrículo izquierdo. Todos los valores de p<0,05 se consideraron estadísticamente significativos. El análisis estadístico se hizo con la versión 25 del sistema SPSS (IBM Corporation, Estados Unidos). El estudio fue aprobado por el comité de ética local (número CEIm 2019/8745).
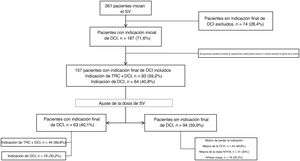
Características basales, seguimiento y resultados de los pacientes en función de la indicación final de DCI
| Total(n=157) | Sin indicación final de DCI (n=94) | Con indicación final de DCI (n=63) | p* | |
|---|---|---|---|---|
| Características iniciales | ||||
| Mujeres | 41 (26,1) | 27 (28,7) | 14 (22,2) | 0,363 |
| Edad (años) | 69,6±11,4 | 70 ±11 | 70 ±12 | 0,379 |
| Hipertensión | 112 (71,3) | 71 (75,5) | 41 (65,1) | 0,156 |
| Dislipemia | 104 (66,2) | 61 (64,9) | 43 (68,3) | 0,663 |
| Diabetes | 78 (49,7) | 46 (49,5) | 32 (5,8) | 0,870 |
| Tabaquismo | 26 (16,6) | 16 (17) | 10 (15,9) | 0,696 |
| ERC | 61 (38,9) | 31 (33,3) | 39 (47,6) | 0,073 |
| FA o aleteo auricular | 74 (47,1) | 43 (45,7) | 31 (49,2) | 0,670 |
| MCP isquémica | 77 (49) | 43 (45,7) | 34 (54) | 0,312 |
| Parámetros ecocardiográficos | ||||
| FEVI (%) | 28,51±4,8 | 29 ±5 | 28±5 | 0,052 |
| DTDVI (mm) | 61,22±7,9 | 60±8 | 64±7 | 0,001 |
| VTDVI (ml) | 179,6±62,2 | 163±64 | 182±58 | 0,051 |
| IM moderada-grave (III-IV) | 22 (14) | 13 (14) | 9 (14,5) | 0,925 |
| Conducción intraventricular | ||||
| BRIHH | 68 (43,3) | 42 (44,7) | 26 (41,3) | 0,267 |
| Ausencia de BRIHH | 24 (15,3) | 12 (12,8) | 12 (19) | |
| MP | 16 (1,2) | 7 (7,4) | 9 (14,3) | |
| QRS basal (ms) | 138,7±30 | 133±25 | 147±34 | 0,004 |
| NYHA | ||||
| II | 119 (75,8) | 76 (8,9) | 43 (68,3) | 0,037 |
| III | 36 (22,9) | 18 (19,1) | 18 (28,6) | |
| IV | 2 (1,3) | 0 (0) | 2 (3,2) | |
| Implante previo de un DCI | ||||
| TRC | 17 (1,9) | 11 (11,7) | 6 (9,5) | 0,954 |
| DAI | 32 (2,4) | 17 (18,1) | 15 (23,8) | |
| Parámetros clínicos y de laboratorio | ||||
| PAS | 121,3±18,1 | 122±19 | 120±16 | 0,066 |
| TFGe (ml/min/1,73 m2) | 65,4±21,3 | 66±21 | 65±23 | 0,971 |
| Potasio (mmol/l) | 4,55±0,6 | 4,49±0,55 | 4,64±0,57 | 0,331 |
| NT-proBNP (pg/ml) | 2.368 [1.281-4.950] | 1.942 [1.136-4.675] | 3.652 [1.548-5.230] | 0,020 |
| Tratamiento médico previo | ||||
| Inhibidores del SRAA | 130 (82,8) | 81 (86,2) | 49 (77,8) | 0,172 |
| Bloqueadores beta | 147 (93,6) | 87 (93,5) | 60 (95,2) | 0,740 |
| ARM | 102 (65) | 64 (68,1) | 38 (6,3) | 0,317 |
| iSGLT2 | 13 (8,3) | 7 (8,5) | 6 (9,5) | 0,837 |
| Ivabradina | 24 (15,3) | 15 (16) | 9 (14,3) | 0,775 |
| Diuréticos del asa | 119 (75,8) | 69 (73,4) | 50 (79,4) | 0,393 |
| Tiempo diagnóstico de IC-inicio del SV (años) | 2,75 [0,25-6,67] | 1,3 [0,25-4,67] | 4,58 [1,17-8] | 0,004 |
| Hospitalización por IC en los 12 meses previos al SV | 75 (47,8) | 47 (5,5) | 28 (44,4) | 0,455 |
| Seguimiento | ||||
| Duración del seguimiento (meses) | 16 (9-27) | 15 (9-29) | 16 (8-27) | 0,666 |
| Dosis de SV tras el ajuste | ||||
| SV 24/26mg 2 veces al día | 39 (24,8) | 19 (2,2) | 20 (31,7) | 0,095 |
| SV 49/51mg 2 veces al día | 37 (23,6) | 20 (21,3) | 17 (27) | |
| SV 97/103mg 2 veces al día | 81 (51,6%) | 55 (58,5) | 26 (41,3) | |
| Dosis media o alta de SV | 118 (75,2) | 75 (79,8) | 43 (68,3) | 0,101 |
| FEVI tras el ajuste de la dosis (%) | 35,6±11,3 | 41±12 | 28±5 | 0,001 |
| NYHA tras el ajuste de la dosis | ||||
| I | 50 (31,8) | 50 (53,2) | 0 (0) | 0,001 |
| II | 95 (6,5) | 43 (45,7) | 52 (82,5) | |
| III | 12 (7,6) | 1 (1,1) | 11 (17,5) | |
| Resultados | ||||
| Mortalidad por cualquier causa | 23 (14,6) | 14 (14,9) | 9 (14,3) | 0,916 |
| Muerte CV | 17 (1,8) | 9 (9,6) | 8 (12,7) | 0,537 |
| Episodios de arritmia | 3 (1,9) | 2 (7,1) | 1 (4,5) | 1 |
| Ingreso hospitalario por IC | 35 (22,3) | 18 (19,1) | 17 (27) | 0,248 |
ARM: antagonistas del receptor mineralocorticoideo; BRIHH: bloqueo de rama izquierda del haz de His; CV: cardiovascular; DAI: desfibrilador automático implantable; DCI: dispositivo cardiaco implantable; DTDVI: diámetro telediastólico del ventrículo izquierdo; ERC: enfermedad renal crónica; FA: fibrilación auricular; FEVI: fracción de eyección del ventrículo izquierdo; IC: insuficiencia cardiaca; IM: insuficiencia mitral; iSGLT2: inhibidores del cotransportador de sodio y glucosa tipo 2; MCP: miocardiopatía; MP: marcapasos; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; NYHA: clase funcional de la New York Heart Association; PAS: presión arterial sistólica; SRAA: sistema renina-angiotensina-aldosterona; SV: sacubitrilo-valsartán; TFGe: tasa de filtrado glomerular estimada; TRC: terapia de resincronización cardiaca; VTDVI: volumen telediastólico del ventrículo izquierdo.
Los valores expresan n (%), media ± desviación estándar o mediana [intervalo intercuartílico].
Esquema del estudio. DAI: desfibrilador automático implantable; DCI: dispositivo cardiaco implantable; FEVI: fracción de eyección del ventrículo izquierdo; NYHA: clase funcional de la New York Heart Association; TRC: terapia de resincronización cardiaca; SV: sacubitrilo-valsartán.
Durante el periodo de estudio, 261 pacientes con IC-FEr crónica sintomática iniciaron tratamiento con SV. Se constató una indicación inicial de DCI en 187 pacientes (71,6%). Tras excluir a los pacientes perdidos durante el seguimiento, los que suspendieron precozmente el tratamiento con SV y los que fallecieron durante el periodo de ajuste de la dosis, en el análisis final se incluyó a 157 pacientes (figura 1). Las características basales de los pacientes se describen en la tabla 1. Antes del tratamiento con SV, 93 pacientes (59,2%) cumplían las indicaciones de las guías de la Sociedad Europea de Cardiología (ESC)1 para el implante de TRC más DAI y 64 (40,8%), solo para DAI. Tras la titulación del tratamiento con SV, la mayoría de los pacientes perdieron la indicación de DCI (94 [59,9%]; p<0,001) (figura 1). Antes de iniciar el tratamiento con SV, 49 pacientes ya llevaban implantado un DCI (31,3%) (17 TRC y 32 DAI). Cabe destacar que aproximadamente el 30% de los pacientes portadores de DCI perdieron la indicación durante el seguimiento. Los pacientes que perdieron la indicación de DCI tras el ajuste de la dosis de SV presentaban una clase funcional de la NYHA menos avanzada, un QRS más estrecho, menores diámetro y volumen telediastólicos del ventrículo izquierdo y una concentración inferior de NT-proBNP cuando se inició el tratamiento con SV (tabla 1). Y lo que es más importante, en los pacientes con menos tiempo entre el diagnóstico de la IC y el inicio del tratamiento con SV fue más probable la ausencia de indicación final de DCI (1,3 [0,25-4,67] frente a 4,58 [1,17-8] años; p<0,004). La dosis de SV alcanzada tras el ajuste de dosis no se relacionó con la indicación final de DCI (p <0,101).
El RIVI fue la razón principal relacionada con la pérdida de indicación de DCI (n=44; 46,8%), seguido de la mejora de los síntomas (NYHA I, n=31, 33%) o de ambas cosas (n=19, 20,2%). Tras el análisis multivariante, los únicos factores basales relacionados de manera independiente con la pérdida de indicación de DCI fueron: menos tiempo entre el diagnóstico de la IC y el inicio del tratamiento con SV (hazard ratio [HR] ajustada = 0,90; intervalo de confianza del 95% [IC95%], 0,83-0,99; p <0,025), una clase funcional de la NYHA menos avanzada (HR ajustada = 0,30; IC95%, 0,13-0,70; p <0,005) y un menor DTDVI (HR = 0,93; IC95%, 0,88-0,99; p <0,023). El seguimiento medio fue de 16 (9-27) meses. Durante el seguimiento, no se observaron diferencias en cuanto a mortalidad, episodios arrítmicos o descompensaciones de IC entre los pacientes en quienes se mantuvo la indicación de DCI y quienes no (tabla 1).
El principal hallazgo de este estudio es que el tratamiento con SV redujo de manera considerable la necesidad de DCI en los pacientes con IC-FEr. Cabe destacar que en casi un 60% de los pacientes con una indicación inicial de DCI, esta dejó de cumplirse tras el tratamiento con SV, fundamentalmente por el RIVI, una de las mayores ventajas observadas del tratamiento con SV3,4. En estudios recientes con SV se ha demostrado la relación entre el RIVI y los resultados clínicos en el paciente con IC-FEr5. El impacto en el RIVI de otros tratamientos para pacientes con IC-FEr es inferior3,6, lo que puede representar una menor capacidad para reducir la indicación de DCI. En el presente estudio, un menor tiempo entre el diagnóstico de la IC y el inicio del tratamiento con SV, una mejor clase funcional de la NYHA y la menor dilatación del ventrículo izquierdo fueron factores basales predictores independientes de la pérdida de indicación de DCI. Estos hallazgos destacan la importancia de optimizar el tratamiento de la IC-FEr en las primeras etapas de la enfermedad para favorecer el rápido RIVI y la mejora clínica2. Por último, los resultados de este estudio muestran que una estrategia que priorice el tratamiento con SV antes de considerar un DCI evitaría la necesidad de tal dispositivo en casi el 60% de los casos y reduciría las posibles complicaciones a corto y largo plazo de estos dispositivos, además de relacionarse con un menor gasto sanitario total sin alterar el pronóstico de los pacientes. Las principales limitaciones de este estudio son su naturaleza retrospectiva y el reducido porcentaje de pacientes tratados con inhibidores del SGLT2, un fármaco también relacionado con una mejora pronóstica de los pacientes con IC-FEr2. No obstante, vale la pena mencionar que la mayoría de los estudios que analizan el impacto del tratamiento con SV en el remodelado no evalúan el papel de los inhibidores del SGLT23–6, seguramente porque cuando se llevaron a cabo este fármaco aún no estaba aprobado para el tratamiento de la IC-FEr.
En conclusión, el tratamiento con SV se relaciona con una disminución de casi el 60% en la indicación de DCI en los pacientes con IC-FEr. Puesto que una enfermedad menos avanzada y un tiempo más corto hasta el inicio del tratamiento con SV influyen en la indicación de DCI, convendría iniciar el SV lo antes posible y siempre antes de considerar los DCI.
FINANCIACIÓNEsta investigación no recibió financiación externa.
CONTRIBUCIÓN DE LOS AUTORESConceptualización, metodología, conservación de los datos, análisis formal: L. C. Belarte-Tornero y N. Farré; investigación: L.C. Belarte-Tornero, N. Farré y D. Mojón; preparativos para la redacción del borrador original: L.C. Belarte-Tornero y D. Mojón; revisión y edición del artículo: N. Farré y L.C. Belarte-Tornero; visualización: D. Mojón, E. Solé-González, S. Ruiz-Bustillo y S. Valdivielso-More; supervisión: N. Farré. Todos los autores han leído y aceptado la versión publicada del artículo.
CONFLICTO DE INTERESESL.C. Belarte-Tornero comunica subvenciones, honorarios de conferencias y apoyo económico por asistir a reuniones de Novartis, Rovi y AstraZeneca. N. Farré comunica honorarios de conferencias por parte de Novartis. S. Valdivielso-More comunica honorarios por actividades docentes y apoyo económico por asistir a reuniones de Novartis.