Describir la epidemiología y el tratamiento administrado recientemente a una amplia cohorte de pacientes con insuficiencia cardiaca (IC).
MétodosEstudio observacional retrospectivo de base poblacional, realizado utilizando la base de datos BIG-PAC, que incluye a personas de edad ≥ 18 años que solicitaron atención por IC en 2017-2019. Las principales variables fueron: prevalencia/incidencia-anual, comorbilidades, variables clínicas y medicación administrada.
ResultadosSe identificó a 19.762 pacientes con IC de un total de 1.189.003 sujetos que requirieron atención médica en 2017-2019 (en 2019, media de edad, 78,3 años; el 53,0% varones). De ellos, la distribución por tipo de fracción de eyección del ventrículo izquierdo (FEVI) fue: el 51,7% con FEVI reducida, el 40,2% con FEVI conservada y el 8,1% con FEVI en rango medio. En el año 2019, la prevalencia fue del 1,89% (IC95%, 1,70-2,08), con una tasa de incidencia de 2,78 casos nuevos por cada 1.000 sujetos/año. No se observaron diferencias estadísticamente significativas en prevalencia y/o incidencia durante el periodo 2017-2019. De los pacientes con IC-FEr, solo un 64% tomaba bloqueadores beta; el 80,5%, inhibidores de la enzima de conversión de la angiotensina/antagonistas del receptor de la angiotensina II o sacubitrilo-valsartán, y un 29,8%, un antialdosterónico. Además, desde el diagnóstico (basal) hasta los 24 meses de seguimiento, se muestra una discreta optimización del tratamiento, más destacada entre los primeros 3-6 meses.
ConclusionesLos datos epidemiológicos se mantienen estables, con una prevalencia inferior a la reportada en estudios de base no poblacional. Existe un amplio margen de mejora en la optimización del tratamiento médico de la IC-FEr.
Palabras clave
La insuficiencia cardiaca (IC) es un síndrome clínico complejo, resultado de una alteración cardiaca estructural o funcional. Se caracteriza por la progresión de los síntomas que conducen a hospitalizaciones frecuentes, mala calidad de vida y alta tasa de mortalidad1–3.
Según la fracción de eyección del ventrículo izquierdo (FEVI), se han definido 3 fenotipos básicos: a) con FEVI reducida (IC-FEr), ≤ 40%; b) con FEVI conservada (IC-FEc), ≥ 50%, y c) con FEVI en rango medio (IC-FEm), del 41-49%3,4. Alrededor del 40-50% de los pacientes muestran una IC-FEr2,4,5. La diferenciación de los pacientes con IC según la FEVI es importante, dada su relación con diferentes etiologías subyacentes, comorbilidades y, sobre todo, la respuesta al tratamiento1–3.
De hecho, la modulación neurohormonal con inhibidores de la enzima de conversión de la angiotensina (IECA) o antagonistas del receptor de la angiotensina II (ARA-II), combinados con bloqueadores beta y antagonistas de la aldosterona (AA), además de otras dianas terapéuticas, como la potenciación del sistema de péptidos natriuréticos y otros sistemas vasodilatadores endógenos, se ha demostrado repetidamente como modificador del pronóstico de la enfermedad en la IC-FEr y de modo menos robusto en la IC-FEm6,7.
La prevalencia estimada de la IC se sitúa alrededor del 2% de los adultos en países desarrollados, y aumenta a más del 10% en los mayores de 70 años8. En España, se han reportado cifras incluso > 5%, quizá por carecerse de estudios de base poblacional nacional que permitan dimensionar el impacto real de la enfermedad5,9. Además, el conocimiento del tratamiento médico recibido se basa en registros procedentes de unidades especializadas de IC, que pueden no representar el mundo de la población real10. Por todo ello, sería de enorme interés disponer de datos poblacionales recientes que permitan conocer la prevalencia real y la aplicación de tratamientos modificadores del pronóstico, con el fin de poder planificar adecuadamente intervenciones presentes o futuras. El objetivo del estudio es describir la epidemiologia (prevalencia/incidencia), las características basales y el tratamiento administrado a la población con IC, especialmente a los pacientes con IC-FEr, durante 2017-2019 en situación de práctica clínica habitual en España. El estudio se conoce como PATHWAYS-HF, dado que se pretende aportar información respecto al estado actual de la IC y el recorrido terapéutico de estos pacientes.
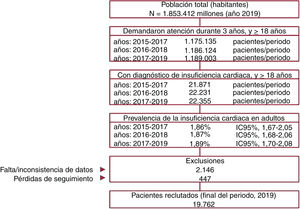
MÉTODOSDiseño y población de estudioSe efectuó un estudio observacional de carácter retrospectivo. Los registros médicos electrónicos (RME) se obtuvieron de la base de datos administrativa BIG-PAC (fuente de datos secundaria). Cuenta con una población de 1.853.412 personas y su propietario es Atrys Health. Los datos primarios proceden de los registros informatizados de 7 áreas sanitarias integradas que incluyen centros de atención primaria y hospitales de referencia públicos de 7 comunidades autónomas españolas. Antes de su exportación a BIG-PAC, se realiza un riguroso proceso de anonimización en los centros/hospitales de origen; por lo tanto, cuando se importan a BIG-PAC ya están disociados y por ello no es posible conocer el territorio, el proveedor sanitario, el profesional, el paciente y/o alguna característica que permita algún tipo de identificación de carácter personal. Con este proceso, se asegura el cumplimiento de la Ley General de Protección de Datos de Carácter Personal vigente. Cabe destacar que el algoritmo de encriptación de los registros se aplica en los centros de origen, y es desconocido e irreversible para Atrys Health. Por esta razón, esta no tiene ninguna posibilidad de acceso a las fuentes de datos primarias. BIG-PAC está registrada en la Agencia Europea del Medicamento.
Los datos de BIG-PAC son representativos de la población española general, como lo demuestra el estudio de comparación demográfica que se realizó en 2019 y cuyos resultados se muestran en la . Para la obtención de los datos epidemiológicos y de la medicación del presente estudio, se incluyó a todos los pacientes que requirieron atención durante 2017, 2018 y 2019. Se realizó un análisis más detallado en los pacientes con un nuevo diagnóstico de IC-FEr en el primer año estudiado para evaluar los cambios de medicación administrada durante un periodo de 2 años.
Criterios de inclusión y exclusiónLos criterios de inclusión fueron: a) edad ≥ 18 años; b) pacientes activos en la base de datos un mínimo de 12 meses antes de iniciarse el estudio; c) estar en el programa de prescripciones para la obtención de las recetas médicas (con registro constatado de la dosis diaria, el intervalo de tiempo y la duración de cada tratamiento administrado, con al menos 2 recetas durante el periodo de seguimiento), y d) que se pudiera garantizar el seguimiento regular de los pacientes (al menos 2 registros sanitarios en el sistema informático). Los criterios de exclusión fueron: a) sujetos desplazados o fuera de zona; b) pacientes en instituciones geriátricas permanentemente; c) enfermedad mental grave, terminal o en diálisis, y d) carencia de la FEVI (ecocardiograma).
Definición del diagnósticoLos registros de los pacientes con IC se obtuvieron a partir de la Clasificación Internacional de Enfermedades (novena edición) Modificación Clínica (CIE-09-MC; código: 428). Los criterios para establecer el diagnóstico de IC fueron clínicos, a consideración del médico tratante, según la presencia de signos/síntomas, así como el hallazgo de una anomalía estructural/funcional en el corazón según el resultado de la ecocardiografía.
Prevalencia puntual y tasa de incidenciaLa prevalencia se determinó como el número total de casos diagnosticados de IC entre la población atendida (año, edad y sexo) y se calculó por periodos temporales de 3 años consecutivos (figura 1). La tasa de incidencia se calculó como el número de casos de IC de nuevo diagnóstico/1.000 sujetos/año entre la población atendida (periodo temporal, 2017, 2018 y 2019). No se estandarizaron los resultados debido a la similitud de la pirámide poblacional (edad y sexo) de los pacientes del estudio con la población etaria española, que se presenta en la .
Variables demográficas y comorbilidadesObtenidas para el año 2019, las variables sociodemográficas y de comorbilidad (CIE-09-MC) fueron las siguientes: edad (continua) y sexo, así como los antecedentes personales de hipertensión arterial, dislipemia, diabetes, obesidad, enfermedad cerebrovascular (ictus isquémico, accidente isquémico transitorio), arteriopatía periférica, anemia, insuficiencia renal (criterio establecido: tasa de filtrado glomerular < 60ml/min/1,73 m2 por el método de la Chronic Kidney Disease Epidemiology Collaboration [CKD-EPI]), tasa de filtrado glomerular < 30ml/min/1,73 m2, enfermedad pulmonar obstructiva crónica, neoplasias malignas y fibrilación auricular. Se determinó la proporción de fallecimientos (causa cardiovascular o no cardiovascular). Como variable de comorbilidad general, se utilizó el índice de comorbilidad de Charlson11.
Medicación administradaLa información se obtuvo de los registros procedentes de la dispensación farmacológica de medicamentos, según la Anatomical Therapeutic Chemical Classification System (ATC)12. Se seleccionaron los siguientes grupos terapéuticos/principios activos: ivabradina (C01EB17), diuréticos (C03, excepto antagonistas de la aldosterona C03DA), antagonistas de la aldosterona (C03DA), agentes bloqueadores beta (C07), IECA (C09A-C09B), ARA-II (C09C-C09D, excepto sacubitrilo-valsartán, C09DX04), sacubitrilo-valsartán (C09DX04) e inhibidores del cotransportador de sodio-glucosa tipo 2. La elección del medicamento para un paciente en concreto fue a criterio del médico (práctica clínica).
Variables clínicasA partir de los RME, se obtuvieron los datos de cada paciente atendiendo a: a) el fenotipo de IC según la FEVI (IC-FEr, ≤ 40%; IC-FEm, 41-49%, e IC-FEc, ≥ 50%); b) la etiología de la cardiopatía que llevó a la IC (isquémica y no isquémica), y c) la clase funcional de la New York Heart Association (NYHA) I-IV. Estos valores se obtuvieron de las historias clínicas informatizadas, y se consideró el primer valor disponible a partir de la fecha de inclusión. Durante la evolución temporal se consideró el valor disponible más próximo al periodo indicado.
Análisis estadísticoLos criterios de búsqueda en la base de datos fueron a partir de sentencias informáticas (SQL script). Se revisaron cuidadosamente los datos, mediante análisis exploratorio y preparación de estos para el análisis, observando sus distribuciones de frecuencia y buscando posibles errores de registro o de codificación. Se efectuó un análisis estadístico descriptivo-univariante. Para los datos cualitativos: frecuencias absolutas y relativas. Para los datos cuantitativos: media ± desviación estándar. Los intervalos de confianza del 95% (IC95%) se basaron en el número total de sujetos. En el análisis bivariante se utilizaron las pruebas de la χ2 y ANOVA para grupos independientes. También se relazó una prueba de McNemar para establecer la significación estadística para grupos apareados (comparación temporal), p < 0,05. Se utilizó el programa SPSSWIN versión 23.
RESULTADOSCaracterísticas basales (2019)De las 1.853.412 personas incluidas en la base de datos BIG-PAC en 2019, se excluyó a la población menor de 18 años, por lo que para el análisis se consideró a 1.189.003 personas adultas que solicitaron atención médica entre 2017 y 2019.
De ellas, se identificó a 22.355 pacientes con diagnóstico de IC. Se excluyó a 2.593 por datos incompletos (principalmente falta de datos de la FEVI) o pérdidas para el seguimiento. Por lo tanto, la población de partida para el análisis son 19.762 pacientes. En la figura 1 se muestra el diagrama de flujo general de la población del estudio.
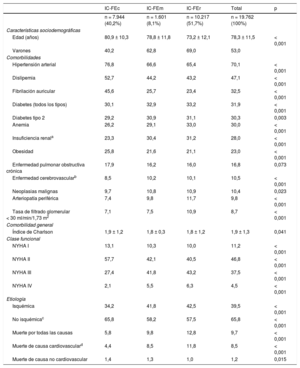
Para la población total de IC, la media de edad fue de 78,3 ± 11,5 años; el 53,0% eran varones. De este conjunto de pacientes, el 70,1% tenía hipertensión arterial; el 47,1%, dislipemia y el 32,5%, fibrilación auricular. El promedio del índice de Charlson fue 1,9 puntos. La distribución del fenotipo por FEVI fue: a) reducida, 51,7%; b) conservada, 40,2%, y c) en rango medio, 8,1%. La clase NYHA más frecuente fue la II (46,8%).
Los pacientes con IC-FEr son más jóvenes (media de edad, 73,2 ± 12,1 años; el 69,0% varones); el 65,4% tenía hipertensión arterial; el 43,2%, dislipemia y el 31,1%, diabetes mellitus tipo 2. El promedio del índice de Charlson fue 1,8 puntos. La mortalidad fue mayor que entre la población general (el 12,8% en IC-FEr frente al 9,7% en la IC general; p < 0,001). La tabla 1 muestra las características basales de la población.
Características basales de la serie por fenotipo según la FEVI (2019)
| IC-FEc | IC-FEm | IC-FEr | Total | p | |
|---|---|---|---|---|---|
| n = 7.944 (40,2%) | n = 1.601 (8,1%) | n = 10.217 (51,7%) | n = 19.762 (100%) | ||
| Características sociodemográficas | |||||
| Edad (años) | 80,9 ± 10,3 | 78,8 ± 11,8 | 73,2 ± 12,1 | 78,3 ± 11,5 | < 0,001 |
| Varones | 40,2 | 62,8 | 69,0 | 53,0 | |
| Comorbilidades | |||||
| Hipertensión arterial | 76,8 | 66,6 | 65,4 | 70,1 | < 0,001 |
| Dislipemia | 52,7 | 44,2 | 43,2 | 47,1 | < 0,001 |
| Fibrilación auricular | 45,6 | 25,7 | 23,4 | 32,5 | < 0,001 |
| Diabetes (todos los tipos) | 30,1 | 32,9 | 33,2 | 31,9 | < 0,001 |
| Diabetes tipo 2 | 29,2 | 30,9 | 31,1 | 30,3 | 0,003 |
| Anemia | 26,2 | 29,1 | 33,0 | 30,0 | < 0,001 |
| Insuficiencia renala | 23,3 | 30,4 | 31,2 | 28,0 | < 0,001 |
| Obesidad | 25,8 | 21,6 | 21,1 | 23,0 | < 0,001 |
| Enfermedad pulmonar obstructiva crónica | 17,9 | 16,2 | 16,0 | 16,8 | 0,073 |
| Enfermedad cerebrovascularb | 8,5 | 10,2 | 10,1 | 10,5 | < 0,001 |
| Neoplasias malignas | 9,7 | 10,8 | 10,9 | 10,4 | 0,023 |
| Arteriopatía periférica | 7,4 | 9,8 | 11,7 | 9,8 | < 0,001 |
| Tasa de filtrado glomerular < 30 ml/min/1,73 m2 | 7,1 | 7,5 | 10,9 | 8,7 | < 0,001 |
| Comorbilidad general | |||||
| Índice de Charlson | 1,9 ± 1,2 | 1,8 ± 0,3 | 1,8 ± 1,2 | 1,9 ± 1,3 | 0,041 |
| Clase funcional | |||||
| NYHA I | 13,1 | 10,3 | 10,0 | 11,2 | < 0,001 |
| NYHA II | 57,7 | 42,1 | 40,5 | 46,8 | < 0,001 |
| NYHA III | 27,4 | 41,8 | 43,2 | 37,5 | < 0,001 |
| NYHA IV | 2,1 | 5,5 | 6,3 | 4,5 | < 0,001 |
| Etiología | |||||
| Isquémica | 34,2 | 41,8 | 42,5 | 39,5 | < 0,001 |
| No isquémicac | 65,8 | 58,2 | 57,5 | 65,8 | < 0,001 |
| Muerte por todas las causas | 5,8 | 9,8 | 12,8 | 9,7 | < 0,001 |
| Muerte de causa cardiovasculard | 4,4 | 8,5 | 11,8 | 8,5 | < 0,001 |
| Muerte de causa no cardiovascular | 1,4 | 1,3 | 1,0 | 1,2 | 0,015 |
FEVI: fracción de eyección del ventrículo izquierdo; IC: insuficiencia cardiaca; IC-FEc: insuficiencia cardiaca con fracción de eyección conservada; IC-FEm: insuficiencia cardiaca con fracción de eyección en rango medio; IC-FEr: insuficiencia cardiaca con fracción de eyección reducida; NYHA: New York Heart Association.
Los valores expresan porcentaje o media ± desviación estándar.
Insuficiencia renal: tasa de filtrado glomerular < 60ml/min/1,73 m2 según método Chronic Kidney Disease Epidemiology Collaboration (CKD-EPI).
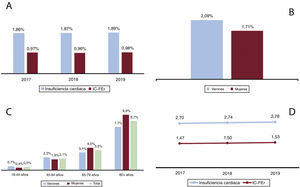
La prevalencia de la IC fue: a) 2015-2017, el 1,86% (IC95%, 1,67%-2,05%); b) 2016-2018, el 1,87% (IC95%, 1,68%-2,06%), y c) 2017-2019, el 1,89% (IC95%, 1,70%-2,08%). Estas discretas diferencias no alcanzaron significación estadística (p = 0,574).
En las figura 2A-C se describen respectivamente las prevalencias de la IC total y la IC-FEr (2017-2019), por sexo y por sexo y franjas de edad (2019). Como puede observarse, en 2019 la prevalencia de IC estaba próxima al 2%, el 51% corresponde a IC-FEr y es más prevalente en el varón. La prevalencia es muy baja en menores de 45 años, pero se acerca al 9% en octogenarios.
En el último periodo estudiado de 2019, la tasa de incidencia de IC fue de 2,78/1.000 personas/año y la de IC-FEr, 1,53. A lo largo de los 3 periodos evaluados hubo un ligero incremento que no alcanzó significación estadística (p = 0,213) (figura 2D).
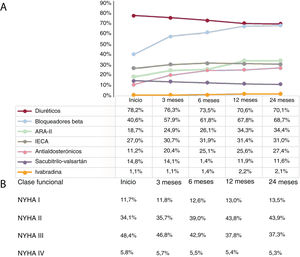
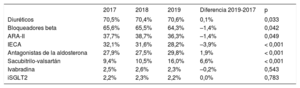
Evaluación del tratamiento administrado (2017-2019)Para analizar la medicación empleada en el tratamiento del paciente con IC, se escogió la IC-FEr, pues se dispone de guías con evidencia sólida y fármacos capaces de modificar el pronóstico de la enfermedad. Durante 2019, el 64,3% de los pacientes recibían tratamiento con bloqueadores beta; el 80,5%, IECA/ARA-II o sacubitrilo-valsartán, y el 29,8%, AA (tabla 2). Para conocer la optimización del tratamiento, de los 1.550 pacientes diagnosticados de IC-FEr en 2017, se analizó el patrón de tratamiento hasta 24 meses (figura 3A). Solo al 40,6% de los pacientes se los trató inicialmente con un bloqueador beta, y es el grupo que más se incrementó durante el seguimiento hasta alcanzar el 68,7% a los 24 meses (p < 0,001). Para IECA y ARA-II, de una prescripción del 45,7% inicial se alcanzó un 65,4% al final del seguimiento (p < 0,001). Los pacientes tratados con AA eran solo el 11,2% al inicio y alcanzaron un escaso 27,4% a los 24 meses (p < 0,001). Llama la atención que el sacubitrilo-valsartán tuvo una evolución inversa, ya que descendió del 14,8 al 11,6% durante el seguimiento (p = 0,012).
Medicación administrada a los pacientes con IC-FEr en 2017-2019
| 2017 | 2018 | 2019 | Diferencia 2019-2017 | p | |
|---|---|---|---|---|---|
| Diuréticos | 70,5% | 70,4% | 70,6% | 0,1% | 0,033 |
| Bloqueadores beta | 65,6% | 65,5% | 64,3% | –1,4% | 0,042 |
| ARA-II | 37,7% | 38,7% | 36,3% | –1,4% | 0,049 |
| IECA | 32,1% | 31,6% | 28,2% | –3,9% | < 0,001 |
| Antagonistas de la aldosterona | 27,9% | 27,5% | 29,8% | 1,9% | < 0,001 |
| Sacubitrilo-valsartán | 9,4% | 10,5% | 16,0% | 6,6% | < 0,001 |
| Ivabradina | 2,5% | 2,6% | 2,3% | –0,2% | 0,543 |
| iSGLT2 | 2,2% | 2,3% | 2,2% | 0,0% | 0,783 |
ARA-II: antagonistas del receptor de la angiotensina II; IC-FEr: insuficiencia cardiaca con fracción de eyección reducida; IECA: inhibidores de la enzima de conversión de la angiotensina; iSGLT2: inhibidores del cotransportador de sodio-glucosa tipo 2.
Evolución temporal del tratamiento administrado (por grupos terapéuticos) y clase funcional de los pacientes con IC-FEr diagnosticados en 2017 (n = 1.550). Valores expresados en porcentaje. Resultados estadísticamente significativos en todas las comparaciones (inicio frente a 24 meses), p < 0,01. ARA-II: antagonistas del receptor de la angiotensina II; IC-FEr: insuficiencia cardiaca con fracción de eyección reducida; IECA: inhibidores de la enzima de conversión de la angiotensina; NYHA: New York Heart Association.
Cabe destacar que la optimización del tratamiento se concentró en los primeros 12 meses y se estabilizó el año siguiente. Respecto a la clase funcional, el 82,5% se clasificó en NYHA II y III al diagnóstico, y el 81,2% a los 24 meses (p = 0,142). Se detecta que al inicio el 48,4% de los pacientes estaban en NYHA III y este porcentaje disminuyó al 37,3% a los 24 meses (p < 0,001). La disminución ocurrió principalmente en los primeros 12 meses, y especialmente de los meses 6 a 12 (reducción del 5,1%). La clase NYHA II tiene el comportamiento opuesto, pasa del 34,1% al inicio al 43,9% a los 2 años (p = 0,002). De los valores extremos, al diagnóstico un 5,8% de los pacientes estaban en NYHA IV, pero eran 5,3% a las 24 meses (una reducción del 0,5%; p < 0,001). Solo un 13,5% se clasificó en NYHA I a los 2 años tras el diagnóstico (figura 3B).
DISCUSIÓNEste estudio es, hasta donde se ha podido conocer, el mayor estudio de base poblacional sobre IC llevado a cabo en España hasta la fecha. Se trata de una cohorte amplia, reciente y representativa de la población española, que permite obtener una aproximación a la situación real. Los principales hallazgos del estudio son que la prevalencia de la IC en España en el año 2019 era del 1,89% de la población de 18 o más años, con una incidencia de 2,78/1.000 sujetos/año, y que ambas se han mantenido estables en los últimos 3 años. Además, la IC es un problema de salud asociado con el envejecimiento, y alcanza una prevalencia del 9% de los octogenarios; el fenotipo más frecuente es la IC-FEr (51,7%). Por último, en contra de la creencia avalada por registros nacionales e internacionales, la optimización del tratamiento de los pacientes con IC-FEr dispone de un amplio margen de mejora según las recomendaciones de guías clínicas1,3.
Durante el periodo analizado, los datos epidemiológicos se mantienen estables, con una ligera tendencia incremental que no alcanza la significación estadística. Las tasas de incidencia se mantuvieron alrededor de 2,8 casos/1.000 pacientes/año. En nuestro país los estudios epidemiológicos publicados previamente son escasos y con prevalencias diversas en función de la población estudiada y el territorio analizado. Así, en el estudio PRICE13 (15 hospitales y 55 centros de salud de 9 comunidades autónomas), con una muestra aleatoria de pacientes de edad ≥ 45 años, la prevalencia fue del 6,8%. El estudio EPISERVE14 mostró una prevalencia del 2% en atención primaria, el 17% en cardiología y el 12% en medicina interna. Cortina et al.15 (n = 391) describen en Asturias una prevalencia del 4,9%. Sin embargo, en los estudios de base poblacional, los resultados muestran unas cifras de prevalencia sensiblemente inferiores. En este sentido, Farre et al.16 describen en Cataluña una prevalencia del 1,2% de los mayores de 15 años y el 2,7% en los mayores de 44. Estos datos están alineados con el estudio de Carmona et al.17, en la comunidad de Madrid. Es decir, los estudios de base no poblacional de nuestro país han ofrecido cifras de prevalencia muy superiores a las reales. Sin embargo, en los estudios de base poblacional, la prevalencia está en consonancia con los resultados de nuestro estudio1–4,18,19
En el estudio que se presenta, la proporción de pacientes con IC-FEr fue del 51,7% y con IC-FEc, del 40,2%. La distribución de fenotipos por FEVI muestra resultados discretamente superiores a los publicados4,5,10. Sin embargo, las comorbilidades más destacadas (hipertensión arterial, dislipemia, fibrilación auricular, diabetes e insuficiencia renal) están en consonancia con las cifras observadas en otros estudios4,15,16. Conde et al.5 describieron que las comorbilidades asociadas con la IC a menudo son la causa de los reingresos hospitalarios y que el perfil de un paciente ingresado es de edad avanzada, con múltiples comorbilidades que dificultan su diagnóstico y su tratamiento, complican la evolución y se asocian con un peor pronóstico de la enfermedad. En función de las publicaciones revisadas, las cifras de comorbilidades tienen ciertas oscilaciones2,5,13,15,16,20, aunque todos los estudios coinciden en la elevada comorbilidad y que la IC-FEr oscila en un 40-60% de los pacientes1,3,7.
Cuando se analiza el tratamiento médico de los pacientes con IC-FEr en el periodo más reciente (2019), destaca que el 35,7% de los pacientes no reciben tratamiento con bloqueadores beta; el 19,5%, IECA/ARA-II o sacubitrilo-valsartán, y el 70,2%, AA. Por lo tanto, la optimización terapéutica debe constituir uno de los principales pilares para mejorar síntomas, capacidad funcional y calidad de vida y reducir hospitalizaciones y mortalidad1–4,9. Para el tratamiento de la IC-FEr, la guía recomienda, con una indicación de clase I y nivel de evidencia A, un IECA/ARA-II, un bloqueador beta y un AA3. Recientemente, y con base en la creciente información sobre los beneficios del sacubitrilo-valsartán, se recomienda la sustitución de los IECA/ARA-II por sacubitrilo-valsartán21. Sin embargo, al analizar diferentes estudios se comprueba la brecha existente entre la indicación y la práctica clínica real22–25. Nuestros resultados difieren de los procedentes de los 2.834 pacientes españoles incluidos en el registro Europeo de Insuficiencia Cardiaca, según el cual el uso de IECA/ARA-II, bloqueadores beta y AA fue del 92, el 93,3 y el 74,5% respectivamente10; aunque refleja la vida real, lo hace desde la perspectiva específica de las unidades de IC, mientras que cuando se analizan cohortes amplias de base poblacional y no vinculadas a unidades especializadas de IC, los resultados son muy similares a los nuestros. Como muestra, el reciente registro americano CHAMP-HF26 evidenció que, en ausencia de contraindicaciones, el 27, el 33 y el 67% de los pacientes con IC-FEr no recibían IECA/ARA-II o sacubitrilo-valsartán, bloqueadores beta o AA respectivamente. Por lo tanto, existe un claro margen de mejora para optimizar del tratamiento de la IC-FEr.
En la muestra de 1.550 pacientes con diagnóstico de IC-FEr en 2017, se observa una optimización del tratamiento en los primeros 3-6 meses, con una estabilización a los 12-24 meses. Estos resultados de evolución temporal, a nuestro entender, indican que es posible mejorar el tratamiento de estos pacientes y que subyace un componente importante de inercia terapéutica. Pero también es posible que existan factores o características de los pacientes, como contraindicaciones para determinados fármacos, que no se han evaluado en el estudio y podrían explicar parcialmente estos resultados10. En este sentido, los autores creen que sería importante establecer programas de formación y vías clínicas sencillas para mejorar la adecuación de la práctica clínica a las guías1,2 y establecer estrategias de mejora de la adherencia al tratamiento27fomentando la coordinación entre niveles asistenciales, especialmente en las fases de transición.
Por último, en nuestro estudio hubo un 40% de pacientes con IC de causa isquémica (coronaria). A pesar de que hay cierta variabilidad en este tipo de datos en función de la bibliografía disponible, es posible que nuestros resultados sean inferiores a los de algunas series revisadas (> 60%)28. Esta discrepancia puede deberse a 2 factores: a) en un porcentaje no despreciable de casos, es difícil atribuir a una única etiología específica de IC, ya que se produce solapamiento de 2 o más causas; son bien conocidos el hallazgo de enfermedad coronaria arterioesclerótica, que no siempre justifica la IC que padece el paciente, o el protagonismo otorgado en otros a la presencia de HTA como factor de riesgo de cardiopatía isquémica o directamente como causa intrínseca de IC, y b) al tratarse de un estudio retrospectivo, podría darse un infrarregistro de los casos de etiología isquémica. No obstante, nuestros resultados parecen estar en consonancia con otros estudios reportados4,25. Las posibles limitaciones del análisis son las propias de las revisiones retrospectivas con bases de datos, como el infrarregistro de la enfermedad, la posible variabilidad de los profesionales y de los pacientes, al ser un diseño observacional, la posible existencia de un sesgo de clasificación, la posible inexactitud de la codificación diagnóstica, la ausencia de ciertos biomarcadores pronósticos, como los péptidos natriuréticos, puesto que no se determinó sistemáticamente, o algunas variables, como la FEVI o la clase NYHA, falta de registro de cambios de dosis o falta del grado de adherencia al tratamiento y ausencia de información sobre recetas emitidas en atención médica privada o recetas en papel, lo que podría haber llevado a una subestimación del porcentaje de tratamiento. Además, habría sido interesante conocer la distribución de los distintos tratamientos farmacológicos según los 3 fenotipos de IC según la FEVI. No obstante, no se consideró como un objetivo del estudio, dado que en la IC el fenotipo con FEVI reducida es el único que tiene tratamiento modificador del pronóstico de la enfermedad. Finalmente, los resultados de muerte de causa cardiovascular pueden haberse subestimado, por no tener en consideración la causa del fallecimiento de los pacientes que murieron en el domicilio.
CONCLUSIONESDurante el periodo analizado, los datos epidemiológicos sobre IC se mantienen estables, con una prevalencia próxima al 2%, inferior a la reportada en otros estudios de base no poblacional, pero en consonancia con lo descrito en países de nuestro entorno. Gran parte de los pacientes presentan múltiples comorbilidades, y hay un amplio margen de mejora en la optimización del tratamiento de la IC-FEr para adaptarse a las recomendaciones de las sociedades científicas.
FINANCIACIÓNEl presente trabajo ha sido financiado por AstraZeneca, España.
CONTRIBUCIÓN DE LOS AUTORESEn la concepción y el diseño del manuscrito participaron todos los autores. A. Sicras-Navarro se encargó de la recogida de los datos y el análisis estadístico. Todos los autores llevaron a cabo la interpretación de los datos, la redacción, la revisión y la aprobación del manuscrito remitido.
CONFLICTO DE INTERESESA. Sicras-Mainar y A. Sicras-Navarro son consultores independientes en relación con el desarrollo de este manuscrito. B. Palacios y L. Varela son empleados de AstraZeneca.
- -
La IC es un síndrome clínico complejo, resultado de una alteración cardiaca estructural o funcional.
- -
La prevalencia estimada en nuestro país muestra cierta variabilidad, con posibles datos sobrestimados.
- -
El conocimiento del tratamiento médico administrado se basa mayormente en registros procedentes de unidades cardiacas especializadas.
- -
La prevalencia de la insuficiencia cardiaca en España se sitúa alrededor del 2% de la población adulta (edad ≥ 18 años). Es un problema de salud asociado con el envejecimiento.
- -
El fenotipo más frecuente es la IC-FEr (51,7%).
- -
La optimización del tratamiento médico en pacientes con IC-FEr está muy lejos de lo deseable y dispone de un amplio margen de mejora.
Se puede consultar material adicional a este artículo en su versión electrónica disponible en https://doi.org/10.1016/j.recesp.2020.09.014