El objetivo de este estudio es comparar los resultados de la resonancia magnética y la gated-SPECT de perfusión miocárdica en la valoración de la función ventricular y la viabilidad en pacientes con infarto de miocardio en fase crónica.
MétodosSe estudió con resonancia magnética y gated-SPECT a 104 pacientes (media de edad, 61 ± 12 años; el 87,5% varones) con infarto previo. Se correlacionaron los volúmenes y la fracción de eyección del ventrículo izquierdo y los criterios clásicos de viabilidad con realce tardío con gadolino (< 75% de transmuralidad) con los de la SPECT (captación > 50%) en los 17 segmentos del ventrículo izquierdo. Se valoró la motilidad, el engrosamiento y la isquemia en la gated-SPECT de los segmentos no viables o con criterios dudosos con el realce (un 50-75% de transmuralidad).
ResultadosSe observó buena correlación entre ambas exploraciones para los volúmenes y la fracción de eyección (p<0,05) y para la masa necrótica estimada (p<0,01). De los 264 segmentos con realce > 75%, 82 (31%) tenían captación > 50% en la SPECT. De los 106 segmentos con criterios dudosos de viabilidad (un 50-75% de realce) en la resonancia magnética, en la SPECT 68 (64%) tenían una captación > 50%; 41 (38,7%), motilidad conservada; 46 (43,4%), engrosamiento conservado, y 17 (16%), criterios de isquemia.
ConclusionesUna tercera parte de los segmentos considerados no viables en la resonancia magnética muestran captación > 50% en la SPECT. El análisis de la motilidad, engrosamiento y presencia de isquemia en la gated-SPECT es de utilidad en los segmentos de dudosa viabilidad en la resonancia magnética.
Palabras clave
La resonancia magnética (RM) es una exploración que, además del análisis de los volúmenes y la fracción de eyección del ventrículo izquierdo (FEVI), permite valorar el miocardio en riesgo y delimitar la transmuralidad y la extensión de la necrosis miocárdica mediante realce tardío de gadolinio (RTG)1–3. Se acepta que una transmuralidad de la necrosis superior al 75% de la pared miocárdica2,4 o > 4,5mm5 es un índice de inviabilidad o irrecuperabilidad de la función contráctil tras la revascularización. Asimismo, se viene adoptando como criterio de inviabilidad en la tomografía computarizada por emisión monofotónica (SPECT) de perfusión miocárdica6 o para la tomografía por emisión de positrones (PET) de metabolismo con fluorodesoxiglucosa5 una captación < 50% respecto a la máxima del ventrículo izquierdo (VI). Sin embargo, hay valores intermedios (entre el 50 y el 75% de transmuralidad para la RM y entre el 30 y el 50% de captación para las pruebas isotópicas) con los que hay dudas respecto al umbral óptimo para poder predecir más acertadamente la posibilidad de recuperación contráctil. Así, algunos autores han definido el 40% de captación para la SPECT con compuestos tecneciados7 y el 37% para la PET8 como mejores umbrales. Por otra parte, con estas técnicas isotópicas también se puede valorar el grado de engrosamiento sistólico segmentario y la presencia de isquemia si se ha provocado estrés físico o farmacológico, que son otras variables que pueden orientar en el diagnóstico de la viabilidad miocárdica9.
En este estudio se pretende comparar los resultados de la RM y la SPECT de perfusión miocárdica de estrés en una serie de pacientes con infarto de miocardio en fase crónica y determinar qué parámetros de la gated-SPECT pueden ser de ayuda en la valoración del miocardio viable.
MÉTODOSPacientesSe ha estudiado a 104 pacientes (media de edad, 61±12 años; el 87,5% varones) no consecutivos con infarto de miocardio previo diagnosticado según las guías internacionales10,11 y estables clínicamente. Todos ellos estaban incluidos en un protocolo de estudio con RM del remodelado ventricular tras infarto, aprobado por el comité ético del centro (PR-HG-36/2000), y se les había practicado una gated-SPECT con 99mTc-tetrofosmina a criterio del clínico responsable, con un intervalo máximo entre ambas exploraciones no superior a 1 año.
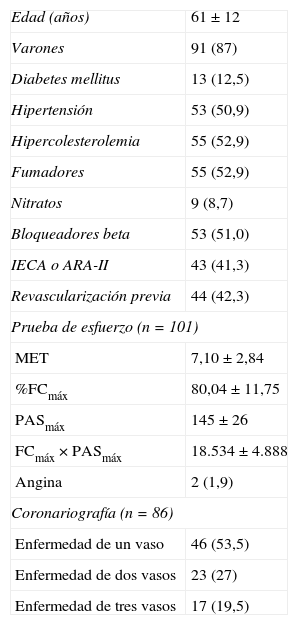
Las características clínicas y coronariográficas de los 104 pacientes se exponen en la tabla 1. El intervalo entre el infarto agudo de miocardio y la SPECT de perfusión miocárdica fue de 8±6 meses y entre la SPECT y la RM, 6±4 meses. En ningún caso hubo complicaciones o reingresos por síndrome coronario agudo entre ambas exploraciones.
Características clínicas, ergométricas y coronariográficas de los pacientes
| Edad (años) | 61±12 |
| Varones | 91 (87) |
| Diabetes mellitus | 13 (12,5) |
| Hipertensión | 53 (50,9) |
| Hipercolesterolemia | 55 (52,9) |
| Fumadores | 55 (52,9) |
| Nitratos | 9 (8,7) |
| Bloqueadores beta | 53 (51,0) |
| IECA o ARA-II | 43 (41,3) |
| Revascularización previa | 44 (42,3) |
| Prueba de esfuerzo (n=101) | |
| MET | 7,10±2,84 |
| %FCmáx | 80,04±11,75 |
| PASmáx | 145±26 |
| FCmáx×PASmáx | 18.534±4.888 |
| Angina | 2 (1,9) |
| Coronariografía (n=86) | |
| Enfermedad de un vaso | 46 (53,5) |
| Enfermedad de dos vasos | 23 (27) |
| Enfermedad de tres vasos | 17 (19,5) |
ARA-II: antagonistas del receptor de la angiotensina II; FC: frecuencia cardiaca; IECA: inhibidores de la enzima de conversión de la angiotensina; MET: equivalentes metabólicos; PAS: presión arterial sistólica.
Los datos expresan n (%) o media±desviación estándar.
Los estudios de RM se realizaron en un equipo de 1,5 T (Avanto, Siemens; Alemania), usando una antena acoplada en fase con 4 elementos. Todas las secuencias se realizaron con sincronización electrocardiográfica y en apnea. Se adquirieron secuencias funcionales de cine-RM segmentadas (TrueFISP; tiempo de eco [TE], 1,4ms; tiempo de repetición [TR] , 55ms; ángulo de inclinación: 52°; ancho de banda, 977Hz/píxel; matriz de 256×212; grosor de corte, 8mm) en planos de eje corto desde la base hasta el ápex del VI, dos cámaras y cuatro cámaras. A los 10 min de la administración del contraste (gadolinio, 0,15mmol/kg), se adquirieron las imágenes de realce tardío mediante secuencia segmentada con prepulso de inversión-recuperación (TurboFlash; TE, 1,2ms; TR, 450ms; ángulo de inclinación, 50°; ancho de banda, 1.180Hz/píxel; matriz de 192×128; grosor de corte, 8mm), eligiendo el tiempo de inversión más adecuado para anular correctamente en la señal del miocardio sano y con posiciones de corte exactamente iguales a las obtenidas en las imágenes de cine-RM.
La cuantificación por RM de la masa necrótica se calculó tras delimitar manualmente los márgenes de las áreas de hiperseñal en la secuencia de RTG, multiplicando la masa específica miocárdica por el volumen estimado del resultado de la suma de las áreas de hiperseñal por el grosor de corte. El grado de transmuralidad de cada segmento miocárdico se valoró visualmente cuantificando el porcentaje del grosor del RTG con respecto al grosor total del segmento, siempre que implicara más de la mitad de este. Se establecieron cinco grupos según el grado de transmuralidad: 1, sin RTG; 2, RTG < 25%; 3, RTG 25 a < 50%; 4, RTG 50 a < 75%, y 5, RTG ≥ 75%.
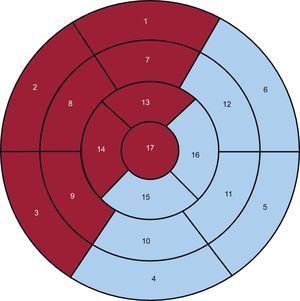
Se dividió el VI en 17 segmentos12, y se definieron dos regiones: la anterior (ANT) que engloba los segmentos anteriores, septales y apical, y la inferolateral (INF-LAT), que abarca los segmentos inferiores y laterales (fig. 1).
Mapa polar de 17 segmentos en el que se diferencia el territorio anterior (fondo granate) del inferolateral (fondo azul). Segmentos: 1, basal anterior; 2, basal anteroseptal; 3, basal inferoseptal; 4, basal inferior; 5, basal inferolateral; 6, basal anterolateral; 7, medio anterior; 8, medio anteroseptal; 9, medio inferoseptal; 10, medio inferior; 11, medio inferolateral; 12, medio anterolateral; 13, apical anterior; 14, apical septal; 15, apical inferior; 16, apical lateral y 17, ápex. Esta figura se muestra a todo color solo en la versión electrónica del artículo.
Las variables estudiadas fueron: volúmenes telediastólico y telesistólico y FEVI; masa necrótica en gramos y porcentaje de esta respecto a todo el VI; masa necrótica estimada por segmentos: número de segmentos con RTG ponderada por el grado de transmuralidad, y grado de transmuralidad segmentaria del RTG clasificado en las cinco categorías descritas.
Gated-tomografía computarizada por emisión monofotónica de perfusión miocárdicaDe los 104 pacientes, se realizó una prueba de esfuerzo limitada por síntomas mediante protocolo de Bruce a 101. De estos, se administró dipiridamol a 16 simultáneamente al esfuerzo por no alcanzar un 80% de taquicardización ni 5equivalentes metabólicos13. Para la SPECT se utilizó un protocolo corto de un solo día con 300MBq de 99mTc-tetrofosmina para el estrés y 900MBq de 99mTc-tetrofosmina para el reposo; a 3 pacientes se les realizó únicamente un estudio en reposo con 900MBq de 99mTc-tetrofosmina. Antes de la inyección del radiofármaco para el estudio en reposo, se administró nitroglicerina sublingual a todos los pacientes. La adquisición se inició a los 30–60min tras el estrés y a los 60–90min tras la inyección en reposo. Se utilizó una gammacámara Siemens E.cam de doble cabezal con los detectores adyacentes a 90°, colimador de baja energía y alta resolución, ventana de 99mTc, zoom de adquisición de 1,45 y matriz de 64×64. El arco de detección se inició en oblicua anterior derecha 45° hasta oblicua posterior izquierda 45°, a razón de una imagen cada 3° y 27 s por imagen. Para la gated-SPECT se estableció una tolerancia R-R del 70%, con un fraccionamiento de 8 imágenes por ciclo. No se realizó la adquisición con corrección de la atenuación. Se realizó la reconstrucción tomográfica de los cortes reorientados del corazón usando una reconstrucción iterativa OSEM, con un filtro Butterworth 0,35/10 para el estudio en estrés (baja dosis) y de 0,45/10 para el estudio en reposo (dosis alta).
La valoración cuantitativa por segmentos del grado de engrosamiento y la gradación cuantitativa de la perfusión se realizó sobre el mapa polar del estudio en reposo utilizando el programa automático QPS para la perfusión y QGS para la gated-SPECT14,15. Además de la puntuación de los segmentos, también se calculó la extensión del defecto mediante la selección de tres niveles de corte para el mapa de blackout: el 30, el 40 y el 50%, mediante Emory Cardiac Toolbox de Emory University16.
Las variables estudiadas fueron:
- •
Volúmenes telediastólico y telesistólico y FEVI.
- •
Porcentaje de extensión del defecto en el mapa polar con captación en reposo < 30, < 40 y < 50.
- •
El porcentaje de captación en cada uno de los 17 segmentos clasificado en cinco categorías: normal, < 30, 30 a < 40, 40 a < 50 y ≥ 50%.
- •
La motilidad segmentaria categorizada en una escala de 6 puntos: 0, normal; 1, hipocinesia ligera; 2, hipocinesia moderada; 3, hipocinesia importante; 4, acinesia, y 5, discinesia.
- •
El engrosamiento segmentario categorizado en una escala de 5 puntos: 0, normal; 1, ligera alteración del engrosamiento; 2, moderada alteración del engrosamiento; 3, gran alteración del engrosamiento, y 4, ausencia de engrosamiento.
Se consideró que un segmento tenía criterios de isquemia en la SPECT cuando la puntuación entre estrés y reposo mejoraba al menos un grado. Se consideró que un segmento tenía la motilidad y el engrosamiento conservados en la gated-SPECT cuando su puntuación era de 0 a 2.
EstadísticaLos resultados de las variables cuantitativas se expresaron en valores medios±desviación estándar e intervalos, mientras que las variables categóricas se expresaron en porcentajes o proporciones. Para la determinación de normalidad, se utilizó el test de normalidad de Kolmogorov-Smirnov. Se determinó la correlación de Pearson para variables de función ventricular y volúmenes obtenidos con gated-SPECT y RM y la correlación intraclase para los grados de transmuralidad de RM en relación con la captación segmentaria de la SPECT. Para la comparación de las variables cuantitativas respecto a categorías, se realizó un análisis de comparación de medias (análisis de la varianza) con corrección de Bonferroni. Se consideró valor estadísticamente significativo p<0,05. Se realizó también un análisis de curva receiver operating characteristic (ROC) entre el grado de captación segmentaria en la SPECT y el grado de transmuralidad segmentaria en la RM tomando como referencia de viabilidad en la RM un RTG < 75% de transmuralidad. Se calculó el índice kappa (k) entre el umbral óptimo de la SPECT obtenido mediante la curva ROC y la RTG < 75% de la RM.
En primer lugar se analizaron estadísticamente las variables de los 104 pacientes; en segundo lugar, para cada uno de los 1.768 segmentos y, finalmente, los segmentos con RTG y aquellos con criterios limítrofes de viabilidad en la RM. Se utilizó el paquete estadístico SPSS versión 15.
RESULTADOSLas correlaciones entre la RM y la gated-SPECT para el volumen telediastólico (144±43 frente a 149±56ml), el volumen telesistólico (78±38 frente a 88ml) y la FEVI (el 45±12% frente al 44±13%) fueron 0,707, 0,762 y 0,707 respectivamente (p<0,05).
La masa necrótica en la RM fue de 21,7±13,7g (16,2±9,9% del VI). En el 55,8% de los pacientes, la necrosis era < 15% del VI; en el 35,6%, un 15–30%, y en el 8,7%, > 30%. Las correlaciones de la masa necrótica valorada con RM respecto a la extensión de la necrosis en el mapa polar de la SPECT para umbrales<30, < 40 y < 50% fueron 0,498, 0,497 y 0,487 respectivamente (p<0,01). Las correlaciones entre la masa necrótica estimada con RM por segmentos y la extensión de la necrosis en el mapa polar de la SPECT para umbrales<30, < 40 y < 50% fueron 0,543, 0,523 y 0,512 respectivamente (p<0,01).
Análisis segmentarioSe analizó un total de 1.768 segmentos (17 segmentos de 104 pacientes).
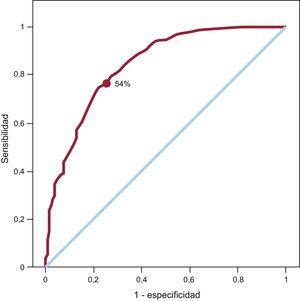
La curva ROC de la SPECT de perfusión miocárdica tomando como criterio de viabilidad una transmuralidad con RTG < 75% se muestra en la figura 2. El resultado es un área bajo la curva de 0,845. El umbral óptimo de captación de SPECT fue del 54%, para el que se dan las máximas sensibilidad y especificidad (el 78 y el 74,7% respectivamente). Para este umbral óptimo de la SPECT, se calculó el índice kappa (κ=0,409).
Curva receiver operating characteristic entre el grado de captación segmentaria en la tomografía computarizada por emisión monofotónica y la resonancia magnética tomando como referencia de viabilidad una transmuralidad del realce tardío de gadolinio < 75%. Área bajo la curva=0,845. El punto escogido de captación para la tomografía computarizada por emisión monofotónica (54%) es el que maximiza la importancia conjunta de la sensibilidad (78%) y la especificidad (74,7%).
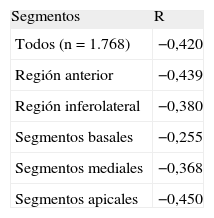
La correlación intraclase entre el incremento del grado de transmuralidad con RTG y la reducción del grado de captación de la SPECT en las regiones ANT e INF-LAT y a nivel de los segmentos basales, medios y apicales se muestra en la tabla 2. La mejor correlación entre el grado de transmuralidad con RTG y el grado de reducción de la captación en la SPECT se observó a nivel de los segmentos apicales.
Correlación intraclase entre el grado de transmuralidad del realce tardío con gadolinio y el grado de captación en la tomografía computarizada por emisión monofotónica
| Segmentos | R |
| Todos (n=1.768) | −0,420 |
| Región anterior | −0,439 |
| Región inferolateral | −0,380 |
| Segmentos basales | −0,255 |
| Segmentos mediales | −0,368 |
| Segmentos apicales | −0,450 |
Mostraron RTG 477 de los 1.768 segmentos, de los cuales el 80,1% se localizaba en la región ANT y el resto (19,9%), en la región INF-LAT. Un 7,5% de estos segmentos con RTG eran de localización basal, el 34,8% eran de localización media y el 57,7%, de localización apical. El grado de transmuralidad era < 25% en un 5% de los segmentos, del 25-50% en un 17,4%, del 50-75% en un 22,2% y > 75% en un 55,3%. Es decir que, desde el punto de vista de la RM, más de la mitad de los segmentos con RTG no tenían criterios de viabilidad.
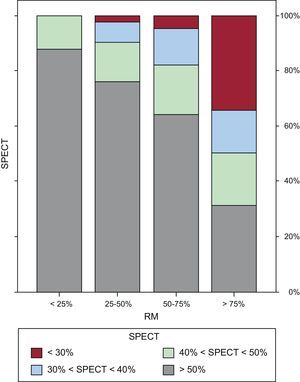
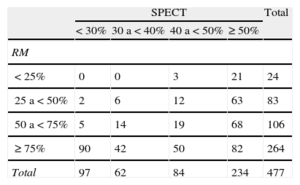
En la tabla 3 y la figura 3 se expone la relación entre el porcentaje de captación en la SPECT y el grado de transmuralidad del RTG expresado en número de segmentos. De los 264 segmentos sin criterios clásicos de viabilidad en la RM (transmuralidad de RTG > 75%), 82 (31%) tenían un captación > 50% en la SPECT (fig. 4); 106 segmentos (el 22,2% de los segmentos con RTG) tenían criterios dudosos (RTG de un 50-75%) de viabilidad en la RM; 68 (64%) de estos tenían una captación > 50% en la SPECT; 41 (38,7%), motilidad conservada; 46 (43,4%), engrosamiento conservado, y 17 (16%), criterios de isquemia.
Relación entre el porcentaje de captación en la tomografía computarizada por emisión monofotónica y el grado de transmuralidad del realce tardío con gadolinio en la resonancia magnética expresado en número de segmentos
| SPECT | Total | ||||
| < 30% | 30 a < 40% | 40 a < 50% | ≥ 50% | ||
| RM | |||||
| < 25% | 0 | 0 | 3 | 21 | 24 |
| 25 a < 50% | 2 | 6 | 12 | 63 | 83 |
| 50 a < 75% | 5 | 14 | 19 | 68 | 106 |
| ≥ 75% | 90 | 42 | 50 | 82 | 264 |
| Total | 97 | 62 | 84 | 234 | 477 |
RM: resonancia magnética; SPECT: tomografía computarizada por emisión monofotónica.
Gráfico de barras que expresa la relación entre el porcentaje de captación en la tomografía computarizada por emisión monofotónica y el grado de transmuralidad del realce tardío de gadolinio en la resonancia magnética. RM: resonancia magnética; SPECT: tomografía computarizada por emisión monofotónica.
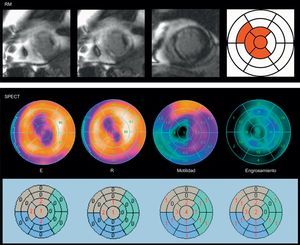
Ejemplo de discordancia respecto a viabilidad entre la resonancia magnética y la tomografía computarizada por emisión monofotónica, en un paciente con infarto de miocardio anterior. El grado de transmuralidad del realce tardío de gadolinio es > 75% en cuatro segmentos (en rojo), mientras que en los mapas polares de la tomografía computarizada por emisión monofotónica se observa reversibilidad entre estrés y reposo, motilidad conservada (puntuación 1-2) y engrosamiento conservado (puntuación 1-2) y en estos segmentos, salvo en el segmento apical (puntuación 4) y el septo apical (puntuación 3). E: estrés; R: reposo; RM: resonsancia magnética; SPECT: tomografía computarizada por emisión monofotónica. Esta figura se muestra a todo color solo en la versión electrónica del artículo.
Los resultados del presente estudio muestran que, aunque la correlación general entre RM y gated-SPECT para la estimación de los volúmenes y la FEVI es buena, hay discrepancias entre ambas técnicas en la cuantificación de la extensión de la necrosis y la valoración de la viabilidad miocárdica. La RM con RTG se ha demostrado superior a la SPECT de perfusión miocárdica para la delimitación transmural de la necrosis miocárdica, sobre todo en los infartos subendocárdicos17,18. La explicación para esta sensibilidad subóptima de la SPECT es su menor resolución espacial. Ahora bien, el umbral de transmuralidad de la necrosis para aceptar como viable o inviable determinado segmento miocárdico no está bien establecido. Entre otros factores, ello puede deberse a que la transmuralidad de la necrosis no es necesariamente homogénea en todo el segmento miocárdico. Por este y otros motivos, la superioridad de la RM, incluso sobre la PET, sigue siendo motivo de controversia19,20. Existe otro punto que justifica la comparación entre ambas técnicas, y es que en ciertas circunstancias la práctica de una RM puede presentar limitaciones: pacientes portadores de marcapasos o desfibrilador automático implantable, ausencia de ritmo regular estable, imposibilidad de controlar un mínimo de apnea, insuficiencia renal o claustrofobia.
Aunque en nuestra serie hemos observado que hay una aceptable correlación entre la masa necrótica general del VI estimada por RM y la extensión de la necrosis en la SPECT, la comparación segmento a segmento entre ambas técnicas no es óptima. El territorio basal es donde se da la mayor discrepancia entre el grado de transmuralidad de la necrosis por RTG y el porcentaje de captación en la SPECT. Ello es atribuible principalmente a que la cuantificación del grado de captación isotópica en los segmentos anteroseptales a nivel basal en el mapa polar de la SPECT presenta problemas, ya que la longitud del septum es menor que la de la pared lateral del VI, con lo que, en muchas ocasiones, estos segmentos muestran un porcentaje de captación muy bajo, que corresponde principalmente a actividad extracardiaca.
Uno de los problemas de la RM y de la SPECT en la interpretación de los resultados de la viabilidad es la observación de criterios dudosos o limítrofes o, en otras palabras, la obtención de «resultados probables» y no «resultados definitivos». Así, aunque la RM muestra imágenes con mayor resolución espacial, la interpretación puede ofrecer dudas acerca de la viabilidad de determinado territorio. Kim et al2 observaron resultados equívocos o no diagnósticos en 293 de 804 (36%) segmentos. Para esos autores, cuando el RTG ocupa un área > 75% de un segmento, se lo considera inviable, y cuando la extensión es < 25%, se lo considera viable. Entre estos valores, la probabilidad de recuperación contráctil tras la revascularización es de sólo el 50%. Otros autores han propuesto valores de corte absolutos como criterios de viabilidad para la RM: grosor < 4,5mm de RTG5 o > 3mm de ausencia de RTG8. Kühl et al8, en una serie de 26 pacientes con miocardiopatía isquémica (fracción de eyección, 31%±11%), observaron una clara correlación inversa entre el grado de RTG y el nivel de captación de la 18F–fluorodesoxiglucosa. Mediante análisis de curvas ROC, obtuvieron el umbral del 37% de captación con PET que mejor diferenciaba el miocardio viable del no viable. Tomando como referencia este valor de la PET, la sensibilidad y la especificidad de la RM para el diagnóstico de miocardio no viable fueron del 96 y el 84% respectivamente. En 2006, Kühl et al21, en una serie de 29 pacientes con miocardiopatía isquémica (fracción de eyección, 32±10%) y considerando un área de RTG > 50% a nivel segmentario como criterio de inviabilidad y una captación < 50% para PET/SPECT, obtuvieron un valor predictivo positivo de recuperación contráctil del 73%, igual para ambas técnicas, mientras que el valor predictivo negativo era superior para la RM (el 93 frente al 77%).
En nuestra serie, hemos corroborado esta correlación negativa entre el grado de transmuralidad del RTG y el grado de captación isotópica con SPECT, sobre todo a nivel de los segmentos apicales, pero también hemos observado discrepancias entre RM y SPECT. Un 31% de los segmentos sin criterios clásicos de viabilidad en la RM (RTG > 75%) tenían un porcentaje de captación > 50% en la SPECT. Por otra parte, un 22% de los segmentos con RTG tenían criterios dudosos de viabilidad (RTG 50-75%) en la RM. En estos, la SPECT podía proporcionar una ayuda al diagnóstico de viabilidad, ya que en un 64% había captación > 50%, en un 39% la motilidad estaba conservada, en un 43% el engrosamiento estaba conservado y en un 16% se observaron criterios de reversibilidad estrés-reposo (isquemia). La RM también permite una valoración del engrosamiento, la motilidad y la isquemia en caso de que se realice con estrés, lo cual podría suponer una disminución de los resultados dudosos obtenidos sólo con la valoración del RTG.
Es evidente que el estudio segmentario de la necrosis y la viabilidad no permite extraer conclusiones acerca de la recuperabilidad contráctil general del VI una vez revascularizado el paciente, ya que otros factores clínicos y coronariográficos tienen un papel importante en el pronóstico de estos enfermos22–24. Mientras que en algunas series se ha considerado que un 15% del VI era la cantidad de miocardio viable requerida para mejorar la función contráctil general25, Inaba et al26, en un metanálisis de 29 estudios que incluían a 4.167 pacientes, estimaron que la cantidad de miocardio viable necesaria para mejorar la supervivencia después de revascularización quirúrgica en la miocardiopatía isquémica era del 25,8% con PET, el 35,9% con ecografía de estrés y el 38,7% con SPECT.
LimitacionesLa inclusión de pacientes en este estudio no fue consecutiva y los resultados obtenidos tan sólo reflejan los resultados de un único centro a través de su disponibilidad y experiencia en las exploraciones practicadas. Por otra parte, el perfil de los pacientes incluidos probablemente no sea el ideal para el estudio de la viabilidad miocárdica, ya que un porcentaje considerable tenía una FEVI > 40%. El estudio SPECT de estrés+reposo es más completo que la RM en reposo y la metodología utilizada para la valoración segmentaria de la transmuralidad con RTG es visual, mientras que para la SPECT se ha realizado mediante un programa automático14,15 de valoración semicuantitativa plasmado en el mapa polar del VI. En nuestro estudio no se ha valorado con la RM la motilidad y el engrosamiento; sin embargo, la correlación de esta técnica con la obtenida mediante gated-SPECT es buena. Whaba et al27 observaron una concordancia entre ambas técnicas del 80% (κ=0,66) para motilidad y del 83% (κ=0,70) para engrosamiento en pacientes con infarto previo. No aplicar automáticamente un mapa polar de similares características para la RM dificulta una estricta comparación segmento a segmento entre ambas técnicas. Se podrá superar esta limitación con la aplicación de mapas polares que reflejen más objetivamente la extensión del RTG. Por otra parte, nuestro análisis estadístico se ha centrado en la comparación de segmentos, y se debe tener en cuenta que los distintos segmentos de un mismo paciente no son independientes entre sí. Si en nuestra serie hubiéramos dispuesto de corrección de atenuación, probablemente la correlación con los resultados de la RM habría sido todavía más ajustada. Raja et al28 han mostrado una excelente concordancia entre SPECT y PET para la valoración de la viabilidad con la administración de nitratos y la corrección de atenuación en la SPECT. Finalmente, la ausencia de resultados tras la revascularización no ha permitido estimar la eficacia diagnóstica de la RM y la SPECT en la predicción de recuperabilidad contráctil.
CONCLUSIONESLa correlación entre RM y gated-SPECT para volúmenes y FEVI y la masa necrótica estimada es buena, aunque la correlación entre el grado de transmuralidad en la RM y el grado de captación en la SPECT es subóptima, sobre todo en el territorio basal del VI. Una tercera parte de los segmentos considerados no viables en la RM (RTG > 75%) muestran captación > 50% en la SPECT. De los segmentos considerados limítrofes en la RM (RTG 50-75%), en la gated-SPECT dos terceras partes tienen una captación > 50% en la SPECT, un 39% tiene motilidad conservada, el 43,4% muestra engrosamiento conservado y un 16%, isquemia. Estos resultados pueden tener implicaciones clínicas en los centros en que la RM en reposo se emplee como primera opción para el diagnóstico de viabilidad y sus resultados no sean concluyentes, ya que permiten conocer la aportación que ofrece la gated-SPECT de estrés-reposo ante esta eventualidad.
CONFLICTO DE INTERESESNinguno.