La hiperpotasemia es una preocupación creciente en el tratamiento de los pacientes con insuficiencia cardiaca y fracción de eyección reducida, pues limita el uso de fármacos eficaces. Este trabajo ofrece estimaciones de la magnitud de este problema en la práctica clínica habitual en España, los cambios en las concentraciones de potasio en el seguimiento y los factores asociados.
MétodosPacientes con insuficiencia cardiaca aguda (n=881) y crónica (n=3.587) seleccionados en 28 hospitales españoles del registro europeo de insuficiencia cardiaca de la European Society of Cardiology y seguidos 1 año para diferentes desenlaces, incluidos cambios en las cifras de potasio y su impacto en el tratamiento.
ResultadosLa hiperpotasemia (K+> 5,4 mEq/l) está presente en el 4,3% (IC95%, 3,7-5,0%) y el 8,2% (6,5-10,2%) de los pacientes con insuficiencia cardiaca crónica y aguda; causa el 28,9% de todos los casos en que se contraindica el uso de antagonistas del receptor de mineralocorticoides y el 10,8% de los que no alcanzan la dosis objetivo. Del total de 2.693 pacientes ambulatorios con fracción de eyección reducida, 291 (10,8%) no tenían registrada medición de potasio. Durante el seguimiento, 179 de 1.431 (12,5%, IC95%, 10,8-14,3%) aumentaron su concentración de potasio, aumento relacionado directamente con la edad, la diabetes mellitus y los antecedentes de ictus e inversamente con los antecedentes de hiperpotasemia.
ConclusionesEste trabajo destaca el problema de la hiperpotasemia en pacientes con insuficiencia cardiaca de la práctica clínica habitual y la necesidad de continuar y mejorar la vigilancia de este factor en estos pacientes por su interferencia en el tratamiento óptimo.
Palabras clave
En los últimos años, múltiples causas que actúan en el mismo sentido han aumentado la carga de enfermedad que supone la insuficiencia cardiaca (IC) en los países industrializados, como España, hasta convertirla en un gran problema de salud. Es previsible que esta carga siga aumentando en España1.
En paralelo, determinados tratamientos, incorporados ya a las guías de práctica clínica2,3, se han demostrado eficaces en pacientes con deterioro de la función sistólica. Estos tratamientos que interfieren en el sistema renina-angiotensina-aldosterona (SRAA) multiplican por 2 o 3 el riesgo de hiperpotasemia en pacientes con IC3,4. La hiperpotasemia se asocia con trastornos de la conducción y riesgo de arritmias potencialmente mortales y no es en absoluto una rareza, ya que estimaciones de hace 20 años ya indicaban prevalencias entre el 1 y el 10% de los pacientes hospitalizados5. Datos más recientes entre nuevos usuarios de inhibidores de la enzima de conversión de la angiotensina (IECA) indican en el primer año el 5,6% y el 1,7% con cifras de potasio> 5 y> 5,5 respectivamente6. Los pacientes con IC están en riesgo alto de hiperpotasemia no solo por los fármacos que reciben, sino también por la presencia frecuente de comorbilidades (enfermedad renal o diabetes mellitus, por ejemplo)7. La IC y la insuficiencia renal se relacionan bidireccionalmente. La prevalencia de IC aumenta mucho con peores filtrados glomerulares8 y, en un subanálisis del estudio RALES en pacientes con IC, el riesgo de hiperpotasemia fue mayor tanto para los que tenían un reducido filtrado glomerular estimado basal como para los que mostraron empeoramiento de la función renal durante la fase de titulación. Este efecto fue aún mayor en el grupo aleatorizado a espironolactona9.
Estos fármacos bloqueadores del SRAA tienen una indicación IA en las guías de práctica clínica para los pacientes con fracción de eyección reducida2,3 y su uso está cada vez más generalizado, por lo que la hiperpotasemia es una preocupación creciente en el tratamiento de estos pacientes7.
Pese a esto, no hay información prospectiva que estime el problema de la hiperpotasemia en pacientes con IC crónica (ICC) en la práctica clínica cotidiana en España. Un estudio transversal reciente muestra que 1/4 pacientes que tendrían indicado un antagonista del receptor de mineralocorticoides (ARM) no los recibe. De los que los reciben, 3/4 pacientes no alcanzan las dosis objetivo. La hiperpotasemia es la causa principal en al menos el 8,5% de los pacientes que no reciben el fármaco y en más del 10% de los que no alcanzan dosis10, lo que subraya su importancia.
España participa en el registro de IC a largo plazo de la Sociedad Europea de Cardiología (ESC) ESC Heart Failure Long-Term Registry (ESC-HF-LT)11 y aporta alrededor de 1/4 o 1/5 pacientes incluidos en Europa10. Este registro ofrece una buena oportunidad para estimar la magnitud del problema de la hiperpotasemia en la población actual de pacientes con IC en España, así como su papel en que no se alcancen las dosis objetivo de los fármacos según las guías de práctica clínica, objetivos ambos de este trabajo, y ofrece al mismo tiempo información única acerca de los cambios producidos durante el seguimiento.
MÉTODOSLa metodología del registro ya se ha descrito en detalle con anterioridad, tanto en general10 como en España11. En resumen, en España participaron 28 centros con diferentes grados de complejidad en su oferta de atención cardiológica que, durante el periodo de reclutamiento, incluyeron a todos los pacientes ambulatorios con IC mayores de 18 años atendidos en la consulta externa seleccionada, así como los hospitalizados ese mismo día por IC aguda (bien IC de novo o descompensación aguda de IC previa) por requerir tratamiento intravenoso (inotrópicos, vasodilatadores o diuréticos). La estrategia de reclutamiento cambió en el tiempo, desde 1 día a la semana durante el primer año del registro hasta 5 días consecutivos por trimestre a partir de finales de 2013. El registro es dinámico, en el sentido de que los centros pueden haberse incorporado a él en diferentes momentos y haber incluido a pacientes durante periodos distintos. Se presenta la información de los pacientes incluidos entre julio de 2011 y diciembre de 2016.
Se siguió a los pacientes según la práctica habitual en cada centro, salvo la visita obligatoria de seguimiento a los 12 meses para recoger información de morbilidad y mortalidad. Se sustituyó esta visita por una llamada telefónica cuando no fue posible ver a los pacientes en la consulta.
El registro ESC-HF-LT tiene un programa de calidad que incluye la realización de auditorías a alrededor del 10% de los centros participantes, seleccionados al azar. Dos centros fueron auditados en 2013 en España. El estudio fue aprobado por el comité de ética para la investigación de cada centro y todos los pacientes otorgaron su consentimiento informado antes de su inclusión.
Se presenta información de la visita basal de ambos grupos, de IC aguda y de ICC. Debido a la gran variabilidad de situaciones y tratamientos durante los ingresos, que pueden actuar como factores de confusión de control muy difícil, se presenta toda la información de seguimiento solo del grupo de pacientes en situación estable, el de ICC.
Definiciones de aplicación en este estudioPara el análisis de la concentración de K+, en este trabajo se utilizan los de mayor aplicabilidad clínica: normal, K+ ≤ 5 mEq/l; elevación leve, entre 5,1 y 5,4 mEq/l; elevación moderada, entre 5,5 y 5,9 mEq/l y elevación importante, ≥ 6 mEq/l. Hipopotasemia se define como K+ <3,5 mEq/l e hiperpotasemia, K+> 5,4 mEq/l. Entre los ingresados, se clasificó como con hiperpotasemia o hipopotasemia, respectivamente, a todos los pacientes con al menos una determinación de K+> 5,4 o <3,5 mEq/l durante el ingreso. Se consideró antecedente de enfermedad renal cuando se hubiera documentado una creatinina sérica> 1,5 mg/dl, mientras que la función renal evaluada en la visita mediante el filtrado glomerular estimado con la fórmula MDRD (Modification of Diet in Renal Disease) se clasificó como normal o discretamente reducido (≥ 60ml/min/1,73 m2), con afección moderada (30-59ml/min/1,73 m2) o grave (< 30ml/min/1,73 m2)12. Se definió IC con fracción de eyección reducida una fracción de eyección del ventrículo izquierdo ≤ 40%2,3.
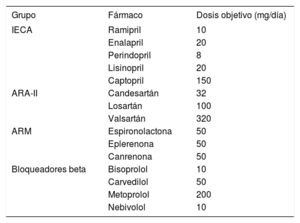
En cuanto a las dosis objetivo (tabla 1), la propia aplicación de entrada de datos del registro propone unas dosis objetivo de cada fármaco basadas en las guías de práctica clínica2. Se utilizaron esas mismas dosis, con la excepción de las de enalapril, pues en la recomendación de la aplicación indica que es 40 mg/día, cuando las guías recientes indican 10-20mg/día como dosis objetivo, y carvedilol, 100mg/día en la aplicación y 50mg/día en las guías recientes.
Dosis objetivo de los fármacos para los pacientes con insuficiencia cardiaca y fracción de eyección reducida
| Grupo | Fármaco | Dosis objetivo (mg/día) |
|---|---|---|
| IECA | Ramipril | 10 |
| Enalapril | 20 | |
| Perindopril | 8 | |
| Lisinopril | 20 | |
| Captopril | 150 | |
| ARA-II | Candesartán | 32 |
| Losartán | 100 | |
| Valsartán | 320 | |
| ARM | Espironolactona | 50 |
| Eplerenona | 50 | |
| Canrenona | 50 | |
| Bloqueadores beta | Bisoprolol | 10 |
| Carvedilol | 50 | |
| Metoprolol | 200 | |
| Nebivolol | 10 |
ARA-II: antagonista del receptor de la angiotensina II; ARM: antagonista del receptor de mineralocorticoides; IECA: inhibidor de la enzima de conversión de la angiotensina.
Las variables continuas se presentan como media± desviación típica y las categóricas, como porcentajes. En estimaciones poblacionales se presentan las estimaciones puntuales y su intervalo de confianza del 95% (IC95%) cuando corresponde. Las comparaciones entre grupos se realizan mediante la prueba de la t de Student o la prueba exacta de Fisher en función del tipo de variable. Se utilizó regresión logística para analizar los factores asociados con el empeoramiento de las cifras de K+ en el seguimiento. Se consideró empeoramiento cuando en la visita de seguimiento se clasificaba a los pacientes en una categoría de K+ sérico más alta que en la visita basal según las categorías definidas con anterioridad. Los factores identificados en el análisis univariado (p <0,1) se incluyeron en un modelo multivariado retrógrado, manteniendo las variables con p <0,1 y forzando la presencia de edad y sexo en el modelo.
Todos los análisis se realizaron centralizadamente con el paquete estadístico STATA 12.0.
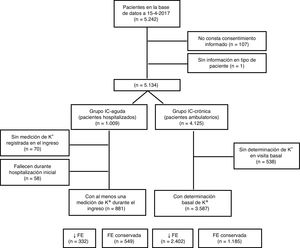
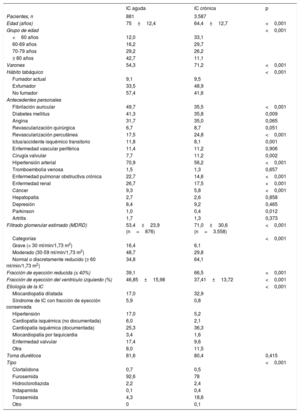
RESULTADOSDe los 5.242 pacientes incluidos en la base de datos en España a 10 de marzo de 2017, se descartó a 108 sin confirmación del consentimiento o con información incompleta respecto al tipo de paciente (agudo o crónico) y otros 58 que murieron durante la hospitalización. De los 5.076 restantes, 4.468 pacientes (88%) tuvieron al menos una medición de potasio en la visita basal (881 hospitalizados, el 35,5% con IC de nuevo diagnóstico, y 3.587 ambulatorios), por lo que constituyen el grupo de pacientes para el análisis de la fase basal (figura 1). Las características basales de ambos grupos se recogen en la tabla 2. Son perfiles de pacientes muy diferentes; de más edad y más mujeres en el grupo de pacientes con IC aguda, con mayor proporción de IC con fracción de eyección conservada y, en general, más presencia de comorbilidades, salvo los antecedentes de cardiopatía isquémica, estos en relación con diferencias entre los grupos en la etiología de la IC.
Comparación de las características basales entre pacientes de los grupos de IC aguda (ingresados) e IC crónica (ambulatorios)
| IC aguda | IC crónica | p | |
|---|---|---|---|
| Pacientes, n | 881 | 3.587 | |
| Edad (años) | 75±12,4 | 64,4±12,7 | <0,001 |
| Grupo de edad | <0,001 | ||
| <60 años | 12,0 | 33,1 | |
| 60-69 años | 16,2 | 29,7 | |
| 70-79 años | 29,2 | 26,2 | |
| ≥ 80 años | 42,7 | 11,1 | |
| Varones | 54,3 | 71,2 | <0,001 |
| Hábito tabáquico | <0,001 | ||
| Fumador actual | 9,1 | 9,5 | |
| Exfumador | 33,5 | 48,9 | |
| No fumador | 57,4 | 41,6 | |
| Antecedentes personales | |||
| Fibrilación auricular | 49,7 | 35,5 | <0,001 |
| Diabetes mellitus | 41,3 | 35,8 | 0,009 |
| Angina | 31,7 | 35,0 | 0,065 |
| Revascularización quirúrgica | 6,7 | 8,7 | 0,051 |
| Revascularización percutánea | 17,5 | 24,8 | <0,001 |
| Ictus/accidente isquémico transitorio | 11,8 | 8,1 | 0,001 |
| Enfermedad vascular periférica | 11,4 | 11,2 | 0,906 |
| Cirugía valvular | 7,7 | 11,2 | 0,002 |
| Hipertensión arterial | 70,9 | 56,2 | <0,001 |
| Tromboembolia venosa | 1,5 | 1,3 | 0,657 |
| Enfermedad pulmonar obstructiva crónica | 22,7 | 14,6 | <0,001 |
| Enfermedad renal | 26,7 | 17,5 | <0,001 |
| Cáncer | 9,3 | 5,8 | <0,001 |
| Hepatopatía | 2,7 | 2,6 | 0,858 |
| Depresión | 8,4 | 9,2 | 0,465 |
| Parkinson | 1,0 | 0,4 | 0,012 |
| Artritis | 1,7 | 1,3 | 0,373 |
| Filtrado glomerular estimado (MDRD) | 53,4±23,9 (n=876) | 71,0±30,6 (n=3.558) | <0,001 |
| Categorías | <0,001 | ||
| Grave (< 30 ml/min/1,73 m2) | 16,4 | 6,1 | |
| Moderado (30-59 ml/min/1,73 m2) | 48,7 | 29,8 | |
| Normal o discretamente reducido (≥ 60 ml/min/1,73 m2) | 34,8 | 64,1 | |
| Fracción de eyección reducida (≤ 40%) | 39,1 | 66,5 | <0,001 |
| Fracción de eyección del ventrículo izquierdo (%) | 46,85±15,98 | 37,41±13,72 | <0,001 |
| Etiología de la IC | <0,001 | ||
| Miocardiopatía dilatada | 17,0 | 32,9 | |
| Síndrome de IC con fracción de eyección conservada | 5,9 | 0,8 | |
| Hipertensión | 17,0 | 5,2 | |
| Cardiopatía isquémica (no documentada) | 6,0 | 2,1 | |
| Cardiopatía isquémica (documentada) | 25,3 | 36,3 | |
| Miocardiopatía por taquicardia | 3,4 | 1,6 | |
| Enfermedad valvular | 17,4 | 9,6 | |
| Otra | 8,0 | 11,5 | |
| Toma diuréticos | 81,6 | 80,4 | 0,415 |
| Tipo | <0,001 | ||
| Clortalidona | 0,7 | 0,5 | |
| Furosemida | 92,6 | 78 | |
| Hidroclorotiazida | 2,2 | 2,4 | |
| Indapamida | 0,1 | 0,4 | |
| Torasemida | 4,3 | 18,6 | |
| Otro | 0 | 0,1 | |
IC: insuficiencia cardiaca, MDRD: Modification of Diet in Renal Disease.
Salvo otra indicación, los valores expresan % o media±desviación estándar.
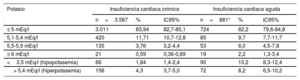
La distribución de las cifras de potasio y la prevalencia de hiperpotasemia en ambos grupos se presentan en la tabla 3. La hiperpotasemia en los pacientes ingresados fue prácticamente el doble que en los ambulatorios.
Distribución de los valores de potasio y prevalencia de hiperpotasemia (K+> 5,4 mEq/l) en la visita basal de pacientes con insuficiencia cardiaca aguda y crónica
| Potasio | Insuficiencia cardiaca crónica | Insuficiencia cardiaca aguda | ||||
|---|---|---|---|---|---|---|
| n=3.587 | % | IC95% | n=881* | % | IC95% | |
| ≤ 5 mEq/l | 3.011 | 83,94 | 82,7-85,1 | 724 | 82,2 | 79,6-84,8 |
| 5,1-5,4 mEq/l | 420 | 11,71 | 10,7-12,8 | 85 | 9,7 | 7,7-11,7 |
| 5,5-5,9 mEq/l | 135 | 3,76 | 3,2-4,4 | 53 | 6,0 | 4,5-7,8 |
| ≥ 6 mEq/l | 21 | 0,59 | 0,36-0,89 | 19 | 2,2 | 1,3-3,4 |
| <3,5 mEq/l (hipopotasemia) | 66 | 1,84 | 1,4-2,4 | 90 | 10,2 | 8,3-12,4 |
| > 5,4 mEq/l (hiperpotasemia) | 156 | 4,3 | 3,7-5,0 | 72 | 8,2 | 6,5-10,2 |
IC95%: intervalo de confianza del 95%.
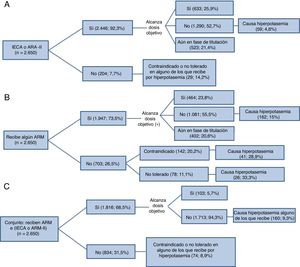
Toda la información presentada de aquí en adelante se refiere al grupo de pacientes en situación estable, el de ICC. La figura 2 resume, en el grupo de pacientes con ICC (ambulatorios), fracción de eyección reducida e información completa de fármacos (n=2.650), el problema de la hiperpotasemia como causa de que no se administren o no se alcancen las dosis objetivo de fármacos con demostrada eficacia y también afectan a las concentraciones de potasio (IECA, antagonistas del receptor de la angiotensina II [ARA-II] y ARM). Otras causas se detallan en la . No se incluye el sacubitrilo-valsartán porque no estaba incluido inicialmente en la base de datos y hay información de pocos pacientes: solo lo recibían 14, y 19 lo tenían contraindicado (no se registró la causa). La hiperpotasemia fue la causa de que no se administrara el fármaco en cuestión o no se alcanzara la dosis objetivo de ARM con más frecuencia que con los otros fármacos, en especial a expensas de no recibir el fármaco. En total, 1.784 pacientes (67%) no recibieron ARM (n=703) o no alcanzaron las dosis objetivo (n=1.081); otros 402 pacientes (15,9%) estaban aún en fase de titulación. En cuanto a los IECA/ARA-II, 1.494 pacientes (56,4%) no los recibieron (n=204) o no alcanzaron las dosis objetivo (n=1.290), mientras que 523 pacientes (19,7%) estaban en fase de titulación. Con los ARM, la hiperpotasemia fue la causa del 28,9% de todos los casos en que se contraindicó el fármaco y el 33,3% de todos los casos en que no se toleró (el 14,2% de las causas de contraindicación o intolerancia de los IECA/ARA-II), así como del 15% de todos los casos en que no se alcanzó la dosis objetivo (el 4,6% en el caso de los IECA/ARA-II). Del total de pacientes que no recibieron ARM o no alcanzaron las dosis objetivo (n=1.784), el 12,8% (n=229) se debió a hiperpotasemia a juicio del médico que trató al paciente. Las cifras correspondientes a los IECA/ARA-II son 88 (5,9%) de 1.494. Al considerar conjuntamente recibir IECA/ARA-II y ARM, solo una minoría recibió fármacos de ambos grupos a las dosis recomendadas. En el resto, la hiperpotasemia estaba presente como causa en el 9,2% (234/2.547) de los casos.
Uso de fármacos inhibidores del sistema renina-angiotensina-aldosterona en pacientes con fracción de eyección reducida e hiperpotasemia como obstáculo al tratamiento con IECA-ARA-II (A), ARM (B) y ambos grupos (C) en la visita basal. ARA-II: antagonista del receptor de la angiotensina II; ARM: antagonista del receptor de mineralocorticoides; IECA: inhibidor de la enzima de conversión de la angiotensina.
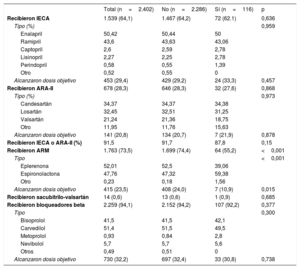
Del total de 2.693 pacientes ambulatorios con fracción de eyección reducida, 291 (10,8%) no tenían registrada medición de potasio en la visita basal (las características de los grupos se presentan en la ). La tabla 4 complementa a la figura 2 y compara los fármacos de interés que los pacientes recibieron basalmente en función de si presentaban o no hiperpotasemia en esa visita. Alrededor del 90% de los pacientes recibieron IECA o ARA-II y el 73,5% recibieron ARM, si bien solo una pequeña proporción, un 20-30%, había alcanzado las dosis objetivo de cualquiera de estos fármacos en la visita basal.
Comparación de los fármacos de interés recibidos en la visita basal por los pacientes con insuficiencia cardiaca crónica y fracción de eyección reducida en función de la presencia o ausencia basal de hiperpotasemia (K+> 5,4 mEq/l)
| Total (n=2.402) | No (n=2.286) | Sí (n=116) | p | |
|---|---|---|---|---|
| Recibieron IECA | 1.539 (64,1) | 1.467 (64,2) | 72 (62.1) | 0,636 |
| Tipo (%) | 0,959 | |||
| Enalapril | 50,42 | 50,44 | 50 | |
| Ramipril | 43,6 | 43,63 | 43,06 | |
| Captopril | 2,6 | 2,59 | 2,78 | |
| Lisinopril | 2,27 | 2,25 | 2,78 | |
| Perindopril | 0,58 | 0,55 | 1,39 | |
| Otro | 0,52 | 0,55 | 0 | |
| Alcanzaron dosis objetivo | 453 (29,4) | 429 (29,2) | 24 (33,3) | 0,457 |
| Recibieron ARA-II | 678 (28,3) | 646 (28,3) | 32 (27,6) | 0,868 |
| Tipo (%) | 0,973 | |||
| Candesartán | 34,37 | 34,37 | 34,38 | |
| Losartán | 32,45 | 32,51 | 31,25 | |
| Valsartán | 21,24 | 21,36 | 18,75 | |
| Otro | 11,95 | 11,76 | 15,63 | |
| Alcanzaron dosis objetivo | 141 (20,8) | 134 (20,7) | 7 (21,9) | 0,878 |
| Recibieron IECA o ARA-II (%) | 91,5 | 91,7 | 87,8 | 0,15 |
| Recibieron ARM | 1.763 (73,5) | 1.699 (74,4) | 64 (55,2) | <0,001 |
| Tipo | <0,001 | |||
| Eplerenona | 52,01 | 52,5 | 39,06 | |
| Espironolactona | 47,76 | 47,32 | 59,38 | |
| Otro | 0,23 | 0,18 | 1,56 | |
| Alcanzaron dosis objetivo | 415 (23,5) | 408 (24,0) | 7 (10,9) | 0,015 |
| Recibieron sacubitrilo-valsartán | 14 (0,6) | 13 (0,6) | 1 (0,9) | 0,685 |
| Recibieron bloqueadores beta | 2.259 (94,1) | 2.152 (94,2) | 107 (92,2) | 0,377 |
| Tipo | 0,300 | |||
| Bisoprolol | 41,5 | 41,5 | 42,1 | |
| Carvedilol | 51,4 | 51,5 | 49,5 | |
| Metoprolol | 0,93 | 0,84 | 2,8 | |
| Nevibolol | 5,7 | 5,7 | 5,6 | |
| Otros | 0,49 | 0,51 | 0 | |
| Alcanzaron dosis objetivo | 730 (32,2) | 697 (32,4) | 33 (30,8) | 0,738 |
ARA-II: antagonista del receptor de la angiotensina II; ARM: antagonista del receptor de mineralocorticoides; IECA: inhibidor de la enzima de conversión de la angiotensina.
Salvo otra indicación, los valores expresan n (%).
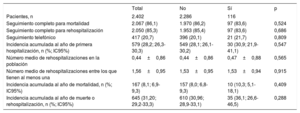
Hay información completa del seguimiento de la mortalidad y las hospitalizaciones del 86 y el 85,3% de los 2.402 pacientes ambulatorios con fracción de eyección reducida y medición de potasio basal respectivamente, sin diferencias entre aquellos con y sin hiperpotasemia en la visita basal ni en la proporción de pérdidas ni en el tipo de visita (presencial o telefónica). No se observaron diferencias estadísticamente significativas en rehospitalización o muerte entre ambos grupos ni en ninguno de los dos desenlaces por separado (tabla 5).
Hospitalización y mortalidad al año según la presencia o ausencia basal de hiperpotasemia
| Total | No | Sí | p | |
|---|---|---|---|---|
| Pacientes, n | 2.402 | 2.286 | 116 | |
| Seguimiento completo para mortalidad | 2.067 (86,1) | 1.970 (86,2) | 97 (83,6) | 0,524 |
| Seguimiento completo para rehospitalización | 2.050 (85,3) | 1.953 (85,4) | 97 (83,6) | 0,686 |
| Seguimiento telefónico | 417 (20,7) | 396 (20,1) | 21 (21,7) | 0,809 |
| Incidencia acumulada al año de primera hospitalización, n (%; IC95%) | 579 (28,2; 26,3-30,3) | 549 (28,1; 26,1-30,2) | 30 (30,9; 21,9-41,1) | 0,547 |
| Número medio de rehospitalizaciones en la población | 0,44±0,86 | 0,44±0,86 | 0,47±0,88 | 0,565 |
| Número medio de rehospitalizaciones entre los que tienen al menos una | 1,56±0,95 | 1,53±0,95 | 1,53±0,94 | 0,915 |
| Incidencia acumulada al año de mortalidad, n (%; IC95%) | 167 (8,1; 6,9-9,3) | 157 (8,0; 6,8-9,3) | 10 (10,3; 5,1-18,1) | 0,409 |
| Incidencia acumulada al año de muerte o rehospitalización, n (%; IC95%) | 645 (31,20; 29,2-33,3) | 610 (30,96; 28,9-33,1) | 35 (36,1; 26,6-46,5) | 0,288 |
IC95%: intervalo de confianza del 95%.
Salvo otra indicación, los valores expresan n (%) o media±desviación estándar.
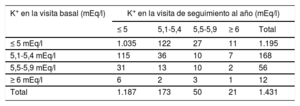
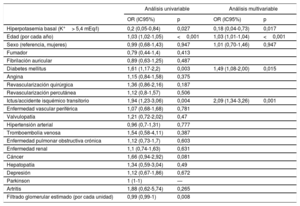
La tabla 6 muestra los cambios de categoría de las cifras de potasio entre las visitas basal y al año de todos los pacientes con este dato disponible (n=1.431). En el 16,8% de las mediciones (480 de 2.862), 2 por paciente, se observó un K+> 5 mEq/l. Empeoraron su categoría (aumento respecto al valor basal) 179 pacientes (12,5%; IC95%, 10,8-14,3%), pero la proporción en que este empeoramiento haría necesario algún cambio terapéutico fue menor (n=55 [3,8%; IC95%, 2,8-4,9]). Diversas características basales tienen asociación univariable con el riesgo de empeoramiento (tabla 7), pero en el análisis multivariable, ajustado por edad y sexo, solo permanecen en el modelo los antecedentes de accidente cerebrovascular y diabetes mellitus. La presencia de antecedentes personales de hiperpotasemia en la visita basal es la característica que se relacionó más intensamente (de manera inversa) con el riesgo de aumento de las cifras de potasio en el seguimiento.
Evolución de las concentraciones de potasio entre la visita basal y la de seguimiento de los pacientes con insuficiencia cardiaca crónica
| K+ en la visita basal (mEq/l) | K+ en la visita de seguimiento al año (mEq/l) | ||||
|---|---|---|---|---|---|
| ≤ 5 | 5,1-5,4 | 5,5-5,9 | ≥ 6 | Total | |
| ≤ 5 mEq/l | 1.035 | 122 | 27 | 11 | 1.195 |
| 5,1-5,4 mEq/l | 115 | 36 | 10 | 7 | 168 |
| 5,5-5,9 mEq/l | 31 | 13 | 10 | 2 | 56 |
| ≥ 6 mEq/l | 6 | 2 | 3 | 1 | 12 |
| Total | 1.187 | 173 | 50 | 21 | 1.431 |
Asociación de las características basales con el aumento de la hiperpotasemia en el seguimiento de pacientes con insuficiencia cardiaca crónica (los 179 pacientes que aumentan de nivel señalados en la tabla 6)
| Análisis univariable | Análisis multivariable | |||
|---|---|---|---|---|
| OR (IC95%) | p | OR (IC95%) | p | |
| Hiperpotasemia basal (K+> 5,4 mEq/l) | 0,2 (0,05-0,84) | 0,027 | 0,18 (0,04-0,73) | 0,017 |
| Edad (por cada año) | 1,03 (1,02-1,05) | <0,001 | 1,03 (1,01-1,04) | <0,001 |
| Sexo (referencia, mujeres) | 0,99 (0,68-1,43) | 0,947 | 1,01 (0,70-1,46) | 0,947 |
| Fumador | 0,79 (0,44-1,4) | 0,413 | ||
| Fibrilación auricular | 0,89 (0,63-1,25) | 0,487 | ||
| Diabetes mellitus | 1,61 (1,17-2,2) | 0,003 | 1,49 (1,08-2,00) | 0,015 |
| Angina | 1,15 (0,84-1,58) | 0,375 | ||
| Revascularización quirúrgica | 1,36 (0,86-2,16) | 0,187 | ||
| Revascularización percutánea | 1,12 (0,8-1,57) | 0,506 | ||
| Ictus/accidente isquémico transitorio | 1,94 (1,23-3,06) | 0,004 | 2,09 (1,34-3,26) | 0,001 |
| Enfermedad vascular periférica | 1,07 (0,68-1,68) | 0,781 | ||
| Valvulopatía | 1,21 (0,72-2,02) | 0,47 | ||
| Hipertensión arterial | 0,96 (0,7-1,31) | 0,777 | ||
| Tromboembolia venosa | 1,54 (0,58-4,11) | 0,387 | ||
| Enfermedad pulmonar obstructiva crónica | 1,12 (0,73-1,7) | 0,603 | ||
| Enfermedad renal | 1,1 (0,74-1,63) | 0,631 | ||
| Cáncer | 1,66 (0,94-2,92) | 0,081 | ||
| Hepatopatía | 1,34 (0,59-3,04) | 0,49 | ||
| Depresión | 1,12 (0,67-1,86) | 0,672 | ||
| Parkinson | 1 (1-1) | — | ||
| Artritis | 1,88 (0,62-5,74) | 0,265 | ||
| Filtrado glomerular estimado (por cada unidad) | 0,99 (0,99-1) | 0,008 | ||
IC95%: intervalo de confianza del 95%; OR: odds ratio.
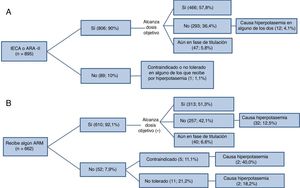
En la figura 3 se presenta la situación de los tratamientos de interés en el seguimiento de los pacientes que basalmente no tenían problemas con el potasio. Una elevada proporción de los pacientes que recibieron ARM no alcanzaron las dosis objetivo (42,1%); de estos, el 12,5% se debió a hiperpotasemia.
Uso de fármacos inhibidores del sistema renina-angiotensina-aldosterona: IECA/ARA-II (A) y ARM (B) en la visita de seguimiento de pacientes con fracción de eyección reducida y sin problemas en la visita basal atribuibles a la hiperpotasemia*. ARA-II: antagonista del receptor de la angiotensina II; ARM: antagonista del receptor de mineralocorticoides; IECA: inhibidor de la enzima de conversión de la angiotensina. *Pacientes que basalmente estaban con el fármaco y alcanzaron las dosis objetivo o no las alcanzaron porque aún estaban en aumento de dosis.
Este estudio, que refleja la situación en centros que disponen, de una u otra manera, de una estructura dedicada al tratamiento crónico de la IC, pone de manifiesto varios hechos relevantes: en pacientes con IC y fracción de eyección reducida, la presencia de hiperpotasemia en algún momento no es una rareza (el 4,3% de los pacientes ambulatorios la presentan y casi el doble entre los pacientes ingresados en algún momento de su ingreso) y, además, se le presta menos atención de la que precisa, como indica que no consta la medición de potasio en la visita basal del 10,8% de los pacientes ambulatorios con fracción de eyección reducida, una medición imprescindible para guiar el tratamiento. Además, la hiperpotasemia es una causa incidente con relativa frecuencia de retirada de fármacos y, sobre todo, de no alcanzar las dosis objetivo durante el seguimiento.
En un estudio reciente de un único centro en España13, en el 7,8% de todas las mediciones de potasio (16.116 en un grupo de 2.164 pacientes) realizadas tras el alta por el ingreso índice por IC, se observa hiperpotasemia (definida, en este caso, como K+> 5 mEq/l). Esta cifra es del 17% en el presente estudio, lo que es importante por la conocida relación entre las elevaciones de potasio, incluso discretas, y la mortalidad13-16. El punto de corte para hiperpotasemia (K+> 5,4 mEq/l), aunque comúnmente aceptado, puede subestimar la magnitud real del problema, ya que un reciente estudio mostró que elevaciones pequeñas (incluso valores entre 4,8 y 5,0) respecto a los valores de comparación de potasio (4,2-4,4) se asociaron con mayor riesgo de muerte17.
El escaso seguimiento de las recomendaciones de vigilancia de la concentración de potasio2 de los pacientes tratados con fármacos inhibidores del SRAA se ha observado con anterioridad. En el proyecto SCREAM6, en el primer año de seguimiento tras el inicio de tratamiento con IECA o ARA-II, al 24% de los pacientes no se les midió el potasio. Son pacientes con bajo riesgo de hiperpotasemia, pues solo el 7% tenía antecedentes de IC y el 4% utilizaba diuréticos ahorradores de potasio (ambos factores se identificaron asociados con el riesgo de hiperpotasemia en este estudio, con odds ratio [OR] entre 1,5 y 2,0). Los pacientes de este estudio considerados para este análisis tienen un riesgo de hiperpotasemia mucho mayor, pues todos son pacientes con IC y fracción de eyección reducida y la gran mayoría reciben fármacos que pueden afectar a la concentración de potasio. Las guías de la ESC recomiendan, en lo relativo al uso de ARM e IECA/ARA-II, comprobar la bioquímica sanguínea (incluido el K+) con frecuencia (después de 1 y 4 semanas tras el inicio/incremento de la dosis y a las 8 y 12 semanas; después, cada 4 meses)2. Por ello, disponer de la medición de potasio en una visita clínica es imprescindible para guiar el tratamiento, y el 10,9% de pacientes a los que no se midió el potasio sirve como estimación, probablemente a la baja, del margen de mejora disponible aún.
La hiperpotasemia es causa relativamente frecuente de no alcanzar en el seguimiento las dosis recomendadas de fármacos inhibidores del SRAA y lo es aún más entre los pacientes con problemas con los tratamientos en la visita basal atribuibles a la hiperpotasemia.
Incluso en el entorno muy controlado de los ensayos clínicos, el uso de fármacos que bloquean el SRAA se asocia con mayor frecuencia de hiperpotasemia18-20. De hecho, cuando se observó eficacia en los eventos clínicos sin la contrapartida de hiperpotasemias, se atribuyó el logro a la monitorización cuidadosa del potasio21. Esta complicación, sin embargo, se presenta en la práctica clínica habitual22 y puede contrarrestar los efectos beneficiosos de los inhibidores del SRAA (en especial los ARM) si se relaja la monitorización cuidadosa del potasio.
El presente estudio confirma la dificultad, debida a problemas de tolerancia, de alcanzar las dosis objetivo con estos fármacos. Así sucede en ensayos con fármacos que inhiben el SRAA, pese a la vigilancia intensiva que permiten los ensayos clínicos y difícilmente es posible en la práctica clínica habitual. En el estudio CONSENSUS, solo el 22% de los pacientes del grupo de tratamiento activo alcanzaron la dosis objetivo de 40mg de enalapril23. En el estudio SOLVD, con menor dosis objetivo de enalapril (20mg/día) y una fase de run-in para excluir a los intolerantes a dosis bajas, al final del estudio muchos pacientes no tomaban la medicación y, en el grupo de enalapril, el 27,5% de los que la tomaban lo hacían en dosis menores que las objetivo18. Ensayos más recientes, también con fase de run-in, como el PARADIGM, observaron una tasa de abandono de alrededor del 20% en el grupo con IECA24. Los hallazgos en ensayos con AMR son similares19,20.
Todos estos hechos son importantes para acentuar la necesidad de intensificar la vigilancia de las cifras de potasio en estos pacientes, ya que los que mantienen alterados los valores de potasio en el seguimiento tienen mayor riesgo de muerte que quienes los mantienen normales o que en el seguimiento los normalizan13. En el estudio no se observa relación entre las cifras de potasio en la visita basal y el riesgo de hospitalización o muerte en el seguimiento, hecho que creemos debe atribuirse a limitaciones del estudio en lo que respecta a mediciones previas de potasio y poder determinar correctamente las relaciones temporales entre mediciones y cambios terapéuticos y desenlaces.
Finalmente, hasta un 12,5% de los pacientes aumentan la concentración de potasio en el seguimiento y el 3,8% se sitúa en cifras que obligan a la retirada de fármacos demostrado beneficio en el pronóstico. Los factores asociados directamente en el análisis univariable con elevaciones de los valores de potasio (considerados como cambios en la categoría respecto a la situación en la visita basal) fueron edad, diabetes mellitus, antecedentes personales de accidente cerebrovascular o cáncer y la tasa de filtrado glomerular. Los antecedentes de hiperpotasemia en la visita basal sirven de alerta a los clínicos y «protegen» de aumentos en el seguimiento.
La guía del ACC/AHA de 2005 recoge ya el problema de la hiperpotasemia en pacientes con IC, en particular los tratados con inhibidores de la aldosterona, y se proponen 8 medidas para minimizar este riesgo25. La guía europea vigente2, además de hacer énfasis en la importancia de la valoración frecuente de electrolitos y de la función renal, como otras recomendaciones más recientes26, apunta la próxima disponibilidad de fármacos eficaces en reducir el potasio (patiromer y sodium zirconium cyclosilicate) y evitar la recurrencia de hiperpotasemia en pacientes con IC tratados con inhibidores del SRAA, lo que abre en el corto o medio plazo una nueva perspectiva para el tratamiento de estos pacientes. Además, el desarrollo de nuevos ARM no hormonales, como la finerenona, puede aportar ventajas por su menor asociación con hiperpotasemia.
Es importante conocer las limitaciones de este trabajo para su correcta interpretación y aplicabilidad. Así, mientras que, en nuestra opinión, constituye una buena aproximación a la situación del problema de la hiperpotasemia en la práctica clínica habitual para los pacientes con IC y fracción de eyección reducida en centros españoles en los que se realiza un seguimiento estructurado de esta enfermedad, esto se refleja también en la falta de exhaustividad de la información disponible, incluidas las mediciones de potasio, limitación muy común a este tipo de estudios. Un reciente análisis transversal del registro sueco de IC reconoce la ausencia de medición de potasio en el 39,6% de los pacientes que no toman ARM y más aún (43,7%; p <0,001) en el grupo que los toma27. El mismo estudio reconoce, como este, la limitación que supone en muchos registros la falta de información que refleje adecuadamente la relación temporal con otras mediciones de potasio que pueden haber condicionado cambios de tratamiento.
CONCLUSIONESDebido a que la hiperpotasemia es una preocupación creciente en el tratamiento de los pacientes con IC y fracción de eyección reducida por su relación con el riesgo de arritmias y muerte y su asociación con la propia presencia de IC y comorbilidades frecuentes, así como con fármacos de demostrada eficacia en estos pacientes, este trabajo, realizado en condiciones de práctica clínica habitual en centros y unidades con seguimiento estructurado de la IC, trae a primer plano la necesidad de intensificar la atención a la hiperpotasemia en la práctica clínica con estos pacientes y propone algunos grupos en los que la atención debe ser aún mayor.
FINANCIACIÓNEste trabajo está co-financiado con Fondos FEDER. Instituto de Salud Carlos III.
CONFLICTO DE INTERESESM.G. Crespo-Leiro declara honorarios por labores de consultoría de Novartis y Abbott y haber recibido remuneración como ponente, actividades educativas y gastos de viaje de Novartis, Astellas, MSD, Boehringer Ingelheim y HeartWare, y tiene pendiente de recibir una beca a su institución de CIBERCV, SEC y FMM, todo esto no relacionado con el presente trabajo.
J. González-Costello declara honorarios por labores de consultoría para Abbott, Pfizer y Alnylam, y haber recibido remuneración por gastos de viaje, alojamiento y asistencia a reuniones de Servier, Novartis, Rovi, Bayer, Bristol, Pfizer, Abbott y Astellas, todo esto no relacionado con el presente trabajo.
A. Bayés-Genís declara honorarios por labores de consultoría de Vifor y está pendiente de recibir una beca de Vifor con cargo a su institución, todo esto no relacionado con el presente trabajo.
D.A. Pascual-Figal declara honorarios por labores de consultoría de Novartis y Roche; una beca pendiente de recibir por parte de Novartis y roche a su institución, y haber recibido remuneración como ponente, actividades educativas y gastos de viaje de Novartis, Roche, Servier y MSD, todo esto no relacionado con el presente trabajo.
F. Ridocci-Soriano declara haber recibido remuneración como ponente y gastos de viaje, alojamiento y asistencia a reuniones de Novartis, Servier y Menarini, todo esto no relacionado con el presente trabajo.
L.H. Lund declara haber recibido una beca de Relypsa y honorarios por las labores de consultoría de Vifor Pharma y AstraZeneca relacionados con este trabajo.
J. Muñiz declara haber recibido honorarios por consultoría y por la redacción o revisión del manuscrito de la Sección de IC de la SEC.
A.P. Maggioni declara haber recibido remuneración de Servier para la preparación de manuscritos y es miembro de comités de estudio patrocinados por Novartis, Bayer y Fresenius, todo esto no relacionado con este trabajo.
El resto de los autores no declara conflicto de intereses.
- –
Varios fármacos eficaces en el tratamiento de pacientes con IC y fracción de eyección reducida y de uso muy generalizado interfieren en el SRAA y multiplican por 2 o 3 el riesgo de hiperpotasemia de estos pacientes.
- –
La hiperpotasemia se asocia con trastornos de la conducción y riesgo de arritmias potencialmente mortales, por lo cual es una preocupación creciente en el tratamiento de estos pacientes.
- –
Pese a esto, no existe información prospectiva que estime el problema de la hiperpotasemia en pacientes con IC en la práctica clínica cotidiana en España.
- –
Se presentan estimaciones actuales de la magnitud del problema de la hiperpotasemia en los pacientes con IC en España y su papel en que no se alcancen las dosis objetivo de los fármacos según las guías de práctica clínica, así como información única acerca de los cambios en las concentraciones de potasio durante el seguimiento de estos pacientes en condiciones de práctica clínica habitual en España.
- –
El trabajo trae a primer plano la necesidad de intensificar la atención a la hiperpotasemia en la práctica clínica con estos pacientes y propone algunos grupos en los que la atención debe ser aún mayor.
.
Para la realización de los análisis de datos necesarios, este trabajo contó con un patrocinio no condicionado de Vifor Pharma a través de un acuerdo con la Sección de Insuficiencia Cardiaca de la Sociedad Española de Cardiología.