Full English text available from: www.revespcardiol.org/en
El implante percutáneo de válvula aórtica (TAVI) es actualmente el método de elección para el tratamiento de los pacientes con valvulopatías aórticas sintomáticas cuando el equipo multidisciplinario considera que son inoperables o tienen un riesgo quirúrgico elevado.
Con el empleo del sistema Edwards Sapien, el estudio Partner demostró una tasa de mortalidad similar a la de la cirugía a los 30 días (el 3,4 frente al 6,5%; p = 0,07) y a 1 año (el 24,2 frente al 26,8%; p = 0,44)1. Con el sistema Medtronic CoreValve se dio un paso más y se demostró una tasa de supervivencia a 1 año significativamente superior a la de la cirugía (el 14,2 frente al 19,1%; p = 0,04)2. Sin embargo, con estos dispositivos de primera generación había dificultades como las complicaciones vasculares1–3, la fuga paravalvular4–7, la necesidad de marcapasos permanentes8,9 y el ictus10. Aunque la selección de los pacientes y la experiencia de los operadores podrían haber explicado algunos de estos resultados, se cree que las dificultades asociadas a los dispositivos han sido factores contribuyentes.
La válvula Edwards SAPIEN 3 y el sistema de aplicación Commander, con su e-vaina de tamaño 14-16 Fr, son los avances más recientes en el sistema de Edwards para TAVI. La válvula SAPIEN 3 tiene una falda externa destinada a reducir la fuga paravalvular. El sistema de aplicación Commander, con su doble capacidad de flexión y el perfil reducido de la vaina, se ha diseñado para mejorar la aplicación y el despliegue de la válvula. Los resultados de los estudios iniciales indican una mejora de los resultados en comparación con sus predecesores11. La válvula Medtronic Evolut R, con el catéter de aplicación Enveo y la vaina InLine, es la generación actual del sistema de Medtronic para TAVI12. La válvula supraanular es más deformable, con objeto de reducir la fuga paravalvular mediante una mayor adherencia al tejido circundante. El nuevo sistema de aplicación permite que la válvula sea totalmente reposicionable y recapturable antes de haberla liberado por completo. La vaina InLine incorporada permite introducir todo el sistema en el paciente sin uso de una vaina, lo que reduce el perfil total del sistema, que es similar al diámetro externo de una vaina de tamaño 14 Fr; esto hace que la válvula Evolut R sea el sistema de TAVI comercializado de menor perfil. El estudio inicial de marca CE ha mostrado que las tasas totales de eventos para los parámetros clave con la válvula Evolut R son mejores que las de la CoreValve12. Otros dispositivos de nueva generación (sistemas para TAVI Lotus de Boston Scientific y Portico de St. Jude Medical) han obtenido buenos resultados similares en los estudios iniciales13,14. En la tabla se resumen algunos de los resultados clave de los sistemas para TAVI de nueva generación.
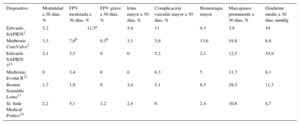
Resumen de los resultados a 30 días con los dispositivos para TAVI de primera generación y de la generación actual
| Dispositivo | Mortalidad a 30 días, % | FPV moderada a 30 días, % | FPV grave a 30 días, % | Ictus mayor a 30 días, % | Complicación vascular mayor a 30 días, % | Hemorragia mayor | Marcapasos permanente a 30 días, % | Gradiente medio a 30 días, mmHg |
|---|---|---|---|---|---|---|---|---|
| Edwards SAPIEN1 | 5,2 | 11,5a | 3,8 | 11 | 9,3 | 3,8 | 10 | |
| Medtronic CoreValve2 | 3,3 | 7,6b | 0,3b | 3,1 | 5,9 | 13,6 | 19,8 | 8,8 |
| Edwards SAPIEN 311 | 2,1 | 3,5 | 0 | 0 | 5,2 | 2,1 | 12,5 | 10,9 |
| Medtronic Evolut R12 | 0 | 3,4 | 0 | 0 | 8,3 | 5 | 11,7 | 8,1 |
| Boston Scientific Lotus13 | 1,7 | 1,9 | 0 | 3,4 | 5,1 | 8,5 | 29,3 | 11,3 |
| St. Jude Medical Portico14 | 2,2 | 5,1 | 1,2 | 2,4 | 6 | 2,4 | 10,8 | 8,7 |
FPV: fuga paravalvular.
Queda por ver qué resultados aportan estos nuevos dispositivos en la práctica clínica real. En el artículo publicado en Revista Española de Cardiología, Perrin et al.15 presentan su experiencia de un solo centro con el sistema Medtronic Evolut R. Se trató a 71 pacientes con el nuevo sistema, lo cual supone un 85,5% del total de intervenciones de TAVI de su centro en un periodo de 14 meses. Los eventos de los objetivos clínicos se validaron de manera independiente según los criterios del Valve Academic Research Consortium (VARC)-2. Aunque en el estudio de marca CE, con 60 pacientes tratados, no hubo mortalidad a 30 días12, el 2,8% observado en esta serie de pacientes no seleccionados (all-comer) fue similar a los resultados recientemente publicados (tabla). En total, 4 pacientes necesitaron una segunda válvula o una válvula quirúrgica; esto parece estar relacionado con las dificultades técnicas o de la intervención, lo cual señala la necesidad de una curva de aprendizaje para los nuevos dispositivos, si bien no está claro cuándo se produjeron en su experiencia.
Perrin et al. indican recolocación de la válvula en un 21% de los pacientes para optimizar la colocación, con lo que se obtuvieron unas tasas favorables de fugas paravalvulares a 30 días (el 1,6% de carácter moderado)15. Sin embargo, las tasas de marcapasos permanentes fueron mayores que en el estudio de marca CE (el 23,9 frente al 11,7%). Los autores consideraron que podía deberse a una posición final de la válvula inferior en comparación con el estudio de CE. Tiene importancia señalar que, como en el estudio de CE, la recolocación de la vaina no se asoció a la aparición de ictus y que la tasa de ictus de carácter mayor observada por Perrin et al. fue baja, de un 1,4% (n = 1). Se observaron complicaciones vasculares mayores en un 8,3% de los pacientes del estudio de marca CE, frente a la inferior (4,2%) observada por Perrin et al. Estas cifras corresponden a una mejora respecto al 5,9% observado con la válvula de Medtronic CoreValve2 y el 11% con la Edwards SAPIEN1.
La definición del VARC-2 del éxito del dispositivo requiere la combinación de lo siguiente: a) ausencia de mortalidad en la intervención; b) posición correcta de una única válvula protésica, y c) funcionamiento pretendido de la válvula protésica (ausencia de discrepancia entre tamaño de la prótesis y el paciente [DPP], media de gradiente valvular < 20 mmHg o velocidad máxima < 3 m/s, y sin fuga moderada o grave de la válvula protésica). Si no se cumple alguno de estos 3 parámetros, se considera que ha habido un fallo del dispositivo. Perrin et al. describieron un 90,1% de éxitos del dispositivo, lo cual es superior a lo descrito con la válvula Evolut R en el estudio de CE (78,6%)12. El porcentaje de éxitos del dispositivo observado en el estudio de CE fue inferior al esperado, y ello se debió principalmente a la presencia de una DPP estimada en 9 pacientes y a la falta de datos de otros 5. Son bien conocidas las dificultades para estimar la DPP con la ecocardiografía transtorácica, en vez de la ecocardiografía transesofágica. En el artículo no queda claro si se estimó la DPP; no obstante, los resultados de Perrin et al. son tranquilizadores y confirman que los resultados del estudio de marca CE fueron en cierta medida un artefacto causado por el conjunto de datos de DPP disponible. El gradiente medio a 30 días descrito por Perrin et al. fue de 7,7 ± 4,1mmHg, lo cual puede compararse favorablemente con el estudio de marca CE, en el que fue de 8,1 ± 3,3mmHg.
Los pacientes incluidos en los primeros estudios en humanos o los estudios de marca CE suelen estar controlados por unos criterios de inclusión y exclusión que tienden a seleccionar para el estudio a pacientes que son mejores candidatos al TAVI. No obstante, las mejoras en algunos resultados clave son evidentes si se comparan los estudios en los que se utilizaron dispositivos de primera generación con los que han empleado dispositivos de la nueva generación (tabla). Aunque algunas de estas mejoras podrían atribuirse a una mejor selección de los pacientes, la experiencia de los operadores o el uso de la tomografía computarizada cardiaca, los avances tecnológicos han influido positivamente en los resultados clínicos. Igual importancia tiene el modo en que estos resultados se trasladan a la experiencia de la práctica clínica real y, para ello, los resultados publicados por Perrin et al. con el sistema Evolut R incrementan nuestro conocimiento sobre las repercusiones que tienen los sistemas de TAVI de nueva generación en nuestros pacientes. A pesar de estos avances tecnológicos, la diligencia y el cuidado del operador en las etapas preoperatoria, perioperatoria y posoperatoria serán de extraordinaria importancia si se pretende aprovechar las posibles ventajas de los sistemas para TAVI de nueva generación16.
CONFLICTO DE INTERESESG. Manoharan ha recibido pagos como asesor y honorarios de Medtronic, St. Jude Medical y Boston Scientific.