No está clara la asociación entre los inhibidores de la enzima de conversión de la angiotensina (IECA) o los antagonistas del receptor de la angiotensina II (ARA-II) y la mortalidad de los pacientes con síndrome coronario agudo (SCA) sometidos a intervención coronaria percutánea (ICP) con fracción de eyección del ventrículo izquierdo (FEVI) conservada. Nuestro objetivo es determinar dicha asociación en pacientes con FEVI conservada o reducida.
MétodosSe analizaron datos procedentes del registro BleeMACS. El objetivo principal fue la mortalidad a 1 año. Se aplicaron ponderación por la probabilidad inversa del tiempo de supervivencia y ajustes por regresión de Cox, puntuación de propensión y variables instrumentales.
ResultadosDe los 15.401 pacientes con SCA sometidos a ICP, se prescribieron IECA/ARA-II al 75,2%. Se produjeron 569 muertes (3,7%) durante el primer año tras el alta hospitalaria. Después del ajuste multivariado, los IECA/ARA-II se asociaron con menor mortalidad, pero solo en los pacientes con FEVI ≤ 40% (HR=0,62; IC95%, 0,43-0,90; p=0,012). Con los IECA/ARA-II, la reducción del riesgo relativo de la mortalidad estimada fue del 46,1% en los pacientes con FEVI ≤ 40% y del 15,7% en aquellos con FEVI> 40% (pinteracción=0,008). En los pacientes con FEVI> 40%, los IECA/ARA-II se asociaron con menor mortalidad solo por infarto agudo de miocardio con elevación del segmento ST (HR=0,44; IC95%, 0,21-0.93; p=0,031).
ConclusionesEl beneficio de los IECA/ARA-II en mortalidad tras ICP por SCA se concentra en pacientes con FEVI ≤ 40% y aquellos con FEVI> 40% e infarto agudo de miocardio con elevación del segmento ST. Se precisan estudios contemporáneos que analicen el impacto de los IECA/ARA-II en pacientes con SCA sin elevación del segmento ST y FEVI> 40%.
Palabras clave
Los inhibidores de la enzima de conversión de la angiotensina (IECA) y los antagonistas del receptor de la angiotensina II (ARA-II) forman parte de los 4 tratamientos farmacológicos basados en la evidencia tras un síndrome coronario agudo (SCA), junto con el tratamiento antiagregante plaquetario doble (TAPD), los bloqueadores beta y las estatinas1,2. No obstante, la evidencia acerca de los efectos positivos de los IECA/ARA-II provienen de un escenario clínico muy distinto del actual, con una incidencia muy baja (< 20%) de intervención coronaria percutánea (ICP) y tratamiento con TAPD y estatinas3–7. A excepción de los pacientes con fracción de eyección del ventrículo izquierdo (FEVI) reducida (≤ 40%), en quienes las pruebas son muchas y consistentes8–10 —complementadas por ensayos llevados a cabo en el ámbito de la insuficiencia cardiaca (IC)11,12—, la evidencia sobre el impacto pronóstico de los IECA/ARA-II en pacientes con una FEVI> 40% tratados con ICP, TAPD y estatinas es escasa e incluso contradictoria13–16. A pesar de estos indicios obsoletos y anticuados, las recomendaciones sobre la práctica clínica siguen a favor de recurrir a los IECA/ARA-II para todos los pacientes que han sufrido un SCA, además de los pacientes con FEVI ≤ 40%1,2.
Teniendo en cuenta esta «brecha temporal» entre los ensayos clínicos y las recomendaciones actuales, la disponibilidad de datos exploratorios que analicen si los resultados de los ensayos clínicos anteriores a la ICP siguen siendo válidos en la era actual de las ICP debería ser de gran valor clínico. En este estudio, el objetivo era analizar el impacto de los IECA/ARA-II tras un SCA en pacientes que se sometían a una ICP y recibían tratamiento conforme a las recomendaciones actuales, con una incidencia elevada de TAPD, bloqueadores beta y estatinas.
MÉTODOSDiseño del estudio y poblaciónLos análisis se basan en datos provenientes del registro BleeMACS. BleeMACS es un registro de cohortes multicéntrico, observacional y retrospectivo que consta de 15.401 pacientes consecutivos. Los criterios de inclusión y exclusión, la recogida de datos y las variables ya se han descrito con anterioridad17. Resumiendo, los pacientes elegibles fueron todos los pacientes adultos consecutivos (edad ≥ 18 años) dados de alta con un diagnóstico definitivo de SCA, establecido según las guías clínicas1,2 como enfermedad coronaria significativa documentada en una coronariografía (estenosis ≥ 50% en la arteria coronaria izquierda principal o ≥ 70% en las demás coronarias) con posterior realización de ICP. Todos ellos tuvieron un seguimiento de 1 año. Los participantes procedían de 15 hospitales de América del Norte y Sudamérica (Canadá y Brasil), Europa (Alemania, Polonia, Países Bajos, España, Italia y Grecia) y Asia (China y Japón). La participación se inició en noviembre de 2003 y se prolongó hasta junio de 2014. Sobre el diseño del ensayo BleeMACS y la población a estudio, se muestra más información en el material adicional (Información sobre el registro BleeMACS). El protocolo del estudio se ajusta a las recomendaciones éticas de la Declaración de Helsinki de 1975, tal como se refleja en una aprobación a priori del comité de ética de cada centro. El estudio se registró en ClinicalTrial.gov (NCT02466854).
Seguimiento y resultadosEl resultado principal es la mortalidad por cualquier causa, en una comparación de los pacientes tratados con IECA/ARA-II en el momento del alta frente a los no tratados. La prescripción de los IECA/ARA-II se basó en el criterio clínico del médico que llevaba a cabo el tratamiento. Todos los pacientes fueron sometidos a un seguimiento sistemático durante 1 año para evaluar el estado vital, determinado por coordinadores del estudio cualificados en cada centro participante. Los datos sobre el estado vital se obtuvieron del hospital y los registros de datos administrativos, estableciendo contacto telefónico con los pacientes o sus familiares cuando era necesario.
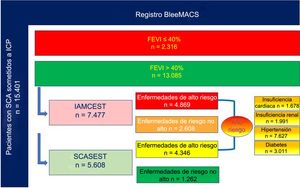
Análisis estadísticoEl análisis estadístico se realizó con los programas informáticos SPSS versión 24.0, R versión 3.2.2 y Stata MP64 versión 14. Las características iniciales en función del tratamiento con IECA/ARA-II se describieron utilizando el número y el porcentaje para datos categóricos y la diferencia promedio estandarizada para los datos continuos respectivamente. Las diferencias en las características se evaluaron utilizando las pruebas de la χ2 y las pruebas de la t de Student para 2 muestras. La asociación entre la exposición a IECA/ARA-II y la mortalidad a 1 año se estudió en modelos robustos de riesgos proporcionales de Cox con ajuste ante posibles factores de confusión en el momento inicial. El ajuste del riesgo del modelo multivariable se llevó a cabo con todas las variables asociadas con la mortalidad posterior al alta en función de la plausibilidad clínica o el valor de p <0,05 en los análisis univariantes de Cox (análisis univariante de Cox y tabla 1). Dada la presencia de diferencias importantes en lo que respecta a las características iniciales clave en función de la prescripción de un tratamiento con IECA/ARA-II (tabla 1), se complementó el análisis utilizando un análisis de la puntuación de propensión (propensity score). La puntuación de propensión se calculó utilizando un modelo de regresión logística multivariable y no parsimonioso, en el que el tratamiento con IECA/ARA-II conformaba las variables dependientes y las características que diferían entre pacientes tratados y no tratados con IECA/ARA-II (tabla 1), las covariables. A continuación se llevó a cabo la correspondencia de las puntuaciones de propensión para reunir una cohorte en la que todas las covariables medidas estuviesen bien equilibradas en todo el grupo de comparación (se proporcionan más detalles en el análisis de puntuaciones de propensión, tabla 2 y ). En la población emparejada por la puntuación de propensión (formada por 2 grupos de 3.765 pacientes con características similares en función de si tenían prescripción de IECA o no), la reducción de la mortalidad se comparó utilizando un modelo de regresión de Cox estratificado y robusto. También se utilizó el análisis de la puntuación de propensión de ponderación por la probabilidad inversa (PPI) del tiempo de supervivencia para evaluar la asociación entre el uso de IECA/ARA-II y la mortalidad. El efecto de los IECA/ARA-II se representó gráficamente por medio de las curvas de Kaplan-Meier ajustadas en función de la PPI, para equilibrar la distribución de las covariables entre el tratamiento y las observaciones de control, así como por las covariables asociadas con la mortalidad tras el alta en los análisis univariantes de Cox, para posteriormente atenuar los factores residuales de confusión en el modelado de la supervivencia. El análisis se complementó con una PPI aumentada (PPIA) para estimar el efecto promedio del tratamiento, siguiendo un método doblemente robusto que combinaba las propiedades tanto del estimador basado en la regresión como del estimador de la PPI. El coeficiente del efecto promedio del tratamiento evalúa la diferencia en el riesgo absoluto de la mortalidad a 1 año entre los pacientes tratados con IECA/ARA-II y los no tratados con dichos fármacos. Dado que la puntuación de propensión se ajusta únicamente por los factores de confusión medidos, se utilizó un análisis de las variables instrumentales con los índices anuales de cada hospital en lo que respecta a la prescripción de tratamientos indicados por las directrices (TAPD, bloqueadores beta, estatinas y IECA/ARA-II) como instrumento para evaluar además el posible sesgo de selección (más información en el análisis de variables instrumentales y en la ). El coeficiente de análisis de las variables instrumentales muestra la reducción relativa del riesgo en la mortalidad con IECA/ARA-II. Los análisis se llevaron a cabo con toda la cohorte de pacientes con SCA y de manera independiente en los casos con FEVI ≤ 40% y> 40% (el límite para una FEVI del 40% se basaba en las recomendaciones de las directrices europeas para el SCA1,2). En el grupo de pacientes con FEVI> 40%, se analizó por separado a los pacientes con infarto agudo de miocardio con elevación del segmento ST (IAMCEST) y con enfermedades de alto riesgo (IC, insuficiencia renal, diabetes mellitus [DM], hipertensión arterial) (figura 1). Estas enfermedades de alto riesgo se definieron según las recomendaciones de las guías europea y estadounidense para el tratamiento del SCA1,2. Se llevó a cabo una prueba de interacción en los modelos de regresión de Cox realizados en el estudio para evaluar la interacción entre el tratamiento y el subgrupo. Se consideró estadísticamente significativo un valor de p <0,05.
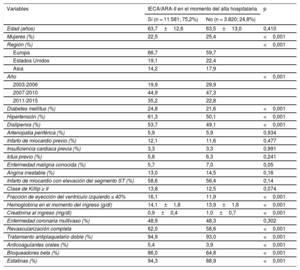
Características iniciales en función de si se prescriben IECA/ARA-II en el momento del alta o no
| Variables | IECA/ARA-II en el momento del alta hospitalaria | p | |
|---|---|---|---|
| Sí (n = 11.581; 75,2%) | No (n = 3.820; 24,8%) | ||
| Edad (años) | 63,7±12,6 | 63,5±13,0 | 0,410 |
| Mujeres (%) | 22,5 | 25,4 | <0,001 |
| Región (%) | <0,001 | ||
| Europa | 66,7 | 59,7 | |
| Estados Unidos | 19,1 | 22,4 | |
| Asia | 14,2 | 17,9 | |
| Año | <0,001 | ||
| 2003-2006 | 19,9 | 29,9 | |
| 2007-2010 | 44,9 | 47,3 | |
| 2011-2015 | 35,2 | 22,8 | |
| Diabetes mellitus (%) | 24,8 | 21,6 | <0,001 |
| Hipertensión (%) | 61,3 | 50,1 | <0,001 |
| Dislipemia (%) | 53,7 | 49,1 | <0,001 |
| Arteriopatía periférica (%) | 5,9 | 5,9 | 0,934 |
| Infarto de miocardio previo (%) | 12,1 | 11,6 | 0,477 |
| Insuficiencia cardiaca previa (%) | 3,3 | 3,3 | 0,991 |
| Ictus previo (%) | 5,8 | 6,3 | 0,241 |
| Enfermedad maligna conocida (%) | 5,7 | 7,0 | 0,05 |
| Angina inestable (%) | 13,0 | 14,5 | 0,16 |
| Infarto de miocardio con elevación del segmento ST (%) | 58,6 | 56,4 | 0,14 |
| Clase de Killip ≥ II | 13,8 | 12,5 | 0,074 |
| Fracción de eyección del ventrículo izquierdo ≤ 40% | 16,1 | 11,9 | <0,001 |
| Hemoglobina en el momento del ingreso (g/dl) | 14,1±1,8 | 13,9±1,8 | <0,001 |
| Creatinina al ingreso (mg/dl) | 0,9±0,4 | 1,0±0,7 | <0,001 |
| Enfermedad coronaria multivaso (%) | 48,9 | 48,3 | 0,302 |
| Revascularización completa | 62,0 | 58,6 | <0,001 |
| Tratamiento antiplaquetario doble (%) | 94,9 | 93,0 | <0,001 |
| Anticoagulantes orales (%) | 5,4 | 3,9 | <0,001 |
| Bloqueadores beta (%) | 86,0 | 64,8 | <0,001 |
| Estatinas (%) | 94,3 | 88,9 | <0,001 |
ARA-II: antagonistas del receptor de la angiotensina II; IECA: inhibidores de la enzima de conversión de la angiotensina.
Análisis para evaluar el impacto pronóstico de los inhibidores de la enzima de conversión de la angiotensina/bloqueadores del receptor de la angiotensina en la mortalidad a un año
| Población | Análisis | Casos completos | |
|---|---|---|---|
| Población total | |||
| Regresión de Cox | HR | IC95% | p |
| Univariante | 0,617 | 0,518-0,734 | <0,001 |
| Multivariable* | 0,762 | 0,633-0,917 | 0,004 |
| Ajustado por la PPI | 0,777 | 0,645-0,935 | 0,008 |
| Tras emparejar por puntuación de propensión | 0,713 | 0,572-0,888 | 0,004 |
| PPIA | Coeficiente | IC95% | p |
| Efecto promedio del tratamiento (diferencia de riesgo) | –0,008 | –0,015 a –0,001 | 0,034 |
| Variable instrumental | Coeficiente | IC95% | p |
| Reducción del riesgo relativo | –0,234 | –0,328 a –0,132 | 0,001 |
| Subgrupos por FEVI | |||
|---|---|---|---|
| FEVI ≤ 40 | |||
| Regresión de Cox | HR | IC95% | p |
| Univariante | 0,397 | 0,284-0,555 | <0,001 |
| Multivariable* | 0,620 | 0,428-0,899 | 0,012 |
| Ajustado por la PPI | 0,523 | 0,357-0,765 | 0,001 |
| Tras emparejar por puntuación de propensión | 0,417 | 0,262-0,665 | 0,001 |
| PPIA | Coeficiente | IC95% | p |
|---|---|---|---|
| Efecto promedio del tratamiento (diferencia de riesgo) | –0,026 | –0,055 a 0,005 | 0,076 |
| Variable instrumental | Coeficiente | IC95% | p |
|---|---|---|---|
| Reducción del riesgo relativo | –0,461 | –0,663 a –0,259 | <0,001 |
| Subgrupos por FEVI | |||
|---|---|---|---|
| FEVI> 40 | |||
| Regresión de Cox | HR | IC95% | p |
| Univariante | 0,677 | 0,549-0,833 | <0,001 |
| Multivariable* | 0,809 | 0,650-1,007 | 0,058 |
| Ajustado por la PPI | 0,876 | 0,703-1,092 | 0,239 |
| Tras emparejar por puntuación de propensión | 0,838 | 0,652-1,077 | 0,174 |
| PPIA | Coeficiente | IC95% | p |
|---|---|---|---|
| Efecto promedio del tratamiento (diferencia de riesgo) | –0,005 | –0,012 a 0,001 | 0,121 |
| Variable instrumental | Coeficiente | IC95% | p |
|---|---|---|---|
| Reducción del riesgo relativo | –0,157 | –0,264 a –0,049 | 0,004 |
FEVI: fracción de eyección del ventrículo izquierdo; HR: hazard ratio; IC95%: intervalo de confianza del 95%; PPI: ponderación de probabilidad inversa; PPIA: ponderación por la probabilidad inversa aumentada.
Ajustado por edad, sexo femenino, país, año, diabetes mellitus, hipertensión, dislipemia, arteriopatía periférica, infarto de miocardio previo, insuficiencia cardiaca previa, ictus previo, enfermedad maligna conocida, angina inestable, infarto agudo de miocardio con elevación del segmento ST, clase de Killip> II, fracción de eyección del ventrículo izquierdo, hemoglobina en el momento del ingreso, creatinina en el momento del ingreso, enfermedad coronaria multivaso, revascularización completa, tratamiento antiplaquetario doble, anticoagulantes orales, bloqueadores beta y estatinas.
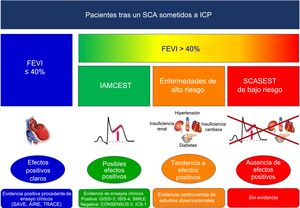
Población en estudio según la FEVI (> 40% o ≤ 40%), tipo de SCA (IAMCEST o SCASEST) y enfermedades de alto riesgo (insuficiencia cardiaca, insuficiencia renal, diabetes mellitus, hipertensión). FEVI: fracción de eyección del ventrículo izquierdo; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; SCA: síndrome coronario agudo; SCASEST: SCA sin elevación del segmento ST.
Los datos no disponibles se abordaron mediante múltiples asignaciones utilizando el método completo de especificación condicional (un algoritmo iterativo de Monte Carlo con cadenas de Markov), generando 10 conjuntos de datos asignados utilizando todas las variables de ajuste aplicables y todas las variables de resultado como factores de predicción (). El efecto del tratamiento con IECA/ARA-II en la mortalidad se computó por separado en los 10 conjuntos de datos asignados y a continuación se situó por encima de los conjuntos de datos utilizando las leyes de combinación de Rubin (análisis de conjuntos de datos asignados y ). Se realizaron varios análisis de sensibilidad (se proporcionan más detalles en las ).
RESULTADOSPrescripción de IECA/ARA-IISe prescribieron IECA/ARA-II al 75,2% (n=11.581) de los 15.401 pacientes. Se observaron diferencias significativas en las características iniciales entre los pacientes con y sin IECA/ARA-II (tabla 1). En particular, en los pacientes que recibieron IECA/ARA-II, el riesgo de isquemia tendía a ser más alto (DM, hipertensión y dislipemia) comparado con los que no los tomaban. En los pacientes tratados con IECA/ARA-II era peor la función renal, pero con valores de FEVI mayores, que en los pacientes no tratados con IECA/ARA-II, y el uso concomitante de TAPD, bloqueadores beta y estatinas fue más frecuente con la prescripción de IECA/ARA-II.
Efectos positivos de los IECA/ARA-II en el conjunto de la población con SCADe toda la cohorte (N=15.041), se produjeron 569 defunciones (3,7%) durante el primer año después del alta hospitalaria. La mortalidad a 1 año sin ajustar fue considerablemente inferior entre los pacientes que recibieron IECA/ARA-II que en los que no (el 3,2 frente al 5,1%; p <0,001). Tras la ponderación y el ajuste, utilizando el ajuste del análisis multivariable de Cox para las variables asociadas con la mortalidad en el análisis univariante (), así como para las técnicas de la puntuación de propensión (correspondencia de las puntuaciones de propensión, PPI y PPIA), el tratamiento con IECA/ARA-II siguió asociado con menor mortalidad a 1 año (tabla 2). Concretamente, se constató una diferencia significativa en el riesgo absoluto del 0,8% en la mortalidad al cabo de 1 año del alta hospitalaria entre los pacientes con y sin IECA/ARA-II, así como una reducción significativa del riesgo relativo de mortalidad a 1 año del 23,4%, según el ajuste de regresión de la PPIA y el análisis de la variable instrumental respectivamente (tabla 2).
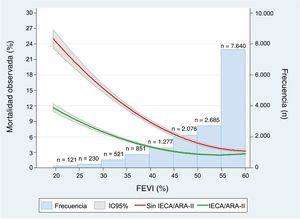
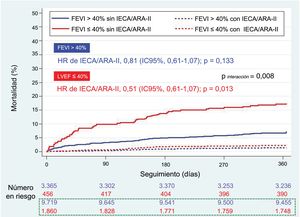
IECA/ARA-II en función de la FEVIDe los 2.316 pacientes (15,0%) con FEVI ≤ 40%, 1.861 (80,4%) fueron tratados con IECA/ARA-II. De los 13.085 pacientes (85,0%) con FEVI> 40%, 9.720 (74,3%) fueron tratados con IECA/ARA-II. La mortalidad a 1 año fue del 6,9% (n=161) y del 3,1% (n=409) de los pacientes con y sin FEVI ≤ 40% respectivamente. El tratamiento con IECA/ARA-II se asoció con una mayor reducción de la mortalidad con una FEVI inferior (figura 2). Los IECA/ARA-II se asociaron claramente con una menor mortalidad entre los pacientes con FEVI ≤ 40% tras ponderar y ajustar para los distintos métodos (tabla 2, figura 3), con una reducción de la mortalidad absoluta y relativa del 2,6% (para el efecto promedio del tratamiento según el ajuste de regresión de la PPIA, p = 0,076) y del 46,1% (para el análisis de la variable instrumental, p <0,001). En el caso de los pacientes con FEVI> 40%, el tratamiento con IECA/ARA-II no se asoció con una mortalidad inferior en los diversos análisis de Cox (tabla 2, figura 3) o con el ajuste de regresión de la PPIA (reducción del riesgo relativo del 0,5%; intervalo de confianza del 95% [IC95%], −1,2% a 0,1%). No obstante, el coeficiente del análisis de la variable instrumental mostró una reducción significativa del riesgo relativo del 15,7% (IC95%, −26,4% a −4,9%). El valor de p de la interacción para el tratamiento según la FEVI era significativo (0,008), lo que indica que el efecto clínico positivo de los IECA/ARA-II se concentra en los pacientes con FEVI ≤ 40%. Estos resultados (procedentes de la cohorte de datos imputados) concuerdan con los observados en la cohorte completa ().
Impacto no ajustado de los IECA o ARA-II al alta en la reducción de la mortalidad en función de la FEVI. ARA-II: antagonistas del receptor de la angiotensina II; FEVI: fracción de eyección del ventrículo izquierdo; IC95%: intervalo de confianza del 95%; IECA: inhibidores de la enzima de conversión de la angiotensina.
Curvas de Kaplan-Meier de supervivencia por prescripción de IECA o ARA-II al alta según la FEVI (> 40% o ≤ 40%). ARA-II: antagonistas del receptor de la angiotensina II; FEVI: fracción de eyección del ventrículo izquierdo; IC95%: intervalo de confianza del 95%; IECA: inhibidores de la enzima de conversión de la angiotensina. Número de pacientes en riesgo. En azul los pacientes con fracción de eyección del ventrículo izquierdo> 40% y en rojo los pacientes con fracción de eyección del ventrículo izquierdo ≤ 40%. En el recuadro de línea punteada verde, los pacientes tratados con IECA/ARA-II.
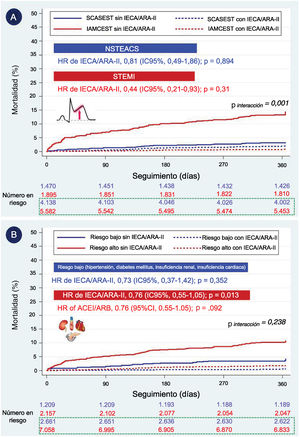
En el grupo de pacientes con FEVI> 40% (n=13.085), 7.477 (57,1%) padecían IAMCEST (figura 3). En estos pacientes con IAMCEST, un análisis específico y robusto de Cox, ajustado por la PPI y por las variables asociadas con la mortalidad en el análisis univariante, mostró una menor mortalidad a 1 año en los pacientes tratados con IECA/ARA-II frente a los no tratados con IECA/ARA-II (hazard ratio [HR] = 0,44; IC95%, 0,21-0,93; p = 0,031), lo cual no se observó en pacientes con SCA sin elevación del segmento ST (SCASEST) (figura 4A). El valor de p de la interacción para el tipo de tratamiento por SCA fue significativo (0,001), lo que indica que el efecto clínico positivo de los IECA/ARA-II en los pacientes con FEVI> 40% solo se observó en pacientes con IAMCEST (no en aquellos con SCASEST). Del número total de pacientes con FEVI> 40%, 1.678 (12,8%) tenían antecedentes de IC –definida como ingreso previo debido a IC o clase de Killip> I en el momento de ingresar por SCA, o IC de novo durante la hospitalización por SCA—, 1.991 (15,2%) padecían insuficiencia renal, definida como estimación de la tasa de filtrado glomerular mediante espectrometría de masas con dilución isotópica (isotope dilution mass spectrometry [IDMS]) —fórmula de la Modification of the Diet in Renal Disease (MDRD) <60ml/min/1,73 m2 en el momento del ingreso—, 3.011 (20,0%) padecían DM y 7.627 (50,6%), hipertensión arterial. Del subgrupo de pacientes con FEVI> 40%, 9.215 pacientes (61,1%) padecían por lo menos una de estas enfermedades de alto riesgo. En este grupo con alto riesgo, el tratamiento con IECA/ARA-II mostró una tendencia a una mortalidad a 1 año inferior (HR = 0,76; IC95%, 0,55-1,05; p = 0,092) en comparación con el grupo sin alto riesgo (figura 4B). No obstante, el valor de p de la interacción para las enfermedades de tratamiento por riesgo no fue significativo (0,238), lo que indica que no hay diferencias en el efecto clínico de los IECA/ARA-II en los pacientes con FEVI> 40% por la presencia o ausencia de enfermedades de alto riesgo. Las curvas de Kaplan-Meier ajustadas para cada una de las enfermedades de alto riesgo se muestran en las , junto con el análisis de casos completos ().
Curvas de Kaplan-Meier de supervivencia ajustadas por prescripción de IECA o ARA-II al alta a pacientes con FEVI> 40% según: A) presencia de IAMCEST o SCASEST; B) enfermedades de alto riesgo (insuficiencia cardiaca, insuficiencia renal, diabetes mellitus, hipertensión). ARA-II: antagonistas del receptor de la angiotensina II; FEVI: fracción de eyección del ventrículo izquierdo; HR: hazard ratio; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; IC95%: intervalo de confianza del 95%; IECA: inhibidores de la enzima de conversión de la angiotensina; SCASEST: síndrome coronario agudo sin elevación del segmento ST.
En este estudio, basado en un amplio registro internacional de pacientes con SCA que se someten a una ICP y son tratados conforme a las recomendaciones actuales de las directrices del SCA, se observa una asociación significativa del tratamiento con IECA/ARA-II con una menor mortalidad a 1 año. Esta asociación se concentra en los pacientes con FEVI ≤ 40% y con IAMCEST. Los IECA/ARA-II también mostraron una tendencia a asociarse con una menor mortalidad a 1 año en los pacientes con IC, insuficiencia renal, DM o hipertensión. En los pacientes con SCASEST sin estos factores de alto riesgo, se constató que no había asociación entre los IECA/ARA-II y menor mortalidad.
Los efectos positivos de los IECA/ARA-II en el contexto del SCA se han probado en la era de la trombolisis, con varios ensayos clínicos3,5,7 y metanálisis18 favorables. No obstante, hay 2 ensayos clínicos, el CONSENSUS II6 y el CCS-14, con una incidencia de trombolisis> 50%, en los que no se ha demostrado que tenga lugar una reducción significativa de la mortalidad a los 6 meses y a las 4 semanas respectivamente, ni tan siquiera en el infarto anterior. En la época actual de la ICP, hay varios estudios observacionales, con resultados controvertidos13–16,19–22. Una explicación posible de estos resultados discordantes radica en las distintas características basales de las poblaciones con SCA (p. ej., porcentaje de pacientes con FEVI ≤ 40%, IC, tipo de SCA, DM, hipertensión, enfermedad renal crónica), junto con diferencias en el tratamiento invasivo (incidencia de ICP) y farmacológico (TAPD, bloqueadores beta y estatinas). A este respecto, Gunnel et al.20 constataron que no se producía ninguna reducción de la mortalidad a largo plazo por añadir IECA/ARA-II al tratamiento clínico con bloqueadores beta y estatinas tras un infarto agudo de miocardio tratado con ICP. En la población del presente estudio, con todos los pacientes tratados con ICP y elevada incidencia de TAPD (> 90%), bloqueadores beta (> 80%) y estatinas (> 90%), se constató una asociación importante entre los IECA/ARA-II y la menor mortalidad a 1 año. No obstante, los resultados del estudio difieren en cuanto a la FEVI. En pacientes con FEVI ≤ 40%, se constató una notable reducción de la mortalidad a 1 año con IECA/ARA-II pero no en pacientes con FEVI> 40%.
En las guías para el SCA, los IECA/ARA-II se consideran un tratamiento obligatorio para los pacientes con FEVI ≤ 40%, con una recomendación de clase I y nivel de evidencia A, a no ser que esté contraindicado1,2. Esta recomendación se basa en 2 ensayos clínicos aleatorizados sobre pacientes con infarto de miocardio —los ensayos SAVE y TRACE8,9— en los que se aleatorizó a 2.231 y 1.749 pacientes con FEVI reducida (≤ 40% en el caso del ensayo SAVE y ≤ 35% en el TRACE) a un tratamiento con captopril o trandolapril, respectivamente, frente a placebo. La reducción del riesgo relativo de la mortalidad fue del 19% en el ensayo SAVE (seguimiento medio, 42 meses) y del 22% en el ensayo TRACE (seguimiento medio, 37 meses), y estos resultados son parecidos a los de los ensayos sobre IC con IECA/ARA-II y FEVI reducida, tales como los ensayos SOLVD y CHARM11,12. No obstante, en ambos el porcentaje de pacientes en tratamiento antiplaquetario fue <60% y el de los tratados con bloqueadores beta, <40%; faltaban datos sobre la prescripción de estatinas y se sometió a ICP a menos del 20% de los pacientes. Estos resultados extrapolan los efectos positivos observados en estos 2 ensayos desde la época de la trombolisis hasta la época contemporánea de la ICP, en una población tratada según las recomendaciones actuales.
En pacientes con FEVI> 40%, con los IECA/ARA-II no se observaron beneficios en general o consistentes. Aunque la mayor parte de los análisis ajustados no fueron significativos en esos pacientes, el análisis de la variable instrumental mostró un efecto positivo de los IECA/ARA-II. Esto indica que, en pacientes que han sufrido un SCA con FEVI> 40%, no está claro si los IECA/ARA-II tienen algún beneficio pronóstico en la reducción de la mortalidad o no. Dada la heterogeneidad de este grupo de pacientes, la prescripción debería individualizarse en función de las características de cada paciente. Cuando en el conjunto de los pacientes con SCA y FEVI> 40% se llevó a cabo un análisis de subgrupos, se observó una reducción significativa del riesgo de fallecer al cabo de 1 año en los pacientes con IAMCEST y una tendencia a una reducción de la mortalidad con IECA/ARA-II en los pacientes con alto riesgo (con IC, insuficiencia renal, DM o hipertensión). En lo que a los autores de este artículo concierne, no existen estudios específicos con muestras de mayor tamaño que analicen la función de los IECA/ARA-II en pacientes con SCA y FEVI> 40%, aparte de un estudio contemporáneo de pequeña escala16. Parashar et al.16 analizaron el impacto pronóstico de los IECA/ARA-II en pacientes tras un IAM, con FEVI> 40%, tratados con ICP y con una tasa de filtrado glomerular> 60ml/min/1,73 m2. Estos autores no hallaron ningún beneficio en la mortalidad a largo plazo por el hecho de utilizar IECA/ARA-II en pacientes sometidos a ICP primaria. En el contexto de la enfermedad coronaria estable con FEVI conservada, hay 3 ensayos clínicos con buena potencia estadística y resultados contradictorios23–25. El estudio HOPE mostró una reducción significativa de la mortalidad a 5 años con ramipril25. Se informó de resultados similares en el ensayo EUROPA con perindopril a 4 años23. En el ensayo PEACE24, se aleatorizó a 8.290 pacientes con enfermedad coronaria estable y FEVI normal o prácticamente normal a recibir trandolapril o placebo. El tratamiento con IECA no se asoció con una menor mortalidad a los 4,8 años. Para interpretar los hallazgos predominantemente negativos de este estudio en el contexto de los informes positivos de HOPE y EUROPA, es útil comparar las características del paciente y la incidencia de eventos en esos 2 ensayos con las del PEACE. Al inicio, los pacientes del ensayo PEACE tenían una FEVI media del 58%, y las concentraciones medias de creatinina y colesterol eran normales24. La presión arterial media inicial era 133/78mmHg, lo cual correspondía al nivel alcanzado con un IECA en ambos ensayos HOPE y EUROPA23,25. Los pacientes del ensayo PEACE también recibieron más tratamiento intensivo contra el factor de riesgo que los de los ensayos HOPE y EUROPA. Al inicio, el 70% de los pacientes (comparado con el 29% en el ensayo HOPE y el 56% en el EUROPA) recibía tratamiento hipolipemiante. Además, el 72% de los pacientes del ensayo PEACE, comparado con el 54% de los pacientes del ensayo EUROPA y el 40% de los del HOPE, se habían sometido a revascularización coronaria antes de formar parte del estudio23–25. Parece razonable que esta estrategia más agresiva pudiera haber contribuido a disminuir el riesgo de eventos adversos en el ensayo PEACE. En consecuencia, no es ninguna sorpresa que con un tratamiento más intensivo de la enfermedad coronaria y con una modificación del factor de riesgo, los resultados cardiovasculares adversos en los pacientes asignados a placebo fueran sustancialmente menores en el ensayo PEACE que en los otros dos.
La guía europea sobre SCA recomienda (también como recomendación de clase I y nivel de evidencia) los IECA/ARA-II, incluso si la FEVI es> 40%, para los pacientes con un SCA y DM, IC e hipertensión1,2, y la estadounidense amplía esta recomendación a los pacientes con enfermedad renal crónica estable. La recomendación de IECA/ARA-II para los pacientes con IAMCEST se basa en 3 ensayos clínicos (GISSI-3 para lisinopril, ISIS-4 para captopril y SMILE-1 para zofenopril3,5,7) que mostraron una reducción significativa de la mortalidad a 6 semanas (5 semanas en el ISIS-4) con IECA en pacientes con IAM (con o sin FEVI> 40%). No obstante, en estos ensayos, no se constató ningún uso sistemático de la ICP (0% en el ensayo SMILE; no se dio información al respecto en los ensayos GISSI-3 o ISIS-4; con> 70% de trombolisis en ambos), con una incidencia muy baja de uso de bloqueadores beta (< 30%) y estatinas (< 10%)3,5,7. De un modo parecido al ensayo PEACE, los resultados del presente estudio no respaldan el uso generalizado de los IECA/ARA-II en los pacientes con SCA y FEVI> 40%. Sin embargo, sí se ha notificado de manera específica un efecto positivo en los pacientes con IAMCEST y FEVI> 40%, así como un posible efecto positivo en los pacientes con alto riesgo y FEVI> 40%. En los pacientes con bajo riesgo, SCASEST y FEVI> 40%, no se observó beneficio alguno con los IECA/ARA-II en la reducción de la mortalidad a 1 año. Aun así, la mayoría de los médicos de todo el mundo siguen prescribiendo IECA/ARA-II a todos los pacientes con SCA, a menudo debido a una tendencia al optimismo terapéutico. Según los resultados del presente estudio y de estudios previos contradictorios, se cree que los pacientes con SCA y FEVI ≥ 40% sin enfermedades de alto riesgo (IAMCEST, IC, DM, hipertensión o enfermedad renal) representan un contexto clínico interesante para un ensayo clínico aleatorizado según las recomendaciones actuales relativas al tratamiento del SCA (figura 5).
Evidencia de IECA o ARA-II tras un SCA en pacientes sometidos a ICP. ARA-II: antagonistas del receptor de la angiotensina II; FEVI: fracción de eyección del ventrículo izquierdo; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; ICP: intervención coronaria percutánea; IECA: inhibidores de la enzima de conversión de la angiotensina; SCA: síndrome coronario agudo; SCASEST: síndrome coronario agudo sin elevación del segmento ST.
Este estudio tiene algunas limitaciones. En primer lugar, solo se estudió a los pacientes que sobrevivieron al ingreso hospitalario, por lo que no se investigó qué papel desempeñaron los IECA/ARA-II durante la hospitalización. En la era de la trombolisis, varios investigadores han puesto de relieve que el beneficio de los IECA/ARA-II tiene lugar durante los primeros días tras sufrir el SCA, lo que indica que otros mecanismos aparte de los efectos positivos en el proceso de remodelación pueden desempeñar un papel importante3,5,7. En segundo lugar, los beneficios de los IECA/ARA-II en supervivencia se compararon en función de la medicación prescrita en el momento del alta. Asimismo, la dosis de la prescripción, la continuidad en el cumplimiento, si se produjo interrupción del tratamiento, la incidencia de efectos adversos y la información relativa al fármaco tras el alta no estaban disponibles en el presente estudio. Además, se carece de datos sobre el uso de IECA/ARA-II antes del ingreso hospitalario. En tercer lugar, no se diferenció entre IECA y ARA-II. Aunque diversos autores han puesto de relieve que tanto los IECA como los ARA-II tienen un mismo efecto positivo, según otros autores hay diferencias notables entre los 2 fármacos26,27, lo que pone de relieve que la tolerancia y la adherencia prolongada al tratamiento28 varían. En cuarto lugar, el presente estudio incluyó una muestra seleccionada y no aleatorizada; asimismo, aunque la puntuación de propensión y el análisis de la variable instrumental se ajustaron por indicación para explicar los factores de confusión, y se realizaron otros ajustes para explicar muchos otros factores de confusión en los modelos de supervivencia, la confusión residual es probable.
CONCLUSIONESEl efecto positivo de los IECA/ARA-II en pacientes que han sufrido un SCA se centra en aquellos con FEVI ≤ 40% y IAMCEST. En cuanto a los pacientes con infarto agudo de miocardio sin elevación del segmento ST (IAMSEST) y FEVI> 40%, se requieren otros estudios contemporáneos para evaluar el impacto a largo plazo de los IECA o los ARA-II en la era actual de la ICP, así como de otros fármacos cardiovasculares recomendados por las guías.
CONFLICTO DE INTERESESNo se declara ninguno.
- –
Los IECA y los ARA-II contribuyen positivamente a reducir la mortalidad después de un SCA en pacientes con FEVI ≤ 40%. Aun así, los beneficios de estos 2 tratamientos en pacientes con SCA y FEVI> 40% sometidos a revascularización coronaria percutánea no se ha probado en ensayos clínicos. Sin embargo, siguen estando recomendados por las guías de práctica clínica para los pacientes con hipertensión, diabetes o disfunción renal.
- –
Tras un SCA tratado con intervención coronaria percutánea, los IECA/ARA-II redujeron la mortalidad entre los pacientes con FEVI ≤ 40%.
- –
En pacientes con SCA y FEVI> 40%, el efecto positivo de los IECA se limitó a los pacientes con IAMCEST.
- –
En el SCASEST con FEVI> 40%, los IECA/ARA-II podrían ser beneficiosos para los pacientes con hipertensión, diabetes, enfermedad renal crónica o IC.
- –
Se requieren otros estudios contemporáneos para evaluar el impacto a largo plazo de los IECA y los ARA-II en la moderna era de la revascularización coronaria percutánea.