Las medidas preoperatorias destinadas a alcanzar un equilibrio correcto entre el flujo pulmonar y el flujo sistémico son de capital importancia en la estabilización preoperatoria de los pacientes con una fisiología de ventrículo único (VU) y en las cardiopatías congénitas con circulación pulmonar o sistémica dependiente del conducto. La caída fisiológica de las resistencias vasculares pulmonares (RVP) que se observa tras el nacimiento conduce a una sobrecirculación pulmonar y a una hipoperfusión sistémica, con aumento del riesgo de edema pulmonar, enterocolitis necrosante1 e ictus cerebral2.
El tratamiento mediante inhalación de nitrógeno reduce la fracción de oxígeno en el aire inspirado e induce una vasoconstricción vascular hipóxica y, por consiguiente, la RVP, con lo que se evita la sobrecirculación pulmonar3 y se mejora el gasto cardiaco y el aporte de sangre al cerebro4. No obstante, el uso de tratamiento con nitrógeno continúa siendo objeto de controversia. Además, no hay ningún estudio que haya evaluado el efecto directo de la inhalación de nitrógeno en la reducción de la sobrecirculación pulmonar.
La ecografía pulmonar (LUS) ha resultado útil para el seguimiento del edema pulmonar en los recién nacidos y niños con cardiopatías congénitas5,6.
Se presenta la experiencia de nuestro centro en el tratamiento de los pacientes con una combinación de reducción de la poscarga y tratamiento inhalado subatmosférico. Se incluyó a los pacientes con fisiología de VU y circulación sistémica dependiente del conducto ingresados en nuestro centro entre 2016 y 2018.
Tras una estabilización apropiada en la sala de partos y a la llegada a la unidad de cuidados intensivos neonatales, se inició una infusión de prostaglandina, infusión de milrinona y tratamiento subatmosférico. La infusión de prostaglandina se comenzó con 0,01 [intervalo intercuartílico, 0,005-0,02] μg/kg/min y la de milrinona a una dosis de entre 0,15 y 1 μg/kg/min. El tratamiento subatmosférico se instauró con la adición de nitrógeno, estableciendo como objetivo una fracción de oxígeno inhalado del 15 al 20%, a través de una cánula nasal de alto flujo o una ventilación no invasiva, en función del estado del paciente.
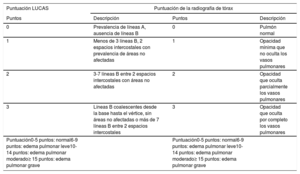
Se evaluó la sobrecirculación pulmonar con la puntuación LUCAS (Lung Ultrasonography in CArdiac Surgery), una puntuación de LUS creada por nuestro grupo (tabla 1). Se estudiaron 6 cortes en cada paciente. Las exploraciones de LUS se realizaron antes del bypass cardiopulmonar y después de este, al cabo de 12, 24, 36, 48 y 72 h. Se comparó esta puntuación con una puntuación de la radiografía de tórax (tabla 1). La radiografía de tórax se realizó en todos los pacientes antes de la intervención quirúrgica e inmediatamente después de ella.
Puntuación LUCAS y puntuación de la radiografía de tórax
| Puntuación LUCAS | Puntuación de la radiografía de tórax | ||
|---|---|---|---|
| Puntos | Descripción | Puntos | Descripción |
| 0 | Prevalencia de líneas A, ausencia de líneas B | 0 | Pulmón normal |
| 1 | Menos de 3 líneas B, 2 espacios intercostales con prevalencia de áreas no afectadas | 1 | Opacidad mínima que no oculta los vasos pulmonares |
| 2 | 3-7 líneas B entre 2 espacios intercostales con áreas no afectadas | 2 | Opacidad que oculta parcialmente los vasos pulmonares |
| 3 | Líneas B coalescentes desde la base hasta el vértice, sin áreas no afectadas o más de 7 líneas B entre 2 espacios intercostales | 3 | Opacidad que oculta por completo los vasos pulmonares |
| Puntuación0-5 puntos: normal6-9 puntos: edema pulmonar leve10-14 puntos: edema pulmonar moderado≥ 15 puntos: edema pulmonar grave | Puntuación0-5 puntos: normal6-9 puntos: edema pulmonar leve10-14 puntos: edema pulmonar moderado≥ 15 puntos: edema pulmonar grave | ||
LUCAS: Lung Ultrasonography CArdiac Surgery.
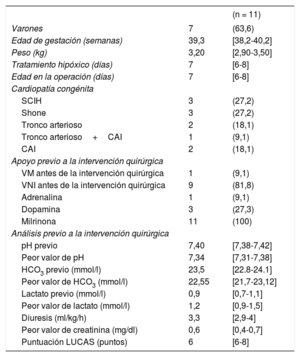
La determinación del gasto cardiaco sistémico se basó en los análisis de gasometría arterial, la diuresis, la creatinina sérica, la necesidad de apoyo inotrópico (excluida la milrinona) y la presencia de enterocolitis necrosante o ictus cerebral (tabla 2).
Datos descriptivos de los pacientes antes de la operación
| (n = 11) | ||
|---|---|---|
| Varones | 7 | (63,6) |
| Edad de gestación (semanas) | 39,3 | [38,2-40,2] |
| Peso (kg) | 3,20 | [2,90-3,50] |
| Tratamiento hipóxico (días) | 7 | [6-8] |
| Edad en la operación (días) | 7 | [6-8] |
| Cardiopatía congénita | ||
| SCIH | 3 | (27,2) |
| Shone | 3 | (27,2) |
| Tronco arterioso | 2 | (18,1) |
| Tronco arterioso+CAI | 1 | (9,1) |
| CAI | 2 | (18,1) |
| Apoyo previo a la intervención quirúrgica | ||
| VM antes de la intervención quirúrgica | 1 | (9,1) |
| VNI antes de la intervención quirúrgica | 9 | (81,8) |
| Adrenalina | 1 | (9,1) |
| Dopamina | 3 | (27,3) |
| Milrinona | 11 | (100) |
| Análisis previo a la intervención quirúrgica | ||
| pH previo | 7,40 | [7,38-7,42] |
| Peor valor de pH | 7,34 | [7,31-7,38] |
| HCO3 previo (mmol/l) | 23,5 | [22.8-24.1] |
| Peor valor de HCO3 (mmol/l) | 22,55 | [21,7-23,12] |
| Lactato previo (mmol/l) | 0,9 | [0,7-1,1] |
| Peor valor de lactato (mmol/l) | 1,2 | [0,9-1,5] |
| Diuresis (ml/kg/h) | 3,3 | [2,9-4] |
| Peor valor de creatinina (mg/dl) | 0,6 | [0,4-0,7] |
| Puntuación LUCAS (puntos) | 6 | [6-8] |
CAI: cayado aórtico interrumpido; HCO3: bicarbonato; LUCAS: Lung Ultrasonography CArdiac Surgery; SCIH: síndrome de corazón izquierdo hipoplásico; VM: ventilación mecánica; VNI: ventilación no invasiva.
Las variables cualitativas se expresan en forma de frecuencia (%) y las variables cuantitativas, en forma de mediana [intervalo intercuartílico].
Se incluyó en esta muestra a 11 pacientes consecutivos. Los datos principales se muestran en la tabla 2.
No hubo correlación alguna entre la puntuación de la LUS y la radiografía de tórax antes de la intervención quirúrgica (p = 0,57) ni después (p = 0,62).
Los análisis de sangre se evaluaron según el peor resultado previo a la operación (tabla 2). Antes de la intervención quirúrgica, todos los pacientes mantuvieron un gasto cardiaco sistémico, una diuresis y unas concentraciones de creatinina adecuados. No hubo ningún episodio de enterocolitis necrosante.
La evaluación de la sobrecirculación pulmonar mediante la LUS mostró valores bajos y tan solo 1 paciente necesitó ventilación mecánica antes de la operación.
Por lo que respecta a los resultados, la duración de la ventilación mecánica tras la cirugía fue de 3 [3-5] días. Sufrió ictus cerebral 1 paciente (9,1%). La mortalidad total tras la operación fue inexistente.
Se observó una estrecha correlación entre la puntuación inotrópica y la puntuación LUCAS (p ≤ 0,05 en todos los momentos de evaluación). Una puntuación LUCAS más alta estaba correlacionada con una mayor medicación inotrópica.
Los análisis de sangre no mostraron diferencias en la presión parcial de oxígeno (PaO2) ni la presión parcial de dióxido de carbono (PaCO2) en los pacientes con una puntuación LUCAS más alta o más baja (p > 0,05)
En los pacientes con fisiología de VU, el cociente de flujo sanguíneo pulmonar/sistémico depende directamente del cociente existente entre las resistencias vasculares. Inmediatamente después del nacimiento, los recién nacidos con fisiología de VU se mantienen bien equilibrados, ya que la circulación continúa como en la vida fetal, con unas RVP elevadas y una resistencia vascular sistémica baja. Este equilibrio se ve alterado por la caída fisiológica de las RVP que se produce tras los primeros días de vida. Se han evaluado varias estrategias para evitar la sobrecirculación pulmonar y la hipoperfusión sistémica, como la acidosis leve permisiva, la hipoventilación, la hipercapnia terapéutica y el tratamiento con gas subatmosférico.
Dado que el flujo sanguíneo sigue el camino de menor resistencia, es extraordinariamente importante reducir la resistencia vascular sistémica para evitar la hipoperfusión sistémica. El uso rápido de milrinona y del tratamiento subatmosférico podría desempeñar un papel importante para equilibrarla.
La determinación del gasto cardiaco y la sobrecirculación pulmonar en los pacientes con VU resulta difícil, y los dispositivos de monitorización invasivos son también difíciles de utilizar. En nuestro estudio se observa que la LUS es una buena herramienta no invasiva para la supervisión de la sobrecirculación pulmonar. A medida que se produce el edema pulmonar, los signos que aparecen normalmente en la LUS consisten en líneas A que cambian luego a múltiples líneas B, que luego evolucionarán hacia líneas B coalescentes6. En estudios previos realizados en niños5,6, la LUS ha resultado útil para el seguimiento del edema pulmonar.
El uso de sistemas de monitorización invasivos y de muestras para analítica frecuentes, que incluyan la saturación de la sangre venosa mixta, el lactato y el equilibrio acidobásico, son los métodos invasivos comúnmente utilizados para evaluar el gasto cardiaco y la idoneidad de la utilización del oxígeno. Según los resultados obtenidos de la clínica y las analíticas en nuestra serie, los pacientes con una puntuación LUCAS más baja alcanzaron un mejor aporte de oxígeno sistémico. En nuestra muestra, en los pacientes con puntuaciones LUCAS superiores, se aumentó el tratamiento diurético para facilitar la reducción de la sobrecarga pulmonar. La necesidad de una ventilación mecánica preoperatoria se asocia con peor resultado clínico general. En nuestra muestra, tan solo 1 paciente (1/11) necesitó ventilación mecánica a causa de una inestabilidad hemodinámica debida a una taquicardia supraventricular.
En nuestra población de pacientes, no se observó relación entre la PaO2 o la PaCO2 y los valores de la puntuación LUCAS. Una explicación plausible es que la fisiología de VU de la cardiopatía subyacente pudiera haber actuado como factor de confusión.
En conclusión, en el presente estudio se demuestra que la combinación de un tratamiento subatmosférico con el empleo de nitrógeno y el uso de un tratamiento vasodilatador sistémico con milrinona constituye una estrategia segura y eficaz para equilibrar la circulación en los pacientes con fisiología de VU o una circulación sistémica dependiente del conducto.