En el síndrome coronario agudo sin elevación del segmento ST de riesgo intermedio o alto, las guías de actuación clínica recomiendan la realización de coronariografía con intención de revascularizar. Sin embargo, para los pacientes muy ancianos la evidencia que avala esta recomendación es muy escasa.
MétodosAnalizamos retrospectivamente a todos los pacientes con síndrome coronario agudo sin elevación del segmento ST y edad ≥ 85 años ingresados en un único centro entre 2004 y 2009. Mediante propensity score, emparejamos 1:1 a los pacientes con abordaje intervencionista con aquellos en que se decidió manejo conservador. Se comparó la supervivencia y la supervivencia libre de eventos isquémicos.
ResultadosSe incluyó a 228 pacientes consecutivos (media de edad 88 [intervalo, 85-101] años). Se decidió abordaje intervencionista en 100 pacientes (128 con manejo conservador). Los enviados a abordaje intervencionista eran más jóvenes y más frecuentemente varones y tenían menos comorbilidad, menos demencia y menos frecuentemente elevación de troponina. Se emparejó a 63 pacientes del grupo de abordaje intervencionista con 63 del grupo de manejo conservador mediante propensity score.
En el seguimiento a 3 años de los pacientes emparejados, el grupo de abordaje intervencionista presentó mayor supervivencia (log rank test=4,24; p=0,039) y mayor supervivencia libre de eventos isquémicos (log rank test=8,63; p=0,003). En la población total, ajustando por quintiles de propensity score, el abordaje intervencionista se relacionó con mayor supervivencia (hazard ratio=0,52; intervalo de confianza del 95%, 0,32-0,85) y mayor supervivencia libre de eventos isquémicos (hazard ratio=0,48; intervalo de confianza del 95%, 0,32-0,74).
ConclusionesCasi todos los pacientes muy ancianos ingresados por síndrome coronario agudo sin elevación del segmento ST están en riesgo intermedio-alto. En estos pacientes, el abordaje intervencionista se relaciona con mayor supervivencia y mayor supervivencia libre de eventos isquémicos.
Palabras clave
La incidencia de cardiopatía isquémica aumenta con la edad y, dado que en la última década se ha producido un envejecimiento progresivo de la población1, los pacientes ancianos representan un porcentaje cada vez mayor de las hospitalizaciones por síndrome coronario agudo. Según el registro GRACE (Global Registry of Acute Coronary Events), se estima que cerca del 20% de pacientes que sufren un evento coronario agudo tienen más de 75 años y un 6% tiene más de 85 años2. Esta prevalencia contrasta con la baja representación de estos pacientes en los ensayos clínicos. Sólo un 9% de los pacientes incluidos en los ensayos clínicos realizados entre los años 1991 y 2000 tenían más de 75 años3.
Los pacientes que se incluye en los ensayos clínicos están altamente seleccionados debido a los estrictos criterios de inclusión4, y los registros también pueden seleccionar a pacientes de menor riesgo y con menos comorbilidad que en la vida real5. Por lo tanto, la aplicabilidad de los resultados de los ensayos clínicos e incluso de los registros puede ser escasa en la práctica clínica en los pacientes muy ancianos y comórbidos.
Las guías de la Sociedad Europea de Cardiología6 hacen hincapié en la estratificación de riesgo para la toma de decisiones terapéuticas. Para los pacientes con riesgo moderado-alto, se recomienda realización sistemática de coronariografía, y para los que tienen riesgo bajo, solamente en caso de isquemia recurrente o test de isquemia positivo. La infrautilización del intervencionismo en los pacientes en alto riesgo se ha asociado a un peor pronóstico en nuestro medio7. En este sentido, el subgrupo de pacientes muy ancianos es el que presenta más riesgo y mortalidad8, por lo que son los que más se pueden beneficiar de dicha terapia. Sin embargo, son precisamente estos pacientes los que presentan mayor riesgo de sufrir complicaciones en los procedimientos invasivos. Esto puede contribuir a que en la práctica clínica diaria su manejo sea menos agresivo y se beneficien en menor medida de los tratamientos recomendados por las guías, incluida la realización de coronariografía9, 10.
Hay pocos datos comparativos y no existen estudios aleatorizados acerca del tratamiento del síndrome coronario agudo sin elevación del segmento ST (SCASEST) en los pacientes muy ancianos. Nuestro objetivo es evaluar si el abordaje intervencionista (AI), que definimos como realización de coronariografía durante el ingreso con intención de revascularizar, es mejor que el manejo conservador (MC) en estos pacientes, analizando las complicaciones durante la hospitalización y el pronóstico a medio plazo.
MÉTODOSSe llevó a cabo un análisis retrospectivo de los pacientes ingresados consecutivamente entre el 1 de enero de 2004 y el 31 de diciembre de 2009 con el diagnóstico de SCASEST, con una edad ≥ 85 años. El estudio se realizó en un único hospital con laboratorio de hemodinámica.
Incluimos a todos los pacientes hospitalizados con diagnóstico de SCASEST: dolor torácico de características isquémicas y carácter inestable (en reposo, de esfuerzo de nueva aparición en el último mes o disminución del umbral en el último mes), acompañado o no de elevación de marcadores de daño miocárdico y cambios en el electrocardiograma (ECG) diferentes de la elevación persistente del segmento ST o bloqueo de rama izquierda de nueva aparición.
Se llevó a cabo una revisión de las historias clínicas y las bases de datos electrónicas hospitalarias. Se generó una base de datos con más de 200 variables referentes a características demográficas, antecedentes personales, características clínicas, exploración física, valores analíticos, características del ECG y del manejo terapéutico. De los pacientes que fueron sometidos a intervencionismo, se registraron variables angiográficas y características del procedimiento.
Se calculó el índice de comorbilidad de Charlson sin edad11 en el momento del ingreso, usando el punto de corte > 3 puntos para definir un nivel alto de comorbilidad.
Se estratificó el riesgo de todos los pacientes mediante el score de riesgo GRACE en el momento del ingreso, según la recomendación de las guías de la Sociedad Europea de Cardiología6, 12. Se utilizó el punto de corte de más de 109 puntos para definir riesgo intermedio y más de 140 puntos para definir riesgo alto6, 12.
Se registraron las complicaciones ocurridas durante la hospitalización: insuficiencia renal, hemorragias TIMI o necesidad de transfusión, ocurrencia de nuevo infarto de miocardio, accidentes isquémicos cerebrales o muerte.
DefinicionesSe definió éxito en el procedimiento como un resultado final con la arteria tratada abierta, con estenosis residual < 50% y con flujo final TIMI III, en ausencia de complicaciones (disección o perforación coronaria).
La función renal se calculó mediante la estimación del filtrado glomerular renal con la fórmula de MDRD (Modification of Diet in Renal Disease)13. Se definió deterioro de la función renal al alta como un empeoramiento del valor de creatinina > 0,5g/dl respecto al valor del ingreso.
Se definió como isquemia recurrente la recurrencia del dolor anginoso durante la hospitalización aunque no se demostraran cambios eléctricos o reelevación de troponina.
Se consideraron las hemorragias TIMI según lo definido previamente14, como hemorragia mayor a cualquier hemorragia intracraneal o hemorragia clínica que se acompaña de un descenso del valor de hemoglobina ≥ 5g/dl, y hemorragia menor, la hemorragia clínica que se acompaña de un descenso del valor de hemoglobina entre 3 y 5g/dl. Se registró asimismo la necesidad de transfusión de algún concentrado de hematíes durante la hospitalización.
Se definió como infarto de miocardio la nueva elevación de troponina asociada a un nuevo episodio clínico, y como ictus un nuevo déficit neurológico acompañado de prueba de imagen compatible (tomografía computarizada o resonancia magnética).
Todos los seguimientos se llevaron a cabo en octubre de 2010, mediante revisión de historias clínicas, bases de datos hospitalarias y contacto telefónico. Se definió como evento la combinación de muerte por cualquier causa o evento cardiovascular adverso mayor (ECAM): reingreso por nuevo síndrome coronario agudo, necesidad de nueva revascularización o ictus durante el seguimiento. Se registraron también los reingresos por insuficiencia cardiaca o hemorragia.
Análisis estadísticoLas variables cuantitativas se expresan como media±desviación estándar; se utilizó el test de la t de Student para la comparación entre los dos grupos. Las cualitativas se expresan como porcentaje y se compararon mediante el test de la χ2 o el test exacto de Fisher si el valor esperado en alguna casilla era < 5.
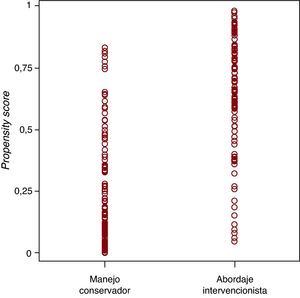
Dado que los pacientes de nuestro estudio no fueron aleatorizados, esperamos un sesgo significativo entre ambos grupos. Para minimizar este sesgo utilizamos la metodología del propensity score (PS)15. Construimos un modelo de regresión logística no parsimonioso en el que la variable dependiente fue la realización de cateterismo cardiaco durante el ingreso y como variables independientes introdujimos las que presentaron diferencias significativas en el análisis univariable y varias comorbilidades que se relacionan con la mortalidad. Las covariables introducidas en el modelo fueron: edad, sexo, dislipemia, infarto previo, hemoglobina, valvulopatía significativa conocida, recurrencia de angina, ictus previo, arteriopatía periférica, demencia, insuficiencia renal, índice de comorbilidad de Charlson, troponina I positiva y el score GRACE. El modelo construido presentó buena discriminación entre ambos grupos, con un estadístico c de 0,854 (intervalo de confianza [IC] del 95%, 0,804-0,903). La distribución del PS en cada grupo se muestra en la Figura 1.
Figura 1. Distribución del propensity score según grupo de tratamiento. Grupo manejo conservador: mediana, 0,18 [0,076-0,476]. Grupo abordaje intervencionista: mediana, 0,68 [0,51-0,84].
Utilizamos la probabilidad estimada por el modelo de recibir AI de dos maneras:
• En primer lugar emparejamos a los pacientes de ambos grupos 1:1 sin reemplazamiento, en función de dicha probabilidad. La condición para cada pareja fue que la diferencia entre las probabilidades estimadas por el modelo fuese menor del 20% de la desviación estándar de las probabilidades. En nuestra serie la desviación estándar de las probabilidades fue 0,3 (20%=0,06)16.
Para valorar si el emparejamiento equilibraba las características basales entre los dos grupos usamos la diferencia estandarizada17 (Tabla 1). Valores absolutos pequeños (≤10%) respaldan el supuesto de equilibrio entre ambos grupos18.
Tabla 1. Características de la población basal y tras emparejamiento en el grupo de manejo conservador y abordaje intervencionista
Población total Población emparejada MC (N=128) AI (N=100) p MC (N=63) AI (N=63) Diferencia estandarizada, % Edad (años) 89±3,4 87±2,4 < 0,001 87,4±2,5 87,3±2,8 3,8 Edad > 90 años 50/128 (39,1) 11/100 (11) < 0,001 10/63 (15,9) 10/63 (15,9) 0 Mujeres 85/128 (66,4) 46/100 (46) 0,002 34/63 (54) 36/63 (57,1) 6,2 Factores de riesgo cardiovascular Hipertensión 95/128 (74,2) 79/100 (79) 0,69 48/63 (76,2) 49/63 (77,8) 3,8 Diabetes mellitus 35/128 (27,3) 25/100 (25) 0,39 19/63 (30,2) 20/63 (31,7) 3,2 Dislipemia 40/128 (31,2) 48/100 (48) 0,01 24/63 (38,1) 26/63 (41,3) 6,5 Tabaquismo activo 2/128 (1,6) 1/100 (1) 0,71 2/63 (3,2) 1/63 (1,6) 10 > 2 FRCV 16/128 (12,5) 14/100 (14) 0,74 10/63 (15,9) 10/63 (15,9) 0 Historia cardiovascular IAM previo 31/128 (24,2) 38/100 (38) 0,02 20/63 (31,7) 22/63 (34,9) 6,8 ICP previo 6/128 (4,7) 13/100 (13) 0,02 6/63 (9,5) 7/63 (11,1) 5,3 CRC previa 3/128 (2,3) 5/100 (5) 0,27 2/63 (3,2) 2/63 (3,2) 0 ICC previa 28/128 (21,9) 13/100 (13) 0,08 11/63 (17,5) 11/63 (17,5) 0 FA/flutter previos 34/128 (26,6) 16/100 (16) 0,05 8/63 (12,7) 7/63 (11,1) 4,9 Ictus previo 18/128 (14,1) 16/100 (16) 0,68 7/63 (11,1) 9/63 (14,3) 9,6 Arteriopatía periférica 12/128 (9,4) 13/100 (13) 0,38 8/63 (12,7) 9/63 (14,3) 4,7 Comorbilidad EPOC 19/128 (14,8) 10/100 (10) 0,27 8/63 (12,7) 8/63 (12,7) 0 Demencia 21/128 (16,4) 4/100 (4) 0,003 5/63 (7,9) 4/63 (6,3) 6,2 IRC 24/128 (18,8) 24/100 (24) 0,33 11/63 (17,5) 11/63 (17,5) 0 Cáncer 26/128 (20,3) 16/100 (16) 0,41 12/63 (19) 11/63 (17,5) 3,9 Hemiplejia 6/128 (4,7) 4/100 (4) 0,81 1/63 (1,6) 2/63 (3,2) 10 Depresión tratada 10/114 (8,8) 8/95 (8,4) 0,92 4/58 (6,9) 6/61 (9,8) 10 Índice Charlson 3,3±2 2,8±1,9 0,1 2,97±1,98 3,06±2,04 4 Índice Charlson > 3 56/128 (43,8) 27/100 (27) 0,009 23/63 (36,5) 22/63 (34,9) 3,3 Características al ingreso Recurrencia de isquemia 28/128 (21,9) 41/100 (41) 0,002 14/63 (22,2) 16/63 (25,4) 7,5 Troponina I positiva 111/128 (86,7) 71/100 (71) 0,001 52/63 (82,5) 50/63 (79,4) 7,9 Descenso de ST 48/128 (37,5) 40/94 (42,6) 0,37 26/63 (41,3) 22/60 (36,7) 9,4 Clase Killip > 1 66/128 (51,6) 29/98 (29,6) < 0,001 21/63 (33,3) 22/62 (35,5) 4,8 AAS previo 53/127 (41,7) 50/96 (52,1) 0,127 32/62 (51,6) 30/61 (49,2) 5 Creatinina 1,48±0,67 1,37±0,49 0,24 1,34±0,49 1,30±0,43 8,6 Aclaramiento de creatinina (MDRD) (mg/dl/1,73 m2) 46,7±19,4 51,2±17,7 0,12 52,6±19,2 51,6±15,9 5,9 Hb (mg/dl) 12±1,8 12,1±1,9 0,48 12,11±2,11 12,18±1,69 3,7 FEVI 53±11 52±10,5 0,57 54±10,6 53±10,1 9,6 FEVI < 35% 9/100 (9) 8/89 (9) 0,99 4/53 (7,5) 3/58 (5,2) 9,4 Valvulpatía (≥ 3+) 47/100 (47) 29/89 (32,6) 0,04 16/53 (30,2) 18/58 (31) 1,7 Estenosis aórtica (≥ 3+) 26/100 (26) 15/89 (16,9) 0,13 9/53 (17) 12/58 (20,7) 9,5 GRACE moderado riesgo 18/128 (14,1) 16/100 (16) 0,68 11/63 (17,5) 11/63 (17,5) 0 GRACE alto riesgo 110/128 (85,9) 79/100 (79) 0,17 52/63 (82,5) 50/63 (79,4) 7,9 AAS: ácido acetilsalicílico; AI: abordaje intervencionista; CRC: cirugía de revascularización coronaria; EPOC: enfermedad pulmonar obstructiva crónica; FA: fibrilación auricular; FEVI: fracción de eyección del ventrículo izquierdo; Hb: hemoglobina; FRCV: factor de riesgo cardiovascular; GRACE: Global Registry of Acute Coronary Events; IAM: infarto agudo de miocardio; ICC: insuficiencia cardiaca congestiva; ICP: intervencionismo coronario percutáneo; IRC: insuficiencia renal crónica; MC: manejo conservador; MDRD: Modification of Diet in Renal Disease.
Los resultados se muestran como media±desviación estándar o n/N (%).La supervivencia fue analizada mediante el método de Kaplan-Meier, usando el log rank test para la comparación entre ambos grupos.
• En segundo lugar, clasificamos a todos los pacientes en quintiles en función de la probabilidad pronosticada por el modelo. Calculamos las hazard ratio (HR) de los eventos en el seguimiento mediante la regresión de Cox ajustando por los quintiles de PS. Calculamos también las HR ajustando por los años de ingreso (2004-2006 frente a 2007-2009).
Se consideró un resultado estadísticamente significativo si p<0,05. Para el análisis estadístico se utilizó el programa SPSS versión 15.0 para Windows (SPSS Inc.; Chicago, Illinois, Estados Unidos).
RESULTADOSEn total, 228 pacientes con 85 años o más ingresaron en el hospital con diagnóstico de SCASEST durante el periodo de análisis: 182 (79,8%) con infarto agudo de miocardio sin elevación del ST, 10 pacientes (4,4%) con descenso de ST sin elevación de troponina y 36 (15,8%) con dolor torácico compatible con angina inestable sin infradesnivel del ST ni elevación de marcadores. Se realizó prueba de detección de isquemia en 9 pacientes (8, ergometría convencional; 1, ecocardiograma de estrés), que fue positiva en 3 pacientes. Estos 3 pacientes y 2 con ergometría negativa fueron remitidos a cateterismo. Se realizó ecocardiograma al ingreso a 189 (82,9%) pacientes (el 78,1% de los pacientes del grupo MC y el 89% del grupo AI; p=0,04).
Según la escala GRACE, 189 pacientes (82,9%) tenían riesgo alto; 34 (14,9%), riesgo intermedio, y 5 (2,2%), riesgo bajo. De estos 5 pacientes, 4 presentaron recurrencia de angina durante el ingreso; por lo tanto, 227 pacientes (99,6%) de nuestra serie tenían indicación de cateterismo según las guías de práctica clínica6.
La decisión de realizar coronariografía se tomó a juicio del médico responsable de cada paciente. En un total de 100 pacientes se optó por AI y en 128, MC.
Los pacientes a los que se manejó invasivamente eran más jóvenes y más frecuentemente varones y tenían mayor prevalencia de dislipemia, antecedente de insuficiencia cardiaca, IAM y revascularización. Los pacientes manejados de forma conservadora tenían más frecuentemente fibrilación auricular, más prevalencia de demencia y mayor comorbilidad. En el momento de la presentación, los pacientes manejados invasivamente tenían un perfil de riesgo menor, con menos presencia de troponina positiva y una clase Killip menor, aunque no hubo diferencias en la fracción de eyección ni en la proporción de pacientes de riesgo en la escala GRACE. Los pacientes con isquemia recurrente durante el ingreso recibieron con más frecuencia AI. En la Tabla 1 se describen las diferencias en las características basales entre los dos grupos.
A medida que trascurrieron los años del estudio, se hizo más frecuente la decisión de enviar a los pacientes a coronariografía. Antes del 1 de enero de 2007, en el 40,6% de los pacientes se decidió AI, y a partir de esa fecha aumentó a un 67% (p<0,001). Encontramos también esta diferencia en los pacientes emparejados (el 36,5 frente al 73%; p<0,001).
Como se describe en la Tabla 1, tras el emparejamiento de los pacientes mediante el PS, los grupos quedaron bien balanceados, y no se encontró ninguna diferencia estandarizada > 10%.
CoronariografíaLas características angiográficas y del intervencionismo se describen en la Tabla 2.
Tabla 2. Características angiográficas y del intervencionismo
| Características angiográficas | |||
| Vasos enfermos, % | Distribución de vasos enfermos, % | ||
| Ningún vaso | 3 | Tronco común izquierdo | 10 |
| 1 vaso | 23 | Descendente anterior | 73 |
| 2 vasos | 33 | Arteria circunfleja | 69 |
| 3 vasos | 41 | Coronaria derecha | 63 |
| Características del procedimiento | |||
| Procedimiento | Stents | ||
| Acceso radial, % | 74 | Stents/paciente, media (intervalo) | 2 (1-7) |
| Dosis contraste (ml) * , media (intervalo) | 193 (75-479) | Stents farmacoactivos, % | 24 |
| ICP ostial/bifurcación, % | 23 | Longitud stent/paciente (mm), media (intervalo) | 35 (9-102) |
| Rotablación/balón de corte, % | 9 | Stent en TCI, % | 8 |
ICP: intervencionismo coronario percutáneo; TCI: tronco coronario izquierdo.
* Iodixanol (Visipaque®).
No se realizó revascularización percutánea al 32% de los pacientes. La razón fue la presencia de enfermedad difusa, lechos finos o paciente no revascularizable en el 65,4%, y la ausencia de lesiones graves en el 34,6% (9 pacientes). Sólo en 1 paciente se decidió revascularización quirúrgica (no llegó a realizarse porque falleció antes de la intervención).
Se llevó a cabo revascularización percutánea al 68% de los pacientes, con implante de stent en todos ellos. La revascularización fue exitosa en el 94% de los casos y completa en el 40%.
Tratamiento médico durante la hospitalizaciónEn la Tabla 3 se describe el tratamiento recibido durante la hospitalización. Los pacientes a los que se realizó coronariografía recibieron más antiagregantes orales, tanto aspirina como clopidogrel, y más estatinas, sin que hubiese diferencias en el resto de la medicación recomendada por las guías de práctica clínica. Recibió anti-GPIIb/IIIa sólo el 6% de los pacientes del grupo AI y ninguno en el grupo MC.
Tabla 3. Tratamiento durante la hospitalización en la población total y la emparejada en función de manejo conservador y abordaje intervencionista
| Población total | Población emparejada | |||||
| MC (N=128) | AI (N=100) | p | MC (N=63) | AI (N=63) | p | |
| AAS | 93/114 (81,6) | 98/100 (98) | 0,001 | 51/58 (87,9) | 62/63 (98,4) | 0,02 |
| Clopidogrel | 26/114 (22,8) | 82/100 (82) | <0,001 | 9/58 (15,5) | 51/63 (80,9) | <0,001 |
| AAS + clopidogrel | 16/114 (14) | 80/100 (80) | <0,001 | 6/58 (10,3) | 50/63 (79,3) | <0,001 |
| Anti-GPIIb/IIIa | 0/114 (0) | 6/100 (6) | 0,004 | 0/58 (0) | 1/63 (1,6) | 0,31 |
| HBPM | 113/114 (99) | 100/100 (100) | 0,9 | 58/58 (100) | 63/63 (100) | 1 |
| Bloqueadores beta | 51/114 (44,7) | 53/100 (53) | 0,22 | 34/58 (58,6) | 29/63 (46) | 0,19 |
| Antagonistas del calcio | 38/114 (33,3) | 28/100 (28) | 0,52 | 23/58 (39,6) | 17/63 (27) | 0,13 |
| IECA/ARA-II | 72/114 (63,2) | 64/100 (64) | 0,91 | 31/58 (53,5) | 32/63 (50,8) | 0,84 |
| Diuréticos de asa | 56/114 (49,1) | 35/100 (35) | 0,36 | 21/58 (36,2) | 26/63 (41,3) | 0,59 |
| Espironolactona | 9/114 (7,9) | 12/100 (12) | 0,17 | 4/58 (6,9) | 6/63 (9,5) | 0,56 |
| Nitratos | 84/114 (73,7) | 59/100 (59) | 0,24 | 42/58 (72,4) | 38/63 (60,3) | 0,17 |
| Estatinas | 55/114 (48,2) | 68/100 (68) | 0,001 | 31/58 (53,4) | 37/63 (58,7) | 0,54 |
| Acenocumarol | 12/114 (10,5) | 10/100 (10) | 0,96 | 6/58 (10,3) | 7/63 (11,1) | 0,84 |
| Antiarrítmico | 9/114 (7,9) | 11/100 (11) | 0,36 | 4/58 (6,9) | 7/63 (11,1) | 0,39 |
| Digoxina | 9/114 (7,9) | 8/100 (8) | 0,95 | 5/58 (8,6) | 5/63 (7,9) | 0,93 |
| Hierro | 20/114 (17,5) | 12/100 (12) | 0,29 | 8/58 (13,8) | 7/63 (11,1) | 0,7 |
AAS: ácido acetilsalicílico; AI: abordaje intervencionista; ARA-II: antagonistas del receptor AT1 de la angiotensina II; GPIIb/IIIa: glucoproteína IIb/IIIa; HBPM: heparinas de bajo peso molecular; IECA: inhibidores de la enzima de conversión de la angiotensina; MC: manejo conservador.
Los resultados se muestran como n/N (%).
Los eventos intrahospitalarios se presentan en la Tabla 4.
Tabla 4. Evolución intrahospitalaria de la población total y la emparejada en función del manejo conservador y el abordaje intervencionista
| Población total | Población emparejada | |||||
| MC (N=128) | AI (N=100) | p | MC (N=63) | AI (N=63) | p | |
| Hemorragia TIMI | 8/114 (7) | 8/89 (9) | 0,62 | 5/58 (8,6) | 5/56 (8,9) | 0,93 |
| Transfusión | 10/126 (7,9) | 8/96 (8,3) | 0,91 | 6/62 (9,7) | 6/62 (9,7) | 1 |
| Deterioro de la función renal | 7/105 (6,7) | 11/95 (11,6) | 0,22 | 3/50 (6) | 7/56 (12,5) | 0,22 |
| Ictus | 4/128 (3,1) | 1/98 (1) | 0,39 | 3/63 (4,8) | 1/62 (1,6) | 0,31 |
| Re-IAM | 0/128 (0) | 4/98 (4,1) | 0,03 | 0/63 (0) | 1/62 (1,6) | 0,31 |
| Muerte | 15/128 (11,7) | 5/100 (5) | 0,08 | 5/63 (7,9) | 2/63 (3,2) | 0,25 |
AI: abordaje intervencionista; MC: manejo conservador; Re-IAM: reingreso por infarto agudo de miocardio.
Los resultados se muestran como n/N (%).
Los pacientes del grupo AI presentaron más reinfarto no fatal. Dos pacientes presentaron trombosis subaguda de stent. El 4% de los pacientes a los que se realizó coronariografía presentaron una complicación intraprocedimiento (3 disecciones coronarias, 1 rotura de arteria sin taponamiento) y el 7%, una complicación vascular (3 perforaciones radiales, 3 hematomas femorales y 1 seudoaneurisma femoral). Ninguna de ellas requirió intervención quirúrgica.
No hubo ninguna hemorragia mayor y no hubo diferencias en la frecuencia de hemorragias menores ni en la necesidad de transfusión intrahospitalaria entre los dos grupos.
En la población emparejada en el PS, no hubo diferencias en la incidencia de los eventos intrahospitalarios analizados (Tabla 4).
Eventos en el seguimiento de la población totalCompletaron 1, 2 y 3 años de seguimiento el 98,2, el 90,8 y el 78,9% de los pacientes respectivamente. Los eventos en el seguimiento de la población total (no ajustados por PS) se describen en la Tabla 5.
Tabla 5. Eventos en el seguimiento a 3 años, en la población total y la emparejada en función de manejo conservador y abordaje intervencionista
| Población total | Población emparejada | |||||
| MC (N=128) | AI (N=100) | p | MC (N=63) | AI (N=63) | p | |
| Muerte | 79/128 (61,7) | 31/98 (31,6) | < 0,001 | 33/63 (52,4) | 21/63 (33,3) | 0,037 |
| Muerte o ECAM | 92/128 (71,9) | 43/98 (43,9) | < 0,001 | 43/63 (68,3) | 26/63 (41,3) | 0,003 |
| Reingreso por IAM | 25/128 (19,5) | 11/98 (11,2) | 0,08 | 16/63 (25,4) | 7/63 (11,1) | 0,038 |
| Reingreso por angina | 9/128 (7) | 9/98 (9,2) | 0,58 | 7/63 (11,1) | 5/63 (7,9) | 0,54 |
| Reingreso por ictus | 8/128 (6,3) | 4/98 (4,1) | 0,45 | 4/63 (6,4) | 4/63 (6,4) | 1 |
| Reingreso por hemorragia | 10/128 (7,8) | 10/98 (10,2) | 0,56 | 4/63 (6,4) | 5/63 (7,9) | 1 |
| Reingreso por ICC | 30/128 (23,4) | 24/98 (24,5) | 0,92 | 14/63 (22,2) | 18/63 (28,6) | 0,41 |
AI: abordaje intervencionista; IAM: infarto agudo de miocardio; ICC: insuficiencia cardiaca congestiva; ECAM: eventos cardiovasculares adversos mayores; MC: manejo conservador.
Los resultados se muestran como n/N (%).
La relación entre la realización de coronariografía y los eventos (muerte y muerte o ECAM) ajustada por los quintiles del PS y por el año de ingreso se presentan en la Tabla 6. Se observa que en la población total, ajustando por los quintiles de PS, la realización de coronariografía se relaciona con menos mortalidad (HR=0,518; IC del 95%, 0,316-0,85) y con menor número de muertes o ECAM en el seguimiento (HR=0,483; IC del 95%, 0,315-0,741). Este resultado no se modifica cuando ajustamos también por año de ingreso (mortalidad, HR=0,465; IC del 95%, 0,279-0,775; muerte o ECAM, HR=0,459; IC del 95%, 0,294-0,715). La relación entre los quintiles de PS y la mortalidad en este análisis multivariable se acerca a la significación (p=0,1).
Tabla 6. Regresión de Cox del abordaje intervencionista ajustado por propensity score: quintiles y emparejamiento
| Wald | p | Hazard ratio | IC del 95% OR | |
| Abordaje intervencionista ajustado por los quintiles delpropensity score | ||||
| Muerte | ||||
| Quintiles del propensity score | 7,71 | 0,103 | ||
| Abordaje intervencionista | 6,789 | 0,009 | 0,518 | 0,316-0,85 |
| Muerte o ECAM | ||||
| Quintiles del propensity score | 4,917 | 0,296 | ||
| Abordaje intervencionista | 11,121 | 0,001 | 0,483 | 0,315-0,741 |
| Abordaje intervencionista ajustado por los quintiles delpropensity scorey año de ingreso (2004-2006 frente a 2007-2009) | ||||
| Muerte | ||||
| Quintiles del propensity score | 7,317 | 0,12 | ||
| Abordaje intervencionista | 8,627 | 0,003 | 0,465 | 0,279-0,775 |
| Año de ingreso | 2,395 | 0,122 | ||
| Muerte o ECAM | ||||
| Quintiles del propensity score | 5,183 | 0,269 | ||
| Abordaje intervencionista | 11,834 | 0,001 | 0,459 | 0,294-0,715 |
| Año de ingreso | 0,805 | 0,37 | ||
| Abordaje intervencionista en la población emparejada | ||||
| Muerte | ||||
| Abordaje intervencionista | 4,125 | 0,042 | 0,567 | 0,328-0,98 |
| Muerte o ECAM | ||||
| Abordaje intervencionista | 8,275 | 0,004 | 0,489 | 0,3-0,796 |
| Abordaje intervencionista en la población emparejada ajustado por año de ingreso (2004-2006 frente a 2007-2009) | ||||
| Muerte | ||||
| Abordaje intervencionista | 5,194 | 0,023 | 0,502 | 0,277-0,908 |
| Año de ingreso | 1,101 | 0,294 | ||
| Muerte o ECAM | ||||
| Abordaje intervencionista | 8,542 | 0,003 | 0,454 | 0,267-0,771 |
| Año de ingreso | 0,589 | 0,443 | ||
IC: intervalo de confianza; ECAM: eventos cardiovasculares adversos mayores; OR: odds ratio.
Analizamos el pronóstico a 3 años de los 126 pacientes emparejados mediante el PS. Sus características se presentan en la Tabla 1.
Entre estos pacientes hubo 2 muertes durante el ingreso en el grupo AI y 5 en el grupo MC. En el análisis de supervivencia incluimos los eventos durante la hospitalización.
Completaron 1, 2 y 3 años de seguimiento el 99,2, el 88,9 y el 75,4% de los pacientes respectivamente. La mediana de seguimiento fue de 151 [intervalo intercuartílico, 110-182] semanas, sin diferencias entre ambos grupos (mediana, 154±59 frente a 150±48; p=0,78).
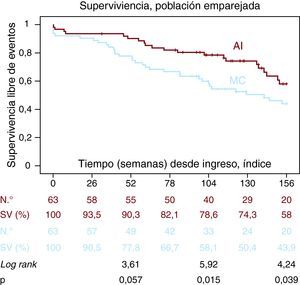
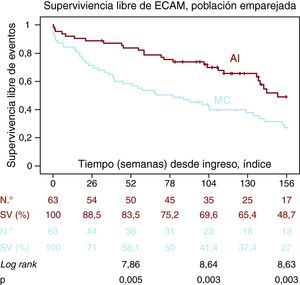
En este periodo, los pacientes manejados de forma invasiva presentaron mayor supervivencia a los 2 años (el 78,6 frente al 58,1%; p=0,015) y a los 3 años (el 58 frente al 43,9%; p=0,039) (Figura 2). También presentaron mayor supervivencia libre del evento combinado ECAM al año (el 83,5 frente al 58,1%; p=0,005) a los 2 años (el 69,6 frente al 41,4%; p=0,003) y a los 3 años (el 48,7 frente al 27%; p=0,003) (Figura 3).
Figura 2. Probabilidad de supervivencia en función de realización de coronariografía (Kaplan-Meier). AI: abordaje intervencionista; MC: manejo conservador.
Figura 3. Probabilidad de supervivencia libre de muerte o eventos cardiovasculares adversos mayores en función de realización de coronariografía (Kaplan-Meier). AI: abordaje intervencionista; ECAM: eventos cardiovasculares adversos mayores; MC: manejo conservador.
No se encontraron diferencias significativas en los reingresos por hemorragia o insuficiencia cardiaca (Tabla 5).
DISCUSIÓNEl principal hallazgo de este estudio es que, en pacientes no seleccionados de edad muy avanzada y alta comorbilidad, la realización de coronariografía durante el ingreso con intención de revascularizar en el SCASEST se asocia a mayores supervivencia y supervivencia libre de ECAM a 3 años, a expensas de una baja tasa de complicaciones relacionadas con el procedimiento y sin aumentar significativamente las hemorragias.
Un estudio previo ha encontrado los mismos resultados en pacientes no tan ancianos (media, 80,4 años)19. Sin embargo, no hemos encontrado estudios con pacientes de edad tan avanzada o que incluyan variables referentes a la comorbilidad. Nosotros hemos incluido el índice de Charlson, que tiene un valor pronóstico demostrado en pacientes que ingresan con un SCA20.
El análisis de nuestra cohorte confirma que los pacientes muy ancianos son un subgrupo con riesgo especialmente alto en el contexto del SCASEST. En nuestra serie, el 97,8% de los pacientes se encuadran en la categoría de moderado o alto riesgo en el score GRACE. El manejo recomendado por las guías de práctica clínica para estos pacientes es la realización de coronariografía6.
En diferentes registros sobre el manejo del SCASEST, tanto en nuestro país (MASCARA21) como internacionales (CRUSADE22, GRACE2), se ha descrito una tendencia a seleccionar para manejo intervencionista a pacientes con un perfil de riesgo menor. Este hecho también se ve reflejado en nuestra cohorte de pacientes muy ancianos. Los que se someten a AI tienen menor puntuación en el score GRACE, menor porcentaje de troponina positiva y menor clase Killip en el momento de la presentación.
En nuestra serie, apreciamos un sesgo del médico que trata al paciente, con tendencia a decidir MC para los pacientes más ancianos y comórbidos. Este hallazgo ya se ha descrito en otras series23, 24. Estos pacientes también reciben en menor medida otras actuaciones recomendadas por las guías de práctica clínica: menos tratamiento con doble antiagregación y con estatinas y menos ecocardiografías durante la hospitalización.
Una de las posibles causas de que no se aplique AI a los pacientes ancianos es la percepción de que el riesgo de complicaciones supera el beneficio de la revascularización22. En nuestro estudio únicamente el 4% de los pacientes sufren complicaciones durante el procedimiento, porcentaje comparable al descrito en otros estudios en población no anciana25. Además, la tasa de hemorragias o necesidad de transfusión durante la hospitalización es baja comparada con otras series21, 26 y no difiere significativamente entre los pacientes con MC y con AI. Esto puede deberse a que el uso de fármacos antiagregantes anti-GPIIb/IIIa es muy bajo en nuestra serie y a que la mayor parte de los procedimientos se realizan por vía radial, lo que se ha demostrado que minimiza el riesgo de hemorragias27. Tampoco hemos encontrado más ingresos por hemorragias en el seguimiento a pesar de recibir en mayor proporción tratamiento con doble antiagregación.
A pesar del uso frecuente del abordaje radial, la tasa de complicaciones vasculares en nuestra serie es mayor que la descrita en otras series en pacientes jóvenes28, algo esperable por las mayores calcificación y tortuosidad arterial en los pacientes de más edad. Ninguna de las complicaciones requirió intervención quirúrgica.
En nuestra serie se revasculariza al 68% de los pacientes enviados a coronariografía, porcentaje similar al descrito en estudios aleatorizados y otras series de pacientes no tan ancianos19, 26.
LimitacionesLa limitación fundamental de nuestro trabajo es el escaso número de pacientes, sobre todo después del emparejamiento con PS. Esto se debe a que hemos escogido a pacientes con edad muy avanzada y se ha realizado en un único centro, lo que podría limitar la generalización de nuestros resultados. No obstante, a pesar del número reducido, hemos encontrado diferencias significativas en el seguimiento a medio plazo similares a las de estudios con pacientes más jóvenes.
Los grupos de tratamiento son muy distintos por un importante sesgo de selección. Se ha realizado un ajuste mediante PS para minimizar dicho sesgo, pero es posible que no haya sido totalmente eliminado. Por un lado, porque lo utilizamos en una población pequeña y, por otro, es posible un sesgo en variables no registradas. Después del emparejamiento comparamos las características basales de los grupos comprobando que habían desaparecido las diferencias. Sin embargo, dada la naturaleza retrospectiva, no ha sido posible registrar variables con influencia pronóstica demostrada en la población anciana con cardiopatía isquémica, como los índices de fragilidad, la capacidad de autocuidado o la institucionalización29. Cabe la posibilidad de que estas variables se distribuyan de forma diferente entre los dos grupos, lo que generaría un sesgo en el resultado.
Otra de las limitaciones consiste en que la decisión de coronariografía fue más frecuente en los últimos años del estudio. Es posible que en este tiempo haya habido avances en el tratamiento (más entrenamiento del cardiólogo intervencionista, cambio de la vía de acceso, mejores dispositivos o nuevos fármacos) que favorezcan al grupo intervencionista. Sin embargo, hemos ajustado por el año de ingreso en el modelo de regresión de Cox, y no se modificó la relación entre la realización de coronariografía y el pronóstico.
Los pacientes del grupo AI recibieron con frecuencia mucho mayor clopidogrel y doble antiagregación. Existe la posibilidad de que esto haya influido en el mejor resultado de este grupo.
CONCLUSIONESEn nuestra serie, los pacientes muy ancianos ingresados por SCASEST tienen riesgo moderado o alto casi en su totalidad, por lo que, siguiendo las guías de práctica clínica actuales, tendrían indicación de coronariografía.
Nuestros datos indican que este manejo confiere un mejor pronóstico a medio plazo, a expensas de una baja tasa de complicaciones relacionadas con el procedimiento y sin aumentar de forma significativa la tasa de hemorragias.
CONFLICTO DE INTERESESNinguno.
Recibido 2 Diciembre 2010
Aceptado 19 Abril 2011
Autor para correspondencia: Donibane Garazi 4, 3C, 20018 San Sebastián, Guipuzcoa, España. inaki.villanuevabenito@osakidetza.es