
La cirugía cardiaca robótica se inició a finales de los años noventa1,2, se ha ido expandiendo lentamente y ha sido adoptada por algunos centros de referencia en Estados Unidos como el abordaje de elección para la cirugía mitral. En Europa su implementación ha sido menor, aunque parece que ha habido un aumento significativo en los últimos años tanto del volumen de casos como de los centros que realizan cirugía robótica3.
El objetivo del presente estudio es describir los resultados de los primeros 120 pacientes intervenidos mediante cirugía cardiaca robótica en nuestro centro (de diciembre de 2019 a julio de 2022). El estudio cuenta con la aprobación del Comité de Ética de nuestro centro (HCB/2021/0248), que no consideró necesario el consentimiento informado de cada paciente.
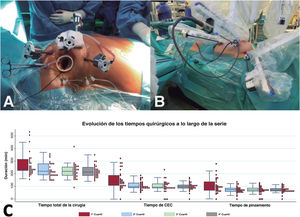
Un único equipo de 2 cirujanos (uno en la consola del robot y otro en la mesa de operaciones) llevó a cabo todas las intervenciones con la plataforma DaVinci Xi (Intuitive Surgical, Estados Unidos). El 82% (n=98) corresponde a cirugía de la válvula mitral. La reparación mitral fue el procedimiento más frecuente (n=86) (figura 1A). Además se practicaron cierre de comunicación interauricular (n=9), cirugía tricuspídea concomitante (n=2), disección robótica de la arteria mamaria interna para revascularizar la descendente anterior sin circulación extracorpórea (CEC) (n=7) (figura 1B), exéresis de tumores (n=3) y sustitución de la válvula aórtica (n=3). La tabla 1 muestra las características de la cohorte.
A: se muestra la colocación de los 4 trócares del robot y del puerto de trabajo en el hemitórax derecho del paciente, disposición usada para la cirugía intracavitaria. B: los 3 trócares que se colocan en el hemitórax izquierdo para disecar la arteria mamaria izquierda en los casos de cirugía coronaria. C: reducción de todos los tiempos quirúrgicos (circulación extracorpórea [CEC], isquemia y tiempo quirúrgico total), separados por cuartiles.
Descripción de la población y resultados
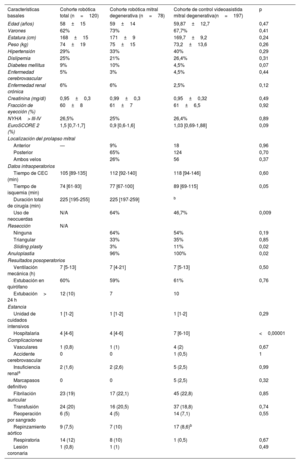
| Características basales | Cohorte robótica total (n=120) | Cohorte robótica mitral degenerativa (n=78) | Cohorte de control videoasistida mitral degenerativa(n=197) | p |
|---|---|---|---|---|
| Edad (años) | 58±15 | 59±14 | 59,87±12,7 | 0,47 |
| Varones | 62% | 73% | 67,7% | 0,41 |
| Estatura (cm) | 168±15 | 171±9 | 169,7±9,2 | 0,24 |
| Peso (kg) | 74±19 | 75±15 | 73,2±13,6 | 0,26 |
| Hipertensión | 29% | 33% | 40% | 0,29 |
| Dislipemia | 25% | 21% | 26,4% | 0,31 |
| Diabetes mellitus | 9% | 10% | 4,5% | 0,07 |
| Enfermedad cerebrovascular | 5% | 3% | 4,5% | 0,44 |
| Enfermedad renal crónica | 6% | 6% | 2,5% | 0,12 |
| Creatinina (mg/dl) | 0,95±0,3 | 0,99±0,3 | 0,95±0,32 | 0,49 |
| Fracción de eyección (%) | 60±8 | 61±7 | 61±6,5 | 0,92 |
| NYHA> III-IV | 26,5% | 25% | 26,4% | 0,89 |
| EuroSCORE 2 (%) | 1,5 [0,7-1,7] | 0,9 [0,6-1,6] | 1,03 [0,69-1,88] | 0,09 |
| Localización del prolapso mitral | ||||
| Anterior | — | 9% | 18 | 0,96 |
| Posterior | 65% | 124 | 0,70 | |
| Ambos velos | 26% | 56 | 0,37 | |
| Datos intraoperatorios | ||||
| Tiempo de CEC (min) | 105 [89-135] | 112 [92-140] | 118 [94-146] | 0,60 |
| Tiempo de isquemia (min) | 74 [61-93] | 77 [67-100] | 89 [69-115] | 0,05 |
| Duración total de cirugía (min) | 225 [195-255] | 225 [197-259] | b | |
| Uso de neocuerdas | N/A | 64% | 46,7% | 0,009 |
| Resección | N/A | |||
| Ninguna | 64% | 54% | 0,19 | |
| Triangular | 33% | 35% | 0,85 | |
| Sliding plasty | 3% | 11% | 0,02 | |
| Anuloplastia | 96% | 100% | 0,02 | |
| Resultados posoperatorios | ||||
| Ventilación mecánica (h) | 7 [5-13] | 7 [4-21] | 7 [5-13] | 0,50 |
| Extubación en quirófano | 60% | 59% | 61% | 0,76 |
| Extubación> 24 h | 12 (10) | 7 | 10 | |
| Estancia | ||||
| Unidad de cuidados intensivos | 1 [1-2] | 1 [1-2] | 1 [1-2] | 0,29 |
| Hospitalaria | 4 [4-6] | 4 [4-6] | 7 [6-10] | <0,00001 |
| Complicaciones | ||||
| Vasculares | 1 (0,8) | 1 (1) | 4 (2) | 0,67 |
| Accidente cerebrovascular | 0 | 0 | 1 (0,5) | 1 |
| Insuficiencia renala | 2 (1,6) | 2 (2,6) | 5 (2,5) | 0,99 |
| Marcapasos definitivo | 0 | 0 | 5 (2,5) | 0,32 |
| Fibrilación auricular | 23 (19) | 17 (22,1) | 45 (22,8) | 0,85 |
| Transfusión | 24 (20) | 16 (20,5) | 37 (18,8) | 0,74 |
| Reoperación por sangrado | 6 (5) | 4 (5) | 14 (7,1) | 0,55 |
| Repinzamiento aórtico | 9 (7,5) | 7 (10) | 17 (8,6)b | |
| Respiratoria | 14 (12) | 8 (10) | 1 (0,5) | 0,67 |
| Lesión coronaria | 1 (0,8) | 1 (1) | 0,49 | |
CEC: circulación extracorpórea; NYHA: clase funcional de la New York Heart Association.
En la cohorte total, la mediana [intervalo intercuartílico] del tiempo total de cirugía fue 225 [195-255] min y las medianas de los tiempos de CEC y de isquemia miocárdica, 105 [89-135] y 74 [61-93] min respectivamente. Todos los tiempos quirúrgicos se redujeron progresivamente (figura) desde el inicio del programa, Q1 frente a Q4: CEC, 136 frente a 98min (p=0,003); isquemia, 92 frente a 70min (p=0,009) y tiempo quirúrgico total, 240 frente a 211min (p=0,02)] (figura 1C).
Se extubó a la mayoría de los pacientes (58%) en el quirófano (mediana de ventilación mecánica de los extubados en quirófano, 7 [5-13] h). Las medianas de estancia en la unidad de cuidados intensivos y de estancia hospitalaria fueron 1 [1-2] y 4 [4-6] días respectivamente. Al igual que sucede con los tiempos quirúrgicos, la estancia hospitalaria se redujo significativamente con la experiencia, Q1 frente a Q4: 5 frente a 4 días (p <0,001). Todos los tiempos son comparables a los de nuestra cohorte de cirugía mitral videoasistida, salvo el tiempo de pinzamiento, que fue inferior en el grupo robótico.
La tasa de reparación en los pacientes con insuficiencia mitral fue del 100% (insuficiencia mitral al alta ligera o menor en el 98,8%). Todos los pacientes fueron dados de alta a su domicilio y ninguno ha requerido reintervención durante el seguimiento. En comparación con el grupo de cirugía videoasistida, la cirugía robótica resultó en una mediana de estancia posoperatoria claramente reducida (4 frente a 7 días; p <0,00001).
Nuestros resultados, pese a ser una experiencia inicial que incluye la totalidad de la curva de aprendizaje, son satisfactorios y concuerdan con series publicadas por centros de gran experiencia4–6 y con nuestros propios resultados en cirugía mitral videoasistida. Creemos que la amplia experiencia previa de todo el equipo en cirugía videoasistida ha facilitado minimizar la curva de aprendizaje y conseguir un nivel muy alto de seguridad y calidad desde el inicio, como demuestran la ausencia de conversiones a esternotomía, la excelente tasa de reparación mitral y la baja incidencia de complicaciones posoperatorias.
En conclusión, la cirugía cardiaca robótica permite realizar, en pacientes seleccionados, un amplio espectro de intervenciones quirúrgicas cardiacas con excelentes resultados y corta estancia hospitalaria posoperatoria. La cirugía robótica es actualmente la opción quirúrgica menos invasiva, pero se trata de una técnica de alta complejidad e importante curva de aprendizaje, que se puede minimizar con una experiencia previa amplia en cirugía videoasistida.
FINANCIACIÓNSin fuentes de financiación externas.
CONTRIBUCIÓN DE LOS AUTORESE. Sandoval: redacción y edición de tablas y figura. A. Muro: recogida de datos y revisión final del manuscrito. R. Navarro: revisión final del manuscrito. A. García-Álvarez: revisión final del manuscrito. M. Castellà: revisión final del manuscrito. D. Pereda: conceptualización, edición de figura, revisión crítica y aprobación final del manuscrito.
CONFLICTO DE INTERESESNinguno de los autores tiene ningún conflicto de intereses que declarar en relación con este estudio.

![A: se muestra la colocación de los 4 trócares del robot y del puerto de trabajo en el hemitórax derecho del paciente, disposición usada para la cirugía intracavitaria. B: los 3 trócares que se colocan en el hemitórax izquierdo para disecar la arteria mamaria izquierda en los casos de cirugía coronaria. C: reducción de todos los tiempos quirúrgicos (circulación extracorpórea [CEC], isquemia y tiempo quirúrgico total), separados por cuartiles. A: se muestra la colocación de los 4 trócares del robot y del puerto de trabajo en el hemitórax derecho del paciente, disposición usada para la cirugía intracavitaria. B: los 3 trócares que se colocan en el hemitórax izquierdo para disecar la arteria mamaria izquierda en los casos de cirugía coronaria. C: reducción de todos los tiempos quirúrgicos (circulación extracorpórea [CEC], isquemia y tiempo quirúrgico total), separados por cuartiles.](https://static.elsevier.es/multimedia/03008932/0000007600000009/v2_202311091723/S0300893223001057/v2_202311091723/es/main.assets/thumbnail/gr1.jpeg?xkr=eyJpdiI6IlA3LzAxeTg0d0tVZ0w5RjVFbjdwOFE9PSIsInZhbHVlIjoiRGxTQ2dKZWt0d2k2RTRieSsweS81Wk1WK2JpVmI0d1ZMYlRCWmZVN0J6ST0iLCJtYWMiOiJjY2U1ZDNkYWJiOWRjMGZiNjg0ZjQxNzQ4ZDQ2ODg0YTk5YjAwYmM4ZGYxMzk2ZDZjNDdiY2ZiOTk3ZjZiOTU3IiwidGFnIjoiIn0=)