En los últimos 25 años se ha producido una evolución creciente en las indicaciones de tratamiento mediante un desfibrilador automático implantable (DAI), sobre todo en la prevención primaria de la muerte súbita. Sin embargo, hay cierta falta de consistencia entre dichas indicaciones en las distintas guías. Repasamos las indicaciones actuales de DAI y realizamos una valoración crítica de éstas, con especial énfasis en las referidas en las guías de más reciente aparición.
Palabras clave
Desde el primer implante de un desfibrilador automático (DAI) en la década de 19801, el incremento en el número de pacientes con estos dispositivos ha sido exponencial y fundamentado en su eficacia reiteradamente demostrada contra la muerte súbita cardiaca de origen arrítmico. La tasa anual de implantes de DAI en Estados Unidos se ha incrementado de 9.000 en 1990 a 143.000 en 2005. A lo largo de la última década, sus indicaciones se han ido extendiendo y concretando, sustentadas en los resultados de diversos ensayos clínicos iniciados fundamentalmente a partir de la publicación del estudio AVID2. Con todo, las variaciones en la jerarquización de las indicaciones, sobre todo en lo referido a la prevención primaria, han sido amplias. El presente capítulo tiene como objetivo revisar de forma resumida la evolución de las indicaciones de implante de estos dispositivos en las distintas guías de práctica clínica aparecidas durante estos últimos años2–10, y a la vez realizar una valoración crítica necesariamente rápida y limitada a algunos puntos concretos de éstas, centrándonos sobre todo en el contraste con las de más reciente aparición. Queda fuera del ámbito de este capítulo lo concerniente a las indicaciones de terapia de resincronización asociada con un DAI.
INDICACIONES EN PREVENCIÓN PRIMARIADebemos reconocer las inconsistencias de las distintas guías a la hora de sentar indicaciones de implante para prevención primaria de muerte súbita. Esta falta de homogeneidad es multifactorial, pero los diferentes puntos de corte de la fracción de eyección del ventrículo izquierdo (FEVI) en los criterios de inclusión de los distintos ensayos han contribuido en gran medida a esta variabilidad. De hecho, no se ha aleatorizado a pacientes con FEVI moderadamente deprimida de forma específica, y los complementos electrofisiológicos para los distintos perfiles de riesgo han sido cambiantes. Más aun, confiar en una cifra mágica sobre un índice de fase de función ventricular como la FEVI, para el que hay una variabilidad interobservador de hasta el 8% en su determinación ecocardiográfica habitual, relativiza y a la vez complica el problema11,12. Las guías más recientes extienden la indicación de clase I de implante de DAI para todos los pacientes con disfunción del ventrículo izquierdo (VI) postinfarto y FEVI<30-40%9, a excepción de los que tienen una FEVI<35% y clase funcional I, que mantendrían una indicación de implante de clase IIa. Resulta lógico pensar que los autores de las actuales guías de 2006 hayan querido integrar en el perfil de riesgo de pacientes con disfunción del VI postinfarto sin inducibilidad de taquiarritmias ventriculares sostenidas las pruebas científicas aportadas por el ensayo SCD-HeFT13, sumado al hecho de que casi dos tercios de los pacientes MADIT-II se encontraban en clase funcional II-III14,15. Con todo, sobre este punto no se aporta ninguna explicación en dichas guías, en las que se echan en falta referencias específicas que sustenten cada recomendación. Por otra parte, un límite de FEVI del 40% fundamentado sólo en el ensayo MUSTT, un estudio que aleatorizaba una estrategia de tratamiento y no el implante de un DAI, podría parecer excesivo. La política de«tabla rasa»de estas últimas guías al asignar al paciente MUSTT una indicación de clase I con un nivel de evidencia A debe pues sorprendernos. El impacto de la«cuarentena»señalado por los resultados del estudio DINAMIT16 se hace patente en dichas guías e indica el implante tras al menos 40 días postinfarto. Por el contrario, las directrices propuestas por el National Institute for Health and Clinical Excellence (NICE) actualizadas en julio de 2006 son muy concretas y aconsejan el implante en pacientes isquémicos con una FEVI<30% y en clase funcional≤III de la New York Heart Association (NYHA) que presenten un complejo QRS prolongado (≥ 120ms), y restringe la indicación a pacientes con un perfil MUSTT si su FEVI es<35%10.
En cuanto a los pacientes con síndrome de Brugada, las actuales guías se alejan de lo notificado en la Segunda Conferencia de Consenso17 sobre dicha entidad, centrándose sólo en los pacientes con patrón de Brugada tipo I espontáneo al que se indica el implante si hay un síncope previo. En los asintomáticos señala la realización de un estudio electrofisiológico sólo para las formas espontáneas y como una indicación de clase IIb. A pesar de la reciente jerarquización del riesgo en pacientes con genotipo en el síndrome de QT largo18, el implante de DAI en pacientes asintomáticos no pasa de ser una indicación de clase IIb en las guías más recientes. Por el contrario, la prevención primaria en pacientes con miocardiopatía hipertrófica asciende en esas directrices a una recomendación de clase IIa ante la presencia de un único factor de riesgo principal. En las tablas 1 y 2 se resumen las indicaciones más actuales para el implante de DAI en el ámbito de la prevención primaria y su comparación con las guías previas.
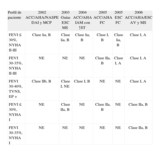
Diferentes niveles de indicación y evidencia en los pacientes postinfarto de miocardio en relación con la terapia con desfibrilador automático implantable en prevención primaria de muerte súbita*
| Perfil de paciente | 2002 ACC/AHA/NASPE DAI y MCP | 2003 Guías ESC MS | 2004 ACC/AHA IAM con ↑ST | 2005 ACC/AHA FC | 2005 ESC FC | 2006 ACC/AHA/ESC AV y MS |
| FEVI≤30%, NYHA II-III | Clase lia, B | Clase lia, B | Clase lia, B | Clase I, B | Clase lia, B | Clase I, A |
| FEVI 30-35%, NYHA II-III | NE | NE | NE | Clase IIa, B | Clase I, A | Clase I, A |
| FEVI 30-40%, TVNS, EP + | Clase IIb, B | Clase I, NE | Clase I, B | NE | NE | Clase I, A |
| FEVI≤30%, NYHA I | NE | Clase IIa, B | NE | Clase IIa, B | NE | Clase IIa, B |
| FEVI 30-35%, NYHA I | NE | NE | NE | NE | NE | Clase IIa, B |
ACC: American College of Cardiology; AHA: American Heart Association; AV: arritmias ventriculares; DAI: desfibrilador automático implantable; ESC: European Society of Cardiology; EP: estimulación ventricular programada; FEVI: fracción de eyección ventricular izquierda; FC: fracaso cardiaco; IAM infarto agudo de miocardio; MCP: marcapasos; MS: muerte súbita cardiaca; NASPE: North American Socitey for Pacing and Electrophysiology: NE: nivel de recomendación y/o evidencia no queda especificado para el correspondiente perfil de paciente en la guía de referencia; NYHA: clase funcional según la New York Heart Association; TVNS: taquicardia ventricular no sostenida.
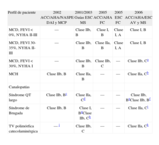
Niveles de recomendación y de evidencia en las guías para el implante de desfibrilador automático implantable en la prevención primaria de muerte súbita en pacientes con miocardiopatía dilatada no isquémica, hipertrófica y canalopatías
| Perfil de paciente | 2002 ACC/AHA/NASPE DAI y MCP | 2001/2003 Guías ESC MS | 2005 ACC/AHA FC | 2005 ESC FC | 2006 ACC/AHA/ESC AV y MS |
| MCD, FEVI<0%, NYHA II-III | — | Clase IIb, B | Clase I, B | Clase I, A | Clase I, B |
| MCD, FEVI 30-35%, NYHA II-III | — | Clase IIb, B | Clase IIa, B | Clase I, A | Clase I, B |
| MCD, FEVI<30%, NYHA I | — | Clase IIb, B | Clase IIb, C | — | Clase IIb, Ca |
| MCH | Clase IIb, B | Clase IIa, B | — | — | Clase IIa, Cb |
| Canalopatías | |||||
| Síndrome QT largo | Clase IIb, Bc | Clase IIa, Cd | — | — | Clase IIb, BeClase IIb, Bf |
| Síndrome de Brugada | Clase IIb, B | Clase I, BgClase IIb, Ch | — | — | Clase IIa, Ci |
| TV polimórfica catecolaminérgica | — j | Clase IIb, C | — | — | Clase IIa, Ck |
ACC: American College of Cardiology; AHA: American Heart Association; AV: arritmias ventriculares; DAI: desfibrilador automático implantable; ESC: European Society of Cardiology; FEVI: fracción de eyección ventricular izquierda; FC: fracaso cardiaco; MCD: miocardiopatía dilatada; MCH: miocardiopatía; MCP: marcapasos; MS: muerte súbita cardiaca; NASPE: North American Society for Pacing and Electrophysiology; NYHA: New York Heart Association; hipertrófica; TV: taquicardia ventricular;
Estas Guías expanden el recorrido de valores de FEVI a 30-35% o menos en pacientes con NYHA de I en una única recomendación.
Justifica su implante en asintomáticos con«fuerte»historia familiar de muerte súbita o cuando el tratamiento no invasivo no es factible.
Incluidos bajo el epígrafe de prevención«primaria»en casos sintomáticos con recurrencias a pesar de los betabloqueantes y como terapia asociada con estos fármacos. También se recomendaría a pacientes con sindactilia, bloqueo auriculoventricular completo y en casos de síndrome de Jerwell.
El 60,5% de los implantes realizados en nuestro país durante 2005 tuvo una indicación por muerte súbita resucitada, taquicardia ventricular (TV) documentada o síncope, frente al 79,3% del año 200219. En cualquier caso, si tenemos en cuenta que la tasa de supervivencia para episodios de parada cardiaca extrahospitalaria es menor del 5% en muchos países industrializados, habremos de reconocer para la prevención secundaria un cierto carácter de terapia para supervivientes. Afortunadamente, este porcentaje se incrementa al 15% para los pacientes en fibrilación ventricular. Por otra parte, es bien conocido que los supervivientes de taquiarritmias ventriculares graves están en riesgo de nuevos episodios, con rehospitalizaciones al año para la mitad de estos pacientes, el 40% de los cuales muere en los 2 años siguientes10. En los estudios AVID2, CASH20 y CIDS21 se incluye a un total de 1.850 supervivientes de una parada cardiaca que han sido objeto de diferentes metaanálisis. Estos estudios demuestran una reducción del 50% en el riesgo de muerte cardiaca (intervalo de confianza [IC] del 95%, 35-65%) y del 25-28% en el riesgo de mortalidad global (IC del 95%, 10-40%) obtenidos con el implante del DAI como prevención secundaria en comparación con el tratamiento con amiodarona u otros antiarrítmicos. Las recomendaciones del NICE10 son claras y están centradas en la indicación de implante para pacientes con un perfil AVID fundamentalmente. Sin embargo, las recientes guías de American College of Cardiology/American Heart Association/European Society of Cardiology (ACC/AHA/ESC) de 2006 mantienen el implante de un DAI como indicación de clase I en la cardiopatía isquémica para: a) pacientes resucitados de fibrilación ventricular con infarto previo (> 48h) y disfunción«significativa»del ventrículo izquierdo (VI) en los que no se pueda llevar a cabo una revascularización coronaria y, debemos entender, cuando no hayan pruebas claras de isquemia como precursora de esa arritmia, y b) en pacientes con TV«inestables»con disfunción de VI postinfarto. Como indicación de clase IIa, y sin ensayo clínico que la soporte, se señala el implante en pacientes con TV recurrentes postinfarto sin disfunción del VI significativa. Aunque en estas guías se incluyen por primera vez recomendaciones conservadoras acerca de la ablación de TV, no se señala en esta última indicación el resultado previo de una ablación mediante catéter, que sí se especifica en el caso de pacientes con cardiopatías congénitas. Siempre a caballo entre la prevención primaria y secundaria, los pacientes con síncope e infarto de miocardio previo no aparecen adecuadamente reflejados en las actuales guías ACC/AHA/ESC de 2006, obviando las directrices señaladas recientemente22. Estas últimas recomiendan el implante de DAI a todos estos pacientes si su FEVI es <35% sobre la base de evidencias en prevención primaria. Finalmente, en estas guías de 2006 se desliza el concepto que considera a estos dispositivos como un tratamiento útil para los episodios recurrentes de taquiarritmias ventriculares y no sólo un arma eficaz contra la muerte súbita cardiaca de origen arrítmico. Así debemos entenderlo para las indicaciones en pacientes sin disfunción ventricular9. En la tabla 3 se resumen las indicaciones de implante de DAI señaladas por esas guías en el ámbito de la prevención secundaria.
Resumen de las indicaciones de desfibrilador automático implantable en prevención secundaria según las guías ACC/AHA/ESC de 2006
| Grupo según cardiopatía | Recomendación (Nivel de evidencia) |
| a) Disfunción de VI postinfarto de miocardio | |
| 1. Si no puede realizarse revascularización coronaria y hay evidencia de infarto previo y disfunción de VI significativa, la terapia fundamental de pacientes resucitados de fibrilación ventricular debe ser el DAI | Clase I (A) |
| 2. El DAI es terapia eficaz para reducir la mortalidad al reducir la muerte súbita cardiaca en pacientes con disfunción de VI por infarto previo que presentan TV sostenida hemodinamicamente inestable | Clase I (A) |
| 3. El DAI es un tratamiento razonable para la TV recurrente en pacientes postinfarto con función de VI normal o casi normal | Clase IIa (C) |
| b) Cardiopatías congénitas | |
| 1. Está indicado el implante para supervivientes de parada cardiaca tras evaluación que defina la causa del evento y excluir, cualquier causa reversible | Clase I (B) |
| 2. Los pacientes con TV sostenida espontánea requieren evaluación electrofisiológica y hemodinámica invasiva. Se recomienda el implante de DAI si la ablación con catéter o la resección quirúrgica de la TV no tienen éxito | Clase I (C) |
| 3. En ausencia de una causa definida y reversible es razonable el implante de un DAI en pacientes con síncope no explicado y disfunción ventricular | Clase IIa (B) |
| c) Miocarditis | |
| 1. El implante de un DAI puede ser beneficioso en pacientes con arritmias ventriculares graves que no están en la fase aguda de miocarditis tal y como se indica en las guías AHA/ACC/NASPE de 2002 para el implante de marcapasos o dispositivos antiarrítmicos | Clase IIa (C) |
| d) Miocardiopatías infiltrativas, enfermedades endocrinas/diabetes, fracaso renal terminal*, obesidad/anorexia | Clase I (C) |
| 1. En general, las arritmias ventriculares graves de estos pacientes deben ser tratadas de la misma forma que se tratarían en otras enfermedades, incluido el implante de marcapasos y DAI | |
| e) Miocardiopatía dilatada | |
| 1. Se debe implantar un DAI cuando hay disfunción ventricular significativa y se ha documentado TV sostenida o fibrilación ventricular | Clase I (A) |
| 2. Puede ser beneficioso el implante de un DAI en estos pacientes con síncope no explicado y disfunción de VI significativa | Clase IIa (C) |
| 3. Puede ser beneficioso el implante de un DAI para la terminación de TV sostenidas en pacientes con miocardiopatía dilatada no isquémica y función venticular normal o casi normal | Clase IIa (C) |
| f) Miocardiopatía hipertrófica | |
| 1. Se debe implantar un DAI en los pacientes que han sufrido una TV sostenida y/o fibrilación ventricular | Clase I (B) |
| g) Miocardiopatía arritmogénica ventricular derecha | |
| 1. Se recomienda el implante de DAI para prevención de muerte súbita cuando se ha documentado TV sostenida o FV | Clase I (B) |
| 2. El implante de DAI puede ser eficaz en la prevención de muerte súbita en paciente con enfermedad extensa, incluidos los que tienen disfunción de VI, familiares con muerte súbita o síncope no explicado cuando la presencia de TV o fibrilación ventricular no se han excluido como causa de éste | Clase IIa (C) |
| h) Insuficiencia cardiaca | |
| 1. Se recomienda la terapia DAI para prevención secundaria de pacientes supervivientes de una fibrilación ventricular o una TV hemodinamicamente inestable, o una TV sincopal con FEVI<40% | Clase I (A) |
| 2. Amiodarona, sotalol y/o otros betabloqueantes se recomiendan en combinación con el DAI para la supresión de arritmias ventriculares sintomáticas sostenidas y no sostenidas | Clase I (C) |
| 3. La terapia DAI es razonable para pacientes con TV estable recurrente y FEVI normal o próxima a la normalidad | Clase IIa (C) |
| i) Síndrome de QT largo | |
| 1. Se recomienda el implante de DAI junto con el uso de betabloqueantes para pacientes con el síndrome y parada cardiaca previa | Clase I (A) |
| 2. El implante de DAI junto con el uso de betabloqueantes puede ser útil para reducir la muerte súbita de estos pacientes que experimentan síncope y/o TV con tratamiento betabloqueantes | Clase IIa (B) |
| j) Síndrome de Brugada | |
| 1. Se indica un DAI para estos pacientes con una parada cardiaca previa resucitada | Clase I (C) |
| 2. El implante de un DAI es razonable en estos pacientes con un patrón ECG espontáneo y síncope | Clase IIa (C) |
| 3. Un DAI es razonable en pacientes con síndrome de Brugada y TV documentada | Clase IIa (C) |
| k) TV polimórficas catecolaminérgicas | |
| 1. Se indica el implante de un DAI junto con betabloqueantes en estos pacientes si han sobrevivido a una parada cardiaca | Clase I (C) |
| 2. Se indica el implante de un DAI junto con betabloqueantes en estos pacientes con síncope y/o TV sostenida documentada encontrándose bajo tratamiento betabloqueante | Clase IIa (C) |
| l) Arritmias en corazones estructuralmente normales | |
| 1. El implante de un DAI puede ser eficaz para la terminación de TV sostenidas en pacientes con una función ventricular normal o casi normal sin cardiopatía estructural con adecuado tratamiento médico | Clase IIa (C) |
ACC: American College of Cardiology; AHA: American Heart Association; DAI: desfibrilador automático implantable; ECG: electrocardiograma; NASPE: North American Society for Pacing and Electrophysiology; TV: taquicardia ventricular; VI: ventrículo izquierdo.
Especialmente en pacientes a la espera de trasplante renal. En general, se añade a estas recomendaciones la necesidad de un tratamiento médico crónico correcto y una expectativa de vida de al menos un año en buena situación funcional. Tomada de Zipes et al9.
Datos aportados por EUCOMED para 2006 estiman en casi 70 implantes de DAI por millón de habitantes en nuestro país, duplicando lo ocurrido en 2002. En cualquier caso, muy lejos de las ya referidas tasas de implante en Estados Unidos. Se estima que en la actualidad menos del 20% de pacientes en países desarrollados con indicación para un implante de DAI lo reciben de hecho23. En gran medida, los subgrupos analizados en los ensayos constituyen aproximadamente el 30% de todos los pacientes con riesgo de muerte súbita cardiaca24. En consecuencia, un primer reto es identificar a los subgrupos de pacientes que puedan beneficiarse de forma óptima de esta terapia mediante una mejor estratificación del riesgo. Así, en los ensayos clínicos previos que sientan la evidencia actual se ha comparado, en general, el beneficio del implante en un determinado grupo de pacientes y no se ha contrastado, sin embargo, diferentes perfiles de riesgo. Se ha llegado a señalar la generación de sistemas de puntuación que jerarquicen ese riesgo con múltiples predictores12. A los marcadores de este riesgo más clásicos se le añaden los prometedores resultados clínicos obtenidos con la microalternancia de la onda T25, que la hacen merecedora de una recomendación de clase IIa en la estratificación del riesgo de muerte súbita9. La introducción de marcadores genéticos o derivados de la proteómica podrían ser usados para esta identificación de alto riesgo que rentabilice el implante. Por otra parte, el limitante carácter estático y transversal de muchas de estas determinaciones que intentan definir un perfil de riesgo podría desaparecer en el futuro con medidas dinámicas realizadas durante períodos prolongados mediante dispositivos implantados que los analizarían en diferentes entornos de tono autonómico, situación hemodinámica, etc.23. Finalmente, las mejoras tecnológicas23 y avanzar en una comunicación abierta entre la industria, los profesionales y los pacientes que evite los desencuentros recientes acerca de la fiabilidad de los dispositivos ayudarán a una más adecuada difusión de esta terapia.
CONCLUSIONESEn conclusión, resulta clara una cierta inconsistencia en las indicaciones de implante de DAI en las distintas guías. Esto es consecuencia de la variabilidad de perfiles de riesgo definidos en los diferentes ensayos clínicos. En la opinión del autor, las últimas directrices9 aparecidas en 2006 no contribuyen suficientemente a la necesaria clarificación de dichas indicaciones. Una imprescindible depuración de los perfiles de riesgo de muerte súbita cardiaca en futuros estudios aportará mejores niveles de evidencia y perfeccionará las actuales recomendaciones de implante.