Palabras clave
INTRODUCCIÓN
El desfibrilador automático implantable (DAI), desde su introducción en la práctica clínica en 19801, ha evolucionado hasta convertirse en un complejo dispositivo multiprogramable capaz de emplear diversas terapias escalonadas para taquiarritmias ventriculares, así como estimulación antibradicardia2,3. La eficacia del DAI para evitar la muerte súbita en pacientes de alto riesgo ha sido claramente demostrada4,5; sin embargo, estos dispositivos pueden también inducir o agravar arritmias, fenómeno descrito como proarritmia6. El mecanismo más conocido consiste en la aceleración o degeneración de una taquicardia ventricular espontánea por activación de la terapia de estimulación antitaquicardia7. También se ha descrito la inducción de arritmias ventriculares por sobrestimulación o choque durante una arritmia supraventricular8 y por terapia antibradicardia inapropiada secundaria a fallos de detección9. Más infrecuente parece la proarritmia secundaria a terapia antibradicardia apropiada, es decir, a la estimulación ventricular resultante del uso correcto de la función de marcapasos del DAI. Esta forma de proarritmia ha sido descrita en casos clínicos aislados10 y en una serie de 7 pacientes11. Aunque su incidencia no parece despreciable11, hay pocos datos en la bibliografía sobre sus características y a menudo no se describe en las revisiones sobre posibles complicaciones del DAI6,12,13, por lo que es probable que algunos de estos casos pasen desapercibidos en la práctica clínica habitual. El objetivo del presente estudio es evaluar la incidencia, características y manejo de los episodios de arritmia ventricular inducidos por estimulación apropiada antibradicardia en una serie de pacientes portadores de DAI.
PACIENTES Y MÉTODO
Revisamos con carácter retrospectivo los registros de seguimiento de 180 pacientes portadores de DAI de tercera generación (con registro de electrogramas intracavitarios) seguidos en la consulta externa específica de dos hospitales de referencia entre los años 1996 y 1999.
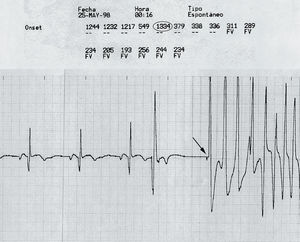
Analizamos todos los episodios espontáneos de arritmia ventricular detectados por el DAI con electrograma documentado, evaluando el registro de los intervalos RR, el electrograma de cada uno de ellos y la programación de los parámetros de marcapasos en el momento del episodio. Los episodios fueron clasificados como taquicardia ventricular (TV) o fibrilación ventricular (FV) en función de los electrogramas almacenados. Se definió como episodio inducido por la estimulación aquel que empezó inmediatamente después de un estímulo de marcapasos apropiado en un paciente con ritmo propio habitual y latidos esporádicos de marcapasos (fig. 1). En caso de existir episodios de este tipo se registraron el número y las características de los mismos, el mecanismo de comienzo (estimulación tras extrasístole, pausa durante la fibrilación auricular, estimulación por bradicardia o pausa sinusal) y los cambios de programación introducidos para intentar evitarlos, evaluando su efectividad en las revisiones sucesivas. Se revisaron los informes clínicos de los pacientes con episodios inducidos por estimulación y se registraron las variables demográficas, clínicas y el resultado del estudio electrofisiológico previo a la colocación del DAI, si fue practicado. Todas las variables recogidas fueron tabuladas para su presentación y, en su caso, se calcularon los porcentajes sobre el total de pacientes revisados.
Fig. 1. Intervalos RR y electrogramas de un episodio de inducción de taquicardia ventricular polimórfica por estimulación ventricular. Se aprecian 3 latidos sinusales seguidos de una extrasístole ventricular; tras una pausa de 1.334 ms (estaba programado a 45 lat/min) un latido de marcapasos (flecha) induce la arritmia ventricular.
RESULTADOS
De un total de 180 pacientes revisados, nueve (5%) presentaron episodios inducidos por estimulación. Las variables demográficas y clínicas de estos pacientes se describen en la tabla 1. Todos los pacientes eran varones, con edades comprendidas entre los 68 y 77 años, y la mayoría tenían cardiopatía isquémica con infarto de miocardio previo y disfunción ventricular izquierda como enfermedad de base.
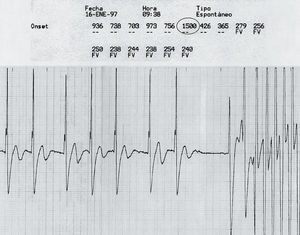
El número de episodios por paciente (tabla 2) fue muy variable y en varios de ellos (pacientes 2, 4, 5, 8 y 9) no había otro tipo de episodios registrados cuando se detectó el problema. La mayoría (7/9) recibió terapia por ellos, en todos los casos efectiva, incluyendo choques en 5 pacientes. En cuanto a la forma de inicio, observamos dos tipos: estimulación tras una pausa en la fibrilación auricular (FA) (fig. 2) y estimulación tras una pausa posterior a la extrasístole ventricular. Uno de los enfermos (paciente 3) tuvo varios episodios que empezaban tras 2 o más latidos estimulados, en el resto de los pacientes, y en la mayoría de los episodios de éste, la arritmia se iniciaba tras el primer latido estimulado. Sólo en 2 pacientes el marcapasos entraba en funcionamiento con frecuencia (pacientes 4 y 9, en el primer caso por FA lenta y en el segundo por bradicardia sinusal). Salvo en un caso, todos los pacientes presentaron este problema en los primeros meses posteriores a la colocación del DAI.
Fig. 2. Intervalos RR y electrogramas de un episodio de inducción de taquicardia ventricular monomórfica por estimulación ventricular tras pausa en fibrilación auricular. Se observan 7 latidos de fibrilación auricular y, tras una pausa de 1.500 ms (estaba programado a 40 lat/min), un latido de marcapasos induce la arritmia ventricular.
En la tabla 3 se exponen los cambios introducidos en la programación y su efectividad. En 6 pacientes se cambió el ciclo tras el cual entraba en funcionamiento el marcapasos, en todos, salvo en uno, para acortarlo. Esta medida resultó efectiva en tres de ellos: en uno se había suprimido la histéresis y en los otros dos, que empleaban el marcapasos de manera habitual, se había aumentado la frecuencia de estimulación. En 3 pacientes se disminuyó el voltaje de estimulación, procedimiento que fue efectivo en todos ellos. En dos se utilizó tras fracasar el cambio de frecuencia y en el otro como primera medida. Finalmente, en 4 pacientes se desprogramó el marcapasos basal (manteniendo la función de marcapasos poschoque): en el primero tras el fracaso de los cambios de frecuencia, en dos como primera medida y en el último como precaución, aunque la supresión de la histéresis había sido efectiva a corto plazo (paciente 3).
Tras un seguimiento medio de 24,5 meses (rango, 1-3 años), desde la última modificación en la programación no han vuelto a producirse episodios inducidos por la estimulación antibradicardia apropiada.
DISCUSIÓN
Describimos los casos de 9 pacientes portadores de DAI con episodios de arritmia ventricular sostenida inducida por estimulación apropiada tras pausa postextrasistólica o durante fibrilación auricular. Este fenómeno es un tipo de proarritmia raramente descrito en la bibliografía, siendo nuestra serie la más amplia de las publicadas hasta el momento.
Inducción de arritmias ventriculares por terapias del DAI
Se han descrito varias formas de inducción de arritmias ventriculares por el DAI. Se sabe que las terapias apropiadas de estimulación o choque pueden acelerar una TV o hacerla degenerar en FV7,14 y que las terapias antitaquicardia inapropiadas sobre arritmias supraventriculares pueden inducir una arritmia ventricular8. Existe menos información sobre la inducción de arritmias ventriculares por estimulación antibradicardia. Se ha descrito la inducción de TV por estimulación asincrónica del DAI sobre ritmo sinusal debido a fallos en la detección en 6 pacientes9,15. El mecanismo sería la captura del ventrículo por el estímulo de marcapasos durante el período vulnerable de la repolarización ventricular16. Este fenómeno es muy raro en pacientes portadores de marcapasos convencionales por bradiarritmias, como demuestra el uso rutinario del imán durante las evaluaciones del marcapasos; sin embargo, los pacientes con DAI podrían ser más vulnerables a los efectos de la estimulación asincrónica debido a la frecuente existencia de un sustrato arritmogénico. La inducción de arritmias ventriculares por terapia antibradicardia apropiada ha sido descrita en 4 pacientes con infarto de miocardio previo a los que se implantó un marcapasos VVI17. También se ha comunicado en pacientes portadores de DAI, pero los datos disponibles en la bibliografía sobre esta forma de proarritmia son escasos, pese a que parece un fenómeno relativamente frecuente. Roelke et al11 publicaron una incidencia del 6,5% (5/77) en pacientes portadores de un DAI modelo Ventitrex Cadence. Nuestra serie, más amplia y con varios modelos de desfibrilador, confirma una incidencia similar (5%). El tipo de episodio inducido puede ser taquicardia o fibrilación ventricular. Los pacientes de la serie de Roelke presentaron entre 1 y 16 episodios de TV inmediatamente precedidos por un latido estimulado, mientras en los 2 casos publicados por Vlay et al10 la estimulación antibradicardia apropiada indujo FV. Nosotros observamos tanto arritmias monomórficas como polimórficas. La frecuencia a la que estaba programado el marcapasos cuando se detectó este problema en los pacientes de nuestra serie fue de 40 a 50 latidos por minuto (lat/min), eventualmente con histéresis de 6 o 10 latidos. En otros casos publicados, la frecuencia básica del marcapasos era de 40 y 45 lat/min11. El mecanismo por el que un estímulo ventricular apropiado induce una arritmia ventricular es desconocido. En la mayor parte de los episodios de nuestra serie, el estímulo del marcapasos captura el ventrículo después de una secuencia de ciclo corto-largo. El alargamiento brusco del ciclo cardíaco podría prolongar el período refractario del miocardio ventricular de forma heterogénea, sobre todo en pacientes con enfermedad isquémica subyacente. Como resultado se generaría una dispersión aumentada de la repolarización, facilitando la inducción de arritmias por reentrada funcional18. Una respuesta repetitiva por reentrada local o a distancia provocada por el estímulo del marcapasos podría completar la secuencia de ciclo corto-largo-corto y, actuando sobre el sustrato descrito, sería el elemento desencadenante de la arritmia ventricular.
Manejo de los episodios inducidos por estimulación antibradicardia apropiada
El mecanismo descrito sugiere algunas posibilidades para evitar este tipo de proarritmia. En primer lugar, la programación de una frecuencia básica de marcapasos más elevada y/o la eliminación de la histéresis evitaría los alargamientos del ciclo, que pueden ser críticos para la iniciación de la arritmia. Esta medida fue sugerida por Roelke et al11 y en nuestra serie fue efectiva en 2 de 5 casos en los que se intentó. En un tercer paciente se suprimió inicialmente la histéresis, con lo que desaparecieron los episodios, pero unos meses después se decidió eliminar la función de marcapasos, por lo que no pudimos evaluar de forma adecuada la efectividad de la medida. Otra posibilidad consiste en reducir la frecuencia del marcapasos para disminuir el número de latidos estimulados y, con ello, la probabilidad de generar arritmias. Esta medida aislada fue ineficaz en un caso comunicado por Vlay y Vlay10, siendo asimismo inefectiva en el único paciente de nuestra serie en que se intentó. También se ha sugerido que la disminución de la energía del impulso podría ser útil para evitar este tipo de proarritmia, eficacia que se comprobó en un caso10. El mecanismo por el que actúa no está claro, pero podría estar relacionado con una disminución de las respuestas repetitivas generadas por el estímulo ventricular19. En nuestra serie, esta medida fue efectiva en los 3 pacientes en los que se ensayó (aunque en dos de ellos, además de reducir la intensidad del impulso se aumentó la duración del mismo, el efecto resultante fue de disminución de la energía entregada). Por último, si el paciente no precisa estimulación antibradicardia y el modelo de DAI lo permite, la supresión de la terapia antibradicardia basal manteniendo la estimulación post-choque es una solución radical para eliminar las arritmias inducidas por el marcapasos. Esta medida fue empleada en 4 pacientes de nuestra serie, sin incidencias atribuibles tras un seguimiento de entre 2 y 3 años.
Limitaciones
Al tratarse de un estudio retrospectivo pueden haberse perdido episodios o pacientes y es difícil establecer relaciones con variables que pudieran predecir la presentación del fenómeno. Del mismo modo, las soluciones ensayadas lo han sido de forma empírica, lo que limita su valor.
CONCLUSIONES
La incidencia de este tipo de proarritmia no parece despreciable y en algunos pacientes constituye un problema clínico relevante, por el número de episodios o por la administración de choque para su finalización. Sin embargo, las series publicadas son reducidas y la proarritmia no suele estar incluida entre las potenciales complicaciones del DAI en las revisiones sobre el tema, por lo que puede ser un problema infravalorado en la práctica diaria. Además, el diagnóstico no siempre es obvio, sobre todo si se trata de episodios esporádicos. Se deben revisar los intervalos RR al inicio de la arritmia y reconocer que el intervalo inmediatamente anterior al comienzo de la misma corresponde al intervalo programado en la función de marcapasos. La memoria de electrogramas puede ayudar a reconocer alguna secuencia característica al inicio del episodio (p. ej., ritmo sinusal, extrasístole ventricular, entrada del marcapasos tras la pausa compensadora e inicio de la taquicardia), aunque el artefacto de estimulación no suele ser discernible en el registro intracavitario bipolar. Una vez reconocido el problema, su manejo debe individualizarse y se pueden intentar, por separado o de forma combinada, las opciones comentadas con anterioridad. En pacientes con posibilidad de estimulación auricular, los sistemas de DAI bicameral podrían ayudar a resolver el problema, al evitar los ecos por reentrada secundarios al estímulo ventricular, aunque no se ha publicado ninguna experiencia clínica al respecto. Por último, la eficacia de nuevos algoritmos de estimulación que eliminan los cambios bruscos de la frecuencia cardíaca también necesita ser comprobada antes de poder recomendar su utilización en estos casos.
Correspondencia: Dr. A. García Alberola. Plaza del Roble, 36. 30150 La Alberca. Murcia. Correo electrónico: ALGAMUR@teleline.es Recibido el 30 de octubre del 2000. Aceptado para su publicación el 25 de enero del 2001.