La cardiopatía isquémica es la primera causa de insuficiencia cardiaca. Nuestro objetivo es analizar el riesgo de insuficiencia cardiaca tras un síndrome coronario agudo en pacientes sin insuficiencia cardiaca previa ni disfunción ventricular izquierda.
MétodosEstudio prospectivo de pacientes consecutivos ingresados por síndrome coronario agudo en 2 hospitales. La incidencia de insuficiencia cardiaca se analizó considerando la muerte como evento competitivo.
ResultadosSe incluyó a 5.962 pacientes, y 567 (9,5%) tuvieron al menos 1 reingreso por insuficiencia cardiaca aguda. La mediana de seguimiento fue 63 meses y la mediana de tiempo hasta el reingreso por insuficiencia cardiaca 27,1 meses. La incidencia acumulada de insuficiencia cardiaca fue superior que la de muerte en los primeros 7 años tras el alta. La edad, la diabetes, la cardiopatía isquémica previa, una escala GRACE> 140, la enfermedad arterial periférica, la disfunción renal, la hipertensión arterial y la fibrilación auricular se asociaron con mayor riesgo de reingreso por insuficiencia cardiaca; el tratamiento médico óptimo se asoció con menor riesgo. La incidencia de insuficiencia cardiaca en el primer año fue del 2,73% y no se hallaron variables protectoras. Una sencilla escala de riesgo de insuficiencia cardiaca predijo el riesgo de reingreso por insuficiencia cardiaca.
ConclusionesUno de cada 10 pacientes dados de alta tras un síndrome coronario agudo sin haber tenido antes insuficiencia cardiaca o disfunción ventricular sufrió insuficiencia cardiaca de novo y el riesgo es superior que el de muerte. Una sencilla escala clínica permite estimar el riesgo individual de reingreso por insuficiencia cardiaca, incluso en pacientes que no han tenido antes insuficiencia cardiaca ni disfunción ventricular izquierda.
Palabras clave
La incidencia de insuficiencia cardiaca (IC) crónica ha aumentado de modo exponencial en las últimas décadas1,2, por lo que la detección de los factores de riesgo asociados con su incidencia debe ser un objetivo importante de investigación3. La enfermedad coronaria es la principal causa de IC1,4. El síndrome coronario agudo (SCA) es la forma de presentación más frecuente de la enfermedad coronaria y la que produce el mayor daño miocárdico. La presencia de un infarto de miocardio, ya sea en forma de un SCA o de un evento silente, aumenta la incidencia a largo plazo de la IC4,5 en hasta un 30%.
La IC hospitalaria es uno de los más potentes factores predictivos de la incidencia de IC tras el alta, con independencia de la fracción de eyección del ventrículo izquierdo (FEVI)6; no obstante, la mayor parte de los pacientes con SCA no presentan disfunción del ventrículo izquierdo (VI) ni IC6–9 y la evidencia de factores de riesgo relacionados con la incidencia de la IC a largo plazo o los tratamientos con mayor efecto protector es escasa5,7, posiblemente porque se prevé que la incidencia sea baja. Recientemente se ha propuesto una puntuación de riesgo para identificar a los pacientes con un mayor riesgo de IC después de un SCA, pero dicha puntuación incluye los episodios previos de IC y FEVI < 50%10.
El objetivo del presente estudio es describir la incidencia y los factores de riesgo de la incidencia de IC a corto y a largo plazo, en una amplia cohorte de pacientes con SCA y sin antecedentes de IC o disfunción del VI.
MÉTODOSDiseño del estudioSe llevó a cabo un estudio prospectivo de todos los pacientes consecutivos ingresados por un SCA en 2 centros entre 2006 y 2016. Ingresaron por un SCA entre noviembre de 2003 y diciembre de 2016 un total de 8.771 pacientes. Se excluyo a los pacientes que fallecieron durante la hospitalización (n=450), los que sufrieron IC durante la hospitalización (n=1.641), los diagnosticados de IC antes del SCA (n=349) y los que que tenían una FEVI < 50% determinada en el SCA índice de cualificación para el estudio. Finalmente se incluyó en el presente estudio a 5.237 pacientes (figura 1 del material adicional). El SCA se definió como la presencia de síntomas clínicos característicos de dolor torácico y alteraciones electrocardiográficas compatibles con isquemia o lesión miocárdica y/o una elevación de los marcadores séricos de daño miocárdico11.
El objetivo principal es evaluar la incidencia de una primera hospitalización por IC y el objetivo secundario, la incidencia de IC en el primer año siguiente al SCA. El diagnóstico de IC se codificó según lo que constaba en los informes firmados por el personal médico de cada centro, y se basó principalmente en los criterios diagnósticos de las guías clínicas12. El SCA se clasificó como un infarto agudo de miocardio con elevación del segmento ST y un SCA sin elevación del segmento ST según los signos electrocardiográficos. El riesgo de mortalidad se evaluó con la puntuación GRACE11 y se clasificó a los pacientes según las recomendaciones actuales en los niveles de riesgo bajo (< 108), intermedio (109-139) o alto (> 140). Se evaluó el riesgo de reingreso por IC según la puntuación de IC de CardioCHUS-SanJuan10; se dividió a los pacientes en las 3 categorías de riesgo propuestas en el artículo original (< 9, riesgo bajo; 9-15, riesgo intermedio; > 15, riesgo alto de reingreso por IC). Se determinó la revascularización completa después de la intervención, utilizando el criterio de revascularización «anatómica equivalente» pretendida antes de la intervención, basándose en la numeración de segmentos de los vasos de diámetro > 1,5 mm10.
Personal médico adecuadamente capacitado recogió la información sobre factores de riesgo, antecedentes clínicos, tratamientos, exploraciones complementarias y diagnóstico principal al alta de los pacientes. Los protocolos de diagnóstico y tratamiento del SCA de ambos centros incluyen análisis de sangre en el servicio de urgencias y en ayunas tras el ingreso en el hospital. El filtrado glomerular se estimó a partir de los valores de creatinina en suero con la ecuación de CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration). Para establecer enfermedad coronaria previa, el paciente debía tener un diagnóstico clínico de infarto de miocardio, angina estable o inestable o revascularización coronaria motivada por angina. Se asignó el código de IC previa a los pacientes que habían tenido como mínimo 1 hospitalización con este diagnóstico principal en el informe médico de alta, así como a los que habían tenido sígnos y síntomas característicos de la IC y un diagnóstico compatible en las exploraciones de imagen (radiografía o ecocardiografía). Las comorbilidades se evaluaron con el índice de Charlson, adaptado para los pacientes con enfermedad cardiovascular13, y se consideró que tenían una carga de comorbilidad elevada los que presentaban una puntuación de Charlson > 4. Según lo establecido en las recomendaciones actuales, se consideró que había un tratamiento médico óptimo cuando los pacientes recibían conjuntamente estos 4 tratamientos: antiagregantes plaquetarios, estatinas, bloqueadores beta y un inhibidor de la enzima de conversión de la angiotensina o un antagonista del receptor de la angiotensina II14,15.
El seguimiento de los pacientes tras el alta está especificado en un protocolo bien establecido en cada centro y se realiza mediante llamadas telefónicas y examen de la historia clínica electrónica y las bases de datos de los centros. En caso de ausencia de informes médicos, se verificó la supervivencia mediante llamadas telefónicas. El protocolo del estudio fue aprobado por el comité de ética del hospital que realizaba la coordinación.
Análisis estadísticoLas variables cuantitativas se presentan en forma de media ± desviación estándar y las diferencias se evaluaron mediante la prueba de la t de Student o la prueba de la χ2. Las variables cualitativas se presentan en forma de porcentajes y diferencias y se analizaron con la prueba de ANOVA. Los análisis de la supervivencia se llevaron a cabo tras la verificación del supuesto de riesgos proporcionales mediante la prueba de residuos de Schoenfied. La incidencia de IC tras el alta podía verse afectada por la muerte del paciente y, por consiguiente, las técnicas habituales de análisis de tiempo hasta el evento habrían aportado unos resultados sesgados o ininterpretables debido a la presencia de riesgos competitivos, y la estimación de Kaplan-Meier podría sobrestimar la incidencia real de la IC10,16. Para evitar estos efectos, se aplicó el modelo introducido por Fine y Gray17 para evaluar los eventos competitivos. La incidencia de la IC se presenta mediante gráficos de función de incidencia acumulada y los resultados del análisis multivariante, mediante una subhazard ratio (sHR) con los correspondientes intervalos de confianza del 95% (IC95%). Se utilizó el estadígrafo c de Harrell para evaluar la discriminación del modelo, mientras que la calibración se evaluó con la prueba de Gronnesby y Borgan. A los pacientes perdidos para el seguimiento se los clasificó como no disponibles, al igual que aquellos de los que faltaba alguna de las variables principales para los análisis, aunque estos fueron muy pocos. Se evaluó la capacidad predictiva de la puntuación de riesgo de IC CardioCHUS-SanJuan10 mediante el área bajo la curva de características operativas del receptor de la puntuación.
Se asumió la significación estadística con un valor de p < 0,05. Todos los análisis se realizaron con el programa STATA 14.3 (Stata Statistical Software Versión 14; StataCorp., 2009; College Station, Estados Unidos).
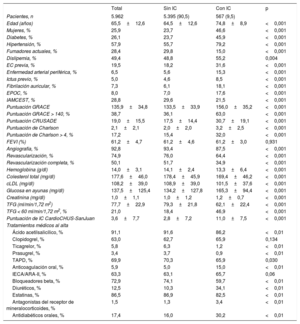
RESULTADOSSe incluyó a 5.962 pacientes dados de alta del hospital tras sufrir un SCA y 567 (9,5%; IC95%, 8,3-9,8) tuvieron como mínimo 1 reingreso hospitalario por IC aguda durante el periodo de seguimiento. En la tabla 1 se muestran las características clínicas de la cohorte. Los pacientes que sufrieron una IC tenían una media de edad superior, eran con mayor frecuencia mujeres y tenían una mayor prevalencia de factores de riesgo cardiovascular y comorbilidades. Por lo que respecta al SCA índice, en los pacientes que tuvieron IC era menos frecuente el infarto agudo de miocardio con elevación del segmento ST, pero las puntuaciones GRACE eran más altas. La media de la puntuación de riesgo de IC CardioCHUS-SanJuan fue significativamente superior en los pacientes con una IC. Se observaron también diferencias pequeñas, pero significativas, en los tratamientos médicos al alta.
Características clínicas de la cohorte según los pacientes sufrieran una insuficiencia cardiaca (IC) de novo o no
| Total | Sin IC | Con IC | p | |
|---|---|---|---|---|
| Pacientes, n | 5.962 | 5.395 (90,5) | 567 (9,5) | |
| Edad (años) | 65,5±12,6 | 64,5±12,6 | 74,8±8,9 | <0,001 |
| Mujeres, % | 25,9 | 23,7 | 46,6 | <0,001 |
| Diabetes, % | 26,1 | 23,7 | 45,9 | <0,001 |
| Hipertensión, % | 57,9 | 55,7 | 79,2 | <0,001 |
| Fumadores actuales, % | 28,4 | 29,8 | 15,0 | <0,001 |
| Dislipemia, % | 49,4 | 48,8 | 55,2 | 0,004 |
| EC previa, % | 19,5 | 18,2 | 31,6 | <0,001 |
| Enfermedad arterial periférica, % | 6,5 | 5,6 | 15,3 | <0,001 |
| Ictus previo, % | 5,0 | 4,6 | 8,5 | <0,001 |
| Fibrilación auricular, % | 7,3 | 6,1 | 18,1 | <0,001 |
| EPOC, % | 8,0 | 7,0 | 17,6 | <0,001 |
| IAMCEST, % | 28,8 | 29,6 | 21,5 | <0,001 |
| Puntuación GRACE | 135,9±34,8 | 133,5±33,9 | 156,0±35,2 | <0,001 |
| Puntuación GRACE > 140, % | 38,7 | 36,1 | 63,0 | <0,001 |
| Puntuación CRUSADE | 19,0±15,5 | 17,5±14,4 | 30,7±19,1 | <0,001 |
| Puntuación de Charlson | 2,1±2,1 | 2,0±2,0 | 3,2±2,5 | <0,001 |
| Puntuación de Charlson > 4, % | 17,2 | 15,4 | 32,0 | <0,001 |
| FEVI (%) | 61,2±4,7 | 61,2±4,6 | 61,2±3,0 | 0,931 |
| Angiografía, % | 92,8 | 93,4 | 87,5 | <0,001 |
| Revascularización, % | 74,9 | 76,0 | 64,4 | <0,001 |
| Revascularización completa, % | 50,1 | 51,7 | 34,9 | <0,001 |
| Hemoglobina (g/dl) | 14,0±3,1 | 14,1±2,4 | 13,3±6,4 | <0,001 |
| Colesterol total (mg/dl) | 177,6±46,0 | 178,4±45,9 | 169,4±46,2 | <0,001 |
| cLDL (mg/dl) | 108,2±39,0 | 108,9±39,0 | 101,5±37,6 | <0,001 |
| Glucosa en ayunas (mg/dl) | 137,5±125,4 | 134,2±127,8 | 165,3±94,4 | <0,001 |
| Creatinina (mg/dl) | 1,0±1,1 | 1,0±1,2 | 1,2±0,7 | <0,001 |
| TFG (ml/min/1,72 m2) | 77,7±22,9 | 79,3±21,8 | 62,1±22,4 | <0,001 |
| TFG < 60 ml/min/1,72 m2, % | 21,0 | 18,4 | 46,9 | <0,001 |
| Puntuación de IC CardioCHUS-SanJuan | 3,6±7,7 | 2,8±7,2 | 11,0±7,5 | <0,001 |
| Tratamientos médicos al alta | ||||
| Ácido acetilsalicílico, % | 91,1 | 91,6 | 86,2 | <0,01 |
| Clopidogrel, % | 63,0 | 62,7 | 65,9 | 0,134 |
| Ticagrelor, % | 5,8 | 6,3 | 1,2 | <0,01 |
| Prasugrel, % | 3,4 | 3,7 | 0,9 | <0,01 |
| TAPD, % | 69,9 | 70,3 | 65,9 | 0,030 |
| Anticoagulación oral, % | 5,9 | 5,0 | 15,0 | <0,01 |
| IECA/ARA-II, % | 63,3 | 63,1 | 65,7 | 0,06 |
| Bloqueadores beta, % | 72,9 | 74,1 | 59,7 | <0,01 |
| Diuréticos, % | 12,5 | 10,3 | 34,1 | <0,01 |
| Estatinas, % | 86,5 | 86,9 | 82,5 | <0,01 |
| Antagonistas del receptor de mineralocorticoides, % | 1,5 | 1,3 | 3,4 | <0,01 |
| Antidiabéticos orales, % | 17,4 | 16,0 | 30,2 | <0,01 |
ARA-II: antagonistas del receptor de la angiotensina II; cLDL: colesterol unido a lipoproteínas de baja densidad; EC: enfermedad coronaria; EPOC: enfermedad pulmonar obstructiva crónica; FEVI: fracción de eyección del ventrículo izquierdo; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; IC: insuficiencia cardiaca; IECA: inhibidores de la enzima de conversión de la angiotensina; TAPD: tratamiento antiagregante plaquetario combinado doble; TFG: tasa de filtrado glomerular.
Salvo otra indicación, los valores expresan n (%) o media ± desviación estándar.
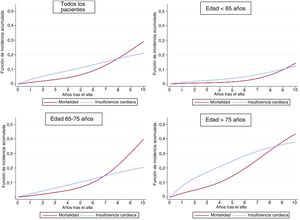
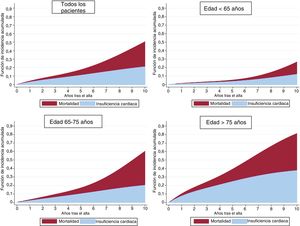
Se dispuso de seguimiento del 98,4% de la cohorte, con una mediana [intervalo intercuartílico] de seguimiento de 63,0 [31-82] meses. Fallecieron en total 998 pacientes (16,7%), y 625 casos (10,5%) fueron atribuibles a causas cardiovasculares. La mediana de tiempo transcurrido hasta el ingreso por IC fue de 31 [8-53] meses. Tal como se muestra en la figura 1, la incidencia acumulada de IC mostró un aumento lineal y fue mayor que la mortalidad en los primeros 7 años siguientes al SCA índice; la incidencia acumulada de mortalidad fue bastante baja en el primer año siguiente al alta hospitalaria.
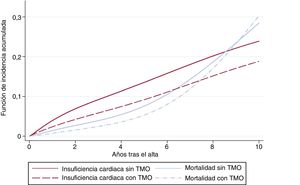
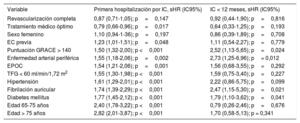
En la tabla 2 se muestran los resultados de la regresión de riesgos competitivos, ajustada por las variables edad, sexo, factores de riesgo, enfermedad cardiovascular previa, tratamientos médicos, FEVI y revascularización. Muchos factores de riesgo se asociaron con mayor riesgo de IC; la edad fue el factor de riesgo principal y sus efectos se intensificaban a medida que aumentaba (figura 2); la única variable asociada con un menor riesgo de IC fue el tratamiento médico óptimo (figura 3). El modelo mostró una buena capacidad de discriminación (estadígrafo c de Harrell = 0,81; IC95%, 0,79-0,82; p < 0,001) y se calibró con exactitud (p = 0,71) (figura 4).
Resultados del análisis de regresión de riesgos competitivos en la incidencia de insuficiencia cardiaca
| Variable | Primera hospitalización por IC, sHR (IC95%) | IC < 12 meses, sHR (IC95%) |
|---|---|---|
| Revascularización completa | 0,87 (0,71-1,05); p=0,147 | 0,92 (0,44-1,90); p=0,816 |
| Tratamiento médico óptimo | 0,79 (0,66-0,96); p=0,017 | 0,64 (0,33-1,25); p=0,193 |
| Sexo femenino | 1,10 (0,94-1-36); p=0,197 | 0,86 (0,39-1,89); p=0,708 |
| EC previa | 1,23 (1,01-1,51); p=0,048 | 1,11 (0,54-2,27); p=0,779 |
| Puntuación GRACE > 140 | 1,50 (1,32-2,00); p <0,001 | 2,52 (1,13-5,65); p=0,024 |
| Enfermedad arterial periférica | 1,55 (1,18-2,06); p=0,002 | 2,73 (1,25-6,96); p= 0,012 |
| EPOC | 1,54 (1,21-2,06); p=0,001 | 1,56 (0,68-3,55); p=0,292 |
| TFG < 60 ml/min/1,72 m2 | 1,55 (1,30-1,98); p <0,001 | 1,59 (0,75-3,40); p=0,227 |
| Hipertensión | 1,61 (1,29-2,01); p <0,001 | 2,22 (0,86-5,75); p=0,099 |
| Fibrilación auricular | 1,74 (1,39-2,29); p <0,001 | 2,47 (1,15-5,30); p=0,021 |
| Diabetes mellitus | 1,77 (1,45-2,12); p <0,001 | 1,79 (1,10-3,62); p=0,041 |
| Edad 65-75 años | 2,40 (1,78-3,22); p <0,001 | 0,79 (0,26-2,46); p=0,676 |
| Edad > 75 años | 2,82 (2,01-3,87); p <0,001 | 1,70 (0,58-5,13); p = 0,341 |
EC: enfermedad coronaria; EPOC: enfermedad pulmonar obstructiva crónica; IC: insuficiencia cardiaca; IC95%: intervalo de confianza del 95%; sHR: sub-hazard ratio; TFG: tasa de filtrado glomerular.
Se evaluó la incidencia de IC en el primer año de seguimiento. En este periodo, 163 pacientes (2,73%; IC95%, 2,31-3,14) ingresaron por una IC aguda, mientras que la mortalidad fue < 1%. La mediana de tiempo hasta el reingreso fue de 111 [37-218] días. Tal como se muestra en la tabla 2, la diabetes, la fibrilación auricular, la escala GRACE > 140 y la enfermedad periférica fueron las variables asociadas con mayor riesgo de IC en el primer año siguiente al SCA, y no se identificó ninguna variable con un efecto protector. El modelo mostró una capacidad de discriminación aún mejor (estadígrafo c de Harrell = 0,84; IC95%, 0,77-0,90; p < 0,001) y se calibró con exactitud (p = 0,69). El área bajo la curva de la puntuación de riesgo de IC CardioCHUS-SanJuan (figura 2 del material adicional) para la predicción del primer reingreso por IC fue de 0,78 (IC95%, 0,76-0,79; p < 0,01) y para el reingreso durante el primer año fue de 0,79 (IC95%, 0,77-0,82).
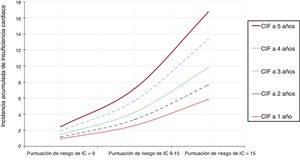
Dado que la mayor parte de las variables clínicas asociadas con un reingreso por IC se incluían en la puntuación de riesgo de IC CardioCHUS-SanJuan, se evaluó la incidencia de las categorías de riesgo de IC. Tal como se muestra en la figura 5, hubo un aumento gradual de la incidencia anual de reingresos por IC en cada categoría de riesgo. El análisis multivariante puso de manifiesto que los pacientes con una puntuación de riesgo de IC CardioCHUS-SanJuan de 9-15 (sHR = 1,51; IC95%, 1,20-1,90; p < 0,001) y especialmente aquellos con una puntuación > 15 (sHR = 2,38; IC95%, 1,83-3,09) mostraban un aumento del riesgo de reingreso por IC.
DISCUSIÓNEl objetivo de nuestro estudio es describir la IC de nueva aparición en pacientes dados de alta tras un SCA, a los que generalmente se considera con riesgo bajo de IC, ya que no tienen disfunción del VI ni antecedentes de IC. No obstante, el seguimiento a largo plazo de nuestro estudio resalta que un 10% de estos pacientes sufrieron una IC de novo y que hay muchas variables que muestran una asociación positiva con esta complicación de gran importancia. La IC en el primer año después del alta fue menos frecuente y se asoció con apenas unos pocos factores de riesgo. Dado que las manifestaciones clínicas y las tasas de mortalidad fueron similares a las de estudios previos4,8,9,18–23, creemos que nuestros resultados podrían ser representativos de lo que sucede en la práctica clínica diaria. Creemos también que nuestros resultados tienen consecuencias importantes en el tratamiento agudo y a largo plazo de los pacientes ingresados por un SCA.
La incidencia y la prevalencia de la IC han aumentado en las últimas décadas a causa de múltiples variables, como la mayor esperanza de vida, el aumento de los factores de riesgo12,24,25 y las reducciones de la mortalidad hospitalaria de los pacientes ingresados por un SCA; todos estos factores generan una población cada vez mayor de pacientes con alto riesgo de sufrir eventos recurrentes4,7,10,26,27, y recientemente la guía de 2019 de la Sociedad Europea de Cardiología ha utilizado para ello el término síndrome coronario crónico28. Así pues, el tratamiento hospitalario y a largo plazo del SCA es algo a lo que hay que dedicar la máxima consideración para prevenir complicaciones posteriores y mejorar los resultados. Las reducciones de la mortalidad hospitalaria y la revascularización o la reperfusión se han establecido claramente como indicadores de la calidad del tratamiento del SCA29, pero los eventos recurrentes tienen una gran repercusión en el pronóstico y deben tenerse también en cuenta. Los eventos no mortales recurrentes influyen de manera notable en la calidad de vida de los pacientes y, lo que tiene aún mayor interés, aumentan la mortalidad al doble en los 2 años siguientes30. Este efecto adquiere una importancia mucho mayor cuando el evento recurrente consiste en una hospitalización por IC, ya que ello se asocia con un incremento del riesgo de muerte en más del cuádruple19,23.
Nuestro estudio pone de manifiesto que 1 de cada 10 pacientes dados de alta con un diagnóstico de SCA tendrá como mínimo 1 reingreso hospitalario por IC en los primeros 5 años siguientes al SCA índice, lo cual es muy superior a la incidencia de otras complicaciones como la hemorragia mayor8,31 o el ictus26. Las hospitalizaciones por IC tienen un fuerte impacto en la familia y los recursos de los pacientes12 y, por consiguiente, merecen la máxima consideración. Se ha demostrado que los protocolos de seguimiento específicos tras el alta, como los de los programas de rehabilitación cardiaca32 o las unidades especializadas27, aportan beneficios en cuanto al control de los factores de riesgo, así como en la reducción de la mortalidad y los reingresos; creemos que nuestros resultados podrían ser útiles para identificar a los pacientes con mayor riesgo de sufrir una IC de novo. Además, la puntuación CardioCHUS-SanJuan tiene una utilidad fiable para la detección de los pacientes con alto riesgo de reingreso por IC.
Se evaluó la capacidad diagnóstica de una puntuación de riesgo específicamente diseñada para predecir el reingreso por IC después de sufrir un SCA10. El área bajo la curva del modelo de la cohorte original, que incluía a pacientes con antecedentes de IC o disfunción del VI, fue de 0,77 (IC95%, 0,76-0,78) y los resultados de nuestro estudio fueron muy similares y coincidentes con los de la publicación original. Un registro similar de pacientes que habían sufrido un SCA, también de España, propuso un riesgo basado en 4 variables que mostró un valor preventivo similar (estadístico c = 0,74)23. Ambas puntuaciones de riesgo tienen varias variables en común, como la edad, la hipertensión y el filtrado glomerular < 60 ml/min/1,72 m2, si bien la puntuación de IC CardioCHUS-SanJuan incluye también la revascularización completa, la diabetes y el tratamiento médico óptimo. No obstante, las variables incluidas en el otro registro fueron las que mostraron resultados estadísticamente significativos en el presente estudio, lo cual respalda el valor de ambas puntuaciones y ambos estudios. Además, creemos que esto refleja la creciente preocupación existente respecto a la incidencia de la IC tras el SCA y la falta de evidencia fiable y contemporánea en este campo.
La revascularización es la piedra angular del tratamiento de la SCA. La revascularización completa se incluyó en la puntuación de riesgo de IC CardioCHUS-SanJuan porque mostraba una asociación independiente con una menor frecuencia de reingresos por IC, pero esto se reprodujo en el presente análisis. El SCA es el momento de máximo daño miocárdico, y se ha demostrado que la revascularización11, los bloqueadores beta33 y los antagonistas del receptor de la angiotensina II34 reducen el daño miocárdico y el remodelado del VI, a la vez que aportan una mejora de la supervivencia. La revascularización completa no se asoció con una menor frecuencia de reingresos por IC en esta cohorte de pacientes con FEVI > 50%, a diferencia de lo observado en la publicación original, y ello podría reflejar el efecto menos determinante en los pacientes con un menor daño miocárdico, cuando menos en lo relativo a la IC posterior.
En cambio, el efecto del tratamiento médico óptimo, que consistía en la combinación de antiagregantes plaquetarios, estatinas, bloqueadores beta, inhibidores de la enzima de conversión de la angiotensina o antagonistas del receptor de la angiotensina II, mostró una asociación positiva con un menor riesgo de reingreso por IC. El tratamiento médico óptimo ha resultado eficiente para la reducción de los eventos cardiovasculares mayores en pacientes con angina estable o con una cardiopatía coronaria crónica14,15 y nuestros resultados respaldan el efecto favorable en cuanto a la prevención del reingreso por IC.
La prevención del desarrollo precoz de una IC después de un SCA constituye un verdadero reto clínico12,23. Tan solo un 3,8% de nuestra población tuvo un reingreso por IC en los 12 meses siguientes al alta tras el SCA, y ello refleja que la carga de ingresos por IC debe evaluarse a largo plazo; no obstante, se identificó que la diabetes y la arteriopatía periférica eran los principales factores de riesgo de reingreso por una IC prematura durante el primer año, y ello podría reflejar la presencia de un daño cardiaco subyacente antes del SCA o una mayor extensión del daño durante este. Una nueva familia de medicamentos antidiabéticos, los inhibidores de SGLT-2, han aportado evidencia sólida respecto al reingreso por IC de los pacientes con alto riesgo y diabetes35 o incluso con IC y disfunción del VI, con independencia de la diabetes mellitus36; nuestros resultados podrían definir una población específica de pacientes que obtienen un especial beneficio con estos fármacos. Los pacientes con diabetes e IC tienen muy mal pronóstico, puesto que la tasa de mortalidad a 5 años es > 55%37, y ello refleja una necesidad médica insatisfecha de tratamientos eficaces para estos pacientes con muy alto riesgo. Un uso muy prematuro de bloqueadores beta en el SCA podría elevar el riesgo de shock cardiogénico o IC33, lo cual podría explicar la ausencia de beneficio con los bloqueadores beta en el reingreso por IC durante el primer año.
Nuestro estudio tiene ciertas limitaciones. En primer lugar, como todos los estudios prospectivos observacionales, tiene algunas limitaciones inherentes como la ausencia de aleatorización, la diversidad a largo plazo de los tratamientos médicos o las variables no controladas, en especial la fragilidad, que tiene consecuencias muy importantes en los pacientes con IC o SCA38. La aparición de la IC podría haberse subestimado, pero dado que se analizaron solo los reingresos hospitalarios, creemos que se incluyeron todos los casos reales de IC y no se tuvo en cuenta otros casos de disnea o trastornos respiratorios. Dado que el periodo de inclusión fue razonablemente largo, el uso de ticagrelor y prasugrel fue bastante bajo, lo cual podría corresponderse bastante bien con el tratamiento actual del SCA, aunque no hay evidencias respecto al papel del tratamiento antiagregante plaquetario en la incidencia de la IC39. Por último, se evaluó solo el tiempo transcurrido hasta el primer ingreso hospitalario y no se analizaron las hospitalizaciones por IC posteriores, que podrían haber aportado una visión más realista del pronóstico real40. Dado que las manifestaciones clínicas y la incidencia de los eventos a largo plazo son similares a lo observado en estudios previos4,8,9,18–23,41, creemos que las limitaciones mencionadas no habrían tenido una repercusión importante en nuestros resultados.
En conclusión, 1 de cada 10 pacientes dados de alta tras un SCA que no tienen antecedentes de IC o disfunción del VI tuvieron como mínimo 1 reingreso por IC. La revascularización completa y los bloqueadores beta tuvieron un efecto protector. Una puntuación clínica tiene una buena capacidad predictiva para la evaluación de los pacientes con mayor riesgo de reingreso por IC después de un SCA y podría ser útil para el seguimiento de estos pacientes.
CONFLICTO DE INTERESESLos autores declaran no tener ningún conflicto de intereses en relación con los resultados de este estudio.
- –
La enfermedad coronaria es la principal causa de IC.
- –
La IC durante la hospitalización por un SCA es el principal factor determinante de una IC posterior.
- –
La aparición de una IC implica un empeoramiento del pronóstico y un deterioro de la calidad de vida.
- –
Uno de cada 10 pacientes sufrirá IC después de un SCA, aunque no haya disfunción del VI ni antecedentes de IC.
- –
En esos pacientes, el riesgo de IC es superior al riesgo de muerte.
- –
El tratamiento médico óptimo reduce el riesgo de IC en este tipo de pacientes.
Los autores de este estudio recibieron apoyo del Centro de Investigación Biomédica en Red de Enfermedades Cardiovasculares (CIBERCV CB16/11/00226 - CB16/11/00420), la Red Nacional Española de Investigación Biomédica en Enfermedades Cardiovasculares.