La enfermedad de Becker es una entidad comprendida entre los trastornos musculares ligados al cromosomaX. Se produce por una mutación en el gen Xp21, que codifica la distrofina1. Esta es una proteína presente tanto en el músculo esquelético como en el músculo cardiaco, por lo que esta enfermedad puede cursar con daño miopático y síntomas cardiovasculares.
El inicio clínico de los pacientes con enfermedad de Becker suele ocurrir a partir de la segunda década de la vida y se manifiesta habitualmente por debilidad de la musculatura de la cintura pelviana2. El daño cardiaco es poco frecuente como forma de presentación, aunque puede ocurrir en algunos casos3,4. La miocardiopatía dilatada es la cardiopatía más frecuente en estos individuos2.
Para los pacientes con distrofia de Becker e insuficiencia cardiaca refractaria, el trasplante cardiaco (TxC) es una opción terapéutica que considerar; no obstante, hay cierto grado de controversia1,3,4. Las dudas que se plantean a la hora de decidir si un paciente con enfermedad de Becker puede ser o no candidato a trasplante cardiaco derivan fundamentalmente de su potencial riesgo perioperatorio, la posibilidad de realizar fisioterapia respiratoria y rehabilitación locomotriz tras la intervención y la posible progresión de la miopatía como consecuencia del tratamiento esteroideo inherente al estado tras el TxC. En este artículo se presenta una breve serie de pacientes con miocardiopatía dilatada relacionada con la enfermedad de Becker que recibieron TxC en un único centro.
Desde 1991 hasta 2017, 781 pacientes recibieron TxC en la institución objeto de estudio. De ellos, 6(0,8%) presentaban un diagnóstico de miocardiopatía dilatada relacionada con la enfermedad de Becker. Las características clínicas basales de estos individuos se resumen en la tabla.
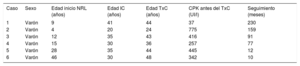
Características basales
| Caso | Sexo | Edad inicio NRL (años) | Edad IC (años) | Edad TxC (años) | CPK antes del TxC (UI/l) | Seguimiento (meses) |
|---|---|---|---|---|---|---|
| 1 | Varón | 9 | 41 | 44 | 37 | 230 |
| 2 | Varón | 4 | 20 | 24 | 775 | 159 |
| 3 | Varón | 12 | 35 | 43 | 416 | 91 |
| 4 | Varón | 15 | 30 | 36 | 257 | 77 |
| 5 | Varón | 28 | 35 | 44 | 445 | 12 |
| 6 | Varón | 46 | 30 | 48 | 342 | 10 |
CPK: creatincinasa; IC: insuficiencia cardiaca; NRL: neurológico; TxC: trasplante cardiaco.
La mediana de edad en el momento del diagnóstico de la distrofinopatía era 13,5años. El inicio clínico de insuficiencia cardiaca aconteció a una mediana de edad de 32,5años y el TxC se realizó a una mediana de edad de 43,5años. El TxC se realizó de urgencia en 4casos (67%). En el momento de la inclusión en lista de espera, todos los pacientes presentaban daño muscular de grado leve y completa autonomía funcional, sin daño ventilatorio significativo.
Todos los pacientes recibieron inmunosupresión con inhibidores de la calcineurina (ciclosporina o tacrolimus) y micofenolato mofetilo, excepto 1paciente que recibó azatioprina. Todos los pacientes recibieron esteroides indefinidamente, si bien la dosis se minimizó en la medida de lo posible (objetivo de mantenimiento, prednisona ≤5mg/día) a partir del sexto mes tras el TxC. Todos los pacientes recibieron tratamiento con estatinas, pero en 2casos (33,3%) se suspendió por toxicidad muscular con elevación marcada de las cifras de creatincinasa sérica.
En el periodo posoperatorio inmediato, 3 pacientes (50%) presentaron insuficiencia renal aguda que precisó diálisis; 2(33%), encefalopatía reversible posterior asociada con inhibidores de la calcineurina, y 1(17%), hipertensión arterial grave de difícil control. Se extubó durante las primeras 24h tras la cirugía a 2pacientes (33%), mientras que la extubación de los 4 restantes fue retardada (entre 5 y 13 días tras la intervención). No se observaron episodios de disfunción precoz del injerto que precisase asistencia circulatoria mecánica ni mortalidad posoperatoria inmediata.
Todos los pacientes sobrevivieron a largo plazo tras el TxC, con un periodo de seguimiento medio de 96(intervalo, 10-230) meses. Hasta el momento actual, solo 1de los pacientes ha fallecido 19años después de la intervención, como consecuencia de una neoplasia pulmonar. Los 5pacientes restantes están vivos y presentan una función del injerto conservada. No se detectaron, hasta el momento, episodios de rechazo del injerto con deterioro hemodinámico en estos individuos. En 3pacientes, tras el trasplante se observó progresión lenta del daño muscular hasta que ha requerido silla de ruedas para la movilización.
La evidencia disponible en la literatura médica, aunque escasa por la poca cantidad de casos comunicados, indica que los resultados a largo plazo del TxC en pacientes afectados de distrofinopatía de Becker son comparables a los de la población general de receptores de TxC por otras cardiopatías4.
Los resultados observados en esta cohorte de receptores de TxC con enfermedad de Becker resultan satisfactorios, con una larga supervivencia y buen pronóstico funcional, lo que refleja una adecuada tolerancia al tratamiento inmunosupresor. Se concluye, por lo tanto, que el TxC puede ser una buena alternativa para pacientes seleccionados, con distrofia muscular de Becker e insuficiencia cardiaca refractaria que presentan una relativa preservación de la función muscular extracardiaca antes de la intervención.