La presión arterial (PA) ambulatoria predice el riesgo de enfermedad cardiovascular (ECV) mejor que las mediciones clínicas (MCPA). Sin embargo, los modelos actuales de estratificación del riesgo de ECV se basan exclusivamente en las MCPA junto con otros factores tradicionales, como edad, sexo, tabaquismo, dislipemia y diabetes.
MétodosSe utilizaron los datos de 19.949 participantes en el Proyecto Hygia, evaluados con monitorización ambulatoria de la PA (MAPA) de 48 h, para comparar la precisión, la discriminación y el rendimiento de la escala de Framingham original (RSOFG) y su versión ajustada a la población del Proyecto Hygia (RSAFG) con un nuevo modelo en el que la MCPA se reemplazó con parámetros pronósticos derivados de la MAPA (RSABPM).
ResultadosTras un seguimiento de hasta 12,7 años, 1.854 participantes sufrieron un evento de ECV (muerte CV, infarto, revascularización, insuficiencia cardiaca, ictus, accidente isquémico transitorio, angina o enfermedad arterial periférica). La media de la PA sistólica (PAS) durante el sueño y la disminución relativa de la PAS en actividad/sueño fueron los marcadores significativos del riesgo de ECV y, por ello, se utilizaron como sustitutos de la MCPA en el modelo RSABPM. Este modelo, en comparación con la RSOFG y la RSAFG, presentó calibración, precisión diagnóstica, discriminación y rendimiento significativamente mayores (p <0,001). La probabilidad de evento derivada del modelo RSAFG del 57,3% de los participantes estuvo fuera del intervalo de confianza individualizado de probabilidad calculado a partir del modelo RSABPM.
ConclusionesLos resultados documentan importantes limitaciones de la estratificación del riesgo de ECV basada en MCPA, incluidas las del modelo de Framingham, y corroboran el valor de la MAPA para diagnosticar hipertensión y estratificar el riesgo de ECV.
Palabras clave
En numerosos ensayos se ha demostrado que la asociación entre la presión arterial (PA) y el riesgo de daño del órgano afectado y de enfermedad cardiovascular (ECV) es mucho más sólida para los parámetros obtenidos a partir de la monitorización ambulatoria de la PA (MAPA) que para las mediciones clínicas de la PA (MCPA)1–6. Por otro lado, investigaciones independientes han demostrado que los eventos de ECV se predicen mucho mejor con medias de PA obtenidas con MAPA durante el sueño que con medias de PA diurna o de 24 h2–7. En múltiples estudios también se ha corroborado que existe una estrecha relación entre una abrupta caída relativa de la PA durante el sueño (patrón de PA nondipper/riser) y el riesgo de sufrir eventos cardiovasculares mortales y no mortales2,3,6,8,9. Con base en la sustancial evidencia de que la PA ambulatoria predice resultados de ECV a largo plazo independientemente de la MCPA diurna, ahora varias guías y recomendaciones internacionales proponen como requisito la MAPA para confirmar el diagnóstico de hipertensión en adultos10–13. Los algoritmos de los modelos de estratificación del riesgo cardiovascular, como el riesgo de ECV a 10 años según la escala de Framingham, incorporan factores de influencia tradicionales, como pueden ser la edad, el sexo, el tabaquismo, la dislipemia o la diabetes, además de la MCPA exclusivamente diurna14–17, a pesar del conjunto de pruebas convincentes de los diversos ensayos clínicos sobre el mejor valor pronóstico altamente significativo de los parámetros de la PA ambulatoria, en particular la media de la PA durante el sueño y la reducción relativa de la PA durante el sueño2–9. El Proyecto Hygia es una red de estudios establecida para ampliar el uso sistemático de la MAPA en atención primaria para diagnosticar y tratar la hipertensión, evaluar la respuesta al tratamiento y estimar el riesgo cardiovascular y otros riesgos de los pacientes18. En este estudio, se utilizó la base de datos actual del Proyecto Hygia para comparar el valor discriminador/predictivo, la discriminación y el rendimiento de la escala de Framingham original (RSOFG)17 y su adaptación específica a la población del estudio (escala de riesgo cardiovascular de Framingham [RSAFG]) con el modelo de estratificación del riesgo cardiovascular que incorpora las mismas variables que la RSOFG y la RSAFG, pero que sustituye la MCPA por parámetros pronósticos más sólidos basados en la MAPA (RSMAPA).
MÉTODOSInclusión de los participantes y criterios de exclusiónEl estudio fue aprobado por el comité de ética de investigación clínica de Galicia. Los detalles de su diseño, gestión, formación de los investigadores, control de calidad, seguridad y evaluación del cumplimiento, procedimientos clínicos y MAPA, criterios para solicitar la MAPA, cálculo del tamaño de la muestra, seguimiento y otros aspectos metodológicos pertinentes se describen en otra parte18. La población consiste en una serie de varones y mujeres caucásicos de 18 años o más, con una rutina de actividad diurna y sueño nocturno, que dieron el consentimiento informado para su inclusión.
Los criterios de exclusión fueron embarazo, antecedentes de alcoholismo o adicción a narcóticos, trabajar de noche o por turnos rotativos, sufrir síndrome de inmunodeficiencia adquirida, hipertensión secundaria conocida, determinadas enfermedades asociadas con ECV (angina inestable, insuficiencia cardiaca, arritmia potencialmente mortal, fibrilación auricular y retinopatía de grado III-IV), intolerancia a la MAPA y ser incapaz de comunicarse y cumplir todos los requisitos del estudio18. De acuerdo con los criterios de inclusión y exclusión utilizados en el estudio Framingham17, se excluyó del análisis a los participantes con antecedentes de eventos de ECV previos. Los investigadores de atención primaria participantes remitieron a 19.949 personas (10.478 varones y 9.471 mujeres), con una media de edad de 58,5±14,2 años, que satisficieron los criterios de inclusión y exclusión y proporcionaron toda la información requerida para el estudio.
Presión arterial ambulatoria y otras evaluacionesEn el proceso de inclusión, a cada participante se le realizaron por lo menos 3 MCPA consecutivas tras permanecer sentado en reposo 10min o más, con un dispositivo oscilométrico automático validado (HEM−705IT, Omron Health Care Inc., Estados Unidos). Inmediatamente después, se inició la MAPA con un dispositivo SpaceLabs 90207 calibrado y validado (SpaceLabs Inc., Estados Unidos) para determinar la presión arterial sistólica (PAS), la presión arterial diastólica (PAD) y la frecuencia cardiaca cada 20min entre las 7.00 y las 23.00 y cada 30min por la noche durante 48 h seguidas para optimizar la reproducibilidad de los resultados19. Los participantes llevaban un diario donde registraban, entre otros datos, a qué hora se acostaban y se levantaban para poder calcular con precisión las medias de la PA diurna y la nocturna de cada participante. Las series de PA ambulatoria se consideraron no válidas para el análisis y, por lo tanto, fue necesario repetir la MAPA (4,1%; intervalo de confianza del 95% [IC95%], 3,9%-4,4%) cuando faltaba el 30% o más de las mediciones programadas, si se carecía de datos durante un intervalo de más de 2 h o si los datos se habían obtenido cuando el programa de actividad-reposo no fue regular durante los 2 días de monitorización o si el periodo de sueño fue < 6 h o> 12 h. En cada visita clínica, cuando se realizaba la MAPA, se recogían muestras de la orina matutina y de sangre (entre las 8.00 y las 9.00) tras toda la noche en ayunas y se analizaban de inmediato mediante técnicas sistemáticas automáticas en las instalaciones del laboratorio del Servicio Galego de Saúde (SERGAS) que cumple los estándares de calidad.
SeguimientoLos investigadores revisaron los registros clínicos completos de todos los participantes por lo menos 1 vez al año y 1 año después de la última evaluación de la MAPA. Los especialistas clínicos externos no investigadores de los servicios de atención especializada correspondientes clasificaron los eventos de ECV en el momento de la hospitalización según los criterios diagnósticos actuales18 y registraron toda la información en la historia clínica electrónica del paciente. El comité de eventos del Proyecto Hygia, formado por médicos independientes que desconocían los registros médicos y los resultados de la MAPA, evaluaron conjunta y periódicamente estos informes clínicos desprovistos de identificadores para determinar y certificar cada evento documentado. Para comparar la RSOFG, la RSAFG y la RSMAPA, el criterio de valoración primario de ECV según el estudio de Framingham17 fue: muerte por ECV, infarto de miocardio, revascularización coronaria, insuficiencia cardiaca, ictus hemorrágico, ictus isquémico, accidente isquémico transitorio, angina o enfermedad arterial periférica.
Métodos estadísticosPara evitar la confusión por el muestreo no equidistante en el cálculo de los valores medios de PA, los periodos de 48 h, vigilia y sueño de cada uno de los participantes se dividieron en un número entero de clases de la misma longitud de tiempo, y a continuación se determinaron las medias de PA respectivas como el promedio de los valores medios de las clases de tiempo pertinentes. La disminución relativa de la PA durante el sueño (índice de dipping de la PA) se calculó como: [(media de la PA ambulatoria durante la actividad – media de la PA ambulatoria durante el sueño) / media de la PA ambulatoria durante la actividad] × 100, con todos los datos válidos de la MAPA de 48 h. Se designó a los participantes como dipper si la reducción relativa de la PAS durante el sueño era ≥ 10% y como nondipper en los demás casos13. Las variables demográficas y clínicas se compararon entre los grupos de participantes que sufrieron un evento o no mediante la prueba de la t de Student (variables cuantitativas) o la prueba no paramétrica de la χ2 (proporciones).
La RSOFG basada en las MCPA para el criterio de valoración primario de ECV definido incluye toma de la PAS en el consultorio más las variables edad, sexo, tabaquismo, colesterol total y colesterol unido a lipoproteínas de alta densidad (cHDL), tratamiento de la hipertensión y diabetes17. Para evitar el posible sesgo debido a las diferencias entre la población de Framingham original y los participantes en el Proyecto Hygia a la hora de evaluar la influencia de la MAPA en la RSOFG, se ajustó el modelo de Framingham original a los participantes en el Proyecto Hygia y se recalcularon los coeficientes de regresión de Cox para cada una de las covariables originales, incluida la PAS clínica. Se hizo una transformación logarítmica de las variables continuas para minimizar la influencia de las observaciones extremas17. La RSMAPA probada incluía las mismas variables, excepto la MCPA, además de los parámetros de la PA ambulatoria de la media de la PAS durante el sueño y la reducción relativa de la PAS durante el sueño. Anteriormente ya se había visto, y también se corrobora en el presente estudio, que estos 2 parámetros de la PAS son las únicas características de la PAS conjuntamente significativas en el análisis de regresión de Cox como predictores del riesgo de ECV6. La falta de colinealidad significativa entre la PAS clínica, la media de la PAS durante el sueño y el descenso de la PAS durante el sueño se determinó calculando los coeficientes de tolerancia y los factores de inflación de la varianza correspondiente.
Se evaluó la calibración —la medida de concordancia entre los eventos de ECV observados y los predichos— de los modelos RSOFG, RSAFG y RSMAPA con la prueba no paramétrica de Greenwood-Nam-D’Agostino (GND), que es la más fiable cuando la tasa de censura es baja20,21. Para ello, se dividió a los participantes de cada modelo de riesgo evaluado en deciles conforme a la probabilidad individualizada estimada de sufrir un evento y se utilizó el estimador de Kaplan-Meier para obtener la incidencia observada de los eventos de ECV20,21. El estadístico C se utilizó para comparar el valor de discriminación del resultado de ECV entre los modelos. Como medida de la precisión diagnóstica17,22, también se calculó la proporción de eventos de ECV que tenían lugar en el quintil superior del riesgo predicho (es decir, sensibilidad del quintil superior) y la proporción de individuos sin eventos no incluidos en el quintil superior del riesgo predicho (es decir, especificidad del quintil superior) para el modelo de predicción del riesgo.
Para solventar la dependencia en la elección de las categorías necesarias para determinar la mejora del índice de reclasificación neta (NRI) clásico (aumento en la categoría de riesgo de los individuos que sufrieron un evento y descenso para los que no), se evaluó el rendimiento de la RSOFG y la RSAFG frente a la RSMAPA mediante NRI continuo (también llamado NRI> 0), mejora de la discriminación integrada (IDI)22 e IDI relativo (RIDI)23 con la RSMAPA como modelo de referencia. El IC95% correspondiente para estos índices de reclasificación se estableció mediante técnicas del método de (re)muestreo por reposición23. También se calculó la equivalencia de las probabilidades estimadas (EEP), definida como el porcentaje de participantes con una probabilidad estimada de sufrir eventos predicha por el modelo RSOFG o el RSAFG, clasificados dentro del IC95% de la probabilidad individual correspondiente de sufrir un evento determinada a partir del modelo de la RSMAPA. Bajo la hipótesis nula de que las probabilidades estimadas de sufrir un evento de ECV de los modelos comparados son equivalentes, este porcentaje debería ser ≥ 95%; esta hipótesis puede verificarse estadísticamente mediante la prueba binomial unilateral de proporciones. Una ventaja importante de la EEP aquí propuesta es que, más allá de los valores de las probabilidades estimadas, también depende de la variabilidad de las estimaciones individualizadas dadas por su IC95%. Las probabilidades individuales de sufrir un evento calculadas y el IC95% correspondiente determinado a partir del modelo RSMAPA también sirvieron para evaluar el rendimiento estableciendo la significación estadística de cualquier aumento/descenso dado del riesgo, que constituye la mejora significativa de la reclasificación neta (NRSI).
Los límites de concordancia entre las probabilidades individuales de sufrir un evento predichas por cada modelo probado se calcularon con el método de Bland-Altman24. Por último, se aplicó el modelo de riesgos proporcionales de Cox para calcular las hazard ratio (HR) y sus IC95% para los eventos documentados de los participantes divididos en quintiles según los riesgos individualizados respectivos RSOFG, RSAFG y RSMAPA. Para el análisis de supervivencia, se estableció el seguimiento como el intervalo de tiempo desde la fecha de realización de la MAPA hasta la fecha de incidencia de ECV confirmada en los participantes que sufrieron algún evento o hasta la última evaluación clínica de los participantes que no registraron ninguno. Los análisis estadísticos se realizaron con la versión 20.0 del software SPSS (SPSS Inc., Estados Unidos) y la versión 3.3.3 del paquete estadístico R (R Foundation for Statistical Computing).
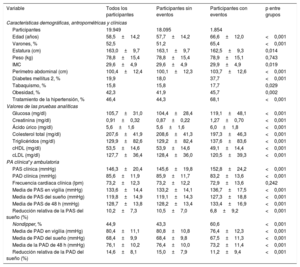
RESULTADOSVariables basales demográficas, analíticas y de la PA como posibles marcadores del riesgo de ECVDurante el seguimiento, que duró hasta 12,7 años, 1.854 participantes tuvieron un primer evento de ECV (muerte por ECV, n=203; infarto de miocardio, n=208; revascularización coronaria, n=216; insuficiencia cardiaca, n=378; ictus, n=271; otros eventos menores, n=578). Los análisis de supervivencia de Cox indicaron que, además de la PA, el mayor riesgo de eventos de ECV se asociaba conjunta y significativamente con las variables incluidas en la RSOFG sexo masculino, edad avanzada, tabaquismo, cHDL reducido, tratamiento antihipertensivo y diabetes (tabla 1). La exploración simultánea de la posible contribución conjunta combinada al riesgo de ECV entre los múltiples parámetros de la PA reveló que la media de la PAS durante el sueño (por cada aumento de 1 desviación estándar, HR = 1,32; IC95%, 1,23-1,41; p <0,001), pero no la de la PAS clínica (HR = 1,04; 0,98-1,10; p=0,180) o la PAS en vigilia (HR = 0,97; 0,90-1,05; p=0,418) es el marcador más significativo de aumento del riesgo de ECV basado en la PA. La contribución conjunta con la media de la PAS durante el sueño al riesgo de ECV solo fue significativa para la reducción relativa de la PAS durante el sueño (media de PAS durante el sueño, HR = 1,29; IC95%, 1,23-1,35; reducción relativa de la PAS durante el sueño, HR = 0,92; IC95%, 0,88-0,97; ambas p <0,001).
Características basales de los participantes en el estudio
| Variable | Todos los participantes | Participantes sin eventos | Participantes con eventos | p entre grupos |
|---|---|---|---|---|
| Características demográficas, antropométricas y clínicas | ||||
| Participantes | 19.949 | 18.095 | 1.854 | |
| Edad (años) | 58,5±14,2 | 57,7±14,2 | 66,6±12,0 | <0,001 |
| Varones, % | 52,5 | 51,2 | 65,4 | <0,001 |
| Estatura (cm) | 163,0±9,7 | 163,1±9,7 | 162,5±9,3 | 0,014 |
| Peso (kg) | 78,8±15,4 | 78,8±15,4 | 78,9±15,1 | 0,743 |
| IMC | 29,6±4,9 | 29,6±4,9 | 29,9±4,9 | 0,019 |
| Perímetro abdominal (cm) | 100,4±12,4 | 100,1±12,3 | 103,7±12,6 | <0,001 |
| Diabetes mellitus 2, % | 19,9 | 18,0 | 37,7 | <0,001 |
| Tabaquismo, % | 15,8 | 15,8 | 17,7 | 0,029 |
| Obesidad, % | 42,3 | 41,9 | 45,7 | 0,002 |
| Tratamiento de la hipertensión, % | 46,4 | 44,3 | 68,1 | <0,001 |
| Valores de las pruebas analíticas | ||||
| Glucosa (mg/dl) | 105,7±31,0 | 104,4±28,4 | 119,1±48,1 | <0,001 |
| Creatinina (mg/dl) | 0,91±0,32 | 0,87±0,22 | 1,27±0,70 | <0,001 |
| Ácido úrico (mg/dl) | 5,6±1,6 | 5,6±1,6 | 6,0±1,8 | <0,001 |
| Colesterol total (mg/dl) | 207,6±41,9 | 208,6±41,3 | 197,3±46,3 | <0,001 |
| Triglicéridos (mg/dl) | 129,9±82,6 | 129,2±82,4 | 137,6±83,6 | <0,001 |
| cHDL (mg/dl) | 53,5±14,6 | 53,9±14,6 | 49,1±14,4 | <0,001 |
| cLDL (mg/dl) | 127,7±36,4 | 128,4±36,0 | 120,5±39,3 | <0,001 |
| PA clínica*y ambulatoria | ||||
| PAS clínica (mmHg) | 146,3±20,4 | 145,6±19,8 | 152,8±24,2 | <0,001 |
| PAD clínica (mmHg) | 85,6±11,9 | 85,9±11,7 | 83,2±13,6 | <0,001 |
| Frecuencia cardiaca clínica (lpm) | 73,2±12,3 | 73,2±12,2 | 72,9±13,6 | 0,242 |
| Media de PAS en vigilia (mmHg) | 133,6±14,4 | 133,2±14,1 | 136,7±17,5 | <0,001 |
| Media de PAS del sueño (mmHg) | 119,8±14,9 | 119,1±14,3 | 127,3±18,8 | <0,001 |
| Media de PAS de 48 h (mmHg) | 128,7±13,8 | 128,2±13,4 | 133,4±16,9 | <0,001 |
| Reducción relativa de la PAS del sueño (%) | 10,2±7,3 | 10,5±7,0 | 6,8±9,2 | <0,001 |
| Nondipper, % | 44,9 | 43,3 | 60,6 | <0,001 |
| Media de PAD en vigilia (mmHg) | 80,4±11,1 | 80,8±10,8 | 76,4±12,3 | <0,001 |
| Media de PAD del sueño (mmHg) | 68,4±9,9 | 68,4±9,8 | 67,5±11,3 | <0,001 |
| Media de la PAD de 48 h (mmHg) | 76,1±10,2 | 76,4±10,0 | 73,2±11,4 | <0,001 |
| Reducción relativa de la PAD del sueño (%) | 14,6±8,1 | 15,0±7,9 | 11,2±9,4 | <0,001 |
cHDL: colesterol unido a lipoproteínas de alta densidad; cLDL: colesterol unido a lipoproteínas de baja densidad; IMC: índice de masa corporal; MAPA: monitorización ambulatoria de la presión arterial; PA: presión arterial; PAD: presión arterial diastólica; PAS: presión arterial sistólica.
Salvo otra indicación, los valores expresan n (%) o media ± desviación estándar.
Obesidad, IMC ≥ 30. La reducción relativa de la PA durante el sueño, el índice de profundidad de la PA, definido como la disminución en porcentaje de la PA media durante el sueño nocturno en relación con la PA media durante la actividad diurna, calculada como: ([media de la PA despierto – media de la PA dormido] / media de la PA despierto) × 100. Nondipper: los individuos con reducción relativa de la PAS durante el sueño < 10%, con datos muestreados mediante MAPA de 48 h consecutivas. Eventos: muerte cardiovascular, infarto de miocardio, revascularización coronaria, insuficiencia cardiaca, ictus hemorrágico, ictus isquémico, crisis isquémica transitoria, angina o enfermedad arterial periférica.
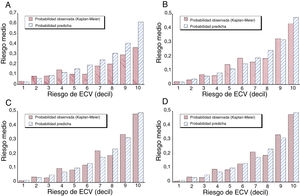
La RSOFG original (sin ajustar) sobrestimó notablemente la frecuencia real de eventos en la población del estudio. Esto es evidente por la comparación de las incidencias (Kaplan-Meier) estimada y observada de la RSOFG de eventos de ECV en los participantes divididos en deciles, que se muestra en la figura 1A y se confirma estadísticamente por la mala calibración del modelo mostrado en la tabla 2 (prueba de bondad de ajuste de GND = 123,40 [p < 0,001] que indica ausencia de ajuste). La precisión diagnóstica y la discriminación también fueron malas, tal como indican los valores relativamente bajos de sensibilidad/especificidad del quintil superior y el estadístico C (tabla 2, primera columna). Comparada con la RSMAPA como modelo de referencia, la RSOFG se desempeñó mal, como indicaron de manera constante todos los parámetros calculados de la reclasificación neta (NRI continuo, NRSI, IDI y RIDI) (tabla 2, primera columna). Solo el 21% de los participantes tenían una predicción de la probabilidad de sufrir eventos según el modelo de la RSOFG clasificado dentro del IC95% respectivo de cada probabilidad individual basada en el modelo de la RSMAPA.
Calibración por decil de la puntuación de riesgo de ECV que compara las probabilidades, observadas de Kaplan-Meier y predichas basadas en el modelo, de un evento de ECV mediante la escala de Framingham original (RSOFG) (A), la escala de Framingham ajustada para la población a estudio (RSAFG) (B), la RSMAPA basada en la MAPA (C) y esta corregida por modelos de MCPA (D). ECV: enfermedad cardiovascular.
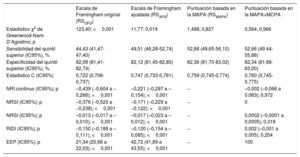
Calibración, precisión diagnóstica, valor de discriminación y rendimiento (mejora de la reclasificación) de la escala de Framingham original, la escala de Framingham ajustada basada en la MAPA y los modelos basados en la MAPA y la MCPA para estratificar el riesgo de ECV
| Escala de Framingham original (RSOFG) | Escala de Framingham ajustada (RSAFG) | Puntuación basada en la MAPA (RSMAPA) | Puntuación basada en la MAPA+MCPA | |
|---|---|---|---|---|
| Estadístico χ2 de Greenwood-Nam-D’Agostino; p | 123,40; <0,001 | 11,77; 0,019 | 1,498; 0,827 | 0,564; 0,966 |
| Sensibilidad del quintil superior (IC95%), % | 44,43 (41,47-47,40) | 49,51 (46,28-52,74) | 52,88 (49,65-56,10) | 52,66 (49,44-55,88) |
| Especificidad del quintil superior (IC95%), % | 82,08 (81,41-82,74) | 82,12 (81,45-82,80) | 82,36 (81,70-83,02) | 82,34 (81,68-83,00) |
| Estadístico C (IC95%) | 0,722 (0,706-0,737) | 0,747 (0,733-0,761) | 0,759 (0,745-0,774) | 0,760 (0,745-0,775) |
| NRI continuo (IC95%); p | –0,439 (−0,604 a –0,266); <0,001 | –0,221 (–0,297 a –0,154); <0,001 | − | –0,002 (–0,066 a 0,063); 0,972 |
| NRSI (IC95%); p | −0,376 (−0,520 a −0,238); <0,001 | −0,171 (−0,229 a −0,122); <0,001 | − | 0 |
| NRSI (IC95%); p | –0,013 (–0,017 a –0,010); <0,001 | –0,017 (–0,023 a –0,012); <0,001 | − | 0,0002 (–0,0001 a 0,0005); 0,318 |
| RIDI (IC95%); p | –0,150 (–0,188 a –0,111); <0,001 | –0,120 (–0,154 a –0,085); <0,001 | − | 0,002 (–0,001 a 0,005); 0,254 |
| EEP (IC95%); p | 21,34 (20,66 a 22,03); <0,001 | 42,72 (41,89 a 43,55); <0,001 | − | 100 |
EEP: equivalencia de las probabilidades estimadas; IC95%: intervalo de confianza del 95%; IDI: mejora integrada de la discriminación; MAPA: monitorización ambulatoria de la presión arterial; MCPA: medición clínica de la presión arterial; NRI: mejora de la reclasificación neta; NRSI: mejora significativa de la reclasificación neta; RIDI: mejora relativa de la discriminación integrada.
Sensibilidad del quintil superior: proporción de participantes que sufren el evento incluidos en el quintil superior del riesgo predicho. Especificidad del quintil superior: proporción de participantes que no sufren eventos y no estaban incluidos en el quintil superior del riesgo predicho. EEP: porcentaje de individuos con probabilidad estimada de sufrir eventos determinada a partir del modelo comparado que cae dentro del IC95% de la probabilidad de eventos correspondiente determinada a partir del modelo de referencia basado en la MAPA. El valor de p de la EEP se determinó mediante la prueba de proporciones binomial unilateral.
La RSAFG, calculada para las mismas variables incluidas en la RSOFG pero basada en los coeficientes de predicción ajustados a la población de estudio, comparada con el modelo de la RSOFG, proporcionó la calibración mejorada esperada, pero aún mala, (GND=11,77; p=0,019 para la bondad de ajuste) (figura 1B), precisión diagnóstica (sensibilidad y especificidad del quintil superior, 49,5% y 82,1%), discriminación (estadístico C = 0,747 frente a C = 0,722; p <0,001) y rendimiento (p <0,001 para todos los parámetros de la reclasificación neta) (tabla 2, segunda columna).
El modelo de la RSMAPA basado en la MAPA, comparado con la RSAFG, mostró mejora de la calibración (GND = 1,498; p=0,827 para la bondad de ajuste) (figura 1C), mayor sensibilidad del quintil superior (el 52,9% frente al 49,5%; p=0,034) y mayor discriminación (estadístico C = 0,759 frente a C = 0,747; p <0,001) de los participantes que en efecto sufrieron un evento de ECV durante el seguimiento. En todos los parámetros de la reclasificación, se demostró además un peor rendimiento de la RSAFG basada en las MCPA comparada con la RSMAPA (valores negativos significativos del NRI continuo, NRSI, IDI y RIDI) (tabla 2, segunda columna), es decir, reclasificación mejorada por el modelo basado en la MAPA de los participantes con respecto a una probabilidad estimada de sufrir eventos más precisa. Por último, la EEP para la RSAFG frente a la RSMAPA fue de 42,7 (p <0,001), lo que significa que en el 57,3% de los participantes la probabilidad de sufrir un evento basada en el modelo de la RSAFG se clasificaba fuera del IC95% de la probabilidad de sufrir eventos individualizada y determinada por el modelo más preciso de la RSMAPA.
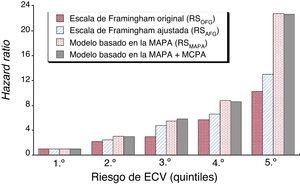
La figura 2 presenta el valor predictivo comparado de los modelos de la RSOFG, la RSAFG y la RSMAPA para la población del estudio dividida en quintiles. Los análisis de regresión de Cox sin ajustar realizados con referencia al primer quintil respectivo de cada una de las puntuaciones de riesgo comparadas de la probabilidad de sufrir eventos revelaron un valor predictivo notablemente mejor de la RSMAPA frente a la RSAFG y la RSOFG, tal como ilustran las HR progresivamente mayores para los primeros en todos los quintiles.
Hazard ratio de eventos de ECV para la población dividida en 5 clases de igual tamaño (quintiles) según la escala de Framingham original (RSOFG), la escala de Framingham ajustada (RSAFG), la RSMAPA basada en la MAPA y la RSMAPA corregida por los modelos de riesgo de la MCPA. ECV: enfermedad cardiovascular; MAPA: monitorización ambulatoria de la presión arterial; MCPA: medición clínica de la presión arterial.
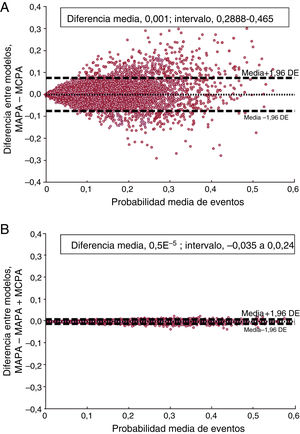
La figura 3A representa los límites de la concordancia en la probabilidad de sufrir un evento de cada participante evaluada por los modelos de la RSAFG y la RSMAPA. La figura muestra que las diferencias individuales en la probabilidad de sufrir un evento entre los modelos basados en la MCPA y la MAPA se distribuyeron por igual alrededor de la diferencia promedio (lo que muestra la línea horizontal punteada central) en todo el intervalo de probabilidad de sufrir un evento (del 0,08 al 59,24%). Por consiguiente, el grado de desacuerdo en la probabilidad calculada de sufrir un evento es independiente del nivel de probabilidad real. Los límites superior e inferior del 95% de concordancia con su respectivo IC95% eran del 7,44% [7,12%-7,78%] y el –7,30% (–6,98% al –7,64%); el intervalo total de desacuerdo observado del –28,8 al 46,5% indicaba la reproducibilidad extremadamente mala de cada una de las puntuaciones de probabilidad de sufrir un evento estimadas al confiar en la MCPA diurna en lugar de en parámetros más significativos de la PAS basados en la MAPA, es decir, la media de PAS durante el sueño y la reducción relativa de la PAS durante el sueño.
Gráficos de Bland-Altman que evalúan el acuerdo en la estimación de la probabilidad de eventos de cada participante evaluado con la RSAFG y la RSMAPA (A) y por la RSMAPA con y sin corrección con la MCPA (B). La línea horizontal punteada de cada gráfico representa el promedio de las diferencias en el conjunto de la población del estudio. Las líneas discontinuas representan los límites del acuerdo. DE: desviación estándar; MAPA: monitorización ambulatoria de la presión arterial; MCPA: medición clínica de la presión arterial.
Posteriormente se evaluaron los posibles impacto y valor predictivo complementario, si es que lo había, de incluir la MCPA en el modelo de la RSMAPA. El análisis de regresión de Cox indicó que la PAS clínica no proporciona valor predictivo significativo del riesgo de sufrir ECV cuando la media de la PAS durante el sueño y la reducción relativa de la PAS durante el sueño ya estaban incluidas en el modelo (HR = 1,00; IC95, 0,94-1,07; p=0,395). No hubo mejora alguna cuando la RSMAPA se ajustó según las MCPA en la calibración (GND = 0,564; p=0,966) (figura 1D), la precisión diagnóstica (sensibilidad y especificidad del quintil superior, el 52,7 y el 82,3% frente al 52,9 y el 82,4% para el modelo de la RSMAPA), la discriminación (estadístico C = 0,760 frente a C = 0,759; p=0,647) y el rendimiento (tabla 2, última columna). Por último, la EEP para el modelo ajustado por MCPA frente al modelo de la RSMAPA fue del 100%, es decir, no hubo ningún participante con una probabilidad de sufrir eventos basada en el modelo ajustado por MCPA que se clasificara fuera del IC95% de la probabilidad correspondiente de sufrir un evento determinada por el modelo de la RSMAPA, lo que vuelve a indicar la ausencia de un valor predictivo añadido proporcionado por la MCPA.
La figura 3B representa el gráfico de Bland-Altman para las probabilidades de sufrir un evento de los participantes evaluados por la RSMAPA, ambos con y sin posterior ajuste por la MCPA. Los límites superior e inferior del 95% de concordancia fueron extremadamente bajos (0,58%; IC95%, 0,56%-0,61%; y –0,58%; IC95%, –0,61 al –0,56%) con el grado total de desacuerdo del (del –3,5% al 2,4)%. Estos resultados indican la altísima reproducibilidad del modelo de predicción basado en la MAPA en la probabilidad estimada de sufrir un evento y el impacto no significativo de su ajuste por inclusión de la MCPA.
Impacto de la duración de la MAPA en la RSMAPALa mayor parte de los estudios previos que tratan del mérito de los biomarcadores de PA determinados por la MAPA frente a la MCPA como factores de riesgo o incluso como predictores de los eventos de ECV se basaron en una evaluación de la MAPA por participante ≤ 24 h1,2,4,5,7,8. Anteriormente se había documentado que la reproducibilidad y la precisión de los parámetros de estimación basados en la MAPA, y por lo tanto su valor pronóstico, dependen notablemente de la duración de la monitorización19. En este sentido, los análisis de las primeras 24 h de la evaluación de la MAPA de 48 h por participante indicaron: a) baja reproducibilidad de la media de la PAS durante el sueño y reducción relativa de la PAS durante el sueño (límites de concordancia del 95% de Bland-Altman,–8,3 a 8,0mmHg y del –7,3 al 6,3%; intervalo total de error, –38,5 a 36,5mmHg y del–21,5 al 36,5%); b) alta tasa de clasificación errónea de la hipertensión real y patrón de dipping (el 11,8 y el 24,9% respectivamente), y c) peores calibración, discriminación y rendimiento al predecir el riesgo de ECV con la RSMAPA de 24 h que con la de 48 h (GND = 17,08; p=0,047; estadístico C = 0,753; IC95%, 0,739-0,768; p=0,014; y EEP = 83,0; IC95%, 82,4-83,6; p < 0,001). Por último, los límites superior e inferior del 95% de concordancia de Bland-Altman para la probabilidad estimada de sufrir un evento con la RSMAPA de 24 h y no con la de 48 h fueron del 3,15% (IC95%, 3,01%-3,29%) y el –3,04% [IC95%, –2,91 al –3,18%), con un intervalo total de desacuerdo del −14,5 al 35,6%. Estos resultados indican malas precisión y reproducibilidad de las probabilidades individuales estimadas de sufrir un evento cuando se confía en la MAPA de 24 h en lugar de la más fiable de 48 h. No obstante, la RSMAPA de 24 h, a pesar de sus limitaciones, comparada con el modelo propuesto y más preciso de 48 h, funciona notablemente mejor que la RSAFG basada en la MCPA.
DISCUSIÓNSegún este estudio prospectivo que corrobora y amplía las conclusiones de estudios previos2–9, la media elevada de la PAS durante el sueño, pero no la MCPA diurna o la media de la PAS en vigilia, y la reducción relativa de la PAS durante el sueño son los únicos indicadores pronóstico conjuntos y significativos, basados en la PA, de un mayor riesgo de morbilidad y mortalidad por ECV. En consonancia con estos resultados, el 24,5% de los participantes mostraron «hipertensión oculta» (que aquí se define como media elevada de la PAS durante el sueño o patrón de PA nondipper, pero MCPA diurna normal) y el 17,1%, hipertensión de consultorio aislada (media de la PAS del sueño normal y patrón de PA dipper pero MCPA diurna elevada). Estos resultados indican que el diagnóstico de hipertensión (es decir, alto riesgo de ECV) en el 41,6% de los participantes, y más probablemente en todos los demás pacientes clínicos, sería incorrecto cuando solo se basa en las MCPA.
Este estudio también documenta que: a) el modelo de predicción de la RSOFG original, así como su versión ajustada a la población disponible (RSAFG), basada en la MCPA diurna, funciona muy mal comparado con la RSMAPA basada en la MAPA, y b) el valor predictivo ya alto de la RSMAPA no aumenta cuando se añade la MCPA al modelo. Comparada con la RSAFG basada en la MCPA, la RSMAPA basada en la MAPA mostró una mejora notable de la calibración (bondad de ajuste significativamente mejor según determinó la prueba de GND), precisión diagnóstica (aumento significativo de la sensibilidad del quintil superior), discriminación (estadístico C significativamente mayor) y rendimiento (reclasificación significativamente mejorada de los participantes respecto a una estimación más precisa de la probabilidad de sufrir un evento) (tabla 2). Y lo que es más importante, la probabilidad de sufrir un evento basada en la RSAFG de prácticamente el 60% de los participantes quedó fuera del IC95% de la probabilidad correspondiente de sufrir un evento determinada por la más precisa RSMAPA. De hecho, el grado de desacuerdo en la probabilidad calculada de sufrir un evento cuando se confía en la MCPA menos precisa, tal como determinaron los límites de concordancia del 95% de Bland-Altman, es un intervalo muy grande (del –7,30 al 7,44%), un 50% mayor que el umbral de la probabilidad de sufrir un evento del 10% actualmente recomendado para definir el alto riesgo de ECV12. El grado total de desacuerdo (del –28,8 al 46,5%) demostró además la reproducibilidad extremadamente mala y clínicamente inaceptable del cálculo individual de la probabilidad de sufrir un evento cuando se confía en las MCPA. En conjunto, estos resultados no solo establecen limitaciones importantes de la estratificación del riesgo de ECV cuando se basa en las MCPA, según establece actualmente la escala de Framingham12,17, sino que también corrobora el requisito clínico de la MAPA para diagnosticar adecuadamente la hipertensión real y cuantificar con precisión el riesgo de ECV.
Las principales limitaciones de este estudio son: a) los resultados sobre el valor pronóstico de la media de la PAS durante el sueño y la reducción relativa de la PAS durante el sueño requieren una validación prospectiva independiente, así como su extrapolación a diversos grupos étnicos; b) las MCPA las obtuvieron profesionales sanitarios en el centro clínico y, por lo tanto, es posible que la PA se hubiera sobrestimado por un posible efecto de «bata blanca», aunque esto refleja la práctica clínica actual y en la mayor parte de los estudios anteriores, como el estudio de Framingham1–5,7,17, y c) se utilizó el modelo de predicción más reciente: la RSOFG del 200817 sin corrección generalizada para la población española, pero ajustada específicamente a la población del estudio. La única RSOFG corregida y actualmente disponible para España25 se desarrolló como una adaptación de las RSOFG de 199814. No obstante, esta escala corregida se basó en: a) una cohorte relativamente pequeña compuesta por individuos de una única provincia nororiental de España, caracterizada por una menor prevalencia de eventos de ECV que el promedio del país, y b) un número más bien reducido de eventos coronarios en lugar de en el más exhaustivo criterio de valoración primario de la ECV definido anteriormente y utilizado en la RSOFG de 2008. En consecuencia, la RSAFG utilizada en este estudio para comparar el modelo basado en la MAPA podría ser más representativa que la escala corregida comunicada anteriormente25.
Los análisis de este estudio también tienen puntos fuertes importantes. El Proyecto Hygia es el único estudio prospectivo de eventos de ECV a gran escala completamente integrado de manera sistemática en atención primaria y, por lo tanto, es representativo de la población evaluada con mayor frecuencia para estratificar el riesgo de ECV. Otros puntos fuertes son el uso de: a) la MAPA de 48 h en lugar de las 24 h habituales para aumentar la reproducibilidad de los resultados de PA; b) un diario del participante debidamente diseñado para establecer el inicio y el final de la vigilia y los periodos de sueño para obtener con precisión las medias de PAS/PAD en la vigilia y el sueño de cada individuo, en lugar de confiar en horas de reloj fijas arbitrarias y presupuestas o imprecisas para obtener los valores diurnos y nocturnos proporcionados por el software del fabricante del dispositivo, tal como se ha hecho en la mayoría de los anteriores estudios de MAPA2,7, y c) múltiples medidas estadísticas (incluidas las del NRSI y EEP descritas por primera vez aquí) para evaluar de manera objetiva la calibración, la precisión diagnóstica, la discriminación y el rendimiento de los modelos de riesgo evaluados.
CONCLUSIONESEsta evaluación prospectiva documenta que el uso de la MCPA, como en la escala de Framingham y otros modelos actuales, limita notablemente la precisión de la estratificación del riesgo de ECV, lo que resulta en una identificación errónea de los sujetos con una susceptibilidad alta o baja. Los resultados colectivos comunicados en este estudio respaldan la importancia crucial de incorporar la MAPA a la práctica clínica habitual, como se ha recomendado recientemente10–13, pero además, desde nuestro punto de vista, para detectar con precisión la existencia de una PA anómala durante el sueño para diagnosticar hipertensión y estratificar de manera fiable la vulnerabilidad a las ECV.
FINANCIACIÓNEl Proyecto Hygia es una red de investigación impulsada por investigadores independientes y financiada por subvenciones del Ministerio de Ciencia e Innovación, Gobierno de España (SAF2009-7028-FEDER); el Instituto de Salud Carlos III, Ministerio de Economía y Competitividad, Gobierno de España (PI14−00205); la Consellería de Economía e Industria, Dirección Xeral de Investigación e Desenvolvemento, Gobierno de la Comunidad Autónoma de Galicia (INCITE08−E1R−322063ES; INCITE09−E2R−322099ES; 09CSA018322PR; IN845B−2010/114); la Consellería de Cultura, Educación e Ordenación Universitaria, Gobierno de la Comunidad Autónoma de Galicia (CN2012/251; GPC2014/078; ED431B−2017/78); el Fondo Europeo de Desarrollo Regional (FEDER) y el Gobierno de la Comunidad Autónoma de Galicia en virtud del acuerdo de financiación del centro de investigación en Tecnologías de la Comunicación (AtlantTIC) y el Vicerrectorado de Investigación, Universidad de Vigo. Este ente financiero no desempeña ninguna función en el diseño, el análisis y la interpretación de los datos del estudio, la redacción de los informes ni la decisión de presentar artículos para su publicación. En otro lugar se ha proporcionado una lista completa de los investigadores del Proyecto Hygia6,18.
CONFLICTO DE INTERESESR.C. Hermida, D.E. Ayala, A. Mojón, M.H. Smolensky y J.R. Fernández tienen acciones de Circadian Ambulatory Technology & Diagnostics (CAT&D), una empresa de tecnología creada por y en colaboración con la Universidad de Vigo. Los demás autores no tienen nada que declarar.
- –
La asociación entre la PA y el riesgo de eventos de ECV es mucho más firme en los parámetros obtenidos de la MAPA que con la MCPA diurna.
- –
No obstante, los modelos actuales sobre estratificación del riesgo de ECV siguen confiando exclusivamente en la MCPA diurna junto con factores tradicionales, como la edad, el sexo, el tabaquismo, la dislipemia o la diabetes.
- –
Los datos de los 19.949 participantes en el Proyecto Hygia, realizado en atención primaria, evaluados mediante MAPA de 48 h y sin eventos de ECV previos sirvieron para comparar la precisión diagnóstica, la discriminación y el rendimiento de la escala de Framingham original (RSOFG) y su versión ajustada a la población del estudio del Proyecto Hygia (RSAFG) con el nuevo modelo de estratificación del riesgo de ECV creado por sustitución de la MCPA por parámetros pronósticos basados en la MAPA (RSMAPA).
- –
La media de la PAS durante el sueño y la reducción relativa de la PAS durante el sueño fueron los únicos factores de riesgo de ECV significativos basados en la PA y, en consecuencia, deberían utilizarse para diagnosticar hipertensión y estratificar debidamente el riesgo de ECV.
- –
Comparada con la RSOFG y la RSAFG, en la RSMAPA se observó una mejora significativa de la calibración, la precisión diagnóstica y el rendimiento, lo que indica que la vulnerabilidad descrita por la RSMAPA mejora considerablemente la discriminación de los participantes que sufrieron un evento de ECV durante el seguimiento.