En el mundo se interviene de cirugía no cardiaca a más de 200 millones de pacientes cada año1, de los que más de 1 millón mueren en los 30 días siguientes a la cirugía. Las complicaciones vasculares mayores (muerte de causa vascular, infarto de miocardio no fatal, parada cardiaca no fatal y accidente cerebrovascular no fatal) son la principal causa de morbimortalidad de estos pacientes, y el infarto agudo de miocardio (IAM) es la más frecuente (5,7%)2.
La fisiopatología del infarto de miocardio perioperatorio es actualmente tema de debate, con dos potenciales mecanismos implicados. El primero de ellos es la formación de un trombo en la arteria coronaria debido al estado inflamatorio y de hipercoagulabilidad inducidos por el estrés quirúrgico y la lesión tisular3,4. Estudios recientes muestran que los pacientes con un síndrome coronario agudo perioperatorio tienen hallazgos angiográficos compatibles con complicaciones trombóticas, y la frecuencia de estos hallazgos es similar a la de los pacientes que presentan un síndrome coronario agudo fuera del contexto quirúrgico5. El segundo mecanismo es el desequilibrio entre oferta y demanda miocárdica de oxígeno6. Por un lado, la respuesta fisiológica al estrés quirúrgico, que persiste varios días después de la intervención, aumenta el consumo de oxígeno y, por otro, múltiples circunstancias no infrecuentes durante la cirugía y el postoperatorio, como hipotensión, anemia, hipoxia o hipovolemia, disminuyen su aporte.
Recientemente, las sociedades europea y americana de cardiología han actualizado la definición universal y los criterios diagnósticos del IAM7. El IAM se define como la presencia de necrosis miocárdica en un contexto clínico de isquemia miocárdica aguda cuyo diagnóstico requiere elevación y/o descenso del valor de biomarcadores cardiacos (preferiblemente troponina) junto con síntomas de isquemia y/o hallazgos electrocardiográficos o ecocardiográficos compatibles. No obstante, cada vez hay más evidencia de que las lesiones miocárdicas detectadas por la elevación de troponinas en el postoperatorio inmediato (48-72h tras la cirugía) no cumplen estos criterios2. En el periodo postoperatorio inmediato, los pacientes reciben medicación analgésica y algunos permanecen sedados y/o en ventilación mecánica, por lo que la mayoría (65,3%) no refiere síntomas de isquemia8. Asimismo, los cambios electrocardiográficos suelen ser poco expresivos y transitorios, por lo que frecuentemente pasan inadvertidos6. Sin embargo, haya o no síntomas, el pronóstico del IAM perioperatorio, que puede ser tanto de tipo 1 como de tipo 2 según la definición universal, es malo, con una mortalidad a los 30 días de la cirugía superior al 11%8.
La estimación del riesgo cardiovascular en el preoperatorio permite mejorar el pronóstico de los pacientes con mayor probabilidad de presentar una complicación cardiovascular en el postoperatorio. Sin embargo, los modelos predictores de riesgo más utilizados hasta ahora9 tienen limitaciones y suelen subestimar este riesgo3,10.
En la cohorte VISION11, un estudio prospectivo internacional, que evaluó las complicaciones vasculares mayores en pacientes intervenidos de cirugía no cardiaca, se observó una mortalidad a los 30 días de la cirugía 3 veces superior a la esperada (1,9%). El estudio incluyó a pacientes mayores de 45 años intervenidos tanto de manera electiva como urgente con anestesia general o regional y que pasaran al menos una noche en el hospital. En la tabla 1 se detallan los tipos de cirugía que se les practicó. En el primer análisis de esta cohorte se incluyó a 15.133 pacientes a los que se determinó la troponina T (TnT) a las 6-12h de la cirugía y en el primero, el segundo y el tercer día postoperatorios. El análisis multivariable mostró que los picos de TnT ≥ 0,02 ng/ml eran potentes predictores independientes de mortalidad por cualquier causa a los 30 días (tabla 2). Por lo tanto, incluso valores de TnT considerados normales (< 0,04 ng/ml) tienen importantes repercusiones pronósticas.
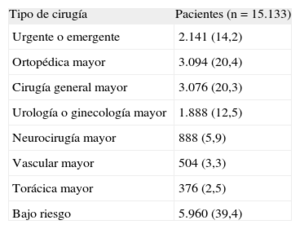
Tipos de intervenciones quirúrgicas practicadas a los pacientes incluidos en el estudio VISION11
| Tipo de cirugía | Pacientes (n=15.133) |
| Urgente o emergente | 2.141 (14,2) |
| Ortopédica mayor | 3.094 (20,4) |
| Cirugía general mayor | 3.076 (20,3) |
| Urología o ginecología mayor | 1.888 (12,5) |
| Neurocirugía mayor | 888 (5,9) |
| Vascular mayor | 504 (3,3) |
| Torácica mayor | 376 (2,5) |
| Bajo riesgo | 5.960 (39,4) |
Los datos expresan n (%).
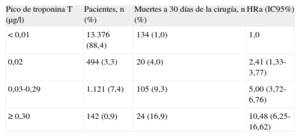
Umbrales pico de troponina T durante los primeros 3 días del postoperatorio que fueron predictores independientes de mortalidad a 30 días
| Pico de troponina T (μg/l) | Pacientes, n (%) | Muertes a 30 días de la cirugía, n (%) | HRa (IC95%) |
| < 0,01 | 13.376 (88,4) | 134 (1,0) | 1,0 |
| 0,02 | 494 (3,3) | 20 (4,0) | 2,41 (1,33-3,77) |
| 0,03-0,29 | 1.121 (7,4) | 105 (9,3) | 5,00 (3,72-6,76) |
| ≥ 0,30 | 142 (0,9) | 24 (16,9) | 10,48 (6,25-16,62) |
IC95%: intervalo de confianza del 95%; HRa: hazard ratio ajustada.
A raíz de estos resultados, investigadores del estudio VISION han propuesto recientemente un nuevo concepto denominado MINS (myocardial injury after noncardiac surgery), definido como toda elevación de troponinas, considerada de causa isquémica, que tiene relevancia pronóstica y ocurre durante la cirugía o en los 30 días siguientes12. Después de ajustar el modelo de regresión no solo por variables preoperatorias, sino también por complicaciones perioperatorias, los autores confirman la asociación independiente de valores de TnT ≥ 0,03 ng/ml con la mortalidad por cualquier causa a 30 días de la cirugía, y proponen como criterio diagnóstico de MINS un valor de TnT ≥ 0,03 ng/ml de etiología isquémica y que ocurre en los primeros 30 días tras la cirugía no cardiaca.
La incidencia de MINS en la cohorte VISION fue del 8%. El 87,1% de los MINS ocurrieron en los primeros 2 días después de la cirugía. Los pacientes que tuvieron un MINS eran más ancianos, tenían más factores de riesgo cardiovascular y enfermedad cardiovascular conocida y el 84,2% no presentó ningún síntoma de isquemia. Un 34,9% tuvo cambios electrocardiográficos; la inversión de la onda T (23,3%) y la depresión del ST (16,4%) fueron los más frecuentes. Se identificaron 12 predictores independientes de lesión miocárdica, entre ellos la edad ≥ 75 años, factores de riesgo cardiovascular (p. ej., insuficiencia renal y diabetes mellitus), enfermedad cardiovascular conocida y cirugía urgente. Los pacientes que presentaron MINS tuvieron mayor riesgo de complicaciones vasculares y su mortalidad fue más elevada que entre los que no lo presentaron (el 9,8 frente al 1,1%). La mortalidad a 30 días de la cirugía entre los que tuvieron MINS con signos y/o síntomas de isquemia (el 41,8% de los pacientes con MINS) fue del 13,5% y entre quienes no presentaron signos ni síntomas de isquemia fue del 7,7%. El 58,2% de las complicaciones isquémicas miocárdicas con relevancia pronóstica hubieran pasado inadvertidas sin la determinación de TnT.
Dado el mal pronóstico del IAM perioperatorio y la dificultad de su diagnóstico clínico8,12, el documento de consenso sobre la tercera definición universal de IAM7 recomienda la determinación sistemática de biomarcadores cardiacos en el perioperatorio (antes de la cirugía y 48-72h tras esta) de pacientes de alto riesgo cardiovascular intervenidos de cirugía mayor. Esta determinación permitirá detectar IAM en ausencia de signos o síntomas de isquemia y también lesiones miocárdicas que no cumplen los criterios propuestos, pero cuyo riesgo de muerte a 30 días de la cirugía es alto. El objetivo es identificar a los pacientes con elevado riesgo de complicaciones cardiovasculares y ofrecerles un adecuado nivel de cuidados postoperatorios.
Entre las estrategias propuestas para la reducción del riesgo de lesión miocárdica en el perioperatorio, la más controvertida actualmente es el uso de bloqueadores beta. Desde hace ya más de una década, las guías de práctica clínica de las sociedades europeas y americanas sobre la evaluación del riesgo preoperatorio y el manejo cardiovascular periopeoperatorios, han formulado recomendaciones a favor del uso de bloqueadores beta en pacientes con riesgo vascular intervenidos de cirugía no cardiaca de riesgo alto o intermedio. No obstante, tras la publicación del estudio POISE (PeriOperative ISchemic Evaluation) y las irregularidades detectadas en los estudios de la familia DECREASE (Dutch Echocardiographic Cardiac Risk Evaluation Applying Stress Echocardiography), la relación riesgo beneficio de los bloqueadores beta es a día de hoy desfavorable. De los dos metanálisis13,14 publicados hasta el momento que incluyen al estudio POISE, el más reciente excluye los resultados de algunos de los estudios DECREASE y muestra que los bloqueadores beta no solo no reducen el riesgo de muerte de cualquier causa a 30 días de la cirugía, sino que lo incrementan en un 27%. En respuesta a ello, las sociedades europeas y americanas de cardiología han anunciado que están trabajando en una nueva actualización de las guías de práctica clínica. Mientras tanto, su recomendación es que el inicio de bloqueadores beta para los pacientes a los que se va a intervenir de cirugía no cardiaca no se debe considerar sistemático, sino que se debe prescribir cuidadosamente valorando en cada caso el riesgo-beneficio. El estudio POISE, es de los estudios incluidos, el que reclutó a mayor número de pacientes (8.351) y es uno de los que presenta menos sesgos, por lo que sus resultados influyen en gran medida en el resultado final de estos metanálisis. Se ha discutido si la dosis de bloqueadores beta usada en el estudio POISE (100 mg de metoprolol succinato 2–4h preoperatorias y 200mg/día durante 30 días postoperatorios) pudo ser excesiva, y al no estar titulada progresivamente en función del efecto, podría haber causado los efectos adversos observados (mayor número de muertes y accidentes cerebrovasculares) que se atribuyó a la mayor frecuencia de hipotensión y bradicardia clínicamente significativas en el grupo de metoprolol. No obstante, otros estudios con diferentes bloqueadores beta, dosis y formas de administración han mostrado también mayor frecuencia de hipotensión en la rama de bloqueadores beta13. Actualmente se desconoce si algún subgrupo de pacientes puede beneficiarse de los bloqueadores beta en el perioperatorio de la cirugía no cardiaca y, en ese caso, con qué dosis, tipo de bloqueador beta y forma de administración más segura, pero en la actualización de la guía europea de 200915, llevada a cabo a raíz del estudio POISE, se recomienda no administrar dosis altas de bloqueadores beta sin una titulación previa. En cuanto a la factibilidad y la efectividad de esta titulación preoperatoria, cuyo objetivo es evitar la hipotensión y la bradicardia excesivas, son discutibles. Por un lado, la titulación preoperatoria, con el volumen de cirugía actual, supondría una sobrecarga de trabajo inasumible en muchos centros; por otro, esa dosis estipulada en el preoperatorio no es en absoluto garantía de que durante el procedimiento o en el postoperatorio, donde la hipotensión es un problema frecuente (el 9,7% de los pacientes del grupo placebo en el estudio POISE), esta no ocurra.
Siguen siendo necesarios estudios controlados y aleatorizados que identifiquen intervenciones capaces de reducir el riesgo de lesión miocárdica en el postoperatorio de cirugía no cardiaca. Mientras tanto, lo más razonable es evaluar el riesgo de los pacientes para adecuar la monitorización y los cuidados intraoperatorios y postoperatorios y seguir evitando y corrigiendo la anemia, la taquicardia y la hipotensión tanto durante como después de la intervención. Técnicas quirúrgicas menos agresivas que la cirugía abierta pueden ser una alternativa para reducir la mortalidad de los pacientes de edad avanzada con múltiples comorbilidades y alto riesgo cardiovascular16.
En cuanto al tratamiento de las lesiones miocárdicas después de la cirugía no cardiaca, tampoco hay hasta el momento suficiente evidencia científica sobre cuáles pueden ser efectivos para mejorar su pronóstico a 30 días de la cirugía. Al igual que ha ocurrido con los bloqueadores beta, las medidas que se han demostrado beneficiosas para los pacientes con IAM en el contexto no quirúrgico pueden no ofrecer el mismo balance riesgo-beneficio favorable para los IAM perioperatorios. Actualmente, se está evaluando en el estudio multicéntrico internacional Management of Myocardial Injury After Noncardiac Surgery (ClinicalTrials.gov: NCT01661101) la efectividad y la seguridad de los anticoagulantes orales en la reducción de la mortalidad a 30 días de la cirugía en pacientes que han tenido un MINS en el postoperatorio.
A la vista de estos datos, los equipos implicados en el manejo perioperatorio de los pacientes, incluida cardiología, deberían organizarse para identificar a los pacientes de riesgo y dar soporte al diagnóstico, la estratificación del riesgo, el tratamiento y el seguimiento de los que presenten lesiones miocárdicas después de una cirugía no cardiaca. Para ello es recomendable la determinación perioperatoria de biomarcadores cardiacos. El aumento en la esperanza de vida y/o la calidad de esta que los pacientes esperan de la cirugía no debería truncarse por complicaciones cardiovasculares que no ha sido posible identificar.
Full English text available from: www.revespcardiol.org/en
CONFLICTO DE INTERESESLos autores de este artículo son investigadores del estudio VISION en España y han recibido financiación del estudio para asistir a reuniones de trabajo.