Hay discrepancia entre la evaluación del riesgo basada en factores de riesgo cardiovascular (FRCV) y la carga de ateromatosis. El objetivo de este estudio es identificar la prevalencia de enfermedades subclínicas con factores de riesgo comunes, como ateromatosis, enfermedad renal oculta, prediabetes y diabetes, en una población de mediana edad con riesgo cardiovascular bajo a moderado para evaluar la distribución vascular y la gravedad de la ateromatosis subclínica.
MétodosEnsayo clínico longitudinal intervencionista aleatorizado. La intervención fue la ecografía vascular en arterias carótidas y femorales para valorar 12 territorios, combinada con parámetros clínicos, antropométricos, de estilo de vida y bioquímicos. Los criterios de inclusión fueron: mujeres (50-70 años) y varones (45-65) con al menos 1 FRCV. Los criterios de exclusión fueron: historia clínica de diabetes, enfermedad renal crónica o evento cardiovascular previo. Se muestran las características basales de la cohorte ILERVAS.
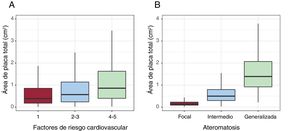
ResultadosSe incluyó a 8.330 participantes asintomáticos de mediana edad, el 50,7% mujeres. El 74,8% tenía 1-2 FRCV. El 52,8% mostró poca adherencia a la dieta mediterránea. Se diagnosticaron varias enfermedades crónicas previamente desconocidas, como dislipemia (21,1%), hipertensión (15,3%), enfermedad renal (15,4%), obesidad (10,6%) y diabetes (2,3%). El 71,4% de los participantes tenían ateromatosis subclínica localizada en la femoral común (54,5%), la bifurcación carotídea (41,1%) y la carótida interna (22%). El 32,6% tenía ateromatosis intermedia (2-3 territorios con placa de ateroma) y el 19,7%, ateromatosis generalizada (más de 3 territorios). Los varones mostraron más área total de placa (0,97 frente a 0,58 cm2; p <0,001). El área total de placa fue mayor en la arteria femoral y aumentó con el número de FRCV.
ConclusionesLa ateromatosis subclínica es muy prevalente en una población de mediana edad con riesgo cardiovascular bajo a moderado, y 1/5 individuos presenta ateromatosis generalizada.
Identificador ClinicalTrials.gov: NCT03228459.
Palabras clave
Pese a haberse identificado los factores de riesgo cardiovascular (FRCV) tradicionales a comienzos de la década de los sesenta y de muchos factores no tradicionales en las décadas siguientes, la enfermedad cardiovascular ateromatosa (ECVA) es la principal causa de mortalidad y discapacidad en la mayoría de los países y causa una tercera parte de las muertes1. La ateromatosis se instaura de forma insidiosa y suele ser ya generalizada cuando aparecen síntomas. Por consiguiente, la detección temprana de la ateromatosis subclínica es de capital importancia. El sistema más ampliamente utilizado para la evaluación del riesgo cardiovascular es la puntuación de riesgo de Framingham2. No obstante, en la población europea existen diferencias significativas que impiden su aplicación directa a nuestra población3. En consecuencia, se recomiendan la European Systematic Coronary Risk Evaluation (SCORE)4 y los gráficos de riesgo de Framingham-REGICOR (Registre Gironí del Cor) en España para estratificar el riesgo de enfermedad cardiovascular5. Según lo indicado en la guía clínicas de 2019, los pacientes se clasifican en función de su SCORE como en riesgo muy alto (SCORE ≥ 10% para un riesgo de ECV mortal en 10 años), riesgo alto (≥ 5% y <10%), riesgo moderado (≥ 1% y < 5%) y riesgo bajo (< 1%). Esta estratificación tiene consecuencias clínicas. Así, el objetivo terapéutico por lo que respecta al colesterol unido a lipoproteínas de baja densidad (cLDL) para los pacientes en riesgo alto es 70mg/dl (1,8 mmol/l) y para los pacientes en riesgo muy alto, 55mg/dl (1,4 mmol/l)4.
Múltiples estudios clínicos han analizado la ateromatosis en poblaciones con riesgo cardiovascular alto, como las que padecen diabetes6, hipercolesterolemia familiar7 o enfermedad renal crónica8. Sin embargo, hay una alta prevalencia de ateromatosis en la población general9,10. De hecho, hay una discrepancia entre el número de factores de riesgo tradicionales y los eventos cardiovasculares, y los eventos adversos relacionados con la ateromatosis son frecuentes incluso en individuos con riesgo cardiovascular bajo a moderado11. Por consiguiente, existe una urgente necesidad de mejores métodos de estratificación del riesgo.
La asociación entre la placa de ateroma y los eventos cardiovasculares está ampliamente confirmada12. Además, la evaluación multiterritorial aumenta su valor predictivo de mortalidad cardiovascular13.
Así pues, la realización de nuevos estudios longitudinales de base poblacional, centrados en la ateromatosis subclínica y destinados a abordar su prevalencia, su extensión multiterritorial y su progresión en individuos con riesgo cardiovascular bajo-moderado podría conducir a un cambio de paradigma, es decir, al tratamiento de la enfermedad subclínica en una fase temprana en vez de los FRCV.
Teniendo en cuenta los datos mencionados, el estudio ILERVAS se diseñó como un ensayo clínico longitudinal aleatorizado de intervención. Los objetivos principales fueron: a) evaluar la prevalencia, la distribución vascular, la gravedad y la progresión de la ateromatosis subclínica en una población de mediana edad con un riesgo cardiovascular bajo-moderado; b) identificar posibles factores predictivos de la ateromatosis generalizada más allá de los FRCV tradicionales; c) identificar la prevalencia de las enfermedades subclínicas con factores de riesgo comunes, como la enfermedad renal crónica oculta, la prediabetes, la diabetes, las enfermedades respiratorias y el síndrome metabólico, y d) evaluar las repercusiones de la detección de la ateromatosis subclínica en la incidencia de eventos cardiovasculares durante un periodo de seguimiento de 10 años. Se presentan aquí las características iniciales de la cohorte ILERVAS centradas en la ateromatosis. Se combinó la evaluación de la ateromatosis subclínica en 12 territorios y el área de placa ateromatosa con los parámetros clínicos, antropométricos, de estilo de vida y bioquímicos.
MÉTODOSEl estudio ILERVAS es un ensayo clínico longitudinal aleatorizado de intervención actualmente en marcha, en una población con riesgo cardiovascular bajo-moderado de la provincia de Lleida (España), con 2 grupos: a) grupo de intervención, en adelante grupo de seguimiento con unidad móvil, y b) grupo sin intervención, en adelante grupo de seguimiento con historia clínica electrónica (código de identificador de ClinicalTrials.gov: NCT03228459).
En el grupo de seguimiento con unidad móvil, la inclusión de los participantes se realizó entre enero de 2015 y diciembre de 2018 en 32 áreas de salud básicas de atención primaria de la provincia de Lleida. Los criterios de inclusión fueron los siguientes: mujeres de 50 a 70 años y varones de 45 a 65 años con al menos 1 de los siguientes FRCV: hipertensión, dislipemia, obesidad (definida como un índice de masa corporal [IMC] ≥ 30), tabaquismo o un familiar de primer grado que hubiera tenido una enfermedad cardiovascular prematura (con un umbral de edad de 55 años los varones y 65 años las mujeres). Los criterios de exclusión fueron: antecedentes clínicos de diabetes, enfermedad renal crónica, enfermedad cardiovascular (angina, infarto de miocardio, ictus, enfermedad arterial periférica, isquemia intestinal u otra isquemia), antecedentes de cirugía arterial, neoplasia activa, esperanza de vida < 18 meses, asistencia en residencia a largo plazo o población internada. Se volverá a evaluar a los participantes en la unidad móvil al cabo de 4 años. Se estableció un periodo de seguimiento de 10 años para el examen de la morbilidad y la mortalidad cardiovasculares y no cardiovasculares.
La población del estudio se asignó a los grupos mediante un muestreo estratificado de la base de datos de historias clínicas electrónicas de atención primaria del Servicio Catalán de Salud (véase información más detallada en el ). Todos los pacientes firmaron un documento de consentimiento informado. El protocolo fue aprobado por el Comité de Ética del Servicio Catalán de Salud (Ref. CEIC-1410 Hospital Arnau de Vilanova, Lleida, España). El estudio se llevó a cabo según los principios de la Declaración de Helsinki. Se incluye una descripción detallada de los métodos en el .
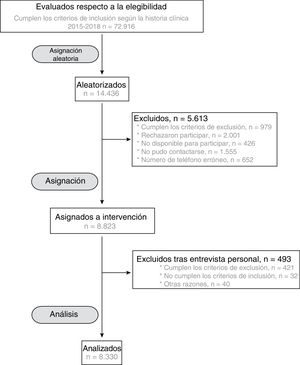
RESULTADOSCaracterísticas basales de la cohorte ILERVASEntre enero de 2015 y diciembre de 2018, se reclutó para el estudio ILERVAS a un total de 8.330 participantes de mediana edad sin eventos cardiovasculares previos. En la figura 1 se muestra el diagrama de flujo de la selección de participantes de la población candidata.
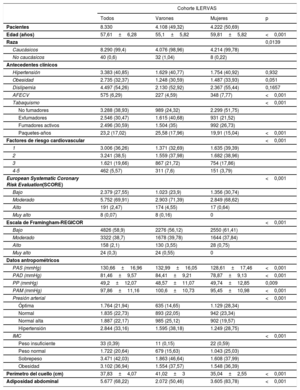
Las características clínicas basales de los pacientes se muestran en la tabla 1. La media de edad de los varones fue 55,1 (45-65) años y la de las mujeres, 59,8 (50-70) años. La mayoría de ellos (99,4%) eran caucásicos. La dislipemia fue el FRCV registrado con más frecuencia (el 54,3% de la población del estudio), seguida de la hipertensión (40,9%) y la obesidad (32,4%). Ninguno de estos factores presentó diferencias entre los sexos. Eran fumadores activos el 35% de los varones (con una media de 25,6 paquetes-años de consumo de tabaco) y el 26,7% de las mujeres (con una media de 19,9 paquetes-años de consumo) (p <0,001). Se observó la presencia de 1 o 2 de los criterios de inclusión de riesgo cardiovascular en un 70,7% de los varones y el 78,4% de las mujeres. Los participantes de más edad tenían un mayor número de factores de riesgo. La prevalencia de 1 FRCV fue del 45,3% entre los varones de 45-49 años y del 25,8% en los de 60-65 años. Se observó una tendencia similar en ambos sexos (). La mayoría (97,5%) de los participantes tenían un riesgo bajo-moderado según la puntuación del European Systematic Coronary Risk Evaluation (SCORE). De igual modo, la puntuación Framingham-REGICOR mostró que el 97,6% de los participantes tenían un riesgo bajo-moderado (tabla 1).
Características basales de los pacientes
| Cohorte ILERVAS | ||||
|---|---|---|---|---|
| Todos | Varones | Mujeres | p | |
| Pacientes | 8.330 | 4.108 (49,32) | 4.222 (50,69) | |
| Edad (años) | 57,61±6,28 | 55,1±5,82 | 59,81±5,82 | <0,001 |
| Raza | 0,0139 | |||
| Caucásicos | 8.290 (99,4) | 4.076 (98,96) | 4.214 (99,78) | |
| No caucásicos | 40 (0,6) | 32 (1,04) | 8 (0,22) | |
| Antecedentes clínicos | ||||
| Hipertensión | 3.383 (40,85) | 1.629 (40,77) | 1.754 (40,92) | 0,932 |
| Obesidad | 2.735 (32,37) | 1.248 (30,59) | 1.487 (33,93) | 0,051 |
| Dislipemia | 4.497 (54,26) | 2.130 (52,92) | 2.367 (55,44) | 0,1657 |
| AFECV | 575 (6,29) | 227 (4,59) | 348 (7,77) | <0,001 |
| Tabaquismo | <0,001 | |||
| No fumadores | 3.288 (38,93) | 989 (24,32) | 2.299 (51,75) | |
| Exfumadores | 2.546 (30,47) | 1.615 (40,68) | 931 (21,52) | |
| Fumadores activos | 2.496 (30,59) | 1.504 (35) | 992 (26,73) | |
| Paquetes-años | 23,2 (17,02) | 25,58 (17,96) | 19,91 (15,04) | <0,001 |
| Factores de riesgo cardiovascular | <0,001 | |||
| 1 | 3.006 (36,26) | 1.371 (32,69) | 1.635 (39,39) | |
| 2 | 3.241 (38,5) | 1.559 (37,98) | 1.682 (38,96) | |
| 3 | 1.621 (19,66) | 867 (21,72) | 754 (17,86) | |
| 4-5 | 462 (5,57) | 311 (7,6) | 151 (3,79) | |
| European Systematic Coronary Risk Evaluation(SCORE) | <0,001 | |||
| Bajo | 2.379 (27,55) | 1.023 (23,9) | 1.356 (30,74) | |
| Moderado | 5.752 (69,91) | 2.903 (71,39) | 2.849 (68,62) | |
| Alto | 191 (2,47) | 174 (4,55) | 17 (0,64) | |
| Muy alto | 8 (0,07) | 8 (0,16) | 0 | |
| Escala de Framingham-REGICOR | <0,001 | |||
| Bajo | 4826 (58,9) | 2276 (56,12) | 2550 (61,41) | |
| Moderado | 3322 (38,7) | 1678 (39,78) | 1644 (37,84) | |
| Alto | 158 (2,1) | 130 (3,55) | 28 (0,75) | |
| Muy alto | 24 (0,3) | 24 (0,55) | 0 | |
| Datos antropométricos | ||||
| PAS (mmHg) | 130,66±16,96 | 132,99±16,05 | 128,61±17,46 | <0,001 |
| PAD (mmHg) | 81,46±9,57 | 84,41±9,21 | 78,87±9,13 | <0,001 |
| PP (mmHg) | 49,2±12,07 | 48,57±11,07 | 49,74±12,85 | 0,009 |
| PAM (mmHg) | 97,86±11,16 | 100,6±10,73 | 95,45±10,98 | <0,001 |
| Presión arterial | <0,001 | |||
| Óptima | 1.764 (21,94) | 635 (14,65) | 1.129 (28,34) | |
| Normal | 1.835 (22,73) | 893 (22,05) | 942 (23,34) | |
| Normal alta | 1.887 (22,17) | 985 (25,12) | 902 (19,57) | |
| Hipertensión | 2.844 (33,16) | 1.595 (38,18) | 1.249 (28,75) | |
| IMC | <0,001 | |||
| Peso insuficiente | 33 (0,39) | 11 (0,15) | 22 (0,59) | |
| Peso normal | 1.722 (20,64) | 679 (15,63) | 1.043 (25,03) | |
| Sobrepeso | 3.471 (42,03) | 1.863 (46,64) | 1.608 (37,99) | |
| Obesidad | 3.102 (36,94) | 1.554 (37,57) | 1.548 (36,39) | |
| Perímetro del cuello (cm) | 37,83±4,07 | 41,02±3 | 35,04±2,55 | <0,001 |
| Adiposidad abdominal | 5.677 (68,22) | 2.072 (50,46) | 3.605 (83,78) | <0,001 |
AFECV: antecedentes familiares de enfermedad cardiovascular; IMC: índice de masa corporal; PAD: presión arterial diastólica; PAM: presión arterial media; PAS: presión arterial sistólica; PP: presión de pulso; REGICOR: Registre Gironí del Cor.
Los valores expresan n (%) para las variables cualitativas y media±desviación estándar para las variables cuantitativas de distribución normal. En el análisis se aplicaron ponderaciones de las muestras. Los datos de antecedentes clínicos se obtuvieron de los registros de historia clínica electrónica y corresponden a los pacientes que tenían un diagnóstico clínico previo de hipertensión, obesidad, dislipemia, un familiar de primer grado que sufrió una ECV prematura (con un umbral de edad de 55 años en los varones y de 65 años en las mujeres) o tabaquismo. La presión arterial óptima se definió como PAS <120mmHg y PAD <80; la normal, como PAS de 120-129 o PAD de 80-84; la normal alta, como PAS de 130-139 o PAD de 85-89; la hipertensión, como PAS ≥140 o PAD ≥90. El peso insuficiente se definió como un IMC < 18,5; el peso normal, como IMC de 18,5-24,9; el sobrepeso, como IMC de 25-29,9 y la obesidad, como IMC ≥ 30. La adiposidad abdominal se definió como un perímetro abdominal ≥ 88cm en las mujeres o ≥ 102 en los varones.
En las mujeres, la presión arterial, el IMC y el perímetro del cuello eran inferiores a los de los varones, pero la adiposidad abdominal era muy superior (el 83,8% de las mujeres frente al 50,5% de los varones; p <0,001).
Los varones realizaban más actividad física enérgica y moderada que las mujeres. En los varones, la actividad total era de 961,6min/semana, mientras que en las mujeres era de 834,7 (p=0,003). Sin embargo, el 60,95% de los participantes tenían poca actividad física; el 33,8%, una actividad moderada y el 5,3%, una actividad enérgica. Un total del 52,8% de los participantes tenían poca adherencia a la dieta mediterránea y el 39,8%, muy poca ().
Se observó una función respiratoria normal en el 68,5% de los varones y el 76,1% de las mujeres. Las alteraciones del patrón respiratorio mostraron una prevalencia superior en los varones. Casi la mitad (45,2%) de los participantes a los que se pudo clasificar mediante el cuestionario de Berlín mostraron alto riesgo de apnea obstructiva del sueño, y en un 2,1% se observó una somnolencia diurna excesiva ().
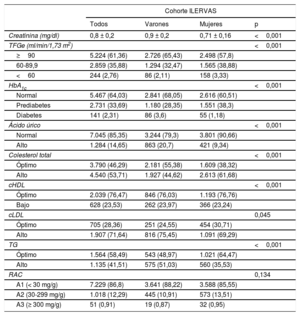
El análisis basal de bioquímica hemática puso de manifiesto que el 2,8% de los participantes tenían una tasa de filtrado glomerular estimada <60ml/min/1,73 m2; el 33,7%, prediabetes (glucohemoglobina [HbA1c], 5,7%-6,49%); el 2,3%, diabetes (HbA1c ≥ 6,5%), y el 14,7%, hiperuricemia (≥ 7,2mg/dl los varones y ≥ 6,4 mg/dl las mujeres). Se observaron concentraciones altas de colesterol (≥ 200mg/dl) en un 53,7% de los participantes, mientras que un 71,6% tenían alto el cLDL (≥130mg/dl); el 41,5%, triglicéridos altos (≥ 150mg/dl), y el 23,5%, concentraciones bajas de colesterol unido a lipoproteínas de alta densidad (≤ 40mg/dl los varones y ≤ 50 mg/dl las mujeres). El análisis de orina reveló que el 12,3% de los participantes tenían una razón de albúmina/creatinina de 30-300mg/g (tabla 2). En la se muestra el coeficiente de correlación intraclase entre los métodos de análisis en el punto de asistencia utilizados en la unidad móvil del estudio ILERVAS y los métodos bioquímicos de referencia.
Parámetros bioquímicos basales
| Cohorte ILERVAS | ||||
|---|---|---|---|---|
| Todos | Varones | Mujeres | p | |
| Creatinina (mg/dl) | 0,8 ± 0,2 | 0,9 ± 0,2 | 0,71 ± 0,16 | <0,001 |
| TFGe (ml/min/1,73 m2) | <0,001 | |||
| ≥90 | 5.224 (61,36) | 2.726 (65,43) | 2.498 (57,8) | |
| 60-89,9 | 2.859 (35,88) | 1.294 (32,47) | 1.565 (38,88) | |
| <60 | 244 (2,76) | 86 (2,11) | 158 (3,33) | |
| HbA1c | <0,001 | |||
| Normal | 5.467 (64,03) | 2.841 (68,05) | 2.616 (60,51) | |
| Prediabetes | 2.731 (33,69) | 1.180 (28,35) | 1.551 (38,3) | |
| Diabetes | 141 (2,31) | 86 (3,6) | 55 (1,18) | |
| Ácido úrico | <0,001 | |||
| Normal | 7.045 (85,35) | 3.244 (79,3) | 3.801 (90,66) | |
| Alto | 1.284 (14,65) | 863 (20,7) | 421 (9,34) | |
| Colesterol total | <0,001 | |||
| Óptimo | 3.790 (46,29) | 2.181 (55,38) | 1.609 (38,32) | |
| Alto | 4.540 (53,71) | 1.927 (44,62) | 2.613 (61,68) | |
| cHDL | <0,001 | |||
| Óptimo | 2.039 (76,47) | 846 (76,03) | 1.193 (76,76) | |
| Bajo | 628 (23,53) | 262 (23,97) | 366 (23,24) | |
| cLDL | 0,045 | |||
| Óptimo | 705 (28,36) | 251 (24,55) | 454 (30,71) | |
| Alto | 1.907 (71,64) | 816 (75,45) | 1.091 (69,29) | |
| TG | <0,001 | |||
| Óptimo | 1.564 (58,49) | 543 (48,97) | 1.021 (64,47) | |
| Alto | 1.135 (41,51) | 575 (51,03) | 560 (35,53) | |
| RAC | 0,134 | |||
| A1 (< 30 mg/g) | 7.229 (86,8) | 3.641 (88,22) | 3.588 (85,55) | |
| A2 (30-299 mg/g) | 1.018 (12,29) | 445 (10,91) | 573 (13,51) | |
| A3 (≥ 300 mg/g) | 51 (0,91) | 19 (0,87) | 32 (0,95) | |
cHDL: colesterol unido a lipoproteínas de alta densidad; cLDL: colesterol unido a lipoproteínas de baja densidad; HbA1c: glucohemoglobina; RAC: razón albúmina/creatinina; TFGe: tasa de filtrado glomerular estimada; TG: triglicéridos.
Los valores expresan n (%) para las variables cualitativas y media ± desviación estándar para las variables cuantitativas de distribución normal. En el análisis se aplicaron ponderaciones de las muestras. La HbA1c normal se definió como ≤ 5,69; la prediabetes, como HbA1c de 5,7-6,49 y la diabetes, como HbA1c ≥ 6,5. El ácido úrico alto se definió como ≥ 6,4mg/dl en las mujeres y ≥ 7,2mg/dl en los varones. El colesterol alto se definió como ≥ 200mg/dl. El cHDL bajo se definió como ≤ 50mg/dl en las mujeres y ≤ 40mg/dl en los varones. El cLDL se consideró alto a una concentración ≥ 130mg/dl. Los TG se consideraron altos a una concentración ≥ 150mg/dl. Las concentraciones de cLDL, cHDL y TG se evaluaron solo en los participantes con colesterol total ≥ 200mg/dl tras 6 h en ayunas o cuando el colesterol total era ≥ 250mg/dl con cualquier tiempo en ayunas.
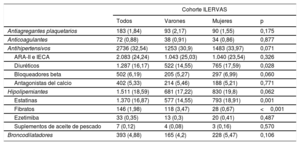
Los tratamientos farmacológicos utilizados se enumeran en la tabla 3. La medicación más frecuente fue la antihipertensiva (32,5%), mientras que el 18,6% de los participantes estaban en tratamiento para la hiperlipemia (el 16,9% con estatinas, el 1,98% con fibratos, el 0,4% con ezetimiba y el 0,1% con suplementos de aceite de pescado).
Tratamientos farmacológicos
| Cohorte ILERVAS | ||||
|---|---|---|---|---|
| Todos | Varones | Mujeres | p | |
| Antiagregantes plaquetarios | 183 (1,84) | 93 (2,17) | 90 (1,55) | 0,175 |
| Anticoagulantes | 72 (0,88) | 38 (0,91) | 34 (0,86) | 0,877 |
| Antihipertensivos | 2736 (32,54) | 1253 (30,9) | 1483 (33,97) | 0,071 |
| ARA-II e IECA | 2.083 (24,24) | 1.043 (25,03) | 1.040 (23,54) | 0,326 |
| Diuréticos | 1.287 (16,17) | 522 (14,55) | 765 (17,59) | 0,028 |
| Bloqueadores beta | 502 (6,19) | 205 (5,27) | 297 (6,99) | 0,060 |
| Antagonistas del calcio | 402 (5,33) | 214 (5,46) | 188 (5,21) | 0,771 |
| Hipolipemiantes | 1.511 (18,59) | 681 (17,22) | 830 (19,8) | 0,062 |
| Estatinas | 1.370 (16,87) | 577 (14,55) | 793 (18,91) | 0,001 |
| Fibratos | 146 (1,98) | 118 (3,47) | 28 (0,67) | <0,001 |
| Ezetimiba | 33 (0,35) | 13 (0,3) | 20 (0,41) | 0,487 |
| Suplementos de aceite de pescado | 7 (0,12) | 4 (0,08) | 3 (0,16) | 0,570 |
| Broncodilatadores | 393 (4,88) | 165 (4,2) | 228 (5,47) | 0,106 |
ARA-II: antagonistas del receptor de la angiotensina II; IECA: inhibidores de la enzima de conversión de la angiotensina.
Los valores expresan n (%). En el análisis se aplicaron ponderaciones de las muestras.
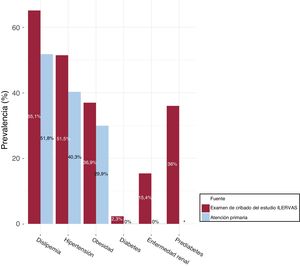
Se compararon los datos proporcionados por la base de datos de historias clínicas electrónicas de atención primaria con los datos obtenidos por la unidad móvil del estudio ILERVAS. El estudio ILERVAS detectó un 15,3% (intervalo de confianza del 95% [IC95%], 14%-16,6%) de participantes con hipertensión no diagnosticada, un 10,6% (IC95%, 9,6-11,7) con obesidad no diagnosticada y un 21,1% (IC95%, 19,7%-22,6%) con dislipemia no diagnosticada. Además, se detectó un 15,4% (IC95%, 14,1%-16,7%) de individuos con enfermedad renal oculta y un 2,3% [IC95%, 1,7%-3,02%] de participantes con diabetes no diagnosticada (figura 2).
Nuevos signos clínicos detectados en el estudio ILERVAS. Las prevalencias de dislipemia, hipertensión, obesidad, diabetes, enfermedad renal y prediabetes descritas en la base de datos de historias clínicas electrónicas de atención primaria se compararon con lo observado en la unidad móvil del ILERVAS. *La prevalencia de prediabetes no se obtuvo de la base de datos de historias clínicas electrónicas de atención primaria.
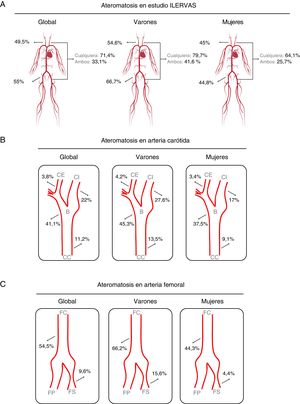
Se identificó placa de ateroma en al menos 1 de los territoritos explorados en el 71,4% de los participantes, y la prevalencia fue mayor en los varones (el 79,7% de los varones frente al 64,1% de las mujeres; p <0,001). La prevalencia de la ateromatosis fue mayor en las arterias femorales que en las carótidas. Así, un 49,5% de los participantes presentaban placas de ateroma en las arterias carótidas y un 55%, en las arterias femorales. Sorprendentemente, el 33,1% tenía placas en las arterias carótidas y en las femorales al mismo tiempo. De nuevo, en los varones se observaron placas de ateroma simultáneas en los 2 lechos vasculares con más frecuencia que en las mujeres (el 41,6 frente al 25,7%; p <0,001) (figura 3A).
Prevalencia de la ateromatosis subclínica en los diversos territorios vasculares en el estudio ILERVAS. Territorios de distribución global (A), de arteria carótida (B) y de arteria femoral (C). B: bifurcación carotídea; CC: carótida común; CE: carótida externa; CI: carótida interna; FC: femoral común; FP: arteria femoral profunda; FS: arteria femoral superficial.
La prevalencia de la ateromatosis carotídea fue mayor en la bifurcación (41,1%), seguida de la carótida interna (22%) y la carótida común (11,2%). La ateromatosis femoral fue más frecuente en la femoral común (54,5%) seguida de la femoral superficial (9,6%) (figura 3B,C).
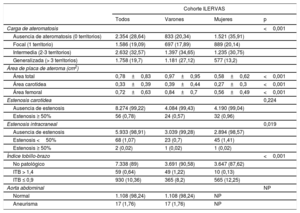
No se observaron placas de ateroma en un 28,6% de los participantes. Se halló una ateromatosis focal (definida por la presencia de placa en 1 del total de 12 territorios) en un 19,1%. Se observó una ateromatosis intermedia (definida por la presencia de placa en 2-3 territorios del total de 12) en un 32,6%, y una ateromatosis generalizada (> 3 territorios) en un 19,7%. En los varones hubo un aumento de la carga de enfermedad vascular (intermedia, el 34,7 frente al 30,8%; generalizada, el 27,1 frente al 13,2%; p <0,001) (tabla 4).
Evaluación vascular subclínica
| Cohorte ILERVAS | ||||
|---|---|---|---|---|
| Todos | Varones | Mujeres | p | |
| Carga de ateromatosis | <0,001 | |||
| Ausencia de ateromatosis (0 territorios) | 2.354 (28,64) | 833 (20,34) | 1.521 (35,91) | |
| Focal (1 territorio) | 1.586 (19,09) | 697 (17,89) | 889 (20,14) | |
| Intermedia (2-3 territorios) | 2.632 (32,57) | 1.397 (34,65) | 1.235 (30,75) | |
| Generalizada (> 3 territorios) | 1.758 (19,7) | 1.181 (27,12) | 577 (13,2) | |
| Área de placa de ateroma (cm2) | ||||
| Área total | 0,78±0,83 | 0,97±0,95 | 0,58±0,62 | <0,001 |
| Área carotídea | 0,33±0,39 | 0,39±0,44 | 0,27±0,3 | <0,001 |
| Área femoral | 0,72±0,63 | 0,84±0,7 | 0,56±0,49 | <0,001 |
| Estenosis carotídea | 0,224 | |||
| Ausencia de estenosis | 8.274 (99,22) | 4.084 (99,43) | 4.190 (99,04) | |
| Estenosis ≥ 50% | 56 (0,78) | 24 (0,57) | 32 (0,96) | |
| Estenosis intracraneal | 0,019 | |||
| Ausencia de estenosis | 5.933 (98,91) | 3.039 (99,28) | 2.894 (98,57) | |
| Estenosis <50% | 68 (1,07) | 23 (0,7) | 45 (1,41) | |
| Estenosis ≥ 50% | 2 (0,02) | 1 (0,02) | 1 (0,02) | |
| Índice tobillo-brazo | <0,001 | |||
| No patológico | 7.338 (89) | 3.691 (90,58) | 3.647 (87,62) | |
| ITB > 1,4 | 59 (0,64) | 49 (1,22) | 10 (0,13) | |
| ITB ≤ 0,9 | 930 (10,36) | 365 (8,2) | 565 (12,25) | |
| Aorta abdominal | NP | |||
| Normal | 1.108 (98,24) | 1.108 (98,24) | NP | |
| Aneurisma | 17 (1,76) | 17 (1,76) | NP | |
CI: arteria carótida interna; ITB: índice tobillo-brazo; NP: no procede; RVSM: razón VSM de CI/carótida común; VSM: velocidad sistólica máxima; VTD: velocidad telediastólica.
Los valores expresan n (%) para las variables cualitativas y media±desviación estándar para las variables cuantitativas de distribución normal. En el análisis se aplicaron ponderaciones de las muestras. Una estenosis carotídea ≥50% se definió como una VSM de la CI ≥125cm/s, una RVSM ≥2,0 y una VTD ≥40cm/s. Una estenosis con casi oclusión se definió como una VSM de la CI variable (alta, baja o indetectable) y una estimación de la placa > 95. La estenosis intracraneal ≥ 50% y < 50% se definió como una VSM ≥155/≥120cm/s (arteria cerebral anterior); ≥ 220/≥155cm/s (arteria cerebral media); ≥145/≥100cm/s (arteria cerebral posterior) respectivamente. El aneurisma de la aorta abdominal se definió como un diámetro de la aorta abdominal ≥ 3cm.
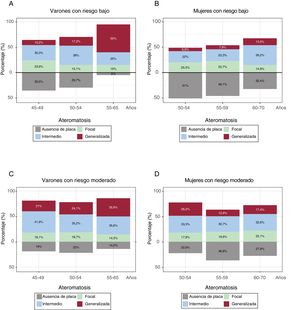
La relación entre la carga de ateromatosis subclínica y la edad se muestra en la figura 4. La ateromatosis generalizada aumentaba con la edad en los varones. El aumento fue mayor en los varones con riesgo bajo que con riesgo moderado, como pone de manifiesto el aumento de 5,4 veces en los varones con riesgo bajo (el 10,2% de los de 45-49 frente al 55% de los de 55-65 años) y de 1,7 veces en los varones con riesgo moderado (el 21% de los de 45-49 años frente al 35,9% de los de 55-65 años). Se observó una tendencia similar en las mujeres con riesgo bajo (el 6,6% de las de 50-54 años frente al 13,5% de las de 60-70 años). En cambio, hubo una reducción con el avance de la edad en las mujeres con riesgo moderado (el 26,2% en las de 50-54 años frente al 17,4% de las de 60-70 años).
Presencia de ateromatosis subclínica según las ecuaciones de riesgo tradicionales. A-D: presencia y carga de ateromatosis según el SCORE de riesgo europeo a 10 años estratificado según el sexo y la edad. La ateromatosis focal se definió como la presencia de placa de ateroma en 1 de los 12 territorios, la intermedia como la placa en 2-3 territorios y la generalizada como la placa en más de 3 territorios.
El área media de placa de ateroma fue mayor en los varones que en las mujeres (0,97 frente a 0,58cm2; p <0,001). Las placas eran mayores en las arterias femorales que en las carótidas (0,72 frente a 0,33; p <0,001) (tabla 4). El área de placa aumentaba en función de la prevalencia de FRCV y del número de territorios con placa (figura 5).
Se observó enfermedad arterial periférica en un 11% de los participantes. Un 10,4% de ellos tenían un índice tobillo-brazo ≤ 0,9 (que indica estenosis) y el 0,64%, > 1,4 (que indica rigidez vascular). La estenosis fue más frecuente en las mujeres, mientras que la rigidez vascular lo fue en los varones (el 12,3 frente al 8,2% y el 1,2 frente al 0,1% respectivamente; p=0,006). En la ecografía transcraneal se identificaron 68 casos (1,1%) con estenosis <50% y 2 casos con estenosis ≥ 50%. Por último, el examen de detección de posibles aneurismas de la aorta abdominal en los varones de más de 60 años identificó 17 casos (1,8%) (tabla 4).
DISCUSIÓNLos resultados más importantes del presente estudio son los siguientes: a) el estudio ILERVAS identificó varias enfermedades crónicas no diagnosticadas previamente, como dislipemia, hipertensión, diabetes, obesidad y enfermedad renal, en una población general por lo demás sana; b) hubo una gran prevalencia de ateromatosis subclínica en una población de mediana edad por lo demás sana, y la localización más frecuente fue la arteria femoral común, seguida de la bifurcación carotídea y la carótida interna; c) una tercera parte de los participantes, clasificados como en riesgo cardiovascular bajo-moderado, tenían una ateromatosis intermedia (2-3 territorios con placa del total de 12 examinados) y una quinta parte, ateromatosis generalizada (> 3 territorios), y d) el área total de placa aumenta a medida que se incrementa el número de FRCV.
El estudio ILERVAS es el primero que ha realizado un examen exhaustivo y global de detección de ateromatosis, enfermedad renal crónica, diabetes y prediabetes ocultas en una población asintomática de mediana edad con al menos 1 FRCV, representativa de la población general. La unidad móvil se desplazó por toda la provincia de Lleida, reclutando a pacientes de todos los municipios para obtener una muestra representativa de la población general que cumplía los criterios de inclusión.
Son pocos los estudios de cohorte en los que se ha investigado la prevalencia de la carga de ateromatosis con ecografía vascular en múltiples localizaciones vasculares en participantes de mediana edad que no han sufrido ningún evento cardiovascular. En cambio, otros estudios similares centrados en la ateromatosis realizados en España, como el PESA y el AWHS, incluyeron solo a empleados del Banco Santander de Madrid (Madrid, España) o de la planta de fabricación de automóviles de General Motors de Figueruelas (Zaragoza, Aragón, España) respectivamente. En consecuencia, hay un claro sesgo de edad e incluso de sexo que podría afectar a los resultados en esas cohortes. Nuestros datos pusieron de manifiesto una prevalencia del 71,4% de ateromatosis subclínica en una población de mediana edad, que es superior a la indicada por el estudio PESA, en el que se identificó ateromatosis en un 63% de los participantes9. La mayor prevalencia de ateromatosis en nuestro estudio podría deberse al hecho de que nuestra cohorte tiene una edad que, en promedio, es 12 años mayor, si bien en nuestra cohorte hay una mayor representación de mujeres (el 51% en el estudio ILERVAS frente al 37% en el estudio PESA). Por otro lado, el estudio AWHS (Aragon Workers’ Health Study), con participantes de menos edad, pero únicamente varones, mostró una prevalencia del 72%14, ligeramente inferior al 79,7% de nuestra subpoblación de varones, probablemente por su edad mayor.
De manera similar a lo observado en los estudios PESA y AWHS14, la arteria femoral fue la localización vascular afectada con más frecuencia, posiblemente por la tensión tangencial y la alteración del flujo sanguíneo debidos a la forma curvada de la arteria15. En las arterias femorales, la asociación de la ateromatosis con los factores de riesgo fue más intensa que en las arterias carótidas o coronarias14. Las placas de ateroma femorales mostraron un valor predictivo de eventos cardiovasculares similar, y la mayor carga de placa, con placas tanto en las arterias carótidas como en las femorales, incrementó el riesgo aún más16. Así pues, la evaluación de la arteria femoral podría mejorar la evaluación del riesgo.
Nuestro trabajo confirmó también la ausencia de correlación entre la evaluación del riesgo cardiovascular a 10 años estimado con los datos clínicos y la presencia real de una ateromatosis subclínica9,17,18. Hasta un 58% de los individuos considerados en bajo riesgo del estudio PESA y un 57% de los del estudio AWHS tenían ateromatosis. En cambio, en la cohorte del estudio ILERVAS, el 71,4% de nuestros participantes con riesgo bajo-moderado presentaban una ateromatosis subclínica. Por lo que respecta a la carga de ateromatosis, una tercera parte de los participantes clasificados como en riesgo bajo-moderado tenían una ateromatosis intermedia (2-3 territorios con placa del total de 12 examinados) y una quinta parte tenía una ateromatosis generalizada (> 3 territorios). Se obtuvieron unos resultados similares en el estudio PESA, en el que una tercera parte de los participantes con riesgo bajo mostraron afección en 2 localizaciones. Tradicionalmente, la ausencia de FRCV convencionales se ha considerado un indicador fiable de un riesgo bajo de ateromatosis. Sin embargo, los investigadores del estudio PESA identificaron una ateromatosis multiterritorial en casi un 30% de los participantes sin FRCV. Así pues, la ateromatosis se asocia con factores que no están incluidos en las escalas de riesgo habituales, aspecto este que requerirá más investigación19.
En concordancia con lo indicado por estudios previos, el estudio ILERVAS reveló que el área de la placa de ateroma era de casi el doble en los varones que en las mujeres20,21. Se ha descrito que la prevalencia de ateroesclerosis en las arterias carótidas es baja en las mujeres antes de la menopausia y que luego pasa a ser similar a la de los varones22. Una posible explicación es que las mujeres obtengan un beneficio con los efectos protectores de las hormonas ováricas y que los varones tengan posiblemente más conductas nocivas para la salud, como el tabaquismo23. Además, se observó un área mayor en las arterias femorales en ambos sexos, aun cuando la presencia de placas fue más frecuente en las arterias femorales de los varones, pero lo fue en cambio en las arterias carótidas de las mujeres. Se obtuvieron unos resultados similares en el estudio PESA con ecografía vascular tridimensional21.
La prevalencia de la estenosis intracraneal fue extremadamente baja en comparación con la del estudio Barcelona-AsiA24 (el 1,72 frente al 8,6%). La cohorte del estudio Barcelona-AsiA era una población de más edad y con un riesgo cardiovascular moderado-alto de un entorno urbano. Otras comparaciones similares con poblaciones asiáticas han mostrado también una reducción drástica al comparar poblaciones urbanas de edad avanzada25 con poblaciones rurales más jóvenes26, con una reducción de la prevalencia que pasa del 24,5 al 4,7%.
En el 45,2% de los participantes había un riesgo alto de apnea obstructiva del sueño (AOS) según lo indicado por el cuestionario de Berlín. Esta prevalencia es superior a la descrita anteriormente en la población general27–29. Esta diferencia podría deberse a que los participantes eran de más edad y tenían como mínimo 1 FRCV. La ASO es un trastorno del sueño frecuente que se asocia con mala calidad de vida, alteraciones cardiometabólicas y presión arterial alta, lo cual contribuye a la patogenia de la enfermedad cardiovascular30.
Limitaciones y puntos fuertesNuestro estudio tiene varias limitaciones que es preciso señalar. En primer lugar, los parámetros de bioquímica hemática se obtuvieron con análisis de mancha de sangre seca y se usaron tiras reactivas de orina para determinar la razón de albúmina/creatinina. Es importante señalar que estos sistemas son métodos de bioquímica clínica ampliamente validados, cuyos resultados muestran una alta correlación con los métodos analíticos estandarizados31–33. En segundo lugar, el perfil lipídico se evaluó solo en los participantes con colesterol total ≥ 200mg/dl tras 6 h en ayunas o colesterol total ≥ 250mg/dl con cualquier tiempo en ayunas. Aunque esta no es la recomendación estándar, las guías recientes proponen que en los adultos de edad ≥ 20 años que no están en tratamiento hipolipemiante (el 81,4% de los participantes de nuestra cohorte), la determinación del perfil lipídico sea en ayunas o no es eficaz para estimar el riesgo cardiovascular ateroesclerótico y registrar el cLDL34. En tercer lugar, la duración de la actividad física y el consumo de alimento se registraron según lo indicado por los propios participantes. En este estudio no se utilizaron dispositivos llevados por los participantes para el registro de la actividad ni se utilizó un registro de la dieta ponderado para obtener un patrón de alimentación detallado. Aunque se trata de cuestionarios validados y utilizados internacionalmente para caracterizar los parámetros de estilo de vida, el cuestionario IPAQ ha mostrado un sesgo sistemático quesubestima el gasto de energía asociado con la actividad física para los niveles de actividad física elevados35. En cambio, el cuestionario MEDAS de 14 ítems mostró una concordancia elevada con un cuestionario detallado y completo de frecuencia alimentaria. Así pues, el cuestionario MEDAS es una herramienta útil en los ensayos clínicos y en la práctica clínica para evaluar la adherencia a la dieta mediterránea36. En cuarto lugar, los parámetros respiratorios y la ecografía transcraneal se registraron en una submuestra de los participantes (6.209 y 6.301 respectivamente). Por último, los resultados del estudio ILERVAS no pueden generalizarse al conjunto de la población, ya que los participantes eran personas españolas de mediana edad y con un riesgo cardiovascular bajo-moderado. Así pues, serán necesarios más estudios en los que estén representados todos los grupos de edad para confirmar nuestros resultados.
Por otra parte, nuestro estudio tiene varios puntos fuertes. En primer lugar, la población de estudio se aleatorizó y se utilizó un muestreo estratificado a partir de los registros de atención primaria con objeto de reducir el sesgo de selección y obtener una cohorte representativa de toda la provincia. En segundo lugar, la unidad móvil se desplazó por toda la provincia de Lleida. Ello nos permitió cubrir pueblos aislados o de difícil acceso que generalmente no se incluyen en los estudios de cohortes, y realizar ecografías llevadas a cabo por el mismo equipo itinerante, con lo que se evita un sesgo interevaluadores. En tercer lugar, en los participantes se realizó un examen de cribado de ateromatosis subclínica, enfermedad renal, trastornos del sueño y función pulmonar. El protocolo fue diseñado y supervisado por varios médicos y enfermeras especialistas. El equipo del estudio ILERVAS es un equipo multidisciplinario formado por especialistas en diagnóstico por la imagen vascular, nefrólogos, médicos de atención primaria, neumólogos, neurólogos, enfermeras, internistas, endocrinólogos y epidemiólogos. Por último, este proyecto tiene un valor añadido por lo que respecta a la prevención primaria. El estudio ILERVAS identificó casos no diagnosticados previamente de varias enfermedades crónicas subclínicas, como ateromatosis, prediabetes, diabetes, enfermedad renal oculta, trastornos respiratorios e incluso aneurismas aórticos, en una población con riesgo cardiovascular bajo-moderado de la región nororiental de España.
CONCLUSIONESEn conclusión, nuestra unidad móvil detectó varias enfermedades crónicas no diagnosticadas con anterioridad, como dislipemia (21,1%), hipertensión (15,3%), enfermedad renal (15,4%), obesidad (10,6%) y diabetes (2,3%), en participantes de mediana edad que no habían sufrido previamente ningún evento cardiovascular. La ateromatosis subclínica tuvo una prevalencia elevada (71,4%) en esta cohorte, clasificada como de riesgo cardiovascular bajo-moderado con los algoritmos actuales. La localización más frecuente de las placas de ateroma fue la arteria femoral común, seguida de la bifurcación carotídea y de la carótida interna, y una tercera parte de la cohorte presentaba una ateromatosis intermedia (2-3 territorios con placas de ateroma) y una quinta parte, una ateromatosis generalizada (> 3 territorios). El área de placa de ateroma fue mayor en las arterias femorales que en las arterias carótidas, y aumentaba a medida que se incrementaban el número de FRCV y el número de territorios vasculares afectados. En los varones las placas fueron mayores que en las mujeres.
- –
La enfermedad cardiovascular ateromatosa es la principal causa de mortalidad y discapacidad en la mayoría de los países.
- –
La asociación de la placa de ateroma con los eventos cardiovasculares está ampliamente confirmada.
- –
Aunque los eventos adversos relacionados con la ateromatosis se producen con frecuencia incluso en personas con riesgo cardiovascular bajo-moderado, solo se han realizado unos pocos estudios en esa población.
- –
El estudio ILERVAS es una cohorte aleatorizada representativa de una población general española, en la que se examina de forma exhaustiva y global la posible presencia de ateromatosis en personas de mediana edad asintomáticas que tienen como mínimo 1 FRCV.
- –
El análisis de los datos reveló que una tercera parte de los participantes tenían una ateromatosis intermedia (2-3 territorios con placa de ateroma) y una quinta parte tenían una ateromatosis generalizada (> 3 territorios).
- –
El área de placa de ateroma fue mayor en las arterias femorales que en las arterias carótidas, y aumentaba a medida que se incrementaban el número de FRCV y el número de territorios vasculares afectados. En los varones las placas fueron mayores que en las mujeres.
Este trabajo fue financiado por subvenciones de la Diputació de Lleida, el Instituto de Salud Carlos III (RETIC RD16/0009/0011) y el Ministerio de Ciencia, Innovación y Universidades (IJC2018-037792-I).
CONFLICTO DE INTERESESNinguno.
Los autores agradecen a Virtudes María, Marta Elias, Teresa Molí, Cristina Domínguez, Noemí Nova, Alba Prunera, Núria Sans, Meritxell Soria, Francesc Pons, Rebeca Senar, Pau Guix, Fundació Renal Jaume Arnó y a los equipos de atención primaria de la provincia de Lleida por la inscripción de los participantes y por sus esfuerzos para facilitar el desarrollo exacto del proyecto ILERVAS. Las muestras se obtuvieron con el apoyo del IRBLleida Biobank (B.0000682) y la Plataforma Biobancos PT17/0015/0027.