En cardiología, los anticoagulantes se utilizan ampliamente para reducir las complicaciones tromboembólicas en pacientes con síndromes coronarios agudos (SCA) o a los que se practica una intervención coronaria percutánea (ICP), en pacientes con válvulas cardiacas mecánicas o que presentan fibrilación auricular (FA) y una puntuación CHADS2 (denominada así por las siglas en inglés de: insuficiencia cardiaca congestiva, hipertensión, edad ≥ 75, diabetes, antecedentes de ictus o accidente isquémico transitorio) ≥ 2 o enfermedad valvular concomitante1. En los pacientes con SCA incluidos en los ensayos clínicos, el riesgo de muerte cardiovascular, infarto de miocardio (IM) no mortal o ictus durante el primer año siguiente a la hospitalización continúa siendo alto (aproximadamente un 10%), a pesar del empleo de los mejores tratamientos antitrombóticos disponibles2. Las posibles alternativas a las heparinas y a los actuales antagonistas de la vitamina K (AVK) son los antagonistas directos del factor de la coagulación (F) Xa («xabanes»), el inhibidor directo de trombina (IDT) dabigatrán etexilato y la tecarfarina, un nuevo AVK, que se encuentran en fases avanzadas de desarrollo clínico (fig. 1 y tabla 1)3-10.
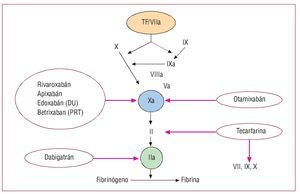
Fig. 1. Esquema de la coagulación. Las flechas punteadas indican lugares de inhibición por la acción de los diversos compuestos. Modificado de Weitz et al3. FVIIa: factor VIIa; TF: factor tisular.
Los xabanes son moléculas de síntesis pequeñas y potentes (constante de disociación [Ki] situada en un intervalo nanomolar bajo) que inhiben de manera reversible la subunidad catalítica del FX activo, tanto en la fase soluble como en la unida al complejo de la protrombinasa11. La inhibición es directa, sin productos intermedios como la antitrombina. Dada la farmacocinética lineal y la ausencia de interacciones con los alimentos, no es necesaria una monitorización sistemática del efecto anticoagulante11. Muchos xabanes se absorben por vía oral, con un tiempo hasta alcanzar la concentración plasmática máxima (tmáx) de unas 2 h y una semivida plasmática (t1/2) de unas 10 h. Constituyen excepciones notables al respecto el otamixabán (Sanofi aventis), que se administra por vía intravenosa (i.v.), con un inicio rápido de la acción y una t1/2 de 30 min6, y el betrixabán (Merck/Portola Pharmaceuticals), con una semivida de 19 h y una excreción casi exclusivamente por vía biliar11. La eliminación renal es > 50% para el edoxabán tosilato (Daiichi Sankyo), de alrededor de 1/3 para el rivaroxabán (Xarelto®, Bayer/Johnsons & Johnson) y para el apixabán (Bristol-Myers Squibb/Pfizer), de un 10-30% para el otamixabán, y muy marginal para el betrixabán6,11. La biodisponibilidad es buena en todos los xabanes orales11.
El IDT oral dabigatrán etexilato (Pradaxa®, Boehringer Ingelheim) es un profármaco que se convierte rápidamente en dabigatrán activo en el intestino, el plasma y el hígado. El dabigatrán se une de modo univalente y reversible al FIIa (es decir, la trombina) tanto soluble como fijado. Parece no ser hepatotóxico. Su biodisponibilidad es baja (alrededor de un 7%). Las concentraciones plasmáticas máximas se alcanzan 2 h después de la toma por vía oral. La t1/2 circulante es de unas 15 h9. Su excreción predominante por vía renal hace que esté contraindicado en pacientes con insuficiencia renal9. A diferencia del rivaroxabán y del apixabán, no se ve influido por el sistema del citocromo P450 (CYP). Dada su farmacocinética predecible, no requiere una monitorización regular9. Debe reducirse la dosis en alrededor de 1/4 si el paciente toma amiodarona, y debe evitarse el empleo de quinidina (prospecto de Pradaxa®). El rivaroxabán y el dabigatrán etexilato se comercializan y han sido autorizados en Europa, Canadá y Reino Unido para la prevención de la tromboembolia venosa después de una artroplastia total de cadera o de rodilla. La tecarfarina (ARYx Therapeutics) es un antagonista de la VK epóxido reductasa, con una semivida terminal media de 119 h. Su mecanismo de acción es idéntico al de la warfarina y la monitorización se realiza mediante la razón normalizada internacional (INR)10. A diferencia de la warfarina, la tecarfarina es metabolizada por esterasas y escapa a los efectos de las interacciones de alimentos o fármacos metabolizados a través del CYP, así como a los de las variaciones genéticas existentes en el sistema del CYP10.
Nuevos anticoagulantes en pacientes con síndromes coronarios agudos o a los que se practican intervenciones coronarias percutáneas electivas
Los anticoagulantes rivaroxabán, apixabán, otamixabán y dabigatrán se han estudiado en cuanto a su seguridad, tolerabilidad y eficacia en estudios piloto, mediante ensayos de fase II, aleatorizados, a doble ciego, de determinación de dosis, que han sido publicados (tabla 1)4-9. En la actualidad, se están realizando estudios de fase III con tres inhibidores del FXa.
Inhibidores de FXa
1. Rivaroxabán en los síndromes coronarios agudos. En el ATLAS ACS-TIMI 46 se estudiaron 4 dosis diferentes de rivaroxabán (5, 10, 15 y 20 mg de dosis diaria total administradas en 1 o 2 tomas) en comparación con placebo, en 3.491 pacientes con SCA (el 52% con IM con elevación del ST, el 10% con IM sin elevación del ST, el 17% con angina inestable, el 64% tratados con ICP) que se incorporaron al ensayo 1-7 días después del ingreso y seguidos durante 6 meses. Se estratificó a los pacientes, a criterio de los investigadores, para usar ácido acetilsalicílico solamente (n = 761) o bien ácido acetilsalicílico y una tienopiridina (n = 2.730). La incidencia de hemorragias mayores y menores según los criterios TIMI (Thrombolysis In Myocardial Infarction), o que requieran atención médica, aumentó con el incremento de las dosis de rivaroxabán: el 6,1, el 10,9, el 12,7 y el 15,3% frente al 3,3% con placebo (p < 0,0001). Las tasas de muerte, IM no mortal, ictus o isquemia recurrente grave con necesidad de revascularización (objetivo primario de la eficacia) fueron del 5,6% con rivaroxabán frente al 7% con placebo (razón de riesgos [HR] = 0,79; p = 0,1), mientras que las tasas del objetivo secundario principal de la eficacia (muerte, IM no mortal o ictus no mortal) fueron del 3,9 frente al 5,5% (HR = 0,69; p = 0,027)4. El ATLAS ACS 2-TIMI 51, un ensayo de fase III, controlado con placebo y basado en los eventos clínicos, está estudiando si el rivaroxabán (2,5 y 5 mg dos veces al día) durante un periodo de al menos 6 meses, añadido a la asistencia estándar, puede reducir el riesgo de muerte cardiovascular, IM o ictus, en un grupo de hasta 16.000 pacientes con un SCA reciente, con unas tasas de hemorragia aceptables (NCT00809965; fecha prevista de finalización, junio de 2011).
2. Apixabán en síndromes coronarios agudos. El APPRAISE-1 incluyó a 1.715 pacientes, en los 7 días siguientes a un SCA (el 63% con IM con elevación del ST, el 30% con IM sin elevación del ST, el 8% con angina inestable) y se los asignó aleatoriamente al tratamiento con 1 de 4 dosis posibles de apixabán (2,5 mg dos veces al día, 10 mg una vez al día, 10 mg dos veces al día o 20 mg una vez al día) o con placebo, durante 6 meses5. Los pacientes incluidos en el ensayo estaban clínicamente estables y presentaban al menos un factor de riesgo adicional para la isquemia recurrente. Casi todos recibieron ácido acetilsalicílico y un 76% recibió también clopidogrel. La 2 dosis superiores de apixabán se interrumpieron a causa de un exceso de hemorragias al combinarlas con el tratamiento antiagregante plaquetario doble. Las tasas de hemorragias con apixabán mostraron un aumento dependiente de la dosis: el 5,7% con 2,5 mg dos veces al día (p = 0,09) y el 7,9% con 10 mg una vez al día (p = 0,005) frente al 3% con placebo. Las hemorragias se definieron según los criterios de la International Society of Thrombosis and Hemostasis (ISTH) como mayores (mortales, intracraneales, intramedulares, intraoculares, retroperitoneales, intraarticulares, intramusculares; con síndrome compartimental, pericárdico, con una reducción ≥ 2 g/dl de la hemoglobina o transfusión ≥ 2 unidades de concentrados de hematíes) o no mayores clínicamente relevantes ([NMCR], es decir, con necesidad de intervención médica o quirúrgica). Las tasas de muerte cardiovascular, IM no mortal, isquemia recurrente grave o ictus isquémico fueron del 7,6% con la dosis de apixabán de 2,5 mg dos veces al día (HR = 0,73; p = 0,21) y del 6% con la dosis de 10 mg una vez al día (HR = 0,61; p = 0,07), en comparación con el 8,7% con placebo. Las tasas de hemorragia aumentaron, y las de episodios isquémicos se redujeron en los pacientes tratados con ácido acetilsalicílico junto con clopidogrel, en comparación con los tratados con ácido acetilsalicílico solo5. En el estudio de fase III APPRAISE-2 se está investigando el empleo de apixabán (5 mg dos veces al día), en comparación con placebo, en lo relativo a la seguridad y la eficacia, al utilizarlo como tratamiento adicional, en hasta 11.000 pacientes en alto riesgo con un IM reciente (NCT00831441; fecha estimada de finalización, noviembre de 2011).
3. Otamixabán en intervenciones coronarias percutáneas y en síndromes coronarios agudos. Se ha investigado el empleo del otamixabán en 2 ensayos de fase II. En el SEPIA-PCI se estudió a 947 pacientes tratados con ICP no urgente, a los que se asignó aleatoriamente a la administración de un bolo i.v. antes de la intervención, seguido de una infusión de 3 h de una de 5 posibles posologías de otamixabán, ajustadas según el peso o bien a heparina no fraccionada (HNF) ajustada según el peso. Al final de las infusiones de dosis crecientes de otamixabán, la mediana de actividad anti-FXa osciló entre 65 y 691 ng/ml y la mediana de los cocientes de tiempo de tromboplastina parcial activado (TTPa) fue de 1,1 a 2,26. Se produjeron hemorragias mayores o menores, según criterios TIMI, durante la hospitalización, en el 2, el 1,9, el 3,8, el 3,9 y el 2,6% de los pacientes, con las dosis crecientes de otamixabán, y en un 3,8% de los controles. Se produjeron episodios isquémicos (muerte, IM, revascularización de vaso diana) en un plazo de 30 días en el 5,8, el 7,1, el 3,8, el 2,5 y el 5,1 de los pacientes, con las dosis crecientes de otamixabán, y en el 5,6% de los controles. Así pues, las dosis 3 y 4 de otamixabán (que correspondían a 0,12 y 0,16 mg/ kg/h) se asociaron a unas tasas inferiores de eventos isquémicos y unas tasas de hemorragia similares a las de la HNF11.
El ensayo SEPIA-ACS1 TIMI 42 comparó a 3.241 pacientes con SCA sin elevación del ST, tratados con una ICP temprana, que recibieron 1 de las 5 dosis distintas de otamixabán i.v. (0,08 mg/kg en bolo seguido de una infusión de 0,035, 0,07, 0,105, 0,14 o 0,175 mg/kg/h hasta el final de la ICP) en comparación con HNF (60 UI/kg i.v. en bolo, seguido de una infusión de 12 UI/kg/h hasta el final de la ICP) junto con eptifibatida (180 μg/kg en bolo i.v., seguido de una infusión de 1-2 μg/ kg/min durante 18-24 h)7. La posología más baja de otamixabán utilizada en el estudio se suspendió prematuramente al observarse una tendencia a un aumento de las tasas de complicaciones trombóticas. La incidencia de muerte por todas las causas, IM, revascularización urgente o uso como medicación de rescate de inhibidores de glucoproteína IIb/IIIa en un plazo de hasta 7 días fue del 7,2, el 4,6, el 3,8, el 3,6 y el 4,3% con las dosis crecientes de otamixabán (p = 0,34 para la tendencia) en comparación con el 6,2% en los controles. Las tasas de hemorragia TIMI mayor o menor no relacionadas con cirugía de revascularización arterial en un plazo de 7 días fueron del 1,6, el 1,6, el 3,1, el 3,4 y el 5,4% con las dosis crecientes de otamixabán (p < 0,0001 para la tendencia) en comparación con el 2,7% en los controles. Las pautas de tratamiento con otamixabán en bolo + infusión de 0,105-0,14 mg/kg/h están siendo consideradas para el uso en un ensayo de fase III7.
Dabigatrán etexilato en síndromes coronarios agudos
En el ensayo RE-DEEM (NCT00621855), recientemente completado pero aún sin publicar, se compararon 4 dosis diferentes de dabigatrán etexilato (50, 75, 110 y 150 mg dos veces al día) con placebo, además del tratamiento antiagregante plaquetario combinado doble, en 1.861 pacientes con IM con (60%) o sin elevación del ST (40%) que tenían un riesgo elevado de sufrir nuevos episodios isquémicos (el 29% con IM previo, el 31% con diabetes mellitus y el 12% con insuficiencia cardiaca). Se practicó una ICP en el 54% de los casos. El tratamiento se inició en un plazo de 14 (media, 7,4) días y tuvo una duración de 6 meses. Los resultados preliminares indican que las tasas de hemorragias mayores, según los criterios de la ISTH, aumentaron de forma moderada al incrementar la dosis de dabigatrán (p para la tendencia < 0,001), con valores del 0,8, el 0,3, el 2 y el 1,2% para las dosis crecientes de dabigatrán, en comparación con el 0,5% con placebo. Los valores de dímero D disminuyeron en un 45% en todos los grupos de dabigatrán en un plazo de 6 meses (p < 0,001 frente a placebo). La tasa global de episodios de muerte cardiovascular, IM no mortal o ictus no mortal fue baja (Oldgren J et al. Randomised dabigatran etexilate dose finding study in patients with acute coronary syndrome post index event with additional risk factors for cardiovascular complications also receiving aspirin and clopidogrel: RE-DEEM. Sesiones científicas de la American Heart Association en Orlando, FL, 18 de noviembre de 2009).
Nuevos anticoagulantes en pacientes con fibrilación auricular
En varios estudios de fase III se está comparando el tratamiento con rivaroxabán, apixabán y edoxabán tosilato con el de warfarina o el de ácido acetilsalicílico en pacientes con FA no valvular (tabla 1). Se ha publicado otro ensayo amplio con dabigatrán etexilato9. La tecarfarina y el betrixabán se han investigado tan sólo en estudios de fase II10.
Inhibidores de FXa
1. Rivaroxabán en la fibrilación auricular. El ROCKET AF es un ensayo de fase III, a doble ciego, con doble placebo y basado en los episodios clínicos, cuyo objetivo es establecer la no inferioridad del rivaroxabán (20 mg una vez al día) comparado con warfarina (objetivo de INR 2,5) en la prevención de la tromboembolia en 14.269 pacientes con FA no valvular y antecedentes de ictus o al menos otros dos factores de riesgo para un futuro ictus. El objetivo primario de eficacia es la combinación de ictus (isquémico y hemorrágico) y embolia sistémica. Los objetivos secundarios de eficacia incluyen los accidentes isquémicos transitorios, la muerte por cualquier causa, la muerte vascular y el IM. El objetivo primario de seguridad es la combinación de hemorragias mayores o NMCR según los criterios de la ISTH. Los pacientes asignados al tratamiento con rivaroxabán reciben este fármaco + placebo de warfarina con el uso de valores simulados de INR. Los pacientes asignados a warfarina reciben warfarina 1 vez al día + placebo de rivaroxabán. El ensayo se inició en diciembre de 2006 y se espera que continúe hasta que se hayan observado 405 episodios del objetivo primario12.
2. Apixabán en la fibrilación auricular:
- El estudio ARISTOTLE (NCT00412984) es un ensayo de fase III, a doble ciego, con doble placebo, basado en los episodios clínicos13, en el que se estudia la no inferioridad del apixabán (5 mg dos veces al día) frente a la warfarina (INR 2-3) en la prevención del ictus y la embolia sistémica en 18.206 pacientes con FA no valvular y una puntuación CHADS2 ≥ 1 (incluidos aproximadamente un 40% de los pacientes no tratados anteriormente con warfarina). El objetivo secundario era la hemorragia mayor según criterios del ISTH. La duración prevista del tratamiento es de 1 a 4 años, para incluir un total de al menos 448 episodios del objetivo primario de eficacia. Dado que el límite para la no inferioridad es de 1,38, el apixabán se declarará no inferior si el intervalo de confianza del 95% excluye la posibilidad de que la frecuencia de los eventos del objetivo principal con apixabán sea > 1,38 veces la observada con warfarina13. Se estima que el estudio se completará en 2011.
- El estudio AVERROES (NCT00496769) es un ensayo de fase III, a doble ciego, con doble placebo, en el que se compara el apixabán 5 mg dos veces al día con el ácido acetilsalicílico 81 a 324 mg una vez al día en 5.600 pacientes con FA y uno o varios factores de riesgo para el ictus, que no toleran los AVK o no son aptos para su uso14. Recientemente se ha anunciado la interrupción prematura de este ensayo a causa de una importante reducción de los ictus y las embolias sistémicas con apixabán, con unas tasas aceptables de hemorragia mayor según los criterios de la ISTH (http://www.news-medical. net/news/20100611/Phase-3-AVERROES-clinical-trial-of-apixaban-for-atrial-fibrillation-closes-early-due-to-clear-evidence-of-efficacy.aspx [citado 7 Ago 2010]).
- En el reciente estudio ACTIVE-A, la combinación de ácido acetilsalicílico y clopidogrel fue una alternativa eficaz al ácido acetilsalicílico solo para la prevención del ictus en la FA, a costa de un aumento de las tasas de hemorragia14. En el estudio AVERROES, no se incluyó a pacientes tratados con la combinación de ácido acetilsalicílico y clopidogrel.
3. Edoxabán tosilato en la fibrilación auricular. Un estudio de fase II ya completado incluyó a 1.146 pacientes con FA no valvular y una puntuación CHADS2 ≥ 2, asignados aleatoriamente al tratamiento con 4 pautas diferentes de edoxabán tosilato (30 o 60 mg de dosis diaria total, administrados en 1 o 2 tomas), con diseño ciego, o al tratamiento abierto con warfarina (INR 2-3), durante 3 meses. La incidencia de hemorragias mayores o NMCR según criterios de la ISTH en los grupos de tratamiento con 30 y 60 mg una vez al día fue similar o mejor que la observada en el grupo de warfarina11. Estas dosis (30 y 60 mg una vez al día) se están comparando con la warfarina (INR 2-3) en el estudio de fase III, a doble ciego y con doble placebo, ENGAGE AF-TIMI 48 respecto a la prevención del ictus, en el que se incluye aproximadamente a 16.500 pacientes con FA no valvular y una CHADS2 ≥ 2. El objetivo primario de eficacia son los ictus y los episodios embólicos sistémicos; el objetivo primario de seguridad son las hemorragias mayores y NMCR según los criterios de la ISTH. La mediana prevista de duración del tratamiento es de 24 meses y se estima que se completará el estudio en la primera mitad de 2012 (NCT00504556).
4. Betrixabán en la fibrilación auricular. El estudio de fase II de determinación de dosis EXPLORE-Xa, recientemente completado, incluyó a 508 pacientes con FA o aleteo (flutter) auricular no valvulares y al menos un factor de riesgo para el ictus, a los que se asignó aleatoriamente a tratamiento con 3 dosis de betrixabán posibles (40, 60 u 80 mg una vez al día), con diseño ciego, en comparación con el tratamiento abierto con dosis ajustadas de warfarina (INR 2-3 a intervalos máximos de 4 semanas). La media de edad fue de 74 años; el 87% de los pacientes estaban siendo tratados anteriormente con AVK; se incluyó en el estudio a pacientes con un deterioro grave de la función renal (pero no a pacientes en diálisis). Tras una mediana de seguimiento de 5 meses, la incidencia de hemorragias mayores o NMCR fue del 0,8, el 3,9 y el 3,2% con las dosis crecientes de betrixabán frente al 3,2% con warfarina (p = 0,035 para 40 mg frente a warfarina). Las tasas de episodios de muerte, ictus, IM u otra embolia sistémica fueron de 0-1 en cada uno de los cuatro grupos. Los acontecimientos adversos más frecuentes con betrixabán fueron la diarrea y las náuseas. Se está desarrollando un antídoto específico para el betrixabán (Ezekowitz MD et al. A phase 2, randomized, parallel group, dose-finding, multicenter, multinational study of the safety, tolerability and pilot efficacy of three blinded doses of oral factor Xa inhibitor betrixaban compared with open-label dose-adjusted warfarin in patients with non-valvular atrial fibrillation [Explore-Xa]. 59.a sesión científica anual del American College of Cardiology, en Atlanta, EEUU, 15 de marzo de 2010).
Dabigatrán etexilato en la fibrilación auricular
El estudio de fase II PETRO incluyó a 502 pacientes con FA no valvular (el 38%, permanente; el 39%, persistente; el 23%, paroxística) y una puntuación CHADS2 ≥ 1, a los que se aleatorizó con diseño ciego al tratamiento con dosis de 50, 150 o 300 mg de dabigatrán etexilato dos veces al día —solo o en combinación con 81 o 325 mg de ácido acetilsalicílico— o a tratamiento abierto con warfarina (INR 2-3), durante 12 semanas8. Los episodios hemorrágicos mayores (según la definición de la ISTH) se limitaron a los pacientes tratados con dabigatrán 300 mg dos veces al día más ácido acetilsalicílico, mientras que los episodios tromboembólicos se limitaron a los grupos de dabigatrán a dosis de 50 mg dos veces al día8.
En el posterior estudio de fase III RE-LY se incluyó a 18.113 pacientes con FA (el 35%, permanente; el 32%, persistente; el 33%, paroxística) a los que se asignó aleatoriamente el tratamiento con diferentes dosis de dabigatrán etexilato (110 o 150 mg dos veces al día), en diseño ciego, o el tratamiento abierto con warfarina a dosis sin ajustar9. La puntuación CHADS2 fue 0-1 en el 32% de los pacientes, 2 en el 35% y 3-6 en el 33% (media, 2,1)9. La mediana de seguimiento fue de 2 años. En los grupos tratados con warfarina, dabigatrán 110 o dabigatrán 150, las tasas de episodios del objetivo primario (ictus o embolia sistémica) fueron del 1,7%/año, el 1,5%/año (p < 0,001 para la no inferioridad frente a warfarina) y el 1,1%/año (p < 0,001 para la superioridad frente a warfarina), respectivamente. Las tasas de hemorragias mayores fueron del 3,4%/año, el 2,7%/año (p = 0,003) y el 3,1%/año (p = 0,31), respectivamente, y las de ictus hemorrágico fueron del 0,38%/año, el 0,12%/año (p < 0,001) y el 0,1%/año (p < 0,001), respectivamente. Las tasas de mortalidad fueron del 4,1%/año, el 3,8%/año (p = 0,13) y el 3,6%/año (p = 0,051), respectivamente. Se produjeron IM con una frecuencia del 0,53%/año, el 0,72%/año (p = 0,07) y el 0,74%/año (p = 0,048), respectivamente9. Así pues, comparado con la warfarina, el dabigatrán a dosis bajas fue igual de eficaz y generalmente más seguro; la dosis superior fue más eficaz e igual de segura, pero con tasas inferiores de ictus hemorrágicos y tasas ligeramente aumentadas de IM.
Tecarfarina en la fibrilación auricular
En un estudio abierto, de fase II, de una duración de 6 a 12 semanas, llevado a cabo en 66 pacientes con FA (el 17%, permanente; el 26%, persistente; el 58%, paroxística), se investigó la seguridad, la tolerabilidad y la posología óptima de la tecarfarina10. La mayor parte de los pacientes (97%) tomaba warfarina en el momento de la inclusión en el estudio, tratamiento que se cambió por el de tecarfarina. Después de 3 semanas de tratamiento, la media de tiempo interpolado de permanencia en el intervalo terapéutico fue del 71,4%. Tan sólo un 10,9% de los pacientes estuvieron algún tiempo en el intervalo terapéutico < 45%. Los tiempos de permanencia en los intervalos extremos de INR < 1,5 y > 4 fueron del 1,2 y el 1,2%, respectivamente10. El estudio señaló que la tecarfarina puede alcanzar unos porcentajes de tiempo de permanencia en el intervalo terapéutico superiores a los obtenidos con la warfarina. Sin embargo, el ensayo EmbraceAC no respaldó por completo esta conclusión; este ensayo de fase II, más amplio, a doble ciego y controlado con warfarina, se llevó a cabo en 612 pacientes (el 75% con FA) con un seguimiento de 6-9 meses. La media de tiempo interpolado de permanencia en el intervalo terapéutico fue del 73% con warfarina frente al 74% con tecarfarina (p = 0,51). Sin embargo, en el grupo preespecificado formado por los pacientes (31%) que tomaban inhibidores del CYP, la tecarfarina sí mostró una ventaja significativa (García D, Milner PG, Canafax DM, Ellis DJ. Results of the EmbraceAC trial: a head-to-head comparison of warfarin with tecarfarin, a new anticoagulant. 51.a reunión y exposición anual de la American Society of Hematology en New Orleans, EEUU, 7 de diciembre de 2009).
Perspectivas futuras
Es probable que las autoridades reguladoras aprueben el IDT oral dabigatrán etexilato para los pacientes con FA no valvular y al menos un factor de riesgo tromboembólico moderado, dado el beneficio clínico neto significativo asociado al empleo de dabigatrán en comparación con warfarina en el ensayo RE-LY9. Sin embargo, no debe pasarse por alto que la insuficiencia renal grave constituye una contraindicación para el uso de dabigatrán, y que debe mantenerse una vigilancia cuidadosa de la seguridad a largo plazo. Podría ser aconsejable el empleo de dosis inferiores de dabigatrán en los ancianos, las mujeres o los pacientes que presentan una insuficiencia renal moderada, teniendo en cuenta que, para una dosis dada, en estos pacientes hay mayor exposición al fármaco (prospecto de Pradaxa®), con el consiguiente riesgo de hemorragia. Durante el próximo año deberá determinarse si los xabanes, incluidos los que no se eliminan de manera predominante por los riñones, pueden resultar también eficaces y seguros en los pacientes con FA no valvular, en comparación con warfarina (tabla 1).
La reversibilidad y la semivida relativamente breve del dabigatrán y los xabanes harán que sean fármacos atractivos para el tratamiento perioperatorio de los pacientes cardiacos en los que hay una indicación para el uso de estos nuevos anticoagulantes; así se evitaría el proceso de tratamiento «puente». Los pacientes portadores de prótesis valvulares mecánicas no se han incluido hasta el momento en los ensayos que investigan el uso de los nuevos inhibidores directos de FXa y de FIIa. El empleo de tecarfarina como alternativa al uso de warfarina podría ser útil en esos pacientes, dado su efecto anticoagulante estable.
En los próximos 12-18 meses se obtendrán los resultados de los ensayos de fase III ATLAS y APPRAISE, en los que se abordan el riesgo y los efectos beneficiosos asociados al tratamiento con rivaroxabán o apixabán añadidos a un tratamiento antiagregante plaquetario combinado doble, tras los SCA. Los resultados preliminares del estudio RE-DEEM señalan que el dabigatrán etexilato puede añadirse al tratamiento antiagregante plaquetario combinado doble en los pacientes con SCA que presentan una FA concomitante, sin que conlleve un riesgo excesivo de hemorragias.
El empleo de anticoagulantes seguros, eficaces y de administración cómoda permitirá que una mayor proporción de los pacientes elegibles reciban realmente un tratamiento apropiado. Sin embargo, en caso de hemorragia, en la actualidad no disponemos de antídotos específicos para los inhibidores directos de FXa y FIIa, ni de análisis de laboratorio bien estandarizados para medir su efecto. Desde el punto de vista de la economía de la salud, será necesario comparar el coste de estos fármacos con el ahorro que pueden proporcionar al evitar la monitorización y respecto a los beneficios clínicos globales.
Full English text available from: www.revespcardiol.org
Correspondencia: Dra. F. Andreotti.
Institute of Cardiology. Catholic University. Largo Gemelli 8. 00168 Roma. Italia.
Correo electrónico: felicita.andreotti@iol.it