La miocardiopatía hipertrófica apical (MHA) es una forma de presentación poco frecuente de la miocardiopatía hipertrófica en Occidente (1-10%), aunque su incidencia alcanza hasta el 40% en países orientales1. Se caracteriza por aumento del grosor en el ápex del ventrículo izquierdo, que puede asociar hipertrofia medioventricular o a otro nivel. El aumento de espesor ventricular en la MHA reduce la cavidad ventricular, con disminución del volumen ventricular y aumento de la presión telediastólica2. Las alteraciones morfológicas de la MHA hacen que el síntoma predominante en estos pacientes sea disnea por insuficiencia cardiaca con fracción de eyección conservada, aunque se han descrito otras complicaciones como muerte súbita o accidente cerebrovascular3. A diferencia de las formas de miocardiopatía hipertrófica con obstrucción del tracto de salida del ventrículo izquierdo, que pueden tratarse con diversos fármacos o con cirugía, el tratamiento de la disfunción diastólica de la MHA es mucho más complejo y con pocas alternativas. Cuando los pacientes presentan una clase funcional avanzada, la única opción es un trasplante cardiaco (TxC).
En 2010, Schaff et al.4 describieron la miectomía apical para el tratamiento de la MHA, que permite la resección del exceso de músculo ventricular a través del ápex del ventrículo izquierdo. Nuestro grupo comenzó un programa para el tratamiento de pacientes con MHA en 2016, y es actualmente el único centro del país con un programa activo. Se presenta nuestra experiencia con esta técnica.
Entre enero de 2016 y agosto de 2020, un total de 6 pacientes con diagnóstico de MHA fueron intervenidos mediante miectomía apical. Sus características basales y el estudio ecocardiográfico se presentan en la tabla 1. De ellos, 5 presentaban obstrucción subaórtica y medioventricular, y ninguno mostraba aneurisma apical. Todos se encontraban en clase funcional de la New York Heart Association (NYHA) III-IV a pesar de tratamiento médico, y 2 de ellos estaban en estudio para TxC. La En todos los casos la intervención fue electiva. Tras la entrada en circulación extracorpórea y pinzamiento aórtico, se realizó una ventriculotomía izquierda apical y una resección amplia del miocardio hipertrófico del septo interventricular, de la pared libre y de la base de los músculos papilares. En 5 pacientes se hizo un acceso por aortotomía para resecar también el músculo del septo subaórtico. Uno de ellos presentaba también una degeneración mixoide, por lo que se reparó la válvula mitral mediante anuloplastia e implante de cuerdas. La mediana de la estancia hospitalaria fue 9 [intervalo intercuartílico, 8-12] días.
Características basales de los pacientes, resultados clínicos y ecocardiográficos
| Variable | |
|---|---|
| Edad (años) | 61 [40-68] |
| Sexo | |
| Varones | 1 (16,7) |
| Mujeres | 5 (83,3) |
| Disnea (NYHA III/IV) | 6 (100) |
| Síncope | 2 (33,3) |
| Angina | 3 (50) |
| DM | 2 (33,3) |
| DAI | 2 (33,3) |
| Dislipemia | 1 (16,7) |
| HTA | 2 (33,3) |
| ACV | 1 (16,7) |
| TV | 0 |
| FA | 1 (16,7) |
| MP | 0 |
| Variable | Preoperatorio | Posoperatorio |
|---|---|---|
| Disnea (NYHA III/IV) | 6 (100) | 1 (16,7) |
| ProBNP (pg/dl) | 2.122 [734-2.418] | 1.040 [732-1.040] |
| Bloqueador beta | 5 (83,3) | 5 (83,3) |
| Disopiramida | 4 (66,7) | 0 |
| IECA | 1 (16,7) | 1 (16,7) |
| Antagonista del calcio | 2 (33,3) | 0 |
| Diuréticos | 5 (83,3) | 3 (50) |
| Ecocardiograma | ||
| FEVI (%) | 68 [61-78] | 55 [44-66] |
| VTDVI (mm) | 60,5 [44,8-70,7] | 98,5 [76,1-141,0] |
| VTSVI (mm) | 21,1 [15,4-24,9] | 42,2 [28,0-66,7] |
| Grosor del septo basal | 18,2 [12,2-24,5] | 13 [8,1-19] |
| Grosor máximo MV | 26 [22,5-28,2] | 16,5 [13,7-19,2] |
| Obstrucción MV | 4 (66,7) | 0 |
| IM> 2 | 1 (16,7) | 1 (16,7) |
| SAM | 2 (33,3) | 0 |
ACV: accidente cerebrovascular; DAI: desfibrilador automático implantable; DM: diabetes mellitus; FA: fibrilación auricular; FEVI: fracción de eyección del ventrículo izquierdo; HTA: hipertensión arterial; IECA: inhibidor de la enzima de conversión de la angiotensina; IM: insuficiencia mitral; MP: marcapasos; MV: medioventricular; SAM: movimiento anterior sistólico de la válvula mitral; TV: taquicardia ventricular; VTDVI: volumen telediastólico del ventrículo izquierdo; VTSVI: volumen telesistólico del ventrículo izquierdo.
Los valores expresan n (%) o mediana [intervalo intercuartílico].
Con una mediana de seguimiento de 18 [6-24] meses, 5 pacientes mejoraron significativamente su clase funcional (NYHA I-II) y 1 paciente se mantuvo en NYHA III. Los resultados clínicos y ecocardiográficos prequirúrgicos y posquirúrgicos se presentan en la tabla 1. El estudio ecocardiográfico se realizó al sexto mes, excepto en el último paciente, a quien se le hizo 1 mes después de la intervención. En todos los casos aumentaron significativamente los volúmenes ventriculares. En la figura 1 se muestran imágenes del campo quirúrgico y volúmenes ventriculares prequirúrgicos y en el seguimiento. Una paciente que mejoró tras la intervención hasta NYHA I-II desarrolló insuficiencia mitral grave por rotura de cuerda 14 meses después de la operación, con nuevo empeoramiento de clase funcional. Requirió implante de dispositivo MitraClip.
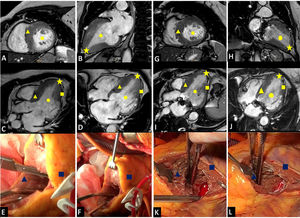
Volúmenes diastólicos del ventrículo izquierdo prequirúrgicos y en el seguimiento; imágenes del campo quirúrgico. A-D: resonancia magnética prequirúrgica en eje corto de 2 cámaras, eje largo de 2 cámaras, eje largo de 3 cámaras y eje largo 4 cámaras respectivamente. E y F: ventriculotomía; campo quirúrgico premiectomía. G-J: seguimiento con resonancia magnética en eje corto de 2 cámaras, eje largo de 2 cámaras, eje largo de 3 cámaras y eje largo de 4 cámaras. K y L: campo quirúrgico posmiectomía. Círculo: volumen telediastólico del ventrículo izquierdo. Triángulo: septo interventricular. Cuadrado: pared libre del ventrículo izquierdo. Estrella: ápex del ventrículo izquierdo.
La MHA es una enfermedad de muy difícil tratamiento en pacientes que no responden adecuadamente a los fármacos, y con una mortalidad superior a la de la población general3.
La miectomía apical se ha propuesto como una alternativa para pacientes con MHA seleccionados. Recientemente el grupo de la Clínica Mayo ha publicado sus resultados en 113 pacientes con MHA e insuficiencia cardiaca avanzada intervenidos entre septiembre de 1993 y marzo de 20175. La mortalidad hospitalaria fue del 4%. El 76% de los pacientes mejoraron su clase funcional y el 3% requirió un TxC en el seguimiento. Describen una supervivencia a 1, 5 y 10 años del 96, el 87 y el 74% respectivamente, superior a la de los pacientes con MHA en lista de espera para TxC en Estados Unidos. En nuestro país, en el periodo 2015-2019 se trasplantó a 115 pacientes con diagnóstico de MH (el 7,5% de todos los TxC realizados), con una tendencia anual creciente (datos no publicados cortesía de Francisco González-Vílchez, Registro Nacional de Trasplante Cardiaco). Aunque se desconoce cuántos de estos pacientes padecían MHA, es probable que algunos pudieran beneficiarse de esta técnica.
Nuestra experiencia inicial, aunque reducida, muestra resultados similares a los publicados por la Clínica Mayo4,5, lo que refleja que, con un programa de entrenamiento adecuado y los correctos diagnóstico y tratamiento perioperatorio, esta técnica puede realizarse con éxito en centros de referencia.
La miectomía apical es una técnica segura y eficaz para el tratamiento de la MHA que puede ser una alternativa al TxC en pacientes en clase funcional avanzada.