El cierre percutáneo de defectos interauriculares es una alternativa a la cirugía que ha ido ganando gran aceptación en los últimos años hasta convertirse en el método de elección en muchos pacientes con este tipo de malformaciones. En España, durante 2006 se han cerrado percutáneamente 500 comunicaciones interauriculares (CIA) (entre niños y adultos) y 192 forámenes ovales permeables (FOP)1.
La afección del septo interauricular es variada y a veces compleja2,3. Las modalidades que pueden ser tratadas mediante cateterismo son las CIA tipo ostium secundum, el foramen oval permeable o los defectos híbridos.
La clave del éxito del procedimiento radica en una clara visualización del defecto, los remanentes septales y su relación con las estructuras adyacentes. Para este fin, la angiografía presenta muchas limitaciones, por lo que el operador debe recurrir a la visión ecográfica del septo interauricular. Esta visión puede ser transtorácica, transesofágica o, más recientemente, intracavitaria, tal como muestran los autores del artículo publicado en este número de Revista Española de Cardiología4.
Ecografía transesofágica
Los modernos sistemas de ecocardiografía transesofágica emiten haces de ultrasonidos perpendiculares al eje mayor de la sonda en un campo de 90°. Las sondas tienen el extremo «deflectable» y además el haz de ultrasonidos puede orientarse electrónicamente de 0° a 180°. La ecografía transesofágica proporciona una excelente visión del septo y sus remanentes desde múltiples angulaciones, pero en la práctica clínica diaria se utilizan tres proyecciones fundamentales5: cuatro cámaras (remanentes superior y auriculoventricular), transversal de aorta (remanentes retroaórtico y posterior) y a nivel de las cavas (remanentes de las cavas superior e inferior). Actualmente es la técnica con la que más experiencia se tiene y sigue siendo el estándar contra el que se debe comparar todas las nuevas modalidades de monitorización.
Ecografía intracardiaca
La ecocardiografía intracardiaca proporciona imágenes de la misma calidad que la transesofágica, pero desde otras angulaciones. Actualmente disponemos de dos sistemas: el Ultra ICE y el AcuNav. El sistema Ultra ICE, descrito en el artículo de este número4, emite en un solo plano perpendicular al eje mayor del catéter y proporciona una imagen bidimensional de un campo de 360° en tiempo real. Por el contrario, el sistema AcuNav emite de forma longitudinal al eje mayor del catéter en un campo de 90°, está disponible en la actualidad en 8 Fr y además incluye Doppler color y punta «deflectable».
Ecografía transesofágica frente a ecografía intracardiaca
Ambas técnicas proporcionan una buena visión bidimensional de las estructuras cardiacas y al mismo tiempo presentan ventajas e inconvenientes6,7. Así, la ecocardiografía transesofágica precisa anestesia general y la presencia de un ecografista durante el procedimiento. Por el contrario, la ecografía intracardiaca no precisa anestesia ni personal adicional. Sin embargo, es preciso comentar que en muchos niños con CIA la anestesia es obligatoria, independientemente del tipo de monitorización ecográfica que se utilice. En relación con la presencia de un ecografista experto en el laboratorio de hemodinámica, más que un inconveniente, pensamos que es una valiosa ayuda. El hecho de que el operador tenga que manipular el catéter de ecografía intracavitario tampoco parece que sea una ventaja, ya que preferimos concentrarnos en las maniobras de implante mientras otra persona supervisa el procedimiento. El precio del catéter de ecografía intracavitario y la necesidad de utilizar otra vía femoral también serían razones a favor de la ecografía transesofágica.
Complejidad de los defectos septales y tipo de monitorización ecográfica
Las CIA pequeñas, con buenos remanentes septales, y los FOP son defectos fáciles de cerrar con una monitorización sencilla. Sin embargo, comunicaciones grandes8, defectos dobles9 o las CIA cribiformes3 precisan una visualización detallada de los defectos, los remanentes, la totalidad del septo y las relaciones con las estructuras adyacentes. Para ello se precisa un estudio ecográfico detallado, y aun así hay una incidencia no despreciable de fracasos en el procedimiento y de embolización del dispositivo.
En el artículo publicado en este número de la Revista, los autores analizan a 52 pacientes con defectos del septo interauricular tratados mediante dispositivos Amplatzer guiados con ecocardiografía intracardiaca4. Obtienen muy buenos resultados en el tratamiento de esta afección y comunican solamente un fracaso sin complicaciones en un paciente. La serie incluye a 2 pacientes con CIA cribiformes y 4 con déficit del remanente retroaórtico. En estos 6 pacientes la ecografía intracavitaria también proporcionó información suficiente para cerrar el defecto con éxito.
La controversia sobre el uso de ecografía transesofágica o intracardiaca en este tipo de procedimientos todavía continúa, pues no se ha demostrado la superioridad de uno sobre el otro. Ninguna de las dos técnicas es perfecta, por lo que en ocasiones el operador tiene que recurrir a medir el defecto con un balón de oclusión (fig. 1). En estos casos, inflamos progresivamente un balón hasta que desaparezca el cortocircuito por Doppler color y entonces asumimos que ése sería el diámetro máximo de la CIA. Aparte de balones esféricos (fig. 1D), también disponemos de balones alargados que permiten medir angiográficamente la muesca que producen los bordes del defecto en el centro del balón (fig. 1C). Las discordancias entre estas técnicas quedan bien explicadas en la discusión del artículo4. A los inconvenientes comentados por los autores sobre el uso del balón (excesiva distensión del septo y, por lo tanto, sobrestimación del tamaño), nosotros añadiríamos la posibilidad de rotura de remanentes finos que a veces son el único sostén para anclar el dispositivo. Pensamos que la medición con balón resulta útil cuando se trata de defectos grandes, ovales o con forma de riñón, en que el operador no está totalmente seguro del diámetro mayor del orificio. En septos muy finos es preciso ser cuidadoso para no dañar los remanentes; muchas veces se puede omitir esta maniobra, ya que, en caso de tamaño ligeramente grande, parte del septo floppy cede y se adapta a la cintura del dispositivo.
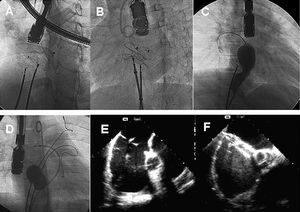
Fig. 1. Situaciones en procedimientos de cierre de CIA dobles en los que resulta útil un doble acceso femoral. A y B: introducción de dos dispositivos y constatación simultánea de su estabilidad antes de la suelta. C: tras colocar un dispositivo, se mide con balón el segundo defecto. D: valoración simultánea con dos balones colocados en defectos diferentes. E y F: visión transesofágica de CIA doble mientras se ocluyen los defectos con dos dispositivos simultáneamente.
Otro aspecto interesante que también merece comentario cuando se abordan defectos complejos es la necesidad de utilizar los dos accesos femorales en el procedimiento, que en el caso de la ecografía intracavitaria quedan anulados (uno para el dispositivo y otro para el ecógrafo). Por el contrario, la monitorización transesofágica deja libre una vena femoral para diferentes utilizaciones (fig. 1): introduccion de dos balones de medición, un segundo balón de medición y un dispositivo o dos dispositivos en caso de CIA múltiples. Esto permite finalizar el procedimiento en un solo tiempo (a diferencia del caso presentado por los autores, que precisó un segundo procedimiento). Con esta estrategia también se puede poner a prueba la estabilidad de los dispositivos simultáneamente (fig. 1) antes de las sueltas definitivas. La femoral contralateral también permite la introducción de un segundo catéter para la corrección de la presentación perpendicular del oclusor10, en caso de aurículas izquierdas pequeñas y CIA grandes.
Perspectivas de futuro
Actualmente no existe una técnica de monitorización perfecta que proporcione una visualización precisa del defecto en toda su extensión. Debemos estar integrando mentalmente mucha información bidimensional para reconstruir una estructura tridimensional (el septo interauricular). Sería deseable disponer de un método que permitiera planimetrar el defecto con exactitud o visualizar simultáneamente todos los posibles orificios, sus diámetros y la distancia entre ellos. De esta forma se podría planificar el tamaño del oclusor o los oclusores y evitar los errores que actualmente cometemos en la estimación de su tamaño. Estos errores conducen a fracasos en la implantación (con el consiguiente gasto) o a complicaciones por embolización del dispositivo11. En nuestra serie tuvimos esta complicación en 7 (2,6%) de 272 pacientes monitorizados con ecografía transesofágica, cifra similar a otras publicadas12. Nuevas generaciones de ecógrafos con sistemas de reconstrucción tridimensinal, o nuevas visiones mediante sistemas radiológicos futuros (tipo tomografía computarizada multicorte o resonancia magnética) que mejoren las prestaciones de los modelos actuales, podrían simplificar y proporcionar mayor seguridad a estas técnicas percutáneas. En cualquier caso, artículos como el de Hernández et al4 abren camino hacia estas nuevas visiones alternativas a la ecocardiografía transesofágica clásica.
Véase artículo en págs. 465-70
Correspondencia: Dr. M. Pan.
Servicio de Cardiología. Hospital Universitario Reina Sofía.
Avda. Menéndez Pidal, 1. 14008 Córdoba. España.
Correo electrónico: manuelpan@telefonica.net
Full English text available from: www.revespcardiol.org