Los inhibidores de la PCSK9 (iPCSK9) son fármacos hipolipemiantes eficaces y seguros pero con un elevado coste. El objetivo del estudio es estimar el número de pacientes candidatos a recibir iPCSK9 según los diferentes criterios publicados.
MétodosLos datos provienen del Sistema de Información para la Investigación en Atención Primaria. Se incluyó a pacientes de edad ≥ 18 años con al menos una determinación de colesterol unido a lipoproteínas de baja densidad entre 2006 y 2014 (n=2.500.907). Los criterios de indicación terapéutica de iPCSK9 analizados fueron: Sistema Nacional de Salud, Sociedad Española de Arteriosclerosis, Sociedad Española de Cardiología, National Institute for Health and Care Excellence y Sociedad Europea de Cardiología/European Atherosclerosis Society Task Force. Se definió como tratamiento lipídico optimizado el que alcanzara una reducción del colesterol unido a lipoproteínas de baja densidad ≥ 50% y un cumplimiento > 80%.
ResultadosEn la población española de 18 o más años el número de posibles candidatos a recibir iPCSK9 en un escenario de tratamiento hipolipemiante óptimo oscila entre el 0,1 y el 1,7% según los diferentes criterios. El subgrupo con mayor porcentaje de candidatos sería el de los pacientes con hipercolesterolemia familiar, y el mayor número absoluto vendría de los pacientes en prevención secundaria.
ConclusionesEl número de posibles candidatos a recibir iPCSK9 en condiciones de práctica clínica es muy alto y varía mucho según las recomendaciones de las diferentes sociedades científicas.
Palabras clave
La enfermedad cardiovascular (ECV) es la mayor causa de muerte prematura y discapacidad en Europa1. Un reciente metanálisis ha mostrado que, a mayor reducción de colesterol unido a lipoproteínas de baja densidad (cLDL), mayor beneficio cardiovascular2. Solo un 25% de los pacientes con ECV3 y el 3,4% de los pacientes con hipercolesterolemia familiar (HF)4 alcanzan los objetivos lipídicos. Además, cerca del 5-20% de los pacientes tratados en condiciones de práctica clínica real y entorno al 2% en ensayos aleatorizados presentan intolerancia a estatinas5. Los inhibidores de la proproteína convertasa subtilisina/kexina tipo 9 (iPCSK9) son fármacos capaces de disminuir hasta un 65% el cLDL y con buen perfil de seguridad6. El estudio FOURIER7 demostró que añadir evolocumab al tratamiento con estatinas reduce un 15% el riesgo relativo del objetivo primario del estudio. En unos meses, el estudio ODYSSEY Outcomes8 contribuirá a aclarar el papel del alicumab en pacientes con enfermedad coronaria.
No obstante, el coste de los iPCSK9 por el momento es una importante limitación para un uso amplio. Estas consideraciones han llevado al Ministerio de Sanidad, Asuntos Sociales e Igualdad9,10 y la SEA (Sociedad Española de Arteriosclerosis)11, la SEC (Sociedad Española de Cardiología)12, el NICE (National Institute for Health and Care Excellence)13,14 y la Sociedad Europea de Cardiología/European Atherosclerosis Society (ESC/EAS) Task Force15 a establecer unas indicaciones de uso.
El objetivo del presente trabajo es estimar el número y el tipo de pacientes candidatos a recibir iPCSK9 en nuestro medio, con una base de datos poblacional de 2.500.907 pacientes, en función de diversos criterios de indicación.
MÉTODOSEstudio observacional que utiliza el Sistema de Información para el Desarrollo de la Investigación en Atención Primaria (SIDIAP), base de datos clínicos de registros longitudinales anónimos de 6.177.972 pacientes entre 2006 y 2014. El SIDIAP incluye información sobre la actividad clínica de 3.414 médicos de 274 centros de atención primaria del Institut Català de la Salut, entidad pública que da cobertura sanitaria al 85% de la población de Cataluña16. Incluye diagnósticos (Clasificación Internacional de Enfermedades [CIE-10]), información de alta hospitalaria (CIE-9/10), laboratorio y medicamentos dispensados por farmacias. La calidad de los datos del SIDIAP para estudiar la epidemiología de las ECV está documentada17. El Comité de Ética e Investigación Clínica del Institut Universitari d’Investigació en Atenció Primària. aprobó el estudio.
En el estudio se incluyeron todos los registros del SIDIAP de los individuos de edad ≥ 18 años vivos en diciembre de 2014 y con al menos una determinación de cLDL entre 2006 y 2014. Se excluyó a los pacientes con antecedentes de hipotiroidismo, síndrome nefrótico o triglicéridos basales ≥ 400 mg/dl.
VariablesSe consideró que los participantes recibían terapia hipolipemiante si estaba registrada al menos una retirada de estatina o ezetimiba de la oficina de farmacia en los 6 meses previos a la determinación de cLDL y no tratado en caso contrario. Para calcular el valor basal previo al inicio del tratamiento en los pacientes que estaban tomando hipolipemiantes, se utilizó un algoritmo con 10 posibles imputaciones según la metodología descrita por Jorgensen et al.18 (). Las copias de imputación se resumieron según las reglas de Rubin, con el fin de corregir la variación existente en cada imputación. Se realizó un análisis de sensibilidad de los resultados realizando 20 imputaciones y también otro análisis con los individuos con datos completos. La adherencia al tratamiento se calculó mediante la medication possession ratio: proporción de días de un periodo de 6 meses que quedan cubiertos por la dispensación de tratamiento hipolipemiante observada en la farmacia. Los tratamientos hipolipemiantes se clasificaron en función de su capacidad para reducir el cLDL: baja, < 30%; moderada, 30-50%; alta, 50-60% y muy alta, > 60% ().
Se consideró tratamiento lipídico optimizado cuando la potencia hipolipemiante fuera ≥ 50% y la adherencia, > 80%.
Se definió fenotipo de HF considerando los puntos de corte de cLDL ajustados por edad definidos previamente en población adulta española: ≥ 18-30 años, > 230 mg/dl; 31-39 años, > 238 mg/dl; 40-48 años, > 260 mg/dl, y > 49 años, > 255 mg/dl19.
El diagnóstico de ECV (enfermedad arterial periférica, enfermedad coronaria e ictus isquémico y la presencia de diabetes mellitus, hipertensión, hipercolesterolemia y tabaquismo) se determinó a partir de la CIE-10 y la CIE-9 en los registros de atención primaria y hospitalaria. Los criterios utilizados para la definición de candidatos a uso de iPCSK9 según los diferentes organismos del SNS (Sistema Nacional de Salud)9,10, SEA11, SEC12, NICE13,14 y ESC/EAS Task Force15 se señalan en la tabla 1. Se incluyeron solo las indicaciones financiadas por el SNS9,10. Se calculó el número de pacientes candidatos a iPCSK9 en el escenario real y en un escenario de tratamiento optimizado aplicando a todos los pacientes la reducción de cLDL observada en los optimizados. También se calculó el porcentaje total de pacientes candidatos a iPCSK9 en la población de estudio y en la española en un escenario supuesto en el que se aplica una reducción del 50% de cLDL respecto al valor basal.
Criterios del SNS, la SEA, la SEC, el NICE y el ESC/EAS Task Force para el uso de inhibidores de la PCSK9
| SNS | SEA | SEC | NICE | ESC/EAS Task Force | |
|---|---|---|---|---|---|
| HF sin ECV | cLDL > 100 mg/dl | cLDL > 130 mg/dl si alto riesgoa cLDL > 160 mg/dl si bajo riesgo | cLDL > 130 mg/dl | cLDL > 193 mg/dl | cLDL > 175 mg/dl si alto riesgob cLDL > 200 mg/dl si bajo riesgo |
| HF con ECV | cLDL > 100 mg/dl | cLDL > 100 | cLDL > 70 mg/dl | cLDL > 135 mg/dl | cLDL > 100 mg/dl si alto riesgoc cLDL > 140 mg/dl si bajo riesgo |
| Sin HF ni ECV | No financiado | cLDL > 130 mg/dl si alto riesgod cLDL > 190 mg/dl si bajo riesgo | cLDL > 130 mg/dl si alto riesgoe | No recomendado | cLDL > 140 mg/dl si alto riesgof |
| Sin HF con ECV | cLDL > 100 mg/dl | cLDL > 100 mg/dl con ECV de alto riesgog cLDL > 130 mg/dl bajo riesgo | cLDL < 70 mg/dlh cLDL > 100 mg/dl si estable | cLDL > 135 mg/dl si alto riesgoi cLDL > 155 mg/dl en bajo riesgo | cLDL > 100 mg/dl si alto riesgoj cLDL > 140 mg/dl si bajo riesgo |
cLDL: colesterol unido a lipoproteínas de baja densidad; ECV: enfermedad dardiovascular; ESC/EAS: Sociedad Europea de Cardiología/European Atherosclerosis Society; HF: hipercolesterolemia familiar; NICE: National Institute for Health and Care Excellence; PCSK9 proproteína convertasa subtilisina/kexina tipo 9; SEA: Sociedad Española de Arteriosclerosis; SEC: Sociedad Española de Cardiología; SNS: Sistema Nacional de Salud.
Alto riesgo en HF en prevención primaria SEA: pacientes mayores de 40 años con otros factores de riesgo cardiovascular (hipertensión, diabetes mellitus, tabaquismo).
Alto riesgo en HF en prevención primaria ESC/EAS Task Force: pacientes con hipertensión arterial o diabetes mellitus.
Alto riesgo en HF en prevención secundaria ESC/EAS Task Force: si ECV progresiva (eventos de repetición o necesidad de repetir revascularización).
Alto riesgo en prevención primaria sin HF SEA: presencia de diabetes mellitus más 2 factores de riesgo cardiovascular o albuminuria o filtrado glomerular < 45 ml/min/1,73 m2.
Alto riesgo en prevención primaria sin HF SEC: diabetes mellitus tipo 2 o tipo 1 con lesión en órgano diana, filtrado glomerular estimado < 60 ml/min/1,73 m2 o SCORE > 10%.
Alto riesgo en prevención primaria sin HF ESC/EAS Task Force: diabetes mellitus tipo 2 con lesión en órgano diana u otro factor de riesgo.
Alto riesgo en prevención secundaria sin HF SEA: si ECV inestable o progresiva (eventos de repetición o necesidad de repetir revascularización) o presencia de diabetes mellitus.
Alto riesgo en prevención secundaria sin HF SEC: ECV inestable, recidivante (eventos de repetición o necesidad de repetir revascularización) o reciente (< 12 meses).
Los resultados se expresan como porcentajes (variables categóricas) y medias (variables continuas). En los pacientes con tratamiento lipídico de los que no se disponía un valor de cLDL previo al tratamiento, se utilizó un algoritmo con 10 posibles imputaciones según la metodología descrita por Jorgensen et al.18 para estimar el valor antes del tratamiento. Las variables incluidas en el modelo de imputación fueron: edad, sexo, dosis y tipo de hipolipemiante y adherencia al tratamiento (). Para realizar la proyección a escala nacional de los candidatos a iPCSK9, se estimó la prevalencia de ECV a partir de la población diagnosticada/población asignada en la base del SIDIAP (independientemente de que los pacientes tuvieran analítica registrada), y para la prevalencia de HF, se extrapoló la observada en nuestro estudio. El análisis estadístico se llevó a cabo utilizando R-software.
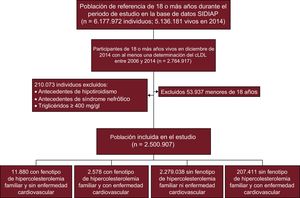
RESULTADOSSe registró al menos una medición de cLDL de 2.764.917 personas. De estos, 2.500.907 pacientes cumplían todos los criterios de inclusión. En la figura 1 se muestra el diagrama de flujo del estudio. Se identificó a 14.458 participantes con fenotipo HF y 207.411 con ECV.
En el total de la población de estudio, los valores imputados de la variable cLDL sin el efecto del tratamiento fueron del 43,3% de los individuos que recibían tratamiento. La media del cLDL antes del tratamiento era 166 mg/dl y la media de cLDL observado (tratados y no tratados), 110 mg/dl. La potencia hipolipemiante media utilizada fue del 32,6% y la adherencia medida presentó una medication possession ratio del 71,3% (tabla 2).
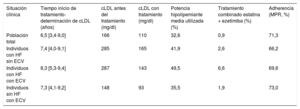
Tiempo entre el inicio del tratamiento hipolipemieante y la determinación del cLDL, valores de cLDL antes y durante el tratamiento, potencia hipolipemiante media utilizada, porcentaje de terapia combinada (estatatina + ezetimiba) y adherencia media en toda la población y en cada subgrupo
| Situación clínica | Tiempo inicio de tratamiento-determinación de cLDL (años) | cLDL antes del tratamiento (mg/dl) | cLDL con tratamiento (mg/dl) | Potencia hipolipemiante media utilizada (%) | Tratamiento combinado estatina + ezetimiba (%) | Adherencia (MPR, %) |
|---|---|---|---|---|---|---|
| Población total | 6,5 [3,4-9,0] | 166 | 110 | 32,6 | 0,9 | 71,3 |
| Individuos con HF sin ECV | 7,4 [4,0-9,1] | 285 | 165 | 41,9 | 2,6 | 66,2 |
| Individuos con HF con ECV | 8,3 [5,3-9,4] | 287 | 143 | 49,5 | 6,6 | 69,6 |
| Individuos sin HF con ECV | 7,3 [4,1-9,2] | 148 | 93 | 35,5 | 1,9 | 73,0 |
cLDL: colesterol unido a lipoproteínas de baja densidad; ECV: enfermedad cardiovascular; HF: hipercolesterolemia familiar; MPR: medication possession ratio.
Salvo otra indicación, los valores expresan mediana [intervalo intercuartílico].
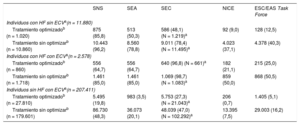
El número de candidatos, según los diferentes criterios, se muestra por subgrupos de pacientes y en función del tratamiento en la tabla 3.
Número y porcentaje de pacientes candidatos a inhibidores de la PCSK9 en la población del estudio en condiciones de práctica clínica real con y sin tratamiento hipolipemiante optimizado en función de los diferentes criterios
| SNS | SEA | SEC | NICE | ESC/EAS Task Force | |
|---|---|---|---|---|---|
| Individuos con HF sin ECVa(n = 11.880) | |||||
| Tratamiento optimizadob (n = 1.020) | 875 (85,8) | 513 (50,3) | 586 (48,1) (N = 1.219)a | 92 (9,0) | 128 (12,5) |
| Tratamiento sin optimizarb (n = 10.860) | 10.443 (96,2) | 8.560 (78,8) | 9.011 (78,4) (N = 11.495)a | 4.023 (37,1) | 4.378 (40,3) |
| Individuos con HF con ECVa(n = 2.578) | |||||
| Tratamiento optimizadob (n = 860) | 556 (64,7) | 556 (64,7) | 640 (96,8) (N = 661)a | 182 (21,1) | 215 (25,0) |
| Tratamiento sin optimizarb (n = 1.718) | 1.461 (85,0) | 1.461 (85,0) | 1.069 (98,7) (N = 1.083)a | 859 (50,0) | 868 (50,5) |
| Individuos sin HF con ECVa(n = 207.411) | |||||
| Tratamiento optimizadob (n = 27.810) | 5.495 (19,8) | 983 (3,5) | 5.753 (27,3) (N = 21.043)a | 206 (0,7) | 1.405 (5,1) |
| Tratamiento sin optimizarb (n = 179.601) | 86.730 (48,3) | 36.073 (20,1) | 48.039 (47,0) (N = 102.292)a | 13.395 (7,5) | 29.003 (16,2) |
ECV: enfermedad cardiovascular; ESC/EAS: Sociedad Europea de Cardiología/European Atherosclerosis Society; HF: hipercolesterolemia familiar; MPR: medication possession ratio; NICE: National Institute for Health and Care Excellence; PCSK9: proproteína convertasa subtilisina/kexina tipo 9; SEA: Sociedad Española de Arteriosclerosis; SEC: Sociedad Española de Cardiología; SNS: Sistema Nacional de Salud.
Los valores expresan n (%).
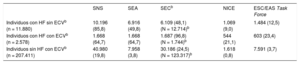
En la tabla 4 se muestra el número de pacientes candidatos en un escenario de tratamiento optimizado. Aproximadamente la mitad de los candidatos a tratamiento con iPCSK9 tienen fenotipo de HF según los criterios de la SEA11 y el NICE13,14. Según los criterios ESC/EAS Task Force15 y en mayor medida el SNS9,10 y la SEC12, más del 75% de los candidatos son pacientes en prevención secundaria.
Número y porcentaje de pacientes candidatos a inhibidores de la PCSK9 en la población del estudio en los diferentes subgrupos con tratamiento hipolipemiante optimizadoa en función de los diferentes criterios
| SNS | SEA | SECb | NICE | ESC/EAS Task Force | |
|---|---|---|---|---|---|
| Individuos con HF sin ECVb (n = 11.880) | 10.196 (85,8) | 6.916 (49,8) | 6.109 (48,1) (N = 12.714)b | 1.069 (9,0) | 1.484 (12,5) |
| Individuos con HF con ECVb (n = 2.578) | 1.668 (64,7) | 1.668 (64,7) | 1.687 (96,8) (N = 1.744)b | 544 (21,1) | 603 (23,4) |
| Individuos sin HF con ECVb (n = 207.411) | 40.980 (19,8) | 7.958 (3,8) | 30.186 (24,5) (N = 123.317)b | 1.618 (0,8) | 7.591 (3,7) |
ECV: enfermedad cardiovascular; ESC/EAS: Sociedad Europea de Cardiología/European Atherosclerosis Society; HF: hipercolesterolemia familiar; MPR: medication possession ratio; NICE: National Institute for Health and Care Excellence; PCSK9: proproteína convertasa subtilisina/kexina tipo 9; SEA: Sociedad Española de Arteriosclerosis; SEC: Sociedad Española de Cardiología; SNS: Sistema Nacional de Salud.
Los valores expresan n (%).
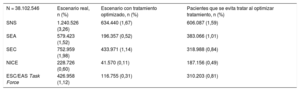
Para la estimación de los pacientes candidatos a tratamiento con iPCSK9 en población española de edad ≥ 18 años, la prevalencia de ECV observada en la población asignada en todo el conjunto de datos de SIDIAP era del 6,2%. La prevalencia de HF, del 0,53%. En un escenario de tratamiento optimizado, los criterios del SNS9,10 serían los que indicarían más candidatos a tratamiento con iPCSK9, el 1,7% de la población española de 18 o más años. Los criterios del NICE13,14 serían los más restrictivos, con el 0,1% (tabla 5).
Porcentaje total de pacientes candidatos a inhibidores de la PCSK9 en la población española en escenario real y en escenario de tratamiento optimizado* y número de pacientes que se evita tratar con inhibidores de la PCSK9 tras optimizar el tratamiento
| N = 38.102.546 | Escenario real, n (%) | Escenario con tratamiento optimizado, n (%) | Pacientes que se evita tratar al optimizar tratamiento, n (%) |
|---|---|---|---|
| SNS | 1.240.526 (3,26) | 634.440 (1,67) | 606.087 (1,59) |
| SEA | 579.423 (1,52) | 196.357 (0,52) | 383.066 (1,01) |
| SEC | 752.959 (1,98) | 433.971 (1,14) | 318.988 (0,84) |
| NICE | 228.726 (0,60) | 41.570 (0,11) | 187.156 (0,49) |
| ESC/EAS Task Force | 426.958 (1,12) | 116.755 (0,31) | 310.203 (0,81) |
ESC/EAS: Sociedad Europea de Cardiología/European Atherosclerosis Society; MPR: medication possession ratio; NICE: National Institute for Health and Care Excellence; PCSK9: proproteína convertasa subtilisina/kexina tipo 9; SEA: Sociedad Española de Arteriosclerosis; SEC: Sociedad Española de Cardiología; SNS: Sistema Nacional de Salud.
La optimización del tratamiento lipídico implica muy importantes reducciones del número de candidatos al tratamiento, hasta la mitad de los candidatos en la mayoría de los criterios, que es máxima en el caso del criterio del SNS9,10 (que pasa del 3,26 al 1,67% de la población) y mínima en el caso del NICE13,14 (que pasa del 0,60 al 0,11% de la población) (tabla 5).
En el escenario supuesto de una reducción de cLDL del 50% respecto al valor basal, el grupo de pacientes candidatos a iPCSK9 se redujo considerablemente respecto al escenario basado en las reducciones de cLDL observadas en la práctica clínica real, entre el 0,89% según el SNS y el 0,04% del NICE ().
En la figura 2 se muestra la distribución de la población en función de los valores de cLDL en condiciones de práctica clínica real. El 77,4% de los pacientes con HF sin ECV, el 44,9% de los pacientes con HF y ECV y el 17,2% de los pacientes con ECV sin HF presentaban valores de cLDL > 130 mg/dl. En la figura 3 se muestra la misma distribución, pero incluyendo solo a los pacientes que recibían tratamiento optimizado. En este caso, el 51,4% de los pacientes con HF sin ECV, el 25,2% de los pacientes con HF y ECV y el 3,3% de los pacientes con ECV sin HF presentaban valores de cLDL > 130 mg/dl. En condiciones de práctica clínica real, entre los pacientes con ECV sin HF, el 44,5% está por encima de 100 mg/dl, mientras que el 81,7% está por encima de 70 mg/dl.
El análisis de sensibilidad de los resultados realizando 20 imputaciones no mostró diferencias relevantes en los resultados, la definición de las poblaciones, los valores de cLDL ni el porcentaje de candidatos a tratamiento con iPCSK9 (). El análisis con datos completos mostró valores de cLDL inferiores y un menor porcentaje de candidatos a tratamiento con iPCSK9 ().
DISCUSIÓNEl presente estudio analiza con base en datos de la práctica clínica real en España el número de pacientes candidatos a recibir iPCSK9 considerando los diferentes criterios de indicación. Entre los diferentes criterios analizados, se observaron diferencias muy importantes en el número de candidatos, entre el 0,1 y el 1,7% de la población de edad ≥ 18 años, así como en el tipo de paciente candidato. El objetivo de cLDL exigido en cada criterio explica en gran medida estas diferencias. La optimización del tratamiento hipolipemiante reduciría de manera importante el número de candidatos. Si la optimización llegara a obtener en todos los individuos una reducción del 50% del cLDL basal, la reducción sería muy relevante.
En el subgrupo de pacientes con fenotipo de HF en prevención primaria, el número de pacientes candidatos tras optimizar el tratamiento se situaría entre el 9% del NICE13,14 y el 86% del SNS9,10; para el subgrupo de HF en prevención secundaria, entre el 21% del NICE13,14 y el 97% de SEC12, y en pacientes con ECV sin HF, entre el 0,8% del NICE13,14 y el 20% del SNS9,10. El porcentaje de pacientes candidatos en población con HF según criterios ESC/EAS Task Force15 obtenido en nuestro estudio (el 12% en prevención primaria y el 23% en prevención secundaria) concuerda con lo publicado por el registro de HF de la SEA20. Gran parte de las diferencias entre criterios, especialmente en pacientes con HF en prevención primaria, se deben al umbral de cLDL que indica el tratamiento, y hay considerables incrementos al pasar de 130 a 100 y de 100 a 70 mg/dl. El 63,8% de los pacientes con ECV sin HF tienen valores de cLDL entre 70 y 130 mg/dl. En nuestra población, pasar de un umbral de cLDL de 100 a 70 mg/dl implica doblar el número de pacientes candidatos (figura 2 y figura 3). En el estudio FOURIER, el 67% de los pacientes en tratamiento con evolocumab alcanzaron cifras de cLDL < 40 mg/dl y el 42%, < 25 mg/dl, y el riesgo absoluto de ECV pasó del 11,3 al 9,8%7. Hay que señalar que, a igualdad de cLDL, los pacientes con HF tienen hasta 4 veces más riesgo de ECV que sin HF21. Es fundamental determinar cuál es el umbral óptimo de cLDL y los criterios de mal pronóstico para indicar iPCSK9 a cada subgrupo de pacientes para que se pueda destacar una u otra recomendación. Los investigadores del Safe-Heart han desarrollado la primera ecuación que puede ayudar a una mejor predicción del riesgo de ECV en la HF22. La enfermedad coronaria reciente, difusa, de imposible revascularización o progresiva indica mal pronóstico en pacientes en prevención secundaria23.
El tipo de pacientes también varía entre criterios. La mayoría de los pacientes con HF estarían tratados según el SNS9,10, la SEA11 y especialmente la SEC12, que se centra en pacientes con HF y enfermedad coronaria. Los criterios que tratarían a más pacientes con ECV sin HF serían los de la SEC12 y ESC/EAS Task Force15.
Otra consideración es que el impacto del colesterol difiere entre enfermedad coronaria y otras manifestaciones de la ECV24. Las recomendaciones de la Sociedad Española de Cardiología12 son exclusivamente para pacientes con enfermedad coronaria.
Otro aspecto que considerar es la falta de estudios sobre el beneficio cardiovascular asociado con las reducciones extremas del cLDL para los pacientes mayores de 75 años en prevención primaria25. Ninguna de las directrices hace referencia a posibles límites de edad.
Un reciente metanálisis sitúa el control lipídico en población española alrededor del 15% en prevención secundaria y hasta un 65% en prevención primaria, y detecta —como en nuestro trabajo— una infrautilización del tratamiento de alta intensidad y del uso combinado con ezetimiba26. Por otro lado, uno de los grandes retos al optimizar el uso racional de los iPCSK9 será evitar el sobrediagnóstico de intolerancia a estatinas5. El uso de sistemas electrónicos en la toma de decisiones puede mejorar el número de pacientes bien controlados27. En el presente trabajo, al simular un escenario con el tratamiento lipídico optimizado, el porcentaje de pacientes candidatos a iPCSK9 según criterios de la SEC12 se reduciría 1,7 veces.
Si se consiguiera en todos los individuos una reducción del 50% del cLDL basal, el porcentaje de según los criterios de la SEC se reduciría 2,7 veces ().
En un trabajo reciente, Cannon et al.28 han creado un modelo de simulación de candidatos a recibir iPCSK9 de población americana con ECV sin HF, a base de ajustes sucesivos de la dosis y la potencia de los hipolipemiantes y con objetivo de cLDL < 70 mg/dl. Estiman un porcentaje de candidatos del 14%, inferior al 24,5% estimado en nuestra población según los criterios de la SEC13, que también marcan un objetivo del cLDL < 70 mg/dl. Estas diferencias se explicarían principalmente por el modelo de simulación empleado. En el mismo artículo se plantean escenarios simulados diferentes y el porcentaje de candidatos a recibir iPCSK9 varía del 6 al 28%. El escenario de simulación se basa en los efectos observados en la práctica clínica real en pacientes optimizados, y desde nuestro punto de vista, este supuesto es más plausible que suponer que el efecto será óptimo y lineal en todos los individuos. En nuestro escenario alternativo de reducción del 50% del cLDL () los candidatos según el mismo criterio serían el 10,9%.
Dado que la prevalencia del fenotipo de HF en nuestro medio es cercana al 0,5%29 y que precisa tratamiento crónico, indicado a edades tempranas, el impacto directo de los iPCSK9 en el sistema sanitario puede ser importante. Hasta la fecha los estudios de coste-efectividad muestran resultados heterogéneos. Un trabajo reciente señala que el número de pacientes que es necesario tratar con iPCSK9 para evitar 1 evento cardiovascular en pacientes en muy alto riesgo con un objetivo de cLDL < 70 mg/dl se situaría en torno a 50 a los 5 años de tratamiento30. Otro trabajo ha mostrado que añadir evolocumab al tratamiento con estatinas y ezetimiba de los pacientes con HF puede ser una medida coste-efectiva31. Un estudio reciente en Estados Unidos concluye que el tratamiento con iPCSK9 debería reducir su coste en torno al 70% para ser coste-efectivo32. Otro estudio en población noruega ha estimado que los iPCSK9 serían coste-efectivos únicamente en prevención secundaria en población de edad avanzada de muy alto riesgo33. El único estudio en población española publicado hasta la fecha ha mostrado que el evolocumab puede ser coste-efectivo en población con HF y pacientes en prevención secundaria, con un incremento de la razón coste-efectividad de 30.893 euros y dentro de los umbrales marcados como coste-efectivos en población española34. No obstante, habrá que esperar a futuros trabajos de coste-efectividad sobre los resultados de los estudios FOURIER8 y ODYSSEY Outcomes8. También serán necesarios futuros trabajos para estratificar el riesgo dentro de cada subgrupo.
Fortalezas y limitacionesEl tamaño de la muestra y la visión basada en datos del mundo real son fortalezas del estudio. También es una fortaleza la representatividad poblacional; prueba de ello es que en el análisis de casos completos se observa un menor porcentaje de candidatos a tratamiento con iPCSK9, ya que se incluiría solo a los pacientes más jóvenes y que han iniciado tratamiento más recientemente ().
Como limitaciones hay que destacar que la población estudiada incluyó a todos los individuos que se realizaron una prueba de cLDL en un periodo de 8 años, lo que representa aproximadamente un 57% de la población general de 18 o más años y el 70% de los de 45 o más. Por lo tanto, no se puede descartar algún sesgo de selección, especialmente en las edades más jóvenes. Por otro lado, el método diagnóstico basado en el fenotipo de HF puede haber sobrestimado su prevalencia real, especialmente debido a casos de hipercolesterolemia poligénica, aunque serían igualmente candidatos a iPCSK9. Otra limitación es que no se dispuso de datos sobre lipoproteína(a) y los antecedentes familiares de ECV. En el presente trabajo no se pudo evaluar cuál sería el posible impacto de la intolerancia a las estatinas en la prescripción de iPCSK9. Otro aspecto que cabe considerar es el infradiagnóstico de la falta de adherencia al tratamiento hipolipemiante, al medirlo únicamente por la retirada de los fármacos de las oficinas de farmacia.
CONCLUSIONESEl número de posibles candidatos a recibir iPCSK9 en condiciones de práctica clínica es muy alto y varía mucho según las recomendaciones de las diferentes sociedades científicas, entre el 0,1 y el 1,7% de la población española de edad ≥ 18 años. El objetivo de cLDL exigido en cada criterio explica en gran medida estas diferencias. El tipo de pacientes también es heterogéneo entre criterios. El subgrupo con mayor porcentaje de posibles candidatos sería el de los pacientes con HF y ECV, aunque en números absolutos el grupo que más casos aporta es el de pacientes en prevención secundaria sin HF. Un tratamiento hipolipemiante intensivo, con estatinas en altas dosis y terapia combinada con ezetimiba, reduciría de manera muy considerable el número de candidatos a iPCSK9.
FINANCIACIÓNMinisterio de Economía a través del Instituto de Salud Carlos III (Red de Investigación Cardiovascular-Programa HERACLES RD12/0042 y redIAPP [Red de Investigación en Actividades Preventivas y Promoción de la Salud] RD12/0007) y Fondo Europeo de Desarrollo Regional, CIBER de Enfermedades Cardiovasculares.. La Generalitat de Catalunya a través de l’Agència de Gestió Ajuts Universitaris de Recerca (2014 SGR 240) y (2014 SGR 902) y a través de l’Agència de Qualitat i Avaluació Sanitàries de Catalunya, Pla Estratègic de Recerca i Innovació en Salut (SLT002/16/00145).
- –
En el tratamiento lipídico de los pacientes con alto o muy alto riesgo cardiovascular, hay necesidades no cubiertas.
- –
La comercialización de los nuevos iPCSK9 constituye una etapa prometedora en el tratamiento lipídico.
- –
En nuestro medio existen diferentes directrices provenientes de sociedades científicas para indicar iPCSK9.
- –
Se desconoce el impacto real de los iPCSK9 en condiciones de práctica clínica real en función de las diferentes directrices.
- –
Una visión general del grado de control y uso de las terapias hipolipemiantes para pacientes con alto riesgo cardiovascular en condiciones de práctica clínica real.
- –
La proporción de la población y el tipo de pacientes con indicación de iPCSK9 según los criterios de diferentes sociedades científicas u organismos científicos.
N. Plana ha realizado ponencias financiadas por Alexion, Amgen, Ferrer, MSD y Sanofi y asistencias a reuniones científicas financiadas por Amgen y Rovi. L. Masana ha realizado ponencias financiadas por Amgen, MSD y Sanofi. À. Vila ha realizado ponencias financiadas por Ferrer, Sanofi y Esteve y asistencias a reuniones científicas financiadas por Amgen y Ferrer.