Algunos estudios han descrito un cambio en el espectro etiológico de la pericarditis constrictiva. Además, no hay datos sobre la relación entre la forma de presentación clínica y la etiología. El objetivo de este estudio es describir las etiologías de la enfermedad, su relación con la forma de presentación clínica y los hallazgos quirúrgicos, así como identificar los factores predictivos de una mala evolución.
MétodosSe analizó a un total de 140 pacientes consecutivos a los que se practicaron intervenciones quirúrgicas por pericarditis constrictiva en un mismo centro en un periodo de 34 años.
ResultadosLa etiología fue idiopática en 76 pacientes (54%) y tras pericarditis aguda idiopática en 24 (17%), pericarditis tuberculosa en 15 (11%), pericarditis purulenta en 10 (7%) y cirugía cardiaca en 5 (4%), radioterapia en 3 (2%) y uremia en 2 (1%). La duración media de los síntomas antes de la pericardiectomía fue de 19 meses (desviación estándar: 44 meses); la forma de presentación clínica más aguda fue la de las pericarditis purulentas (26 [intervalo, 7-60] días) y la más crónica, la de los casos idiopáticos (29 meses [4 días-360 meses]). La mortalidad perioperatoria fue del 11%. No hubo diferencias en la mortalidad según etiologías. La mediana de seguimiento fue de 12 (0,1-33,0) años, durante los cuales fallecieron 50 pacientes. En un análisis de regresión de Cox, la edad en el momento de la operación, la clase funcional de la New York Heart Association avanzada (III–IV) y los antecedentes de pericarditis aguda idiopática se asociaron a una mayor mortalidad durante el seguimiento.
ConclusionesLa mayoría de los casos de pericarditis constrictiva son idiopáticas. La cirugía cardiaca y la radioterapia causan una minoría de los casos. Las presentaciones aguda y subaguda merecen un estudio etiológico. La edad, la clase funcional avanzada y la pericarditis aguda idiopática previa se asocian a mayor mortalidad.
Palabras clave
Desde que Lower describiera por primera vez la pericarditis constrictiva (PC) en 16691, algunos aspectos clínicos pueden haber cambiado. Algunos estudios2 han señalado recientemente que el espectro etiológico se ha modificado en las últimas décadas, debido básicamente a un aumento del número de casos secundarios a cirugía cardiaca (CC) o a una radioterapia previa. Sin embargo, esta observación puede ser engañosa. En primer lugar, estos estudios se realizaron en centros con gran actividad quirúrgica cardiaca3, lo que puede introducir cierto sesgo en el espectro etiológico. Además, la relación entre la duración de los síntomas antes de la pericardiectomía y la etiología de la PC no se ha descrito de manera detallada. Por último, en estudios previos no se incluyó habitualmente información detallada sobre los diferentes métodos diagnósticos o las técnicas de imagen utilizados para el diagnóstico de la PC.
El Hospital Universitari Vall d’Hebron, que es un centro de referencia para las enfermedades pericárdicas, ha utilizado un protocolo estandarizado para el diagnóstico y el tratamiento de la enfermedad pericárdica4,5 desde 1975. En este estudio se describen el espectro etiológico, la relación entre la cronicidad de los síntomas clínicos y la etiología de la PC, el uso de los diferentes métodos diagnósticos y los factores predictivos de mala evolución en una serie de 140 pacientes consecutivos con PC, operados en este centro en los últimos 34 años.
MÉTODOSSe realizó un estudio retrospectivo en un solo centro de nivel terciario. El comité ético del centro aprobó el estudio. Entre enero de 1978 y mayo de 2012, se trató en el Hospital Universitari Vall d’Hebron a un total de 140 pacientes con una pericardiectomía por una PC confirmada. Un único investigador (Andreu Porta-Sánchez) revisó individualmente las historias clínicas, prestando especial atención a la presencia de enfermedades inflamatorias sistémicas, episodios previos de enfermedades pericárdicas agudas, antecedentes de radioterapia torácica o mediastínica o de CC y las exploraciones clínicas o de imagen empleadas. Se cuantificó el tiempo transcurrido desde la posible enfermedad causal hasta el inicio de los síntomas de PC, así como el tiempo transcurrido hasta la pericardiectomía. Se registraron también las características quirúrgicas, prestando atención a la afección de las capas parietal y visceral. Se obtuvieron datos de mortalidad y de seguimiento a través de visitas en la clínica ambulatoria, mediante las historias clínicas electrónicas o por teléfono. Se obtuvieron datos del Instituto Nacional de Estadística de España6 para generar una población igualada en cuanto a edad y sexo, y se generó una curva de supervivencia de Kaplan-Meier estimada para comparar la mortalidad global a largo plazo de los pacientes del estudio con la de la población general.
DefinicionesSe diagnosticó PC idiopática cuando no se identificaba una etiología. El trastorno tras pericarditis aguda idiopática se definió como PC si se produjo después de un episodio bien definido de pericarditis aguda idiopática (dolor torácico típico, roce pericárdico, alteraciones secuenciales del segmento ST en el electrocardiograma). Se definió como PC tuberculosa cuando se hubiera aislado el bacilo de Koch de una muestra pericárdica o se identificaran granulomas caseosos en una muestra de biopsia. Se diagnosticó PC purulenta cuando el líquido pericárdico era purulento macroscópicamente o tenía un contenido elevado de polimorfonucleares (> 90%). Se diagnosticó PC posquirúrgica cuando la PC se producía después de una intervención quirúrgica a corazón abierto. Se definió PC tras radioterapia por la aparición de la PC después de una irradiación terapéutica del tórax y tras la exclusión de otras causas de PC. De un modo arbitrario, se aplicaron los términos PC aguda, subaguda y crónica, respectivamente, a los pacientes que necesitaron una pericardiectomía antes de los 3 meses, entre 3 y 6 meses o después de 6 meses del inicio de los síntomas clínicos. La calcificación pericárdica se definió por la presencia de calcificación en la radiografía de tórax. La función sistólica ventricular izquierda se consideró anormal si la fracción de eyección del ventrículo izquierdo estimada era < 50%. Los siguientes hallazgos en la ecocardiografía Doppler se consideraron diagnósticos: engrosamiento pericárdico y escotadura (notch) en el tabique interventricular, cambios en la velocidad de E superiores al 25% en relación con los movimientos respiratorios, una desaceleración rápida de la onda E, flujo de venas suprahepáticas con morfología en «W» o predominio del componente diastólico con inversión diastólica durante la espiración. La cantidad de derrame pericárdico (DP) se clasificó como leve (< 10mm de espacio sin ecos en los espacios pericárdicos anterior y posterior), moderada (10–20mm) o grave (> 20mm). Se realizaron exploraciones de imagen adicionales para confirmar el engrosamiento y la calcificación pericárdicas (tomografía computarizada [TC]) o para descartar la presencia de una miocardiopatía infiltrante (resonancia magnética). Si el diagnóstico de la PC seguía sin estar claro tras el empleo de las técnicas de imagen, se realizaba un cateterismo cardiaco derecho e izquierdo. La pericardiectomía se llevó a cabo a través de una esternotomía media en todos los casos. Aunque en los últimos 30 años ha habido varios avances quirúrgicos, el abordaje operatorio del tratamiento de la PC no ha cambiado sustancialmente durante este periodo. Se intentó realizar una pericardiectomía amplia (pericardio diafragmático y frénico-frénico), que se llevó a cabo con éxito en el 95% de los casos. La mortalidad perioperatoria se definió como muerte durante la cirugía o en los primeros 30 días tras la hospitalización.
Análisis estadísticoSe utilizó la prueba de análisis de la varianza de una vía para las comparaciones de los distintos grupos etiológicos en cuanto a las variables continuas. Se utilizó la prueba de la χ2 para comparar las frecuencias de las variables cualitativas. Se aplicó un modelo de regresión de Cox bivariable para identificar los posibles factores pronósticos y un análisis de regresión de Cox multivariable para identificar los factores independientes predictivos de la mortalidad. Las variables con un valor de p < 0,2 en el análisis de regresión de Cox bivariable se incluyeron en un modelo de regresión de Cox escalonado. El poder de discriminación del modelo final se evaluó con el estadístico C, que se estimó con un método de remuestreo (bootstrapping) tomando 1.000 muestras. Se verificó gráficamente el supuesto de riesgos proporcionales para cada variable. Para el análisis estadístico se utilizaron los programas SPSS (IBM Corp., Released 2010, IBM SPSS Statistics for Windows, Versión 19.0; Armonk, Nueva York, Estados Unidos).
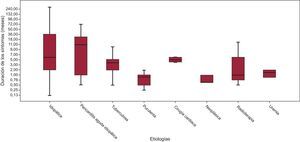
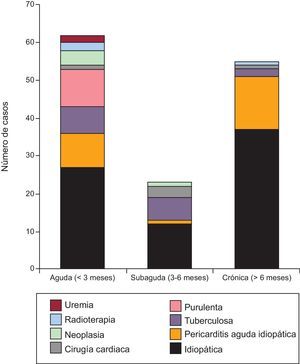
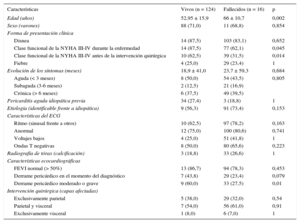
RESULTADOSResultados clínicosEn la tabla 1 se resumen las características demográficas y los hallazgos clínicos de los 140 pacientes, así como la etiología de las PC. La etiología más frecuente fue la idiopática (el 54% de los casos). La pericarditis inflamatoria/infecciosa (pericarditis aguda idiopática/viral, pericarditis tuberculosa y pericarditis purulenta) supuso un 35% del total de casos. Se trató con fármacos antiinflamatorios a todos los pacientes que presentaron una pericarditis aguda o subaguda, con independencia de la sospecha etiológica. De los 140 pacientes, 37 (26,4%) habían tenido un episodio previo de pericarditis aguda. Los antecedentes de pericarditis aguda fueron más frecuentes en el grupo de PC idiopática (59,5%) que en el grupo con PC de etiología identificable (40,5%). Es de destacar que los antecedentes de CC y de radioterapia supusieron solo un 4 y un 2% de los casos respectivamente. La duración de los síntomas para cada etiología se resume en la figura 1. La media global del tiempo de evolución de los síntomas fue de 19,5 meses (8 días-360 meses). En la figura 2 se muestra la distribución por grupos (pericarditis aguda, subaguda o crónica) de las diferentes etiologías de la PC y su relación con el tiempo de evolución de los síntomas antes de la pericardiectomía. Es interesante señalar que casi todos los pacientes con PC purulenta, tuberculosa o neoplásica tuvieron una forma de presentación aguda o subaguda, y que la enfermedad más aguda fue la observada en la PC purulenta, con una media de duración de los síntomas de 0,9 meses. En cambio, la mayoría de los casos de enfermedad crónica se debieron a una PC idiopática o se produjeron después de una pericarditis aguda idiopática.
Características demográficas y manifestaciones clínicas y frecuencias de las etiologías
| Características demográficas | |||
| Sexo (varones) | 99 (70,7) | ||
| Edad a la intervención quirúrgica (años) | 54,6 (17-80) | ||
| Diabetes mellitus | 16 (11,4) | ||
| Hipertensión | 28 (20,0) | ||
| Deterioro de la función renal | 14 (10,0) | ||
| Características clínicas | |||
| Insuficiencia cardiaca congestiva | 124 (87,3) | ||
| Disnea | 117 (82,4) | ||
| Clase funcional de la NYHA prequirúrgica | |||
| I | 26 (18,6) | ||
| II | 65 (46,4) | ||
| III | 34 (24,3) | ||
| IV | 15 (10,7) | ||
| Dolor torácico | 46 (32,6) | ||
| Fiebre | 33 (23,4) | ||
| Síncope | 2 (1,4) | ||
| Etiología | |||
| Idiopática | 32 (54,2)a | 44 (54,3)b | 76 (54,3)c |
| Pericarditis aguda idiopática | 8 (13,6)a | 16 (19,7)b | 24 (17,1)c |
| Tuberculosa | 8 (13,6)a | 7 (8,6)b | 15 (10,7)c |
| Purulenta | 3 (5,1)a | 7 (8,6)b | 10 (7,1)c |
| Neoplásica | 4 (6,8)a | 1 (1,2)b | 5 (3,6)c |
| Cirugía cardiaca | 1 (1,7)a | 4 (4,9)b | 5 (3,6)c |
| Radioterapia | 3 (5,1)a | 0 (0,0)b | 3 (2,1)c |
| Uremia | 0 (0,0)a | 2 (2,5)b | 2 (1,4)c |
| Total | 59 (42,1) | 81 (57,9)b | 140 (100,0)c |
NYHA: New York Heart Association.
Los datos expresan n (%) o media (intervalo).
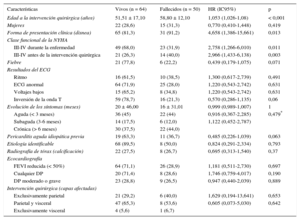
En la tabla 2 se presentan las exploraciones invasivas y técnicas de imagen utilizadas y su rendimiento diagnóstico. Se observó calcificación en la radiografía de tórax en el 26% de los pacientes. La presencia de un DP fue más frecuente en los pacientes con una forma de presentación aguda o subaguda, en comparación con lo observado en las formas de presentación crónica (el 48 y el 35 frente al 9% respectivamente; p < 0,001). La ecocardiografía mostró signos diagnósticos de constricción o de engrosamiento pericárdico en 113 pacientes (83,7%). Se identificó un DP moderado o grave en 43 pacientes (30,7%) durante el curso clínico. La proporción de DP significativos fue diferente entre las distintas etiologías: tres etiologías mostraron un porcentaje importante de pacientes con DP significativos —pericarditis tuberculosa (66,7%), radioterapia (66%), neoplasia (60%), uremia (50%) y pericarditis purulenta (50%)— mientras que el porcentaje de pacientes con un DP significativo fue inferior en los casos de PC posquirúrgica, PC tras pericarditis aguda idiopática o PC idiopática (el 40,0, el 29,2 y el 17,1% respectivamente). La TC, que se realizó en 71 pacientes (50%), mostró la presencia de calcificación o engrosamiento del pericardio (media del grosor del pericardio, 11,4 ± 6,8mm) o un DP en el 93% de los pacientes, y fue normal solo en 5 pacientes. La ventaja de la TC en los pacientes con sospecha de PC es su alto valor predictivo positivo para la detección de calcificación o engrosamiento del pericardio. Se realizó cateterismo cardiaco a 53 pacientes (38%), con hallazgos típicos de constricción (igualación de las presiones telediastólicas con morfología de depresión-meseta de las curvas ventriculares diastólicas y signos de interdependencia ventricular) en 50 de ellos (95%) (media de presión telediastólica ventricular derecha, 18,8 ± 5,1mmHg; media de presión telediastólica ventricular izquierda, 20,8 ± 5,0mmHg).
Pruebas diagnósticas
| ECG | 138 (99) |
| Ritmo sinusal | 107 (76) |
| Fibrilación auricular | 33 (25) |
| Voltajes bajos | 55 (39) |
| Elevación difusa del segmento ST | 8 (6) |
| Ondas T negativas | 88 (63) |
| Normal | 28 (20) |
| Radiografía de tórax | 140 (100) |
| Calcificación | 36 (26) |
| Ecocardiografía | 135 (96) |
| Engrosamiento del pericardio | 71 (53) |
| Derrame pericárdico | |
| Ninguno | 67 (49) |
| Leve (< 10 mm) | 26 (19) |
| Moderado (10-20 mm) | 16 (12) |
| Grave (> 20 mm) | 26 (19) |
| Escotadura septal | 89 (66) |
| Flujos típicos | 97 (72) |
| FEVI anormal | 28 (21) |
| Tomografía computarizada | 71 (51) |
| Engrosamiento o calcificación del pericardio | 53 (73) |
| Derrame pericárdico | 26 (35) |
| Normal | 5 (7) |
| Resonancia magnética | 13 (9) |
| Calcificación | 1 (10) |
| Engrosamiento del pericardio | 4 (30) |
| Derrame pericárdico | 7 (53) |
| Normal | 1 (10) |
| Resultados hemodinámicos en el cateterismo cardiaco | 53 (38) |
| Depresión-meseta | 50 (94) |
| Igualación de las presiones ventriculares telediastólicas | 44 (87) |
| Hallazgos quirúrgicos | 104 (74) |
| Afección exclusivamente parietal | 34 (36) |
| Afección parietal y visceral | 63 (61) |
| Afección exclusivamente visceral | 7 (7) |
| Total | 140 (100) |
ECG: electrocardiograma; FEVI: fracción de eyección del ventrículo izquierdo.
Los datos expresan n (%).
La intervención quirúrgica mostró afección de las dos capas del pericardio en la mayoría de los pacientes (61%), mientras que se observó afección exclusivamente de la capa visceral en solo 5 (7%).
Anatomía patológica microscópicaSe dispuso de datos de anatomía patológica quirúrgica de 120 pacientes. La mayoría de los pacientes (95 [79%]) tenían tejido fibrinoso, mientras que se identificó inflamación linfoplasmocitaria en 5 (5,8%). Se observó inflamación granulomatosa en 10 pacientes (8,3%), y en 4 de ellos se identificó la presencia de Mycobacterium tuberculosis en la biopsia; en 4 pacientes (3%) se identificó un adenocarcinoma en la biopsia; 3 pacientes (2,5%) tenían inflamación aguda, con neutrófilos y linfocitos. Solo 1 paciente presentó signos compatibles con pericarditis purulenta.
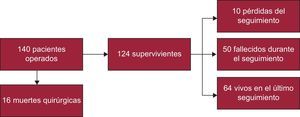
Mortalidad perioperatoriaEn la figura 3 se presenta el diagrama de flujo de la evolución de los pacientes. La mortalidad perioperatoria fue del 11,4% (16 de 140 pacientes). La muerte se debió a un síndrome de bajo gasto cardiaco en 6 pacientes, complicaciones de una estancia prolongada en la unidad de cuidados intensivos que acabó en sepsis en 5 casos, shock mixto cardiogénico y séptico en 2, cáncer avanzado en 1 e ictus en 1. En 1 paciente no fue posible determinar la causa de la muerte. Por lo que respecta a las etiologías, 8 de los 16 pacientes que fallecieron en el primer mes presentaban una PC idiopática; 2 tenían una PC tras CC; 2, PC neoplásica; 2, PC purulenta; 1, PC tras pericarditis aguda idiopática, y 1, PC inducida por radioterapia. En la tabla 3 se presentan las diferencias existentes entre los pacientes que fallecieron y los que sobrevivieron. La mortalidad perioperatoria se asoció a la edad avanzada (66,1 frente a 52,9 años; p < 0,002), la clase funcional de la New York Heart Association avanzada (III-IV) en el momento de la intervención quirúrgica (odds ratio = 3,63; intervalo de confianza del 95% [IC95%], 1,23-10,70) y a la presencia de DP moderado o grave durante el curso de la enfermedad (odds ratio = 3,40; IC95%, 1,20-9,91). Se observó una tendencia a mayor mortalidad en la forma de presentación aguda (el 12,9% de los pacientes agudos frente al 8,7% en la forma subaguda y el 10,9% en la forma crónica). No hubo diferencias de mortalidad perioperatoria entre las etiologías.
Características basales de los pacientes con mortalidad postoperatoria*
| Características | Vivos (n = 124) | Fallecidos (n = 16) | p |
|---|---|---|---|
| Edad (años) | 52,95 ± 15,9 | 66 ± 10,7 | 0,002 |
| Sexo (varones) | 88 (71,0) | 11 (68,8) | 0,854 |
| Forma de presentación clínica | |||
| Disnea | 14 (87,5) | 103 (83,1) | 0,652 |
| Clase funcional de la NYHA III-IV durante la enfermedad | 14 (87,5) | 77 (62,1) | 0,045 |
| Clase funcional de la NYHA III-IV antes de la intervención quirúrgica | 10 (62,5) | 39 (31,5) | 0,014 |
| Fiebre | 4 (25,0) | 29 (23,4) | 1 |
| Evolución de los síntomas (meses) | 18,9 ± 41,0 | 23,7 ± 59,3 | 0,684 |
| Aguda (< 3 meses) | 8 (50,0) | 54 (43,5) | 0,805 |
| Subaguda (3-6 meses) | 2 (12,5) | 21 (16,9) | |
| Crónica (> 6 meses) | 6 (37,5) | 49 (39,5) | |
| Pericarditis aguda idiopática previa | 34 (27,4) | 3 (18,8) | 1 |
| Etiología (identificable frente a idiopática) | 9 (56,3) | 91 (73,4) | 0,153 |
| Características del ECG | |||
| Ritmo (sinusal frente a otros) | 10 (62,5) | 97 (78,2) | 0,163 |
| Anormal | 12 (75,0) | 100 (80,6) | 0,741 |
| Voltajes bajos | 4 (25,0) | 51 (41,8) | 1 |
| Ondas T negativas | 8 (50,0) | 80 (65,6) | 0,223 |
| Radiografía de tórax (calcificación) | 3 (18,8) | 33 (26,6) | 1 |
| Características ecocardiográficas | |||
| FEVI normal (> 50%) | 13 (86,7) | 94 (78,3) | 0,453 |
| Derrame pericárdico en el momento del diagnóstico | 7 (43,8) | 29 (23,4) | 0,079 |
| Derrame pericárdico moderado o grave | 9 (60,0) | 33 (27,5) | 0,01 |
| Intervención quirúrgica (capas afectadas) | |||
| Exclusivamente parietal | 5 (38,0) | 29 (32,0) | 0,54 |
| Parietal y visceral | 7 (54,0) | 56 (61,0) | 0,91 |
| Exclusivamente visceral | 1 (8,0) | 6 (7,0) | 1 |
ECG: electrocardiograma; FEVI: fracción de eyección del ventrículo izquierdo; NYHA: New York Heart Association.
Los datos expresan n (%) o media ± desviación estándar.
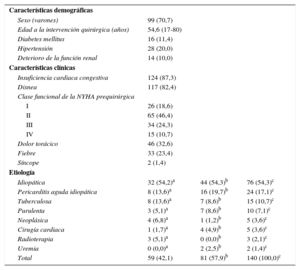
En 10 pacientes se perdió el seguimiento después del alta del hospital. La mediana de seguimiento de los supervivientes fue de 12 (0,1–33,0) años. En la figura 4 se presenta la curva de Kaplan-Meier de la supervivencia global en esta cohorte de pacientes y en una población española igualada por edad y sexo. La media de supervivencia fue de 220 meses (IC95%, 196-245). Tras un seguimiento de 20 años, el 50,9% de los pacientes continuaban con vida. En comparación con la población general española igualada por edad y sexo, la tasa de supervivencia de estos pacientes fue notablemente inferior, aun cuando las curvas tendían a solaparse a partir de los 20 años de seguimiento. Se produjeron 50 muertes después el periodo postoperatorio (30 días). No hubo diferencias de mortalidad entre las diferentes etiologías. El análisis con el modelo de Cox bivariable de los pacientes que sobrevivieron al periodo perioperatorio y completaron el seguimiento (114 pacientes) identificó la edad (hazard ratio [HR] = 1,05; p < 0,001), la presencia de disnea en el momento de la presentación clínica (HR = 4,66; p = 0,013), y la clase funcional de la New York Heart Association III-IV durante la enfermedad o antes de la intervención quirúrgica (HR = 2,76; p = 0,011 y HR = 2,97; p = 0,003 respectivamente) como posibles factores predictivos de mortalidad tardía (tabla 4). En el análisis multivariable, se mantuvo la edad en el momento de la intervención quirúrgica (HR = 1,052; IC95%, 1,017-1,088; p = 0,003), la clase funcional de la New York Heart Association avanzada antes de la intervención quirúrgica (HR = 4,028; IC95%, 1,792-9,054; p = 0,001) y haber presentado un episodio previo de pericarditis aguda (HR = 2,931; IC95%, 1,261-6,810; p = 0,012) como factores predictivos de la mortalidad a largo plazo (tabla 5). El valor del estadístico C en el modelo final fue 0,75, lo que indica un poder de discriminación adecuado.
Curva de Kaplan-Meier para la supervivencia global de los pacientes del estudio (azul) y curva de Kaplan-Meier para una población española igualada por edad y sexo (rojo). Supervivencia en los intervalos de 1, 5, 10 y 20 años. Esta figura se muestra a todo color solo en la versión electrónica del artículo.
Estimaciones de la regresión de Cox univariable para las características clínicas basales
| Características | Vivos (n = 64) | Fallecidos (n = 50) | HR (IC95%) | p |
|---|---|---|---|---|
| Edad a la intervención quirúrgica (años) | 51,51 ± 17,10 | 58,80 ± 12,10 | 1,053 (1,026-1,08) | < 0,001 |
| Mujeres | 22 (28,6) | 15 (31,3) | 0,770 (0,410-1,448) | 0,419 |
| Forma de presentación clínica (disnea) | 65 (81,3) | 31 (91,2) | 4,658 (1,386-15,661) | 0,013 |
| Clase funcional de la NYHA | ||||
| III-IV durante la enfermedad | 49 (68,0) | 23 (31,9) | 2,758 (1,266-6,010) | 0,011 |
| III-IV antes de la intervención quirúrgica | 21 (26,3) | 14 (40,0) | 2,966 (1,433-6,138) | 0,003 |
| Fiebre | 21 (77,8) | 6 (22,2) | 0,439 (0,179-1,075) | 0,071 |
| Resultados del ECG | ||||
| Ritmo | 16 (61,5) | 10 (38,5) | 1,300 (0,617-2,739) | 0,491 |
| ECG anormal | 64 (71,9) | 25 (28,0) | 1,220 (0,543-2,742) | 0,631 |
| Voltajes bajos | 15 (65,2) | 8 (34,8) | 1,220 (0,543-2,742) | 0,631 |
| Inversión de la onda T | 59 (78,7) | 16 (21,3) | 0,570 (0,286-1,135) | 0,06 |
| Evolución de los síntomas (meses) | 20 ± 46,00 | 16 ± 31,01 | 0,999 (0,989-1,007) | 1 |
| Aguda (< 3 meses) | 36 (45) | 22 (44) | 0,916 (0,367-2,285) | 0,479* |
| Subaguda (3-6 meses) | 14 (17,5) | 6 (12,0) | 1,122 (0,452-2,787) | |
| Crónica (> 6 meses) | 30 (37,5) | 22 (44,0) | ||
| Pericarditis aguda idiopática previa | 19 (63,3) | 11 (36,7) | 0,485 (0,226-1,039) | 0,063 |
| Etiología identificable | 68 (89,5) | 8 (50,0) | 0,824 (0,291-2,334) | 0,793 |
| Radiografía de tórax (calcificación) | 22 (27,5) | 8 (26,7) | 0,695 (0,313-1,540) | 0,37 |
| Ecocardiografía | ||||
| FEVI reducida (< 50%) | 64 (71,1) | 26 (28,9) | 1,181 (0,511-2,730) | 0,697 |
| Cualquier DP | 20 (71,4) | 8 (28,6) | 1,746 (0,759-4,017) | 0,190 |
| DP moderado o grave | 23 (28,8) | 9 (26,5) | 0,947 (0,440-2,039) | 0,889 |
| Intervención quirúrgica (capas afectadas) | ||||
| Exclusivamente parietal | 21 (29,2) | 6 (40,0) | 1,629 (0,194-13,641) | 0,653 |
| Parietal y visceral | 47 (65,3) | 8 (53,6) | 0,605 (0,073-5,030) | 0,642 |
| Exclusivamente visceral | 4 (5,6) | 1 (6,7) | ||
DP: derrame pericárdico; ECG: electrocardiograma; FEVI: fracción de eyección del ventrículo izquierdo; hazard ratio; IC95%: intervalo de confianza del 95%; NYHA: New York Heart Association.
Características basales de los pacientes que sobrevivieron el primer mes después de la intervención quirúrgica y completaron el seguimiento a largo plazo (114 pacientes).
Salvo otra indicación, los datos expresan n (%) o media ± desviación estándar.
Predictores independientes de los resultados adversos con ajuste respecto a posibles factores de confusión
| Variable | p | HR (IC95%) |
|---|---|---|
| Edad a la intervención quirúrgica | 0,002 | 1,054 (1,020-1,090) |
| Clase funcional de la NYHA III-IV prequirúrgica | 0,006 | 3,139 (1,397-7,055) |
| Pericarditis aguda idiopática previa | 0,010 | 2,790 (1,274-6,113) |
| Ondas T negativas en el ECG | 0,299 | 0,682 (0,331-1,404) |
HR: hazard ratio; IC95%: intervalo de confianza del 95%; NYHA: New York Heart Association.
Esta es una serie contemporánea formada por un grupo amplio de pacientes con PC tratados con pericardiectomía en un mismo centro que es un centro de referencia para las enfermedades pericárdicas y en el que se utiliza un protocolo estandarizado para su diagnóstico y tratamiento, con un seguimiento de más de 30 años. El análisis de esta serie aporta nuevas perspectivas respecto al espectro etiológico, la forma de presentación clínica, la utilidad de los métodos diagnósticos y los factores pronósticos en esta enfermedad. A diferencia de otros informes contemporáneos previos, este estudio muestra que la mayoría de las PC son idiopáticas y que la CC y la radioterapia explican solo una minoría de los casos. La supervivencia a largo plazo después de la pericardiectomía no se ve afectada por la etiología, mientras que la edad, la clase funcional avanzada y la pericarditis aguda idiopática previa constituyen posibles factores pronósticos.
Espectro etiológicoBasándose en series de pacientes tratados quirúrgicamente entre los años 1970 y 2000, algunos autores2,3,7–9 han señalado un cambio en el espectro etiológico de la PC, con tendencia a mayor porcentaje de pacientes con PC tras CC (del 18 al 37% de los casos) y con PC tras radioterapia (del 9 al 31% de los casos). Concretamente, la CC supuso un porcentaje elevado, de hasta un 37% en una de las series3. En cambio, en esta serie las etiologías más frecuentes fueron la idiopática (el 54% de los casos) y la PC inflamatoria/infecciosa (35%), mientras que la PC posquirúrgica y la PC tras radioterapia fueron solo el 4 y el 2% del total de casos respectivamente. No se observaron cambios en las frecuencias de las etiologías entre los periodos 1978-1995 y 1996-2012. Aunque esta discrepancia puede explicarse en parte por las diferencias en la estructura de los hospitales, parece muy improbable que un volumen diferente de intervenciones de CC, oncología y radioterapia pueda conducir a diferencias tan grandes en estas estimaciones. Según la incidencia de PC después de la CC (0,09–0,30%) que se ha descrito en diferentes estudios2,3, debería haberse observado un número más elevado de casos. Otra explicación plausible es que la PC aparecida después de la CC sea con frecuencia transitoria10,11. Así, cabe proponer que algunas de las pericardiectomías podrían haberse evitado si se hubiera adoptado una estrategia más conservadora12. La práctica habitual consiste en ser especialmente vigilantes respecto a esta posible evolución13 y establecer la indicación de pericardiectomía solo en los casos de constricción grave y persistente.
Es de destacar que, en el presente estudio, la pericarditis aguda viral/idiopática fue la causa de la PC en el 17% de los casos. Esto concuerda con lo indicado por los estudios prospectivos4,14 que han estimado la probabilidad de aparición de PC después de una pericarditis aguda en valores bajos, de hasta solo un 1%.
Relación entre la etiología y las manifestaciones clínicas. Consideraciones para la realización de estudios etiológicosLa PC es la manifestación final común de una amplia gama de agresiones sufridas por el pericardio. El tiempo transcurrido entre la enfermedad causal y la aparición de la constricción puede ser diverso. La relación entre la etiología y la aparición clínica de la constricción no se ha analizado en estudios previos. Esta información es importante por dos motivos: por un lado, en un intento de predecir la posible cronología de la progresión a la constricción después de los diferentes tipos de agresión sufrida por el pericardio y, por otro lado, para establecer si es recomendable realizar estudios etiológicos en los pacientes con constricción. Por ejemplo, casi todos los casos de constricción debidos a causas específicas y potencialmente tratables (principalmente la pericarditis purulenta o tuberculosa) requieren una pericardiectomía en los primeros 6 meses (constricción aguda o subaguda); esta observación concuerda con la experiencia previa respecto a la pericarditis tuberculosa y purulenta15–17. Concretamente, la pericarditis purulenta puede mostrar una progresión hiperaguda a la constricción, con un intervalo que puede llegar a ser de solo 8 días. En consecuencia, en los pacientes con pericarditis purulenta debe realizarse una supervisión cuidadosa en las primeras semanas, y en los pacientes con pericarditis tuberculosa, en los primeros meses. Si no se produce constricción en los primeros 6 meses, es improbable que aparezca con posterioridad. A diferencia de lo observado en los casos agudos y subagudos, no se identificaron etiologías tratables específicas en el grupo de pacientes con PC crónica (más de 6 meses). Estos resultados indican que, para los pacientes con PC, los estudios etiológicos solo están justificados para los casos agudos y subagudos.
Uso y rendimiento diagnóstico de los métodos diagnósticos y las técnicas de imagenEn esta serie, la calcificación del pericardio en la radiografía de tórax se observó solo en el 26% de los casos, lo que concuerda con lo indicado por otras series recientes18. Sin embargo, este hallazgo debe ser objeto de una búsqueda cuidadosa, puesto que su presencia en un paciente con sospecha clínica de PC basta para establecer en firme el diagnóstico. El rendimiento diagnóstico global de la ecocardiografía Doppler fue de aproximadamente el 84%. Un hallazgo insospechado fue el elevado porcentaje de pacientes con DP; esto puede explicarse por que se trató quirúrgicamente al 43% de los pacientes durante los primeros 3 meses de la enfermedad, cuando seguían presentando síntomas a pesar del tratamiento médico (fármacos antiinflamatorios y/o diuréticos cuando estaba indicado). Estos pacientes podrían haber tenido una PC con derrame.19 El rendimiento diagnóstico de la TC fue alto, de hasta un 93%, y solo en 5 pacientes (7%) la TC fue normal. Así pues, aunque se han descrito casos de PC con un grosor pericárdico normal,20 una TC estrictamente normal es un dato que va en contra de un diagnóstico de PC. Sin embargo, esta observación podría estar sesgada, ya que no se puede descartar la posibilidad de que el diagnóstico de PC hubiera pasado inadvertido en algunos pacientes con una TC normal. A pesar del alto rendimiento diagnóstico, se cree que el cateterismo no es necesario en la mayoría de los pacientes. A partir de estos datos, no se puede establecer el rendimiento diagnóstico de la resonancia magnética, puesto que se empleó solo en un 9% de los casos (13 de 140 pacientes). De hecho, la TC puede ser superior a la resonancia magnética debido a su mayor fiabilidad en la detección del calcio. Se realizó cateterismo cardiaco al 38% de los casos (53 de 140 pacientes) y se observaron signos diagnósticos típicos (depresión-meseta con igualación de las curvas de presión ventricular diastólica en el 94 y el 87% respectivamente). El cateterismo cardiaco también fue útil para descartar la enfermedad coronaria en los pacientes con factores de riesgo o síntomas de angina. Durante el periodo en el que se obtuvieron los datos de esta serie, se han realizado varios avances en las técnicas de imagen y ha habido una tendencia a un uso más juicioso de las pruebas diagnósticas invasivas en los pacientes.21 Cuando hay sospecha clínica de PC, la ecocardiografía Doppler (que muestra una fisiología restrictiva) y la TC (que muestra un pericardio engrosado y/o calcificado) deben bastar para establecer el diagnóstico.
Factores pronósticosLa mortalidad perioperatoria observada en esta serie (11,4%) concuerda con la experiencia presentada por otros autores7,22,23. De manera similar a lo observado en otras series, la edad y la clase funcional de la New York Heart Association avanzada fueron factores predictivos de mortalidad. En contra de lo esperado, se observó que la presencia de DP era también más frecuente en los pacientes con mal resultado quirúrgico. La mortalidad fue similar en las formas de presentación aguda, subaguda y crónica, aunque parece haber tendencia a mayor mortalidad en la presentación aguda de la enfermedad. A diferencia de la experiencia de otros autores18, no se observó que la presencia de calcificación pericárdica fuera un factor independiente predictivo de mortalidad perioperatoria.
LimitacionesEl presente estudio tiene varias limitaciones, que derivan principalmente de su diseño retrospectivo y de que solo se analizara a pacientes operados, lo que excluyó a todos los pacientes que no eran candidatos a intervención quirúrgica a causa de comorbilidades o mal estado clínico. Hay un reducido número de diagnósticos de PC que podrían haber pasado inadvertidos, lo que podría introducir cierto sesgo en el rendimiento diagnóstico de los diferentes métodos diagnósticos. Sin embargo, no es de prever que la repercusión de estas limitaciones sea lo bastante alta para comprometer la validez de las conclusiones del estudio.
CONCLUSIONESEn esta experiencia, las pericarditis idiopática y postinflamatoria/infecciosa siguen siendo las causas más frecuentes de PC que motiva una pericardiectomía, mientras que las pericarditis asociadas a la CC y la radioterapia suponen una minoría de los casos. Las pericarditis purulenta, tuberculosa y neoplásica muestran un patrón característico de progresión aguda o subaguda a la constricción. No hay diferencias de mortalidad entre las diferentes etiologías. La ecocardiografía fue la técnica usada con mayor frecuencia para identificar un patrón fisiológico de restricción/constricción, y la TC fue la técnica más fiable para documentar la presencia de engrosamiento o calcificación del pericardio. Los factores predictivos de mal pronóstico quirúrgico o mala evolución a largo plazo son la edad, el estadio clínico avanzado y la presencia de DP moderado o grave.
FINANCIACIÓNEste trabajo ha sido financiado en parte por la red RECAVA (Red Temática de Investigación Cooperativa en Enfermedades Cardiovasculares) de las RETICS (Redes Temáticas de Investigación Cooperativa en Salud) del Instituto de Salud Carlos III del Ministerio de Ciencia e Innovación de España.
CONFLICTO DE INTERESESNinguno.