El estudio ADVANCE III mostró una reducción de terapias del desfibrilador automático implantable (DAI) con el empleo de tiempos de detección de arritmia prolongados. Se describe la adopción y el impacto de dicha estrategia en la incidencia de terapias del DAI.
MétodosEstudio observacional retrospectivo de pacientes con implante de DAI Medtronic (2005-2016) en un registro multicéntrico (UMBRELLA-NCT01561144). Se describe la evolución de la adopción de programación ADVANCE en relación con: publicación del estudio, implementación de una campaña de formación y publicación de un consenso de expertos. Se identificaron con regresión logística los predictores de la adopción. Se comparó la incidencia de terapias en pacientes con y sin programación ADVANCE estimando la razón de tasas de incidencia ajustada (RTIa) mediante regresión binomial negativa.
ResultadosSe incluyó a 3.528 pacientes. Se utilizó la estrategia ADVANCE en el 20% del total y el 44% al final del estudio. La adopción se incrementó tras publicarse el estudio ADVANCE, y en menor grado tras la campaña de formación y consenso de expertos. Predictores de la adopción: DAI con detección nominal 30/40 (ORa=4,4; IC95%, 3,5-5,4), implantador electrofisiólogo (ORa=1,7; IC95%, 1,4-2,2) y prevención secundaria (ORa=3,2; IC95%, 2,6-3,9). El implante de DAI bicameral (ORa=0,6; IC95%, 0,5-0,8) o tricameral (ORa=0,5; IC95%, 0,4-0,7) se asoció con menor adopción. La programación ADVANCE se asoció con reducción de terapias totales (RTIa=0,77; IC95%, 0,69-0,86) y choques inapropiados (RTIa=0,66; IC95%, 0,52-0,85).
ConclusionesLa adopción de la programación ADVANCE es poco amplia y puede mejorarse mediante una adecuada selección de los parámetros nominales. Emplearla se asocia con una reducción de las terapias del DAI.
Palabras clave
Los desfibriladores automáticos implantables (DAI) se han convertido en una de las piezas clave a la hora de tratar a los pacientes con riesgo de muerte súbita arrítmica1,2. El crecimiento en el número de DAI implantados ha llamado la atención sobre sus posibles complicaciones a corto y largo plazo. En concreto, en múltiples estudios se ha constatado que las descargas del DAI, independientemente de su carácter apropiado o inapropiado, pueden causar un empeoramiento de la insuficiencia cardiaca e incrementar la mortalidad3,4. Esto ha llevado al desarrollo de estrategias para reducir las descargas del DAI, tanto las inapropiadas como las potencialmente «innecesarias». En este contexto, en el ensayo ADVANCE III se observó que el uso de una estrategia basada en tiempos de detección de arritmias prolongados reducía las terapias del DAI5. Así, se diseñó un estudio con 3 objetivos principales: a) describir la adherencia en el mundo real a una «estrategia de programación ADVANCE»; b) identificar predictores de la adopción de dicha estrategia, y c) comparar la tasa de terapias del DAI entre los pacientes tratados con la programación ADVANCE y los tratados con la programación estándar.
MÉTODOSDiseño del estudio y poblaciónSe trata de un análisis de cohortes observacional, comparativo y retrospectivo de un registro prospectivo. Los datos basales y de seguimiento se extrajeron de la base de datos UMBRELLA (ClinicalTrials.gov, NCT01561144). En este registro multicéntrico se incluyó a todos los pacientes en España con un DAI Medtronic con capacidad de monitorización a distancia (tanto los primoimplantes como los recambios de generador) desde enero de 2005 (los detalles del registro se han publicado previamente6). En el registro participaron 38 centros. En el análisis se incluyó a todos los pacientes consecutivos incluidos de manera prospectiva en el registro entre el 2005 y abril del 2016 y seguidos con el sistema de monitorización a distancia CareLink. Los dispositivos se programaron a criterio del médico. El seguimiento de los pacientes incluyó transmisiones a través del sistema CareLink, así como visitas presenciales regulares según el protocolo local. Se siguió a los pacientes hasta su última transmisión a distancia. Dos de 3 electrofisiólogos expertos (que desconocían la programación de cada paciente) analizaron todos los episodios del DAI almacenados y los clasificaron como adecuados o inadecuados. En caso de desacuerdo, se reunía el comité de revisión de episodios formado por los 3 expertos.
A efectos del análisis, se dividió a los pacientes en 2 grupos según la programación del dispositivo en el momento del implante (concretamente, en el momento del alta; no se evaluaron los cambios en la programación que tuvieran lugar durante el seguimiento): a) programación ADVANCE, que se definió según el ensayo original (número de intervalos que detectar [NID], 30/40; ventana de detección de fibrilación ventricular <320ms y estimulación antitaquicárdica antes o durante la carga), y b) un grupo de programación «no ADVANCE» (todos los pacientes que no satisfacían los criterios de la programación ADVANCE). Además, para incluir a los pacientes en prevención primaria en la programación ADVANCE, debían carecer de zonas «activas» adicionales por debajo de la ventana de fibrilación ventricular, mientras que estas zonas sí se permitieron en los pacientes en prevención secundaria.
Los cambios en el porcentaje de pacientes a los que se programaron estrategias de tratamiento ADVANCE en el momento del implante se explican por 3 sucesos: la publicación de los resultados del ensayo ADVANCE (mayo del 2013), la implementación de una campaña de «concienciación ADVANCE» para asesores técnicos de Medtronic (enero del 2015) y la publicación del consenso de expertos de HRS/EHRA/APHRS/SOLAECE sobre programación y comprobación óptimas del DAI (noviembre de 2015)7. Así pues, se establecieron 4 periodos de tiempo: periodo 1 (antes de la publicación de los resultados del ADVANCE III), periodo 2 (desde la publicación del ADVANCE III hasta la campaña de «concienciación ADVANCE»), periodo 3 (desde la campaña de «concienciación ADVANCE» hasta la publicación del consenso de expertos) y periodo 4 (después de la publicación del consenso de expertos). Las tasas de adopción se calcularon para cada trimestre dividiendo el número de pacientes que recibieron la programación ADVANCE por el número total de implantes realizados durante cada periodo de 3 meses.
La campaña de «concienciación ADVANCE» incluyó una serie de conferencias, impartidas entre noviembre de 2014 y enero de 2015 por un electrofisiólogo experto, a las que asistieron obligatoriamente todos los asesores técnicos de Medtronic, que en España prestan soporte en todos las intervenciones de implante de DAI o de recambio del generador. El objetivo de las conferencias (que consistieron en 2 sesiones de 1 h) era familiarizar a los asesores técnicos de Medtronic con la evidencia entonces vigente sobre la programación del dispositivo y, en concreto, con la estrategia de programación utilizada en el grupo «activo» del ensayo ADVANCE III, con instrucciones para aconsejar al médico implantador la adopción de tal estrategia. Todos los asesores técnicos de Medtronic recibieron una «tarjeta con propuestas» sobre los ajustes recomendados ( y ) y la presentación se puso a disposición de todos los asistentes para fomentar la retroalimentación y la interacción con los conferenciantes.
Métodos estadísticosLas variables categóricas se expresan como totales y porcentajes y las variables continuas, como media± desviación estándar. Se compararon las variables categóricas con la prueba de la χ2 o la prueba exacta de Fisher según procediera, mientras que las variables continuas se compararon con la prueba de la t de Student, tras evaluar la normalidad con la prueba de Kolmogorov-Smirnov. La fracción de eyección del ventrículo izquierdo se estratificó como <30%, del 30-49% y ≥ 50%.
En primer lugar, se utilizó un modelo de regresión segmentado para evaluar la contribución de cada uno de los 3 hitos mencionados más arriba (publicación de los resultados del ensayo, campaña de concienciación y consenso de expertos) en la adopción de una estrategia de programación ADVANCE III en el momento del implante, con cada uno de estos eventos como un «punto de inflexión» en el modelo. Para cada segmento de tiempo (periodo), se parametrizaron la ordenada en el origen (que representa la tasa de adopción al inicio de cada periodo de tiempo) y la pendiente («B», que representa la tasa de aumento en el cumplimiento ADVANCE durante el periodo). Cada punto de la serie temporal (que representa una ventana de 3 meses) se ponderó según el número total de implantes realizados durante aquel intervalo concreto de 3 meses. La bondad de ajuste se evaluó con el R2, el error absoluto medio y la varianza residual.
En segundo lugar, se utilizó la regresión logística multivariante para identificar predictores independientes de la adopción ADVANCE III. Las variables que mostraron relación con la adopción de ADVANCE en el análisis univariante se incluyeron en el modelo multivariante (criterios de inclusión en el modelo univariante: p <0,2).
En tercer lugar, la carga de terapias del dispositivo en cada grupo se describió como la tasa de incidencia de terapias del DAI, que se expresó como el número de terapias/100 pacientes-año. Para comparar las tasas de incidencia de terapias entre los pacientes con y sin programación ADVANCE, se calcularon las razones de tasas de incidencia ajustadas (RTIa) con su intervalo de confianza del 95% (IC95%) con regresión binomial negativa multivariante, que se seleccionó a tenor de la sobredispersión de las variables dependientes (es decir, las tasas de terapias del DAI) definidas por un exceso de varianza respecto a la media. La sobredispersión se debe principalmente a una falta de independencia entre los eventos contabilizados (es decir, el número de terapias por paciente), que aumenta cuando la ocurrencia de un evento (terapias del dispositivo) influye en la probabilidad de posteriores eventos. La regresión binomial negativa incluye un parámetro de dispersión en el modelo por el cual los intervalos de confianza estimados se ajustan según la variabilidad en el número de eventos por paciente. Se establecieron 3 modelos multivariantes distintos, tal como sigue: a) cualquier terapia del DAI; b) descarga apropiada del DAI, y c) descarga inapropiada del DAI. Cada uno de los 3 modelos se ajustó por la inclusión de variables que: a) podían actuar como posibles factores de confusión, y b) mostraban p <0,20 en el análisis univariante. Se ajustó cada modelo para tener en cuenta las diferencias en la duración del seguimiento entre los grupos ADVANCE y no ADVANCE, y se empleó la transformación logarítmica natural de personas-año para modelar la exposición.
Se estableció la significación estadística en p <0,05. El análisis estadístico se realizó con la versión 17 del sistema SPSS.
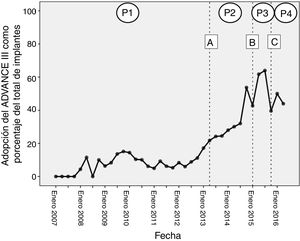
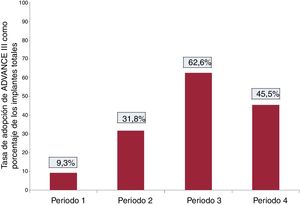
RESULTADOSAdopción en vida real de una estrategia de programación ADVANCE IIIEl análisis incluyó a 3.528 pacientes sometidos a un implante entre enero de 2005 y abril de 2016. En total, se seleccionó una estrategia ADVANCE en el momento de realizar el implante para 717 pacientes (20,3%). La programación ADVANCE se utilizó por primera vez a finales de 2007 y, en consecuencia, actúa como punto de partida en el análisis histórico. La penetración de ADVANCE comenzó con el 8,7%, sin prácticamente aumentar durante el periodo 1 (b=0,0005). La tasa de adopción promedio fue del 9,3% durante este periodo. Durante el periodo 2, la penetración de ADVANCE comenzó al 20,8% y mostró un aumento trimestral del 3,8% que llevó a un cumplimiento promedio del 31,8% durante este periodo. La penetración de la programación ADVANCE durante el periodo 3 aumentó en un 2,2% trimestral, con una adopción promedio del 62,6% durante el periodo. Durante el periodo 4, tras la publicación del consenso de expertos de la programación del DAI, la adhesión a una estrategia de programación ADVANCE comenzó con el 40% y aumentó en un 2,5% por trimestre, dando una adopción promedio durante este periodo del 45,2%. La penetración de ADVANCE al final del periodo de estudio fue del 44%. Los cambios ocurridos con el tiempo en la adopción de una estrategia ADVANCE en el momento del implante se presentan en la figura 1, y la adopción promedio durante cada uno de los 4 periodos se resume en la figura 2.
Tendencias temporales en la adopción (proporción de todos los implantes) de una estrategia de programación ADVANCE en el momento de implantar el dispositivo. A: publicación de los resultados del ensayo ADVANCE III; B: campaña de formación «Concienciación sobre ADVANCE III» para asesores técnicos de Medtronic; C: publicación del consenso de expertos 2015 de HRS/EHRA/APHRS/SOLAECE; P1: periodo 1; P2: periodo 2; P3: periodo 3; P4: periodo 4.
Tasa promedio de adopción del ADVANCE III en el momento del implante para cada periodo del estudio. Periodo 1: desde 2007 (primer paciente del registro programado en ADVANCE) hasta la publicación de los resultados del ensayo ADVANCE III (mayo de 2013); Periodo 2: desde la publicación de los resultados del ensayo ADVANCE III hasta la implementación de la campaña de formación «Concienciación sobre ADVANCE III» para los asesores técnicos de Medtronic (enero de 2015); Periodo 3: desde la implementación de la campaña de formación «Concienciación sobre ADVANCE III» para los asesores técnicos de Medtronic hasta la publicación del consenso de expertos de 2015 de HRS/EHRA/APHRS/SOLAECE sobre programación de los DAI (noviembre de 2015); Periodo 4: tras la publicación del consenso de expertos de HRS/EHRA/APHRS/SOLAECE.
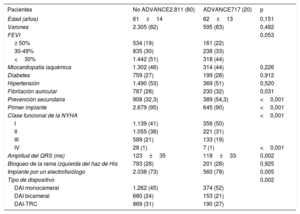
Las características basales de los pacientes de los grupos de programación ADVANCE y no ADVANCE se muestran en la tabla 1. Los predictores univariantes y multivariantes de la adopción ADVANCE se muestran en la tabla 2. En el análisis univariante, las siguientes variables se relacionaron con el cumplimiento de una estrategia de programación ADVANCE: antecedentes de fibrilación auricular, indicación para prevención secundaria, dispositivo con NID nominal (es decir, configuración «de fábrica») 30/40, DAI monocameral e implante por un electrofisiólogo. La fracción de eyección del ventrículo izquierdo <30% se relacionó negativamente con la programación ADVANCE (comparado con la fracción de eyección del ventrículo izquierdo > 50%).
Características basales de la población del estudio
| Pacientes | No ADVANCE2.811 (80) | ADVANCE717 (20) | p |
|---|---|---|---|
| Edad (años) | 61±14 | 62±13 | 0,151 |
| Varones | 2.305 (82) | 595 (83) | 0,482 |
| FEVI | 0,053 | ||
| ≥ 50% | 534 (19) | 161 (22) | |
| 30-49% | 835 (30) | 238 (33) | |
| <30% | 1.442 (51) | 318 (44) | |
| Miocardiopatía isquémica | 1.302 (46) | 314 (44) | 0,226 |
| Diabetes | 759 (27) | 199 (28) | 0,912 |
| Hipertensión | 1.490 (53) | 369 (51) | 0,520 |
| Fibrilación auricular | 787 (28) | 230 (32) | 0,031 |
| Prevención secundaria | 908 (32,3) | 389 (54,3) | <0,001 |
| Primer implante | 2.679 (95) | 645 (90) | <0,001 |
| Clase funcional de la NYHA | <0,001 | ||
| I | 1.139 (41) | 356 (50) | |
| II | 1.055 (38) | 221 (31) | |
| III | 589 (21) | 133 (19) | |
| IV | 28 (1) | 7 (1) | <0,001 |
| Amplitud del QRS (ms) | 123±35 | 118±33 | 0,002 |
| Bloqueo de la rama izquierda del haz de His | 793 (28) | 201 (28) | 0,925 |
| Implante por un electrofisiólogo | 2.038 (73) | 560 (78) | 0,005 |
| Tipo de dispositivo | 0,002 | ||
| DAI monocameral | 1.262 (45) | 374 (52) | |
| DAI bicameral | 680 (24) | 153 (21) | |
| DAI-TRC | 869 (31) | 190 (27) |
DAI: desfibrilador automático implantable; DAI-TRC: desfibrilador automático implantable-terapia de resincronización cardiaca; FEVI: fracción de eyección del ventrículo izquierdo; NYHA: New York Heart Association.
Los valores expresan n (%) o media ± desviación estándar.
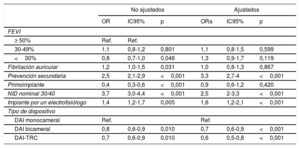
Predictores univariantes y multivariantes de la adopción de una estrategia de programación ADVANCE III en el momento del implante
| No ajustados | Ajustados | |||||
|---|---|---|---|---|---|---|
| OR | IC95% | p | ORa | IC95% | p | |
| FEVI | ||||||
| ≥ 50% | Ref. | Ref. | ||||
| 30-49% | 1,1 | 0,8-1,2 | 0,801 | 1,1 | 0,8-1,5 | 0,599 |
| <30% | 0,8 | 0,7-1,0 | 0,046 | 1,3 | 0,9-1,7 | 0,119 |
| Fibrilación auricular | 1,2 | 1,0-1,5 | 0,031 | 1,0 | 0,8-1,3 | 0,867 |
| Prevención secundaria | 2,5 | 2,1-2,9 | <0,001 | 3,3 | 2,7-4 | <0,001 |
| Primoimplante | 0,4 | 0,3-0,6 | <0,001 | 0,9 | 0,6-1,2 | 0,420 |
| NID nominal 30/40 | 3,7 | 3,0-4,4 | <0,001 | 2,5 | 2-3,3 | <0,001 |
| Implante por un electrofisiólogo | 1,4 | 1,2-1,7 | 0,005 | 1,6 | 1,2-2,1 | <0,001 |
| Tipo de dispositivo | ||||||
| DAI monocameral | Ref. | Ref. | ||||
| DAI bicameral | 0,8 | 0,6-0,9 | 0,010 | 0,7 | 0,6-0,9 | <0,001 |
| DAI-TRC | 0,7 | 0,6-0,9 | 0,010 | 0,6 | 0,5-0,8 | <0,001 |
DAI: desfibrilador automático implantable; DAI-TRC: desfibrilador automático implantable-terapia de resincronización cardiaca; FEVI: fracción de eyección del ventrículo izquierdo; IC95%: intervalo de confianza del 95%; NID: número de intervalos que detectar; OR: odds ratio; ORa: OR ajustada.
Tras el análisis multivariante, el NID nominal 30/40 (odds ratio ajustada [ORa]=4,4; IC95%, 3,5-5,4), la indicación para prevención secundaria (ORa=3,2; IC95%, 2,6-3,9) y el implante por un electrofisiólogo (ORa=1,7; IC95%, 1,4-2,2) emergieron como predictores independientes de la adopción de la programación ADVANCE, mientras que fue menos probable que se tratara con una estrategia de programación ADVANCE a los pacientes a los que se implantaba un DAI bicameral (ORa=0,6; IC95%, 0,5-0,8) o un DAI con terapia de resincronización cardiaca (ORa=0,5; IC95%, 0,4-0,7).
Relación entre la programación del DAI y la carga de terapias del DAIEl seguimiento medio fue de 49±26 meses (52±26 meses en el grupo no ADVANCE y 39±22 meses en el grupo ADVANCE). Durante el periodo de estudio, 1.265 pacientes (el 36% de la población del estudio) recibieron un total de 14.195 terapias del DAI, lo que dio como resultado una tasa de incidencia global de 102 terapias/100 pacientes-año. En total, 215 pacientes del grupo ADVANCE (30%) recibieron al menos una terapia del DAI comparado con los 1.050 (37%) del grupo no ADVANCE. Las tasas de incidencia sin ajustar se resumen en la tabla 3, así como las RTI ajustadas y no ajustadas para cada tipo concreto de tratamiento con dispositivo. Las tasas de incidencia sin ajustar de cualquier terapia apropiada, descarga apropiada y descarga inapropiada fueron de 114,2, 16,6 y 5,2 tratamientos/100 pacientes-año en el grupo no ADVANCE, comparado con 132,6, 21,9 y 4,1 tratamientos/100 pacientes-año en el grupo ADVANCE.
Tasas de incidencia no ajustadas y razones de tasas de incidencias ajustadas y sin ajustar para cada tipo de tratamiento
| Tratamientos cada 100 pacientes-año | RTI | RTI (IC95%) | RTIa | RTIa (IC95%) | ||
|---|---|---|---|---|---|---|
| No ADVANCE | ADVANCE | |||||
| Todas las terapias del DAI | 114,2 | 132,6 | 1,26 | 1,15-1,38 | 0,77 | 0,69-0,86 |
| Descarga del DAI | 21,8 | 26,0 | 1,12 | 0,99-1,28 | 0,86 | 0,74-0,99 |
| MAT | 92,4 | 106,6 | 1,32 | 1,19-1,45 | 0,80 | 0,71-0,90 |
| Terapias del DAI adecuadas | 99,2 | 129,9 | 1,37 | 1,25-1,51 | 0,82 | 0,74-0,92 |
| Descarga del DAI adecuada | 16,6 | 21,9 | 1,29 | 1,14-1,48 | 1,02 | 0,88-1,17 |
| MAT adecuado | 82,6 | 100,0 | 1,39 | 1,27-1,54 | 0,79 | 0,70-0,88 |
| Terapias del DAI inadecuadas | 15,0 | 10,7 | 0,67 | 0,57-0,78 | 0,52 | 0,43-0,62 |
| Descarga del DAI inadecuada | 5,2 | 4,1 | 0,74 | 0,59-0,94 | 0,66 | 0,52-0,85 |
| MAT inadecuado | 9,8 | 6,6 | 0,66 | 0,54-0,8 | 0,54 | 0,44-0,68 |
DAI: desfibrilador automático implantable; IC95%: intervalo de confianza del 95%; MAT: marcapasos antitaquicárdico; RTI: razón de tasas de incidencia; RTIa: RTI ajustadas.
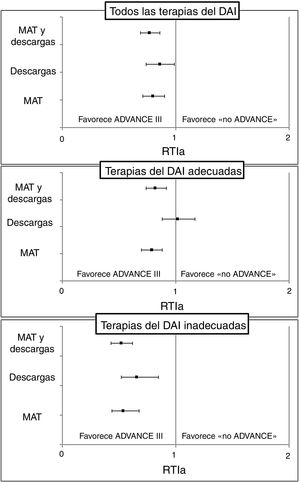
Tras el ajuste multivariante, la estrategia de programación ADVANCE se relacionó con una reducción de cualquier terapia del DAI (RTIa=0,77; IC95%, 0,69-0,86), las terapias de estimulación antitaquicárdica apropiadas (RTIa=0,79; IC95%, 0,7-0,88), las descargas inapropiadas del DAI (RTIa=0,66; IC95%, 0,52-0,85) y las terapias de estimulación antitaquicárdica inapropiadas (RTIa=0,54; IC95%, 0,44-0,68), sin diferencias significativas en las tasas de incidencia de descargas apropiadas del DAI (RTIa=1,02; IC95%, 0,88-1,17). Las RTIa para cada tipo de terapia se presentan como diagramas de bosque en la figura 3. Los predictores univariantes y multivariantes de cada tipo de terapia se proporcionan en la , la y la .
DISCUSIÓNEl presente estudio muestra que: a) la adopción real de estrategias de programación con tiempos de detección prolongados para los DAI sigue siendo baja, a pesar de que hay evidencia clara de beneficio clínico; b) estrategias tales como la publicación del consenso de expertos o las campañas de concienciación para asesores técnicos tienen poco impacto a corto y medio plazo; c) los factores relacionados con la adopción de una programación con tiempos de detección prolongados son los ajustes nominales «de fábrica» del DAI, el implante por un electrofisiólogo y la indicación de prevención secundaria, y d) el cumplimiento riguroso de una estrategia de programación de detección prolongada se relaciona con menor incidencia de terapias del DAI en pacientes reales.
Impacto clínico del cumplimiento de una estrategia ADVANCE IIISe ha observado en varios ensayos clínicos que prolongar los tiempos de detección de arritmia y restringir las terapias del DAI a taquicardias muy rápidas se relaciona con mejora de los resultados clínicos5,8,9, lo que subraya el concepto de terapias del DAI «evitables». El ensayo MADIT-RIT proporcionó la primera evidencia aleatorizada de mejora de resultados con la programación de alta frecuencia/detección prolongada en los DAI Boston Scientific, incluida una reducción de la mortalidad8. Poco después, el ensayo ADVANCE III mostró resultados similares en receptores de DAI de Medtronic aleatorizados a programación con tiempos de detección prolongados (NID 30/40 frente a programación convencional con NID 18/24; con programación de una única zona para pacientes de prevención primaria)5.
En el presente estudio, la estrategia de programación ADVANCE en la práctica diaria se relacionó con una reducción del 23% de todas las terapias del DAI y una reducción del 34% de las descargas inapropiadas. Las incidencias de descargas apropiadas fueron comparables entre los 2 grupos, como también se observó en los ensayos MADIT-RIT, ADVANCE III y PROVIDE. Estos datos confirman, en una población real no seleccionada de receptores de DAI, las observaciones del ensayo aleatorizado ADVANCE III, que reveló una reducción de todas las activaciones del dispositivo y del número de descargas inapropiadas. Estos datos también coinciden con un estudio reciente de Piccini et al.10, quienes informan del impacto de estrategias de programación contemporáneas en una cohorte de 64.769 pacientes y observan que la programación de terapias restringida a taquicardias muy rápidas con detección prolongada se relaciona con una reducción de la incidencia de descargas. También se observaron con el paso del tiempo cambios en las tendencias de programación, lo que indica la penetración progresiva de los resultados de los ensayos aleatorizados en la práctica clínica.
Predictores de la adopción de una estrategia de programación de detección prolongadaUna de las principales conclusiones del presente estudio es que la adopción de la programación de los DAI basada en la evidencia sigue siendo moderada (< 50%) años después de la publicación de ensayos aleatorizados fundamentales. En varios estudios se han destacado las dificultades en la transferencia de la evidencia científica publicada a la práctica clínica11–13. McGlynn et al.11 observaron que, de una muestra aleatoria de 13.275 pacientes estadounidenses, los participantes solo recibieron el 54,9% de las medidas de asistencia básica recomendadas. Por otro lado, aunque se ha descrito un lapso de hasta 17 años entre la publicación de los ensayos clínicos aleatorizados y la implementación de las observaciones en la práctica habitual14, nuestros resultados muestran un aumento inmediato de las tasas de adopción tras la publicación de los resultados del ensayo ADVANCE. De hecho, tal como se muestra en la figura 1, las tasas de adopción empezaron a aumentar ya antes de la publicación del estudio, probablemente por la influencia de los estudios publicados anteriormente8,15,16 y una percepción entre los implantadores de la importancia de las terapias evitables y la necesidad de tiempos de detección más largos. En este contexto, es importante observar que el periodo 1 incluye un intervalo de 6 años (2007-2013) y que la estimación del aumento que se proporciona es un promedio de aquel intervalo. Así pues, en general, este periodo se caracteriza por una pendiente de crecimiento nulo, a pesar del incremento en la programación ADVANCE observado justo antes de publicarse el ensayo.
Con un diseño de estudio similar, Varma et al.17 analizaron la reacción tras la publicación del ensayo MADIT-RIT y el consenso de 2015 en una cohorte estadounidense de gran tamaño extraída de la base de datos ALTITUDE (Boston Scientific). Describieron un cumplimiento inicial de la programación rigurosa del ensayo inferior al 1% que aumentó hasta aproximadamente el 14% el año siguiente a la publicación del MADIT-RIT, con un aumento inferior al 6% a partir de entonces. Los resultados del presente estudio revelan unas tasas de penetración del esquema de programación del ADVANCE III más altas. Este aumento podría relacionarse con el diseño del ensayo más simple que el del estudio MADIT-RIT de 3 grupos, lo que facilitó una traducción más directa de los hallazgos del estudio ADVANCE III al consenso de 2015 y a la práctica clínica. Además, una publicación reciente de Ananwattanasuk et al.18 también destacó que, en una serie de pacientes a los que se implantó un DAI entre 2014 y 2016 en 3 centros distintos, se programó según las recomendaciones pertinentes solo a 1/3.
Por otro lado, nuestros resultados muestran que los implantadores son más propensos a optar por la programación del ADVANCE III en el implante de dispositivos monocamerales que con los bicamerales y los desfibriladores-resincronizadores. Esto podría atribuirse al menor número de parámetros programables en los dispositivos monocamerales, lo que conduce a una programación más simple para estos pacientes (el ensayo MADIT-RIT no incluyó DAI monocamerales). Además, la dependencia de criterios de discriminación de doble cámara en lugar de una detección prolongada también podría contribuir al menor cumplimiento del ADVANCE entre los dispositivos bicamerales y tricamerales.
La indicación de prevención secundaria también se relacionó con un aumento en la adopción de la programación ADVANCE. Una posible explicación de esta observación es que, entre los pacientes en prevención primaria incluidos en este estudio, la activación de zonas de taquicardia «activa» por debajo del umbral de fibrilación auricular fue una de las principales razones de que estos pacientes no satisficieran una definición rigurosa del ADVANCE. Por otro lado, el ensayo ADVANCE III permitió zonas adicionales de taquicardia ventricular en función de las preferencias del médico de los sujetos en prevención secundaria, lo cual facilitó que estos pacientes «cumplieran» los criterios de la programación ADVANCE del presente estudio. El implante por un electrofisiólogo certificado (comparado con un cardiólogo no electrofisiólogo o un cirujano cardiaco) también se relacionó con la adherencia a la estrategia ADVANCE.
Estrategias propuestas para mejorar la adopción de una programación del DAI basada en la evidenciaEn cuanto a los factores que influyen en las opciones de programación, una de las observaciones más pertinentes es la fuerte relación entre los ajustes nominales «de fábrica» (en concreto, NID 30/40) y las prácticas de programación reales. Esta observación pone de manifiesto una oportunidad para que los fabricantes mejoren la atención a los pacientes programando ajustes de fábrica por defecto basados en la evidencia.
Otras estrategias que se han relacionado con una mejor programación de los DAI son los informes de retroalimentación de cada centro en los que se detalla el grado de adherencia a la evidencia19 y la promoción activa de los resultados de los ensayos clínicos (mediante campañas formativas), en lugar de la dependencia pasiva de que se publiquen artículos científicos y recomendaciones7,20. El presente estudio muestra que la implementación de una campaña de formación de «concienciación ADVANCE» dirigida a los técnicos fabricantes que ayudan a los médicos durante los implantes motivó un aumento continuo de las tasas de adopción, si bien a un ritmo más lento que en el periodo posterior a la publicación del ensayo. No obstante, estos resultados indican un efecto más importante de la publicación del ensayo en las prácticas de programación que el de la formación técnica o la publicación del consenso de expertos, una tendencia que también se observó en el estudio de Varma et al.17.
Limitaciones del estudioAl igual que con cualquier diseño retrospectivo, en el presente estudio se puede haber pasado por alto los factores de confusión no cuantificados que influyen en la elección de la programación, así como en la relación entre la programación del dispositivo y las tasas de tratamiento. Por ejemplo, no se dispuso de información sobre el número y el tipo de terapias de estimulación antitaquicárdica programados en cada paciente, lo cual puede influir en las tasas de descargas. El presente estudio se refiere a un único fabricante; no obstante, la evidencia acumulada5,8,9 coincide en mostrar las ventajas de una estrategia terapéutica de detección prolongada con todos los fabricantes evaluados. Además, se describen las prácticas de programación en el momento de implantar el dispositivo. Los cambios en la programación realizados más tarde no se recogieron en la base de datos, pero es posible que influyeran en las terapias ocurridas después. No obstante, la observación de Varma et al.17 de que menos del 2% de los pacientes de la base de datos ALTITUDE reprogramados de algún modo durante el seguimiento fueron reprogramados a ajustes del MADIT-RIT indica que la realización de cambios importantes en la programación durante el seguimiento del dispositivo es anecdótica.
Los intervalos de tiempo entre la campaña para asesores técnicos de Medtronic y la publicación de un consenso de expertos (periodo 3) y desde entonces hasta la fecha de cierre del estudio (periodo 4) fueron relativamente cortos comparados con los periodos de tiempo anteriores. Esto limita la posibilidad de sacar conclusiones definitivas sobre los efectos concretos de la campaña y el consenso de expertos. No obstante, los datos apuntan hacia un realidad clara: un aumento notable de la adopción ADVANCE tras la publicación de los resultados del ensayo aleatorizado, que disminuye lentamente a pesar de la campaña y el consenso de expertos.
Por último, se desconoce el estado vital al final del estudio en un considerable número de pacientes (los que dejaron de transmitir a través de la plataforma de monitorización a distancia pudieron hacerlo por recambio del generador por uno de otro fabricante, por desactivación o sustitución del desfibrilador por un marcapasos, por aspectos técnicos relacionados con el monitor remoto o porque fallecieron), lo que impide un análisis fiable de la mortalidad. Tampoco se dispuso de datos sobre las tasas de síncope.
CONCLUSIONESLa penetración de una estrategia de programación ADVANCE III en la práctica clínica sigue siendo moderada pese a haber evidencia de estudios aleatorizados, una campaña de promoción activa y las recomendaciones del consenso de expertos. La programación del DAI puede mejorarse mediante la selección de los ajustes de fábrica nominales basada en la evidencia. La adopción de una estrategia de programación ADVANCE III se relaciona con reducción de las tasas de terapias en receptores de DAI de la práctica clínica.
- –
Los DAI se han convertido en una de las piezas clave del tratamiento de los pacientes con riesgo de muerte súbita arrítmica.
- –
En múltiples estudios se ha observado que las descargas del DAI, independientemente de que sean adecuadas o inadecuadas, son una posible causa de empeoramiento de la insuficiencia cardiaca y mortalidad.
- –
Se han estudiado varias estrategias en un intento de reducir las descargas del DAI inadecuadas y potencialmente «innecesarias».
- –
El ensayo ADVANCE III mostró que el uso de una estrategia de detección prolongada para detectar la arritmia reduce los tratamientos del DAI.
- –
La adopción de estrategias de programación de detección prolongada para los DAI en la práctica clínica sigue siendo escasa pese a haberse probado sus ventajas clínicas.
- –
Estrategias como la publicación de un consenso de expertos o campañas de concienciación para los asesores técnicos tienen poco impacto a corto y medio plazo en la práctica cotidiana de programación.
- –
El cumplimiento de los parámetros del dispositivo recomendados por la guía puede mejorar mediante una selección de los ajustes de fábrica nominales basada en la evidencia por parte de los fabricantes, así como el implante del DAI por un electrofisiólogo.
- –
La adherencia a programar con detección prolongada se relaciona con una reducción de las tasas de terapias del DAI en pacientes de la práctica clínica.
G. Loughlin ha recibido financiación de Medtronic por asistir a conferencias médicas. La base de datos original utilizada para realizar este estudio es propiedad de Medtronic. Medtronic no tomó parte en el diseño del estudio, el análisis o la preparación y la redacción del manuscrito. Los demás coautores carecen de conflictos de intereses pertinentes que declarar.
Los autores agradecen a Miguel Ruiz su contribución al análisis estadístico.