La insuficiencia tricuspídea (IT) grave es una valvulopatía prevalente con una alta tasa de mortalidad. La guía vigente no define umbrales específicos para considerar a los pacientes para cirugía o procedimientos percutáneos. Por lo tanto, se suele derivarlos para intervención en una etapa tardía de la enfermedad. Este estudio tiene como objetivo evaluar los predictores de los eventos cardiovasculares en una cohorte prospectiva de pacientes con IT grave remitidos para cirugía.
MétodosSe trata de un estudio observacional, prospectivo y no aleatorizado. Todos los pacientes se sometieron a cirugía por IT grave según las guías clínicas vigentes. Se realizó anamnesis completa, análisis de sangre, ecocardiograma, resonancia magnética cardiovascular y cateterismo derecho e izquierdo. Se siguió a los pacientes en la consulta externa y se registró un criterio de valoración combinado (hospitalización por insuficiencia cardiaca o muerte de causa cardiovascular).
ResultadosSe incluyó a 43 pacientes consecutivos (edad, 66,9 ± 9,6 años; el 67,4% mujeres). En todos los casos se realizó anuloplastia tricuspídea. Después de una mediana de seguimiento de 38 meses, 12 pacientes (27,9%) presentaron el criterio combinado y 7 (16,3%) fallecieron. Por encima de todos los datos clínicos, sanguíneos y de imagen, el volumen telediastólico del ventrículo derecho indexado constituyó el mejor predictor del objetivo combinado (HR = 1,1; p = 0,02) y de muerte de causa cardiovascular (HR = 1,1; p = 0,05). Además, el volumen telediastólico del ventrículo derecho indexado se asoció con la recurrencia de la IT después de la cirugía, sin impacto en los resultados clínicos.
ConclusionesEn pacientes con IT grave remitidos para cirugía, el remodelado del ventrículo derecho evaluado por resonancia magnética cardiovascular fue el mejor predictor independiente de desenlace cardiovascular en el seguimiento.
Palabras clave
La insuficiencia tricuspídea (IT) grave es una valvulopatía cardiaca frecuente, que afecta a ≈1,6 millones de personas en Estados Unidos y, si no se trata, resulta en una dilatación e insuficiencia progresivas del ventrículo derecho (VD), con un aumento asociado de la morbilidad y la mortalidad1. La prevalencia de una IT grave aumenta con la edad, y en personas mayores de 70 años se acerca al 1,5% de los varones y el 5,6% de las mujeres2.
A pesar del aumento de la mortalidad asociado con esta IT grave, el tratamiento ha sido clásicamente conservador3. No obstante, en estudios recientes se ha observado que la sobrecarga crónica del VD se relaciona con disfunción irreversible del VD y con mal pronóstico. Así pues, recientemente ha ganado aceptación la estrategia de reparar la válvula tricúspide en el momento en que se operan las válvulas del lado izquierdo4,5. No obstante, sigue siendo controvertido saber cuál es el momento óptimo para esta intervención solo de la IT, y habitualmente se hace en una fase tardía3,4.
La mortalidad en las series quirúrgicas de IT grave es alta, y oscila entre un 15-20% durante la hospitalización y un 17-24% durante el primer año de seguimiento6. Esta alta tasa de mortalidad se ha atribuido al retraso de la cirugía porque los pacientes pueden contraer anemia, disfunción del VD, cirrosis o insuficiencia renal7. En un reciente ensayo ecocardiográfico longitudinal de Axtell et al.7, con una cohorte de 3.276 personas con IT grave, la cirugía no se relacionó con mejora de la supervivencia a largo plazo comparada con el tratamiento médico después de ajustar el sesgo de tiempo inmortal. Esos autores establecen la hipótesis de que un retraso de hasta 8 años entre el diagnóstico y la intervención quirúrgica podría explicar la ausencia de diferencias, y recomiendan que se establezca el momento óptimo de la intervención. En caso de no hacerse así, los próximos ensayos clínicos aleatorizados, con nuevas técnicas percutáneas8,9 para tratar la IT grave, podrían omitir las diferencias en la mortalidad.
Se carece de datos para establecer el momento apropiado de la cirugía y mejorar la supervivencia en los pacientes con IT grave. Así pues, el presente estudio pretende definir los principales predictores de eventos en una cohorte prospectiva de pacientes con IT grave funcional remitidos a intervención quirúrgica. Los resultados podrían ser útiles para planificar la intervención (percutánea o quirúrgica) en esta población y reducir los eventos en el seguimiento.
MÉTODOSSe trata de un estudio observacional, unicéntrico, prospectivo y no aleatorizado. El estudio se hizo en un hospital público con recursos técnicos avanzados, con 1.146 camas y en el que se hacen más de 750 intervenciones a corazón abierto cada año. Entre abril de 2014 y diciembre de 2017, se incluyó a todos los pacientes consecutivos con IT grave funcional e indicación de cirugía de la válvula tricúspide (si fuera necesario, podría agregarse tratamiento quirúrgico de la valvulopatía izquierda). La indicación de tratamiento quirúrgico de la IT partió de la vigente guía de la Sociedad Europea de Cardiología (ESC) sobre el tratamiento de las valvulopatías10,11. El seguimiento de los pacientes con IT grave se hizo mediante ecocardiografía bidimensional con Doppler color. Se remitió a los pacientes a tratamiento quirúrgico cuando presentaban signos y síntomas de insuficiencia cardiaca derecha que no respondían al tratamiento farmacológico óptimo, siempre y cuando la fracción de eyección del VD no fuera<30% o <45% junto con presión arterial pulmonar ≥ 60mmHg (según el protocolo del estudio)3. Se excluyó a los pacientes con marcapasos o que tuvieran contraindicada la resonancia magnética cardiovascular (RMC) o una valvulopatía tricuspídea congénita, valvulopatía izquierda importante (con indicación de tratamiento quirúrgico de por sí) o estenosis o insuficiencia pulmonar grave.
Se evaluó a los pacientes que participaron en el ensayo mediante anamnesis, exploración física completa, análisis de sangre, ecocardiografía bidimensional con Doppler color, RMC, cateterismo cardiaco izquierdo para evaluar la enfermedad coronaria y cateterismo cardiaco derecho para evaluar la presión pulmonar. El seguimiento de los pacientes se hizo en consultas externas y se registraron la clase funcional de la New York Heart Association (NYHA), la hospitalización por insuficiencia cardiaca y la mortalidad cardiovascular y total. No se hicieron pruebas funcionales. El objetivo primario era la combinación de hospitalización por insuficiencia cardiaca y mortalidad cardiovascular en el seguimiento. El objetivo secundario era la mortalidad cardiovascular. Se añadió la mortalidad cardiovascular quirúrgica cuando ocurría en los 30 días posteriores a la intervención, dentro o fuera del hospital, y después de 30 días en la misma hospitalización debida a la intervención12. El seguimiento empezó en el momento de la intervención quirúrgica.
Antes del alta, se hizo un ecocardiograma de seguimiento a todos los pacientes que sobrevivieron las primeras 24 h tras la intervención para determinar la presencia de IT residual y sus principales predictores.
Análisis de sangreSe recogieron muestras de sangre de todos los pacientes y se determinaron los siguientes parámetros: hemoglobina, hematocrito, creatinina, tasa de filtrado glomerular estimada, aspartato aminotransferasa, alanina aminotransferasa, fosfatasa alcalina, glutamil transpeptidasa, bilirrubina, proteína, albúmina, renina, propéptido natriurético cerebral y aldosterona.
Ecocardiografía bidimensional con Doppler colorSe evaluó a todos los pacientes mediante ecocardiografía con el Vivid 9 (GE Healthcare, General Electric, Estados Unidos) y después se procesaron todas las imágenes con un software específico: Echopach (GE Healthcare, General Electric, Estados Unidos). Se evaluaron los siguientes parámetros: la función del VD y el VI, los volúmenes y las áreas auriculares y ventriculares, el diámetro del anillo tricuspídeo, el desplazamiento sistólico del plano anular tricuspídeo (TAPSE) y la imagen de Doppler tisular del anillo tricuspídeo (onda S). La gravedad de la valvulopatía se evaluó a partir del área del chorro central, la amplitud de la vena contracta, el flujo sistólico de la vena hepática y la densidad y la forma del perfil de velocidad de la onda continua por Doppler, tal como recomienda la vigente guía de la ESC13. La IT se clasificó según la nueva propuesta como leve, moderada, grave, masiva y torrencial14. En los pacientes con valvulopatía mitral o prótesis mitral asociada, el estudio se completó con una ecocardiografía transesofágica.
Resonancia magnética cardiovascularTodos los estudios de RMC se hicieron con un equipo de 1,5 T (Sonata o Avanto, Siemens, Alemania). Se calcularon mediante rastreo tisular con la RMC la fracción de eyección del ventrículo izquierdo, el volumen telediastólico del VI indexado, el volumen telesistólico del VI indexado, el índice de masa del VI, la fracción de eyección del VD, el volumen telediastólico del VD indexado, el volumen telesistólico del VD indexado y la deformación (strain) longitudinal, circunferencial y radial global de la pared libre del VD. Además, se obtuvieron los diámetros y los volúmenes del área auricular derecha. A los 10-15min de la administración del contraste, se obtuvieron las secuencias del realce tardío de gadolinio. En el se dan más detalles sobre los aspectos técnicos de la adquisición de la RMC, las secuencias y la cuantificación.
Un observador experto al que se ocultaron todos los datos de los pacientes analizó offline los estudios de RMC con el software personalizado (Cvi42, Circle Cardiovascular Imaging Inc., Canadá).
Cateterismos cardiacos: izquierdo y derechoTodos los cateterismos cardiacos, izquierdos y derechos, se hicieron con un Philips Integris Angio Diagnost 5 antes de la intervención quirúrgica y según las recomendaciones actuales15. Se evaluaron los parámetros siguientes: presencia de una estenosis coronaria importante, presión arterial pulmonar sistólica, presión arterial pulmonar media, presión arterial pulmonar diastólica y resistencia vascular pulmonar indexada. Un observador experto, con los datos de todos los pacientes enmascarados, analizó los resultados.
El comité de ética para la investigación en humanos del hospital aprobó el protocolo del ensayo, que cumplió con las recomendaciones de la Declaración de Helsinki de 1975. Todos los pacientes que participaron en el ensayo firmaron el consentimiento informado antes de su inclusión.
Análisis estadísticoLas variables continuas se expresan mediante media±desviación estándar y las categóricas, mediante el número de casos y las proporciones. Se evaluó la distribución normal de las variables continuas con la prueba de Shapiro-Wilk y se comparó entre los distintos grupos con la prueba de la t de Student o la prueba de Wilcoxon. Las variables categóricas se compararon con la prueba de la χ2 o la prueba exacta de Fisher, según conviniera. Los posibles predictores de eventos se evaluaron con los modelos de regresión de riesgos proporcionales de Cox. Las variables con p <0,10 en los análisis univariantes se introdujeron en el modelo multivariante. Para evitar la multicolinealidad, se excluyeron de la regresión multivariable de Cox las variables con prueba de tolerancia <0,1 o factor de inflación de la variación >5. También se incluyó el análisis de los residuos de Schoenfeld para confirmar que se cumplía la hipótesis proporcional para la exposición de interés. La distribución de residuos de martingala se realizó para probar el supuesto de linealidad para los modelos de Cox y predecir el objetivo compuesto y la mortalidad cardiovascular. Para definir la capacidad de discriminación del modelo logístico y predecir la recurrencia de la IT, se utilizaron las curvas de eficacia diagnóstica (curvas ROC). Este análisis pretendía determinar los principales factores asociados con un mal resultado de la intervención quirúrgica y no el momento de su aparición.
Un valor de p <0,05 se consideró estadísticamente significativo. Para el análisis se utilizó la versión 19.0 del software SPSS (IBM SPSS Statistics, Estados Unidos).
RESULTADOSDurante un periodo de 32 meses, 47 pacientes consecutivos participaron en el ensayo. No obstante, se excluyó a 4 pacientes: 2 por claustrofobia grave y 2 por llevar un marcapasos no compatible con la RMC. Así pues, en el análisis participó una población final de 43 pacientes. Antes de la intervención, todos los pacientes recibían un tratamiento farmacológico óptimo: 11 pacientes (25,6%) con bloqueadores beta, 26 (60,4%) con digoxina, 34 (79%) con inhibidores de la enzima de conversión de la angiotensina o antagonistas del receptor de la angiotensina II, 34 (79%) con antagonistas del receptor de mineralocorticoides y 43 (100%) con diuréticos. Las características demográficas se muestran en la tabla 1. Eran mujeres 29 pacientes (67,4%); la media de edad fue 66,9±9,6 años; 37 pacientes (86,1%) sufrían fibrilación auricular y el 97,6% estaban sintomáticos (NYHA ≥ II). A 19 pacientes (44,2%) se les había practicado una intervención quirúrgica previa: válvula mitral (57,9%), válvula aórtica (10,5%), válvulas mitral y aórtica (10,5%), válvula tricúspide (5,3%), válvula mitral y tricúspide (5,3%), cirugía de revascularización coronaria (5,3%) u otro tipo de intervención (5,3%). La IT fue grave en 6 pacientes (13,9%) y masiva en 37 (86%). No hubo ningún paciente con IT torrencial. Aunque la principal indicación de tratamiento quirúrgico fue la IT, 26 pacientes (60,5%) también requirieron reparación de la válvula mitral (debido a fuga), 4 (9,3%) requirieron bioprótesis aórticas a causa de la estenosis aórtica moderada y 1 paciente (2,3%) requirió reparación de la válvula tricúspide, reparación de la válvula mitral y reemplazo de la válvula aórtica (IT grave con insuficiencia mitral moderada y estenosis aórtica moderada). Se hizo anuloplastia tricuspídea a todos los pacientes. A ninguno se le implantó una prótesis valvular (bioprótesis o una válvula mecánica), ya que en el estudio solo participaron pacientes a los que se trataba por una IT secundaria. Ninguno de los pacientes presentó realce tardío de gadolinio.
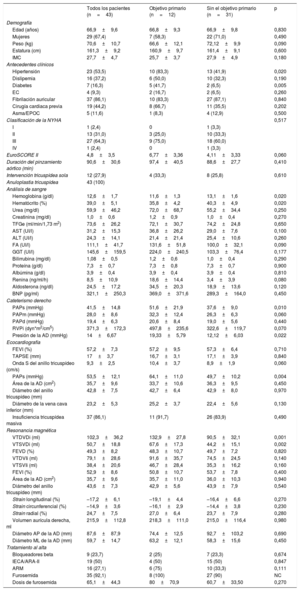
Características basales de todo el grupo de estudio y de los pacientes con o sin el objetivo primario (hospitalización por insuficiencia cardiaca o muerte cardiovascular)
| Todos los pacientes (n=43) | Objetivo primario (n=12) | Sin el objetivo primario (n=31) | p | |
|---|---|---|---|---|
| Demografía | ||||
| Edad (años) | 66,9±9,6 | 66,8±9,3 | 66,9±9,8 | 0,830 |
| Mujeres | 29 (67,4) | 7 (58,3) | 22 (71,0) | 0,490 |
| Peso (kg) | 70,6±10,7 | 66,6±12,1 | 72,12±9,9 | 0,090 |
| Estatura (cm) | 161,3±9,2 | 160,9±9,7 | 161,4±9,1 | 0,600 |
| IMC | 27,7±4,7 | 25,7±3,7 | 27,9±4,9 | 0,180 |
| Antecedentes clínicos | ||||
| Hipertensión | 23 (53,5) | 10 (83,3) | 13 (41,9) | 0,020 |
| Dislipemia | 16 (37,2) | 6 (50,0) | 10 (32,3) | 0,190 |
| Diabetes | 7 (16,3) | 5 (41,7) | 2 (6,5) | 0,005 |
| EC | 4 (9,3) | 2 (16,7) | 2 (6,5) | 0,260 |
| Fibrilación auricular | 37 (86,1) | 10 (83,3) | 27 (87,1) | 0,840 |
| Cirugía cardiaca previa | 19 (44,2) | 8 (66,7) | 11 (35,5) | 0,202 |
| Asma/EPOC | 5 (11,6) | 1 (8,3) | 4 (12,9) | 0,500 |
| Clasificación de la NYHA | 0,517 | |||
| I | 1 (2,4) | 0 | 1 (3,3) | |
| II | 13 (31,0) | 3 (25,0) | 10 (33,3) | |
| III | 27 (64,3) | 9 (75,0) | 18 (60,0) | |
| IV | 1 (2,4) | 0 | 1 (3,3) | |
| EuroSCORE II | 4,8±3,5 | 6,77±3,36 | 4,11±3,33 | 0,060 |
| Duración del pinzamiento aórtico (min) | 90,6±30,6 | 97,4±40,5 | 88,6±27,7 | 0,410 |
| Intervención tricuspídea sola | 12 (27,9) | 4 (33,3) | 8 (25,8) | 0,610 |
| Anuloplastia tricuspídea | 43 (100) | |||
| Análisis de sangre | ||||
| Hemoglobina (g/dl) | 12,6±1,7 | 11,6±1,3 | 13,1±1,6 | 0,020 |
| Hematócrito (%) | 39,0±5,1 | 35,8±4,2 | 40,3±4,9 | 0,020 |
| Urea (mg/dl) | 59,9±46,2 | 72,0±68,7 | 55,2±34,4 | 0,250 |
| Creatinina (mg/dl) | 1,0±0,6 | 1,2±0,9 | 1,0±0,4 | 0,270 |
| TFGe (ml/min/1,73 m2) | 73,6±26,2 | 72,1±30,7 | 74,2±24,8 | 0,650 |
| AST (UI/l) | 31,2±15,3 | 36,8±26,2 | 29,0±7,6 | 0,100 |
| ALT (UI/l) | 24,3±14,1 | 21,4±21,4 | 25,4±10,6 | 0,260 |
| FA (UI/l) | 111,1±41,7 | 131,6±51,8 | 100,0±32,1 | 0,090 |
| GGT (UI/l) | 145,6±159,5 | 224,0±240,5 | 103,3±76,4 | 0,177 |
| Bilirrubina (mg/dl) | 1,08±0,5 | 1,2±0,6 | 1,0±0,4 | 0,290 |
| Proteína (g/dl) | 7,3±0,7 | 7,3±0,8 | 7,3±0,7 | 0,900 |
| Albúmina (g/dl) | 3,9±0,4 | 3,9±0,4 | 3,9±0,4 | 0,810 |
| Renina (ng/ml/h) | 8,5±10,9 | 18,6±14,4 | 3,4±3,9 | 0,080 |
| Aldosterona (ng/dl) | 24,5±17,2 | 34,5±20,3 | 18,9±13,6 | 0,120 |
| BNP (pg/ml) | 321,1±250,3 | 369,0±371,6 | 289,3±164,0 | 0,450 |
| Cateterismo derecho | ||||
| PAPs (mmHg) | 41,5±14,8 | 51,6±21,9 | 37,6±9,0 | 0,010 |
| PAPm (mmHg) | 28,0±8,6 | 32,3±12,4 | 26,3±6,3 | 0,060 |
| PAPd (mmHg) | 19,4±6,3 | 20,6±8,4 | 19,0±5,6 | 0,440 |
| RVPi (dyn*m2/cm5) | 371,3±172,3 | 497,8±235,6 | 322,6±119,7 | 0,070 |
| Presión de la AD (mmHg) | 14±6,67 | 19,33±5,79 | 12,12±6,03 | 0,022 |
| Ecocardiografía | ||||
| FEVI (%) | 57,2±7,3 | 57,2±9,5 | 57,3±6,4 | 0,710 |
| TAPSE (mm) | 17±3,7 | 16,7±3,1 | 17,1±3,9 | 0,840 |
| Onda S del anillo tricuspídeo (cm/s) | 9,3±2,5 | 10,4±3,7 | 8,9±1,9 | 0,060 |
| PAPs (mmHg) | 53,5±12,1 | 64,1±11,0 | 49,7±10,2 | 0,004 |
| Área de la AD (cm2) | 35,7±9,6 | 33,7±10,6 | 36,3±9,5 | 0,450 |
| Diámetro del anillo tricuspídeo (mm) | 42,8±7,5 | 42,7±6,4 | 42,9±8,0 | 0,970 |
| Diámetro de la vena cava inferior (mm) | 23,2±5,3 | 25,2±3,7 | 22,4±5,6 | 0,130 |
| Insuficiencia tricuspídea masiva | 37 (86,1) | 11 (91,7) | 26 (83,9) | 0,490 |
| Resonancia magnética | ||||
| VTDVDi (ml) | 102,3±36,2 | 132,9±27,8 | 90,5±32,1 | 0,001 |
| VTSVDi (ml) | 50,7±18,8 | 67,6±17,3 | 44,2±15,1 | 0,002 |
| FEVD (%) | 49,3±8,2 | 48,3±10,7 | 49,7±7,2 | 0,820 |
| VTDVIi (ml) | 79,1±28,6 | 91,6±35,7 | 74,5±24,5 | 0,140 |
| VTSVIi (ml) | 38,4±20,6 | 46,7±28,4 | 35,3±16,2 | 0,160 |
| FEVI (%) | 52,9±8,6 | 50,8±10,7 | 53,7±7,8 | 0,400 |
| Área de la AD (cm2) | 35,7±9,6 | 35,7±11,0 | 36,0±10,3 | 0,940 |
| Diámetro del anillo tricuspídeo (mm) | 43,6±7,3 | 42,9±5,6 | 43,9±7,9 | 0,540 |
| Strain longitudinal (%) | –17,2±6,1 | –19,1±4,4 | –16,4±6,6 | 0,270 |
| Strain circunferencial (%) | –14,9±3,6 | –16,1±2,9 | –14,4±3,8 | 0,230 |
| Strain radial (%) | 24,7±7,5 | 27,0±6,4 | 23,7±7,9 | 0,280 |
| Volumen aurícula derecha, ml | 215,9±112,8 | 218,3±111,0 | 215,0±116,4 | 0,980 |
| Diámetro AP de la AD (mm) | 87,6±87,9 | 74,4±12,5 | 92,7±103,2 | 0,690 |
| Diámetro ML de la AD (mm) | 59,7±14,7 | 63,2±12,1 | 58,3±15,6 | 0,450 |
| Tratamiento al alta | ||||
| Bloqueadores beta | 9 (23,7) | 2 (25) | 7 (23,3) | 0,674 |
| IECA/ARA-II | 19 (50) | 4 (50) | 15 (50) | 0,847 |
| ARM | 16 (27,1) | 6 (75) | 10 (33,3) | 0,111 |
| Furosemida | 35 (92,1) | 8 (100) | 27 (90) | NC |
| Dosis de furosemida | 65,1±44,3 | 80±70,9 | 60,7±33,50 | 0,270 |
AD: aurícula derecha; ALT: alanina aminotransferasa; AP: anteroposterior; ARA-II: antagonistas del receptor de la angiotensina II; ARM: antagonistas del receptor de mineralocorticoides; AST: aspartato aminotransferasa; BNP: péptido natriurético cerebral; EC: enfermedad coronaria; EPOC: enfermedad pulmonar obstructiva crónica; FA: fosfatasa alcalina; FEVD: fracción de eyección del ventrículo derecho; FEVI: fracción de eyección del ventrículo izquierdo; GGT: gamma-glutamiltransferasa; IECA: inhibidores de la enzima de conversión de la angiotensina; IMC: índice de masa corporal; ML: mediolateral; NC: no calculado; NYHA: New York Heart Association; PAPd: presión arterial pulmonar diastólica; PAPm: presión arterial pulmonar media; PAPs: presión arterial pulmonar sistólica; RVPi: resistencia vascular pulmonar indexada; TAPSE: desplazamiento sistólico del plano anular tricuspídeo; TFGe: tasa de filtrado glomerular estimada; VTDVDi: volumen telediastólico del ventrículo derecho indexado; VTSVDi: volumen telesistólico del ventrículo derecho indexado; VTDVIi: volumen telediastólico del ventrículo izquierdo indexado; VTSVIi: volumen telesistólico del ventrículo izquierdo indexado.
Los valores expresan n (%) o media±desviación estándar.
Se siguió a todos los pacientes una mediana de 38 [intervalo intercuartílico, 14-63] meses.
Predictores del objetivo primarioRequirieron hospitalización por insuficiencia cardiaca o fallecieron por muerte cardiovascular 12 pacientes (27,9%). La mediana de tiempo entre la intervención quirúrgica y el evento fue de 2,5 [0,3-15,3] meses.
Comparados con los pacientes que no sufrieron evento alguno, los que sufrieron el objetivo primario tuvieron una mayor incidencia de hipertensión (p=0,02), diabetes (p=0,005), anemia (menores concentración de hemoglobina y hematocrito; ambos, p=0,02), mayor volumen telediastólico del VD indexado (VTDVDi) (132,9 frente a 90,5ml/m2; p=0,001), mayor volumen telesistólico del ventrículo derecho indexado (VTSVDi) (67,6 frente a 44,2ml/m2; p=0,002) y mayor presión arterial pulmonar sistólica, calculada mediante ecocardiografía (64,1 frente a 49,7mmHg; p=0,004) y cateterismo cardiaco derecho (p=0,01) (tabla 1). La incidencia del evento primario no difirió entre los pacientes sometidos solo a cirugía tricuspídea y aquellos con tratamiento quirúrgico combinado (p=0,61).
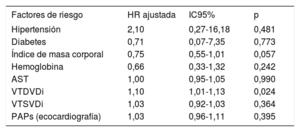
Tras ajustar por hipertensión, diabetes, índice de masa corporal, hemoglobina, aspartato aminotransferasa, VTDVDi, VTSVDi y las variables de la presión arterial pulmonar sistólica mediante análisis multivariante de regresión de Cox, solo el VTDVDi fue el principal predictor del objetivo primario (hazard ratio [HR]=1,1; intervalo de confianza del 95% [IC95%], 1,01-1,13; p=0,024) (tabla 2). La hipótesis de los riesgos proporcionales se confirmó con el análisis de los residuos de Schoenfeld (p=0,90). El estadístico C=0,91 (IC95%, 0,74-0,95) también confirmó que el VTDVDi podía predecir el objetivo primario. En la figura 1A se representan las curvas de supervivencia de Kaplan-Meier para el objetivo primario por terciles del VTDVDi. En particular, la incidencia del objetivo primario en los pacientes con un VTDVDi >104ml/m2 fue un 66% más alta que en aquellos con un menor umbral (10 pacientes frente a 2, respectivamente; rango logarítmico, 16,375; p <0,001).
Predictores del objetivo primario (mortalidad cardiovascular y hospitalización por insuficiencia cardiaca)
| Factores de riesgo | HR ajustada | IC95% | p |
|---|---|---|---|
| Hipertensión | 2,10 | 0,27-16,18 | 0,481 |
| Diabetes | 0,71 | 0,07-7,35 | 0,773 |
| Índice de masa corporal | 0,75 | 0,55-1,01 | 0,057 |
| Hemoglobina | 0,66 | 0,33-1,32 | 0,242 |
| AST | 1,00 | 0,95-1,05 | 0,990 |
| VTDVDi | 1,10 | 1,01-1,13 | 0,024 |
| VTSVDi | 1,03 | 0,92-1,03 | 0,364 |
| PAPs (ecocardiografía) | 1,03 | 0,96-1,11 | 0,395 |
AST: aspartato aminotransferasa; HR: hazard ratio; IC95%: intervalo de confianza del 95%; PAPs: presión arterial pulmonar sistólica; VTDVDi: volumen telediastólico del ventrículo derecho indexado; VTSVDi: volumen telesistólico del ventrículo derecho indexado.
La mortalidad cardiovascular quirúrgica fue del 9,3% y la mortalidad total, del 16,3% (todos los fallecidos por muerte cardiovascular). La mediana de tiempo desde la cirugía hasta la defunción fue de 2 [0,1-16] meses; 4 pacientes fallecieron antes de recibir el alta (2 por shock cardiogénico y 2 por disfunción aguda del VD) y 3 durante el seguimiento (todos por insuficiencia cardiaca del VD).
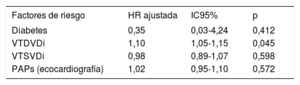
En el análisis univariante; un aumento de la fosfatasa alcalina (p=0,014), un descenso de la concentración de albúmina (p=0,031) y un aumento del VTDVDi (p=0,049) se asociaron con la mortalidad cardiovascular total (). No obstante, en el análisis multivariante de regresión de Cox, el VTDVDi fue el principal predictor de la mortalidad cardiovascular total (HR=1,1; IC95%, 1,05-1,15; p=0,045) (tabla 3). La hipótesis de los riesgos proporcionales también se confirmó con el análisis de los residuos de Schoenfeld (p=0,83). El estadístico C también confirmó la idoneidad del VTDVDi para predecir el objetivo secundario (C=0,82; IC95%, 0,65-0,92). En la figura 1B se representan las curvas de supervivencia de Kaplan-Meier de la mortalidad cardiovascular por terciles del VTDVDi. Así pues, en los pacientes con un VTDVDi> 104ml/m2, la mortalidad cardiovascular fue mayor que en aquellos con un menor VTDVDi (5 frente a 2; rango logarítmico, 5,368; p=0,045).
Predictores de muerte cardiovascular
| Factores de riesgo | HR ajustada | IC95% | p |
|---|---|---|---|
| Diabetes | 0,35 | 0,03-4,24 | 0,412 |
| VTDVDi | 1,10 | 1,05-1,15 | 0,045 |
| VTSVDi | 0,98 | 0,89-1,07 | 0,598 |
| PAPs (ecocardiografía) | 1,02 | 0,95-1,10 | 0,572 |
HR: hazard ratio; IC95%: intervalo de confianza del 95%; PAPs: presión arterial pulmonar sistólica; VTDVDi: volumen telediastólico del ventrículo derecho indexado; VTSVDi: volumen telesistólico del ventrículo derecho indexado.
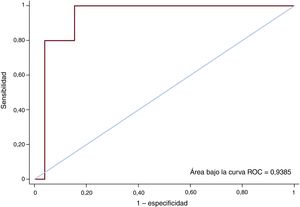
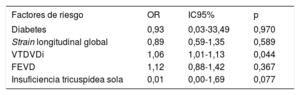
A todos los pacientes (menos a 3 que fallecieron prematuramente) se les hizo un ecocardiograma de seguimiento antes del alta y se observó recurrencia de la IT en 32: 19 (47,5%) leve, 8 (20,0%) moderada y 5 (12,5%) grave. Los predictores de recurrencia de IT importante (grados de insuficiencia II o III/IV evaluados mediante parámetros cuantitativos de Doppler) se muestran en la . Se observaron aumentos de la concentración de renina (p=0,033), el VTDVDi (p=0,025) y la función en el VD: la fracción de eyección del VD (p=0,009), el strain longitudinal global de la pared libre del VD (p=0,002), el strain circunferencial del VD (p=0,009) y el strain radial del VD (p=0,025) fueron las principales variables asociadas con recurrencia importante de la IT, lo cual indica que, cuanto mejor fuera la función del VD, mayor sería la velocidad a través de la válvula tricúspide y, como resultado, mayor la señal Doppler de IT recurrente. No obstante, en el análisis de regresión logística multivariante, solo el VTDVDi se asoció con la recurrencia de la IT (odds ratio [OR]=1,06; IC95%, 1,01-1,13; p=0,044) (tabla 4). El área bajo la curva ROC del modelo logístico para predecir la recurrencia de la IT fue de 0,939 (p <0,01) (figura 2). Paradójicamente, el diámetro del anillo tricuspídeo antes de la intervención quirúrgica no se relacionó con recurrencia de la IT.
Análisis multivariante de la recurrencia de insuficiencia tricuspídea importante
| Factores de riesgo | OR | IC95% | p |
|---|---|---|---|
| Diabetes | 0,93 | 0,03-33,49 | 0,970 |
| Strain longitudinal global | 0,89 | 0,59-1,35 | 0,589 |
| VTDVDi | 1,06 | 1,01-1,13 | 0,044 |
| FEVD | 1,12 | 0,88-1,42 | 0,367 |
| Insuficiencia tricuspídea sola | 0,01 | 0,00-1,69 | 0,077 |
FEVD: fracción de eyección del ventrículo derecho; IC95%: intervalo de confianza del 95%; OR: odds ratio; VTDVDi: volumen telediastólico del ventrículo derecho indexado.
La presencia de una IT recurrente importante (moderada o grave) no se relacionó con el objetivo primario (HR=2,26; IC95%, 0,65-7,83; p=0,197) ni con la mortalidad cardiovascular (HR=2,87; IC95%, 0,48-17,21; p=0,249).
DISCUSIÓNLa IT se ha considerado durante mucho tiempo una entidad olvidada a causa de la creencia de que el tratamiento de las válvulas del lado izquierdo prevenía la aparición de una IT importante3. No obstante, según los estudios de seguimiento, este enfoque conservador se relaciona con una gran incidencia de IT residual considerable en el 25% de los pacientes16,17. Así pues, las guías vigentes de la ESC y la European Association for Cardio-Thoracic Surgery (EACTS)11, así como las del American Heart College (AHA) y el American College of Cardiology (ACC)18, para el tratamiento de las valvulopatías recomiendan la intervención quirúrgica en los pacientes con IT secundaria leve o moderada, con un anillo dilatado (≥ 40mm o> 21 mm/m2 en la ecocardiografía bidimensional), que se someten a cirugía de las válvulas del lado izquierdo (indicación de clase IIa y IIb respectivamente).
La IT importante se relaciona con un aumento de la morbilidad y la mortalidad2,16. Los principales factores de riesgo son una clase funcional avanzada, la dilatación y disfunción del VD, la hipertensión pulmonar, la insuficiencia renal y la disfunción hepática grave. El problema en los pacientes con IT es que pueden permanecer asintomáticos durante mucho tiempo y, cuando los síntomas aparecen, es posible que la IT se encuentre ya en una fase irreversible en la que la disfunción del VD persista a pesar del tratamiento6,7. En un estudio reciente de Axtell et al.7 con 3.276 pacientes con IT sola, se observó que practicar la cirugía hasta 8 años después del diagnóstico no se asociaba con una mejora de la supervivencia a largo plazo frente al tratamiento farmacológico solo y tras ajustar para el sesgo del tiempo inmortal. Por lo tanto, es importante establecer el momento preciso en que debería indicarse la cirugía para evitar la evolución a una fase irreversible. Además, el nuevo tratamiento percutáneo para la IT importante antes de que se produzca la disfunción irreversible del VD podría reducir la mortalidad que el tratamiento quirúrgico conlleva. Es crucial identificar cuál es el «momento óptimo» del tratamiento percutáneo de la IT para evitar intervenciones innecesarias19,20. El presente es el primer estudio prospectivo en pacientes con IT grave que evalúa la función pronóstica de las variables clínicas, analíticas, ecocardiográficas, de la RMC y hemodinámicas como predictores de eventos cardiacos importantes (tales como la mortalidad cardiovascular o la hospitalización por insuficiencia cardiaca). El principal resultado de este estudio es que el VTDVDi, evaluado mediante RMC, es el mejor predictor de eventos cardiovasculares durante el seguimiento. Así pues, un VTDVDi> 104ml/m2 se asoció con un objetivo primario del 23,3% y una mortalidad cardiovascular del 11,6%, y este valor es independiente del grado de hipertensión pulmonar o de la gravedad de la disfunción del VD. Kim et al.21 observaron que un área telesistólica del VD <20cm2 predecía una supervivencia libre de eventos. Asimismo, los resultados de este estudio muestran que la intervención quirúrgica sin presencia de dilatación del VD (> 104ml/m2) podría haber reducido la incidencia del objetivo primario del 23,3 al 4,6% y la mortalidad total del 11,6 al 4,6%. Además, este estudio coincide con un estudio ecocardiográfico y retrospectivo reciente de Dietz et al.22, quienes observaron que la presencia de dilatación del VD (definida como un anillo tricuspídeo ≥ 40mm) junto con disfunción ventricular (definida como un TAPSE <17mm) es el principal predictor de la mortalidad total de los pacientes con IT grave. No obstante, en aquel estudio, solo el 21% de los pacientes presentaban una IT grave y solo se intervino quirúrgicamente al 8% de ellos. De forma parecida a este estudio, Kim et al.23 observaron que, en los 31 pacientes sometidos a cirugía de la válvula tricúspide (reemplazo de la válvula tricúspide en el 81% de los casos), un VTDVDi <164ml/m2 fue el mejor predictor de recuperación de la función del VD durante el seguimiento. No obstante, aunque los pacientes de aquel estudio presentaban un grado de disfunción del VD parecido (el 49,7±8,3% frente al 49,3±8,2% de este estudio), el umbral del VTDVDi obtenido fue claramente distinto (164 frente a 104ml/m2). Estas diferencias pueden explicarse por varias razones: el estudio de Kim et al. solo pretendía determinar la recuperación de la función del VD sin repercusiones en el pronóstico, la población era más joven (56,6±9,1 frente a 66,9±9,6 años), la proporción de varones fue menor (el 13 frente al 33%), la mayoría de los pacientes se sometieron a reemplazo de la válvula tricúspide (el 81% frente a 0), no se incluyó el valor de la presión arterial pulmonar sistólica y, por último, se excluyó a los 6 pacientes que fallecieron durante el seguimiento23.
La cirugía es el tratamiento de elección de la IT grave cuando los pacientes no responden al tratamiento farmacológico. No obstante, este tratamiento conlleva una gran mortalidad (17-24%)24 debido a su indicación tardía cuando los pacientes sufren múltiples enfermedades concomitantes y se asocia con remodelado irreversible del VD. Aunque el remodelado del VD no se afecta solo por la gravedad de la IT, otros factores como la sobrecarga de presión, la muerte celular o la fibrosis miocárdica también intervienen en la fisiopatología del VD22. Además, de un modo parecido a lo que ocurre cuando hay insuficiencia mitral grave, la fracción de eyección del VD no es el mejor método para calcular la función ventricular en la IT grave25. Así, según los resultados de este estudio, tendría que haber unas considerables dilatación y disfunción del VD relacionadas con la IT para que tuviera lugar una insuficiencia cardiaca derecha26,27, que se relaciona con taquiarritmias, ascitis, disfunción hepática, gasto cardiaco bajo y peores eventos cardiovasculares26. Las guías europea11 y estadounidense18 relativas al tratamiento de las valvulopatías cardiacas recomiendan la cirugía con indicaciones IIa y IIb (respectivamente) para pacientes con IT grave o que estén sintomáticos o muestren dilatación y disfunción progresivas del VD, sin disfunción ventricular derecha e izquierda grave y sin hipertensión pulmonar importante. No obstante, el valor discriminatorio específico para indicar cirugía no se ha establecido y, en consecuencia, la indicación se hace de un modo arbitrario según los distintos centros. La mortalidad cardiovascular total de este estudio fue del 16,3%. Por otra parte, la mortalidad cardiovascular quirúrgica fue del 9,3%, similar a la observada por Verdonk et al.28 (5-13%) e inferior a la observada por Rodríguez-Capitán et al.29 (18,5%). De modo imprevisto, la combinación de cirugía de las válvulas del lado izquierdo (necesaria en el 60,5% de los pacientes sin valvulopatía izquierda grave) no se asoció con un aumento de la mortalidad. Esto se explica por el hecho que la indicación de cirugía en la población de este estudio tuvo en cuenta la gravedad de la IT y no la de la valvulopatía izquierda. Además, dado que todos los pacientes recibieron un tratamiento farmacológico óptimo en el momento del alta (tabla 1) según el protocolo asistencial, el tratamiento inadecuado no explicaría la mortalidad a largo plazo.
Como en estudios anteriores, en la serie de este estudio, la mayor parte de los pacientes (97,6%) estaban sintomáticos en NYHA ≥ II aunque, comparados con los pacientes sin eventos clínicos, la clase funcional de la NYHA careció de significación estadística (p=0,51) para predecir eventos, como se publicó en otros estudios30,31. Además, se han evaluado varios factores de riesgo para estratificar el riesgo de eventos cardiovasculares en los pacientes con una IT importante. La presencia de alteraciones en las enzimas hepáticas, la cirrosis o altas concentraciones de bilirrubina se han asociado con aumento de la mortalidad en el tratamiento quirúrgico de la válvula tricúspide6,32. Además, la presencia de anemia se ha relacionado con mala evolución clínica21. Varios mecanismos se han asociado con la anemia de los pacientes con una IT importante, como la baja perfusión renal, la mala absorción, las carencias nutritivas, la hemodilución y el hiperesplenismo (debido a congestión venosa sistémica)21. En este estudio, la hemoglobina y las enzimas hepáticas no tuvieron repercusiones en el pronóstico. La explicación de esto podría ser que en este estudio se evaluó a una población quirúrgica, de modo que los pacientes no se hallaban en una fase terminal de la enfermedad. El papel de la hipertensión arterial pulmonar en los pacientes que se someten a una intervención quirúrgica del VD es controvertida, ya que en algunos estudios se muestra que estos pacientes no recuperan la función del VD, mientras que en otros se observan resultados contrarios3,18. En este estudio, se demostró que la hipertensión arterial pulmonar se asocia con una mayor incidencia de eventos cardiovasculares durante el seguimiento (HR=1,05; p=0,004); no obstante, su papel en la predicción de los eventos está sujeto al grado de dilatación del VD (p=0,395 en el modelo ajustado).
LimitacionesLas principales limitaciones son que se trata de un estudio unicéntrico y con una población pequeña; no obstante, refleja la realidad de esta enfermedad en la que son pocos los pacientes remitidos a intervención quirúrgica (alrededor de un 8% en las series grandes)22 y en su mayor parte en un estadio avanzado de la enfermedad. Sin embargo, este estudio también tiene varias ventajas, como su naturaleza prospectiva y el hecho de que se estudió a todos los pacientes siguiendo un protocolo homogéneo y exhaustivo que incluyó todos los datos clínicos y las técnicas de diagnóstico por la imagen recomendadas por las sociedades científicas. Otra limitación de este estudio es que se remitió a los pacientes a intervención quirúrgica en distintas fases de su enfermedad y no se les realizaron pruebas funcionales a excepción de la NYHA; no obstante, las guías vigentes no recomiendan umbrales específicos para la realización de estas pruebas. En este sentido, este estudio proporciona una aproximación al VTDVDi a partir del cual el riesgo de complicaciones cardiovasculares mayores durante el seguimiento tras la intervención es considerablemente más alto. El análisis multivariante puede sesgar los resultados del estudio cuando el tamaño de la muestra es pequeño y el número de eventos es bajo. No obstante, se trata de un estudio observacional y prospectivo, por lo que disminuye la posibilidad del sesgo de selección. Esto, junto con las pocas diferencias entre los grupos con y sin eventos, permitió utilizar muestras más pequeñas para obtener un buen nivel de precisión. Por último, se analizó la insuficiencia tricuspídea recurrente teniendo en cuenta el análisis Doppler cuantitativo (ya que no se hacía sistemáticamente una ecocardiografía transtorácica tridimensional a todos los pacientes).
CONCLUSIONESEn pacientes con IT sola y grave remitidos a reparación quirúrgica de la válvula tricúspide, un VTDVD> 104ml/m2 se asoció con hospitalización por insuficiencia cardiaca del VD y alta mortalidad cardiovascular durante el seguimiento. Estos resultados indican que la reparación quirúrgica o los procedimientos percutáneos deberían hacerse antes de llegar a este umbral para optimizar los resultados y mejorar la calidad de vida de los pacientes.
FINANCIACIÓNEste estudio contó con la financiación parcial de una beca a un proyecto de investigación clínica en cardiología de la Sociedad Española de Cardiología y la Fundación Española del Corazón. No hay ninguna relación con la industria farmacéutica.
CONFLICTO DE INTERESESI. Ferreira-González es editor jefe de Revista Española de Cardiología. Se ha seguido el procedimiento editorial de la Revista para asegurar la gestión imparcial del artículo. Los demás autores confirman que no tienen nada que declarar con respecto a este artículo.
- –
La mortalidad en la IT grave es alta (15-20%) y suele atribuirse a un retraso en la intervención quirúrgica. A pesar de la elevada mortalidad, no se dispone de datos que definan cuál es el mejor predictor cardiovascular para remitir a los pacientes a intervención quirúrgica y mejorar la supervivencia.
- –
Este estudio muestra que el remodelado del VD evaluado mediante RMC es el mejor predictor independiente de eventos cardiovasculares durante el seguimiento de esta población. Además, podría reducirse la supervivencia si se remitiera a los pacientes a intervención quirúrgica antes de alcanzar un VTDVDi de 104ml/m2.
Agradecemos a Christine O’Hara la revisión en inglés.