Hay una amplia evidencia científica de que las pruebas de cardiología nuclear permiten tomar decisiones médicas trascendentes, incluso en casos seleccionados sin información coronariográfica. Sin embargo, estas técnicas no son utilizadas por todos los clínicos. La información que aporta la gated-SPECT es realmente útil, en especial en pacientes de riesgo intermedio, y su rentabilidad clínica en la toma de decisiones terapéuticas ha sido ampliamente demostrada. En nuestro país, no obstante, todavía hay servicios de cardiología en los que no se incluye la gated-SPECT en el tratamiento sistemático de los pacientes con cardiopatía isquémica crónica. En esta revisión se comenta la literatura científica disponible relativa al pronóstico de la enfermedad coronaria crónica mediante gated-SPECT de perfusión miocárdica y se resumen, a modo de tabla, los datos objetivos, cualitativos y cuantitativos más importantes para la catalogación de los pacientes en riesgo bajo, intermedio o alto.
Palabras clave
fracción de eyección
diferencia entre SSS y SRS
suma de puntuación del defecto en reposo
suma de puntuación del defecto en estrés
ventrículo izquierdo
volumen telediastólico
volumen telesistólico
Los parámetros combinados de perfusión y función que aporta la gated-SPECT permiten mejorar significativamente la exactitud diagnóstica y pronóstica en los pacientes con cardiopatía isquémica1. Además, el elevado rendimiento clínico de la prueba, su escaso riesgo, la facilidad de repetición, el relativo bajo coste y la corta curva de aprendizaje confieren a la gated-SPECT de perfusión miocárdica unas características inmejorables.
Aunque la imagen de perfusión miocárdica es muy adecuada para detectar la región más isquémica, no loes tanto para identificar todas las estenosis coronarias. Por ello, la gated-SPECT tiene muchas veces más interés para el pronóstico y la detección del vaso culpable que para el diagnóstico.
En las últimas décadas, la mortalidad por cardiopatía isquémica ha disminuido significativamente en España2 y en el resto del mundo occidental, debido a los progresos diagnósticos y terapéuticos. La detección de la enfermedad, la valoración de su extensión y gravedad mediante SPECT es más útil en la estratificación de riesgo que los datos clínicos y/o electrocardiográficos3. Actualmente se considera que la SPECT es una de las mejores técnicas para identificar pacientes con riesgo aumentado de complicaciones y a alguno de sus parámetros, como potentes predictores de riesgo, incluso mejores que los derivados de un cateterismo programado en pacientes ambulatorios4.
Según Candell et al5, las indicaciones para estratificar el riesgo en la cardiopatía isquémica diagnosticada o para decidir entre tratamiento médico o revascularizador, constituyen el 60% de todas las indicaciones del medio hospitalario. Este porcentaje incluso ha aumentado en los últimos años. En el ámbito ambulatorio, un resultado normal de un estudio de perfusión de esfuerzo es altamente predictivo de buen pronóstico, incluso en pacientes con enfermedad coronaria conocida6–9, con una incidencia anual de complicaciones muy baja, similar a la población general3.
La importancia de la gated-SPECT en las decisiones clínicas para decidir entre un tratamiento médico o revascularizador parece confirmarse en un estudio retrospectivo sobre 10.627 pacientes10. La mortalidad fue menor cuando se indicaba tratamiento médico en pacientes con estudio normal o levemente patológico, frente a una reducción significativa de muerte cardiaca tras revascularización coronaria en los pacientes con SPECT moderada o gravemente anormal.
La función sistólica del ventrículo izquierdo, expresión del tamaño de la necrosis, y la extensión e intensidad de la isquemia son los factores pronósticos fundamentales en los pacientes con enfermedad coronaria11; la fracción de eyección (FE) lo será prioritariamente en pacientes con infarto de miocardio previo, y la isquemia miocárdica, en los que no lo han presentado o éste ha sido de pequeña magnitud, lo cual es cada vez más frecuente ante los avances en tratamiento fibrinolítico y revascularización precoz.
La mortalidad se incrementa progresivamente a medida que disminuye la FE. Una baja FE en reposo es el indicador más grave de alto riesgo de muerte, pero más aun si la isquemia miocárdica está presente. Es lógico deducir que la gated-SPECT, al informar simultáneamente sobre ambos parámetros, incremente el valor pronóstico, tanto de la prueba de esfuerzo convencional, en los pacientes aparentemente de menor riesgo, como de la coronariografía en los de mayor riesgo con o sin infarto de miocardio previo.
La FE obtenida durante el ejercicio también refleja la gravedad de la enfermedad y ofrece información pronóstica adicional. Cuando la FE aumenta durante el esfuerzo, la supervivencia a los 3 años es claramente mejor12. Su valor absoluto en el ejercicio máximo se correlaciona con la supervivencia en los 5 años siguientes13. En cualquier grupo de pacientes, aunque se encuentren poco sintomáticos e incluso con una FE normal en reposo, el pronóstico es peor si la FE es baja en el ejercicio máximo o disminuye durante el esfuerzo14,15.
Las variables combinadas son más efectivas en la estratificación de riesgo que las variables aisladas. En la predicción de muerte cardiaca e infarto, la FE y el volumen telesistólico (VTS) obtenidos en el postesfuerzo aportan información añadida16 a la gravedad y la extensión del defecto total de perfusión en estrés y a la extensión e intensidad de la isquemia.
Poder obtener información de predictores diferentes para muerte cardiaca e infarto es importante, ya que la mejor prevención del infarto será el tratamiento médico agresivo, mientras que el riesgo de muerte podrá disminuirse en muchos casos con la revascularización17. Aunque la FE es el predictor más potente de mortalidad, la extensión de la isquemia parece el mejor predictor de infarto18.
El valor pronóstico de las variables de perfusión miocárdica se ha incrementado significativamente gracias a la valoración de otros parámetros que incorpora la gated-SPECT y que no expresan directamente perfusión: el comportamiento de la FE al esfuerzo, la dilatación transitoria del ventrículo izquierdo, la captación pulmonar, el engrosamiento sistólico y la motilidad regional.
VARIABLES DE PERFUSIÓNExtensión de la isquemiaLa extensión de la isquemia se analiza visual o cuantitativamente por el número de segmentos con defectos de perfusión reversibles o por su extensión en el mapa polar, expresada en porcentaje afectado respecto al miocardio total o de cada territorio coronario por separado. La presencia de defectos de perfusión extensos, que afectan a más de una región coronaria o a un amplio territorio correspondiente a la descendente anterior, se relaciona con un peor pronóstico19. Ya en 1983 se observó en un análisis multivariable que incluía los datos clínicos, la prueba de esfuerzo y la coronariografía de una serie de 139 pacientes no tratados quirúrgicamente y estudiados con talio-201 planar de esfuerzo7, que el número de segmentos isquémicos (defectos reversibles) era el único factor pronóstico significativo predictivo de muerte cardiaca y/o infarto a 3–5 años en pacientes sin infarto previo, y que la FE angiográfica lo era en pacientes con infarto previo.
La predicción pronóstica por extensión de la isquemia se mantiene con bajo riesgo (< 1%) de complicaciones severas (muerte e infarto) ante una perfusión normal, ya sea con sobrecarga física o farmacológica20, con talio-201 o con tecnecio-99m marcado con tetrofosmina o isonitrilos21, e independientemente de las características clínicas del paciente y de la presencia de una historia de enfermedad coronaria previa1,22. En todos los protocolos, varios hallazgos están asociados con un peor pronóstico23: gran tamaño del defecto (> 20% del ventrículo izquierdo [VI]), gran número de defectos fijos y defectos en más de un territorio arterial coronario.
Intensidad de la isquemiaLa intensidad de la isquemia es también un indicador independiente pronóstico de la gravedad de la enfermedad coronaria9. Se analiza semicuantitativamente mediante una valoración visual de cada región o segmento24. Los pacientes sin defectos o con defectos leves presentan<1% de complicaciones anuales (infarto, muerte cardiaca o necesidad de revascularización), mientras que la probabilidad de estas es doble si hay defectos moderados. Los defectos intensos predicen una mayor incidencia de complicaciones graves en una media de seguimiento de 3,6 años25. En este estudio de Candell et al25 con MIBI, en pacientes no infartados, sólo la presencia de angina en la prueba de esfuerzo y la intensidad de los defectos de perfusión reversibles fueron factores de mal pronóstico. No obstante, aunque las distintas formas de manifestación de la isquemia (sintomática, silente o clandestina) parecen corresponderse con una diferente intensidad o gravedad de ésta, se ha demostrado un pronóstico similar, entre la isquemia clandestina (defecto de perfusión de menor puntuación, sin angina ni depresión significativa del segmento ST) y la isquemia silente (defecto de perfusión de mayor puntuación, isquemia sin angina pero con depresión del segmento ST>1mm). La isquemia sintomática (angina con defectos reversibles) fue predictiva de complicaciones cuando entre ellos se incluyó la necesidad de revascularización.
Cuantificación y pronósticoBasándose en el modelo de segmentación de 17 segmentos26, las puntuaciones SSS (suma de puntuación del defecto en estrés), SRS (suma de puntuación del defecto en reposo) y SSS y SRS' alt='diferencia entre SSS y SRS'>SDS
(diferencia entre SSS y SRS) integran estas 2 variables con poder predictivo independiente (intensidad y extensión) en una sola, semicuantitativa y de fácil utilización, que puede obtenerse de modo automático y que se complementa con el análisis cuantitativo del mapa polar. Estos índices, previamente validados en el modelo de 20 segmentos y con poder predictivo para complicaciones graves24, informan de diferentes aspectos.El SSS, el número de segmentos afectados y el porcentaje de defecto en el mapa polar —todos ellos obtenidos en las imágenes de esfuerzo— expresan la cuantificación del miocardio infartado, isquémico o en riesgo. Para Hachamovitch et al24, el valor medio del SSS para aparición significativa de complicaciones es de 12,7 frente a 2,3 en ausencia de éstas (p=0,001).
El SRS, el número de segmentos con defecto fijo y el porcentaje de defecto en reposo en el mapa polar —todos ellos obtenidos en las imágenes de reposo— traducen la cuantificación del miocardio infartado necrótico no viable y del miocardio hibernado, en caso de estar presente. Su valor de corte fue 2,7, frente a 0,4 para presencia o ausencia de complicaciones, respectivamente (p=0,001).
El SSS y SRS' alt='diferencia entre SSS y SRS'>SDS
(SSS - SRS) y el porcentaje de reversibilidad en el mapa polar indican la presencia de un miocardio isquémico o en riesgo. Su valor de corte fue 9,8, frente a 1,9 para presencia o ausencia de eventos (p=0,001), y fue el mejor predictor de infarto18.Según el porcentaje de afectación del mapa polar en estrés respecto al miocardio total, se clasifica a los pacientes en 4 grupos10: SPECT normal (< 4%), levemente anormal (4-10%), moderadamente anormal (11-20%) y gravemente anormal (> 20%). Siguiendo esta clasificación, en pacientes con cirugía de revascularización coronaria previa frente a tratamiento médico, la segunda SPECT mostró una mejoría discreta de los defectos en ambos grupos de tratamiento, cuando tenían defecto moderado inicial; una mejoría importante si la primera SPECT presentaba defectos extensos, y una ausencia de mejoría en la segunda SPECT cuando los defectos iniciales eran leves10,27. Una extensión>40% del perímetro ventricular es indicativa de enfermedad multivaso o del tronco común28.
VARIABLES FUNCIONALESCaptación pulmonar después del estrésEl incremento de captación pulmonar con talio-201, sobre todo si se valora precozmente después del esfuerzo29, es un importante marcador de disfunción del VI inducida por un incremento de la presión capilar pulmonar en el esfuerzo. Esta captación también se ha observado, con similar valor pronóstico, con MIBI30 (a pesar del retraso de las imágenes), adenosina31 o dipiridamol30. Además, se ha demostrado que la captación pulmonar es un hallazgo adicional indicativo de alto riesgo, que se correlaciona con la presencia de grave enfermedad coronaria y con una mayor severidad y/o extensión de las anomalías de perfusión. La captación pulmonar se valora visualmente en 4 grados (ausente, ligera, moderada o severa, según sea menor, igual o mayor que el miocardio), o cuantitativamente mediante el cociente pulmón/corazón en el esfuerzo. Cada desviación estándar de incremento de este cociente multiplica por 1,5 la probabilidad de complicación, proporcionando una significativa mejoría en la estratificación pronóstica cuando se añade a la clínica, a la prueba de esfuerzo, a la imagen de perfusión y a los volúmenes del VI30. Un cociente>0,5532 indica una disfunción ventricular izquierda relacionada con isquemia importante y es frecuente en pacientes con antecedentes de infarto de miocardio, revascularización coronaria o FE más baja29.
Dilatación isquémica transitoria y aturdimiento después de la sobrecargaLa dilatación transitoria del VI habitualmente se debe a una disfunción isquémica grave, por estenosis de la descendente anterior proximal o enfermedad multivaso con estenosis críticas>90%33. La presencia de esta dilatación transitoria empeora el pronóstico incluso en pacientes con sobrecarga farmacológica, que ya de por sí son más ancianos o están más enfermos (bloqueo de rama izquierda, hipertrofia ventricular izquierda, incapacidad funcional, etc.) aunque con diferentes umbrales de anormalidad34. Se ha indicado que puede ser una«dilatación aparente»causada por una extensa isquemia subendocárdica transitoria, en ausencia de una verdadera dilatación física del VI 29,31,33,35–40. La dilatación transitoria puede observarse cualitativamente o cuando, al valorar el cociente área VI en esfuerzo/reposo, obtenido de modo automático, está aumentado29. Un valor>1,2 indica una estenosis crítica de 2–3 vasos con una sensibilidad del 60% y una especificidad del 95%40. La dilatación transitoria se asocia con un incremento de complicaciones, incluso a pesar de que la imagen de perfusión sea normal36. Posiblemente, en los pacientes en los que la dilatación transitoria se manifieste con alteraciones transitorias de la motilidad regional secundarias al aturdimiento posterior a la sobrecarga37 debería plantearse la posibilidad de una coronariografía.
Comportamiento de la fracción de eyección, el volumen telesistólico y la motilidad regionalLa relación entre la dilatación transitoria del VI con anomalías de la motilidad regional y aturdimiento miocárdico (definido como descenso de la fracción de eyección≥5% postesfuerzo) se confirmó en el estudio de Hung et al34 con dipiridamol. El aturdimiento miocárdico puede producir una depresión prolongada de la FE cuando hay una enfermedad coronaria grave41. En los casos más graves puede prolongarse tanto que persista durante las imágenes de reposo con protocolo esfuerzo/reposo de un solo día, pudiendo encubrirse parcialmente el descenso de la FE. Por este motivo, en algunos pacientes es de gran interés conocer la verdadera FE basal, realizada en otro momento, y así poder evidenciar un mayor grado de aturdimiento miocárdico. No obstante, recientemente se ha descrito que la gated-SPECT de esfuerzo sobreestima respecto a la ecocardiografía el aturdimiento miocárdico global y regional provocado por la isquemia42.
El descenso evidente de la FE durante el esfuerzo (≥ 5%) se ha relacionado significativamente con una mayor probabilidad de enfermedad multivaso43. La frecuencia de complicaciones después de una gated-SPECT, en un grupo de 3.207 pacientes no revascularizados precozmente44, aumentó del 5,1% anual al 7,4% cuando se asociaron alteraciones de la motilidad regional con perfusión anormal, y del 1,6 al 1,8% (p<0,001) cuando se asociaron con una perfusión normal.
Una FE postesfuerzo anormal (< 45%) o un volumen telesistólico (VTS) alto (> 70ml) se asocian con una tasa de mortalidad cardiaca anual de 9,2 y el 8,2%, respectivamente16, incluso con isquemia leve o moderada en las imágenes de perfusión. Por el contrario, con FE y VTS normales (> 45% y≤70ml), las tasas anuales son<1% y<1,2%, respectivamente, incluso coexistiendo con anormalidades importantes de perfusión. Los portadores de bloqueo de rama izquierda presentan también un riesgo aumentado de complicaciones45, pero con un volumen telediastólico (VTD)>160ml, un VTS>100ml o una FE<35%.
Complemento con criterios de riesgo en la prueba de esfuerzo convencionalExcepcionalmente, un estudio de perfusión miocárdica sin defectos segmentarios isquémicos puede corresponder a una enfermedad coronaria homogénea de 3 vasos. Estos pacientes suelen presentar otros hallazgos: una evidente positividad eléctrica en el electrocardiograma de esfuerzo, un comportamiento anómalo de la presión arterial, antecedentes de diabetes mellitus o edad avanzada y criterios de mal pronóstico en la gated-SPECT (dilatación transitoria del VI, descenso de la FE, captación pulmonar y alteraciones de la motilidad global o regional). Por ello, es poco frecuente que una enfermedad grave y de mal pronóstico, del tronco común o multivaso, pase desapercibida como un falso negativo28,46,47
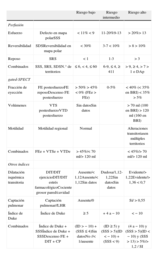
En la tabla 1 se propone, con carácter orientativo, una clasificación de la cardiopatía isquémica crónica en valores de riesgo según variables de la gated-SPECT y de la prueba de esfuerzo, que puede variar ligeramente dependiendo del subgrupo de edad, el sexo, la presencia de infarto o revascularización previas, diabetes y bloqueo de rama izquierda.
Clasificación de la cardiopatía isquémica crónica en grados de riesgo según variables de la gated-SPECT y la prueba de esfuerzo
| Riesgo bajo | Riesgo intermedio | Riesgo alto | ||
| Perfusión | ||||
| Esfuerzo | Defecto en mapa polarSSS | < 11%<9 | 11-20%9-13 | > 20%>13 |
| Reversibilidad | SDSReversibilidad en mapa polar | < 30% | 3-7<10% | > 8>10% |
| Reposo | SRS | <1 | 1-3 | >3 |
| Combinados | SSS, SRS, SSS y SRS' alt='diferencia entre SSS y SRS'>SDSN.° de territorios | ≤ 6, < 4, ≤ 60 | 6-9, ≤ 4, ≥ 411 | > 9, ≥ 4, > 7>1 o DAp |
| gated-SPECT | ||||
| Fracción de eyección | FE postesfuerzoFE reposoDescenso FE postesfuerzo | > 50%>45%<0% (FEe>FEr) | 0-5% | < 40% (< 35% en BRI)<35%>5% |
| Volúmenes | VTS postesfuerzoVTD postesfuerzo | Sin datosSin datos | > 70ml (100 en BRI)>120ml (160 en BRI) | |
| Motilidad | Motilidad regional | Normal | Alteraciones transitoriasen múltiples territorios | |
| Combinados | FEe+VTSe+VTDe | > 45%/< 70ml/> 120ml | < 45%/> 70ml/> 120ml | |
| Otros índices | ||||
| Dilatación isquémica transitoria | DIT/DIT ejercicioDIT/DIT estrés farmacológicoCociente grosor pared/cavidad | Ausente/< 1,12Ausente/< 1,12Sin datos | Dudosa/1,12-1,22Sin datosSin datos | Evidente/> 1,22Evidente/> 1,36<0,7 |
| Captación pulmonar | Captación pulmonar//LHR | Ausente/0 | Sí/ > 0,55 | |
| Índice de Duke | Índice de Duke | ≥ 5 | +4 a −10 | < −10 |
| Combinados | Índice de Duke+SSSÍndice de Duke+SSSDescenso FE+DIT+CP | (ID>−10)+(SSS≤4)Sin datosNo //< 1/ausente | (ID≥5) y (SSS>5)(ID<−10)+(SSS<9) | (4 a −10) y (SSS>5)(ID<−10) y (SSS>13)>5%/> 1,2 / SI |
BRI: bloqueo de rama izquierda; CP: captación pulmonar; DAp: descendente anterior proximal; DIT: dilatación isquémica transitoria; FE: fracción de eyección; ID: índice de Duke; r: reposo; SSS y SRS' alt='diferencia entre SSS y SRS'>SDS: diferencia entre SRS y SSS; SRS: suma de puntuación del defecto en reposo; SSS: suma de puntuación del defecto en estrés; VTS: volumen telesistólico; VTD: volumen telediastólico; VI TIDr: cociente área ventrículo izquierdo en la sobrecarga/área del ventrículo izquierdo en reposo; LHR: cociente pulmón/corazón en la sobrecarga.
Hachamovich et al48 demostraron el beneficio de una SPECT esfuerzo/reposo como estrategia no invasiva para predecir complicaciones dentro de los 2 años siguientes a su realización, en 5.183 pacientes con cardiopatía isquémica conocida. Presentaron una probabilidad de muerte cardiaca e infarto anual de 0,3 y 0,5, respectivamente, para una SPECT normal, de 0,8 y 2,7 para una SPECT ligeramente anormal, de 2,3 y 2,9 si resultaba moderadamente patológica, o de 2,9 y 4,2 si lo era severamente.
Cuando se estudian subgrupos clínicos, estos datos presentan variaciones significativas.
Pacientes con infarto previoInfarto agudo de miocardio con elevación del segmento STLa gated-SPECT aporta varios parámetros pronósticos1 (FE, tamaño del infarto, miocardio residual en riesgo y extensión de la isquemia) y diagnósticos con importantes implicaciones pronósticas (lesión culpable y significación hemodinámica de lesiones moderadas). Spinelly et al49 estudiaron a pacientes de alto riesgo con infarto reciente no complicado, en los que se realizó un tratamiento trombolítico antes del alta, mediante gated-SPECT con dobutamina. La función ventricular, la isquemia (SSS y SRS' alt='diferencia entre SSS y SRS'>SDS
), la perfusión de reposo (SRS) y la motilidad regional agregaban secuencialmente información para estratificar riesgo. En ausencia de isquemia las complicaciones anuales fueron de un 11%, con una isquemia ligera de un 18% y con isquemia moderada o grave de un 40% (p<0,05). Candell et al50 observaron con gated-SPECT con tetrofosmina y ecocardiografía de esfuerzo que una extensión de la isquemia en el mapa polar>15% era la única variable predictiva de infarto al año. Aunque ambas pruebas predijeron la insuficiencia cardiaca, sólo la gated-SPECT predijo complicaciones isquémicas. Mahmarian et al51 también encontraron, con talio-201 y adenosina, una relación entre las complicaciones totales (muerte y reinfarto) con el tamaño del defecto, la extensión de la isquemia y la FE. Diez años después publicaron un estudio multicéntrico52 en el que confirmaron, con sestamibi, los mismos datos.Con vistas a la indicación de cateterismo en estos pacientes se han establecido 4 categorías pronósticas de riesgo, sobre la base de la SSS sobre 20 segmentos y otras 4 categorías combinando la isquemia (SSS y SRS' alt='diferencia entre SSS y SRS'>SDS
) con la extensión de la cicatriz (SRS), con diferencias significativas de mortalidad anual53. Así, la mortalidad era del 0,4% para una SSS<4; del 0,9% para una SSS de 4-8; del 1,7% para una SSS de 9–13; del 3,5% para una SSS>13; del 0,6% para una SRS<4+SDS≤6; del 1,6% para una SRS<4+isquemia moderada/severa (SDS>6); del 3,7% para una SRS≥4+isquemia moderada (SSS y SRS' alt='diferencia entre SSS y SRS'>SDS 6–9), y del 6,6% para una SRS≥4+isquemia severa (SDS>9).Infarto de miocardio sin elevación del segmento ST o en la angina inestable de riesgo intermedio o bajoUna vez estabilizado el cuadro, la gated-SPECT identifica y puede cuantificar la isquemia inducible, la FE, el vaso causante y la isquemia a distancia, y es altamente predictiva de futuras complicaciones. Los mejores predictores son la presencia y la extensión de defectos de perfusión reversibles, pero también es predictiva la extensión de los defectos fijos54. La estratificación de riesgo debe realizarse antes del alta hospitalaria, dado que el 80% de las complicaciones postinfarto ocurre en el primer mes.
Pacientes sin infarto previoEn pacientes con FE basal normal el criterio fundamental para estratificación de riesgo es la intensidad y la extensión de la isquemia. Dado que la revascularización coronaria tiene un riesgo>1%, no debería indicarse con fines pronósticos en grupos de bajo riesgo (mortalidad<1%)55–57. La SPECT de perfusión miocárdica reduce significativamente el subgrupo de pacientes de riesgo intermedio con el índice de Duke24, dado que un resultado severamente anormal desplaza al 14% de ellos al grupo de alto riesgo, con una mortalidad anual del 8,9%, lo que aconseja la realización de coronariografía, mientras que el 70%, con una SPECT normal, puede pasar a formar parte del grupo de bajo riesgo con complicaciones<0,4, por lo que pueden ser controlados con tratamiento conservador. Sólo un 16% del grupo inicialmente de riesgo intermedio continuará en el mismo grupo, que queda así reducido al 9% del total.
En el metaanálisis de Navare et al20 con 14.918 pacientes de 24 estudios20 se compararon el pronóstico (muerte o infarto) de la sobrecarga farmacológica con el de ejercicio, tras excluir a los pacientes con infarto previo o revascularizados. La potencia predictiva de ambas pruebas fue similar, aunque las complicaciones fueron significativamente más numerosos en pacientes con sobrecarga farmacológica: el 1,78 frente al 0,65% para la SPECT normal y el 9,98 frente al 4,3% para la SPECT anormal. Los pacientes en los que se aplicó una sobrecarga farmacológica tenían una mayor prevalencia de factores de peor pronóstico y el análisis de regresión reveló que la capacidad de ejercicio es el predictor independiente más importante de complicaciones cardiacas.
En pacientes con dolor atípico, elevación de troponinas y bajo/intermedio riesgo de síndrome coronario agudo, una SPECT reposo/esfuerzo normal se traduce en un buen pronóstico a los 6 meses. La frecuencia de complicaciones cardiacas se triplica si el resultado es anormal, y éste es un predictor independiente de muerte58.
Pacientes con angina crónica estableEn un análisis multivariable59 con SPECT tetrofosmina y dobutamina o ejercicio se confirmó que la extensión de los defectos de perfusión reversibles era uno de los determinantes mayores de mortalidad, junto con la edad, el sexo masculino, la diabetes, la insuficiencia cardiaca, el tabaquismo y los defectos fijos. En 6 años de seguimiento la mortalidad fue del 1,5% en los casos con perfusión normal frente al 4,5% en los casos con perfusión anormal. La distribución multivaso de los defectos se asoció con una mortalidad del 5,1%, frente a una mortalidad del 3,7% en los casos con defectos en un solo territorio.
A pesar de los progresos en la ecocardiografía de estrés, la gated-SPECT de perfusión miocárdica parece más indicada en algunos grupos específicos de pacientes, al tener mayor valor pronóstico60: pacientes con alto riesgo clínico pero índice de Duke de bajo riesgo, pacientes con marcapasos ventriculares, pacientes con anormalidades no específicas en el ST-T en el electrocardiograma de reposo y en pacientes de edad avanzada.
Las guías clínicas de la ACC/AHA/ACP-ASIM de 199922, actualizadas en 200261 por la ACC/AHA, recomiendan la gated-SPECT como test inicial para la estratificación del riesgo de pacientes con angina crónica estable con ECG de reposo anormal, con ritmo de marcapasos ventricular o que tomen digoxina. También se recomienda la SPECT para evaluar el significado funcional de lesiones coronarias intermedias.
Pacientes asintomáticosNo se han encontrado pruebas científicas suficientes para una indicación pronóstica de la gated-SPECT en este subgrupo de pacientes, generalmente de bajo riesgo y que pueden estratificarse con prueba de esfuerzo convencional. Sólo los casos en los que el resultado de ésta no fuera concluyente o el índice de Duke resultara de riesgo intermedio o alto podrían beneficiase de la gated-SPECT61.
Se podría recomendar la SPECT de esfuerzo o sobrecarga farmacológica para la estratificación de riesgo en pacientes con posible isquemia miocárdica sospechada en el control ECG ambulatorio o con severa calcificación coronaria en la angiotomografía computarizada pero con anomalías asociadas del ECG basal, ya sea por síndrome de preexcitación, descenso del segmento ST>1mm en ECG de reposo, ritmo de marcapasos ventricular o bloqueo de rama izquierda.
Seguimiento: el«período de garantía»Con frecuencia se realiza una prueba de esfuerzo de seguimiento anual, con o sin imagen, en pacientes con enfermedad coronaria crónica estable, pero su valor no ha sido comprobado. Las guías de angina estable las desaconsejan como prueba sistemática, particularmente en pacientes de bajo riesgo. Después de una revascularización coronaria, la frecuencia de complicaciones en los primeros 5 años también es muy baja. Datos observacionales62 de seguimiento a pacientes con SPECT normal muestran que múltiples factores clínicos añaden valor pronóstico y pueden alterar el momento apropiado de la repetición de la prueba. El tipo de estrés, la presencia de diabetes, una historia de enfermedad coronaria conocida, el sexo masculino y la edad avanzada son factores predictivos de mayor probabilidad de complicaciones. El subgrupo de mujeres diabéticas también presenta un peor pronóstico. En cualquier caso, los pacientes de mayor riesgo a pesar de una SPECT normal presentan una probabilidad anual de complicaciones graves del 1,4-1,8%. A partir de estos datos se deduce un«período de garantía»que comprende desde el momento del estudio de perfusión normal, en pacientes sin historia de infarto o revascularización, hasta el momento en que los pacientes alcancen una probabilidad de un 1% de riesgo de eventos cardiacos graves. En pacientes de edad avanzada con historia de enfermedad coronaria, el«período de garantía»es de 12 meses, por lo que se aconseja la realización de una prueba anual en estos pacientes. Por el contrario, en ausencia de diabetes y sin historia de enfermedad coronaria, un estudio de perfusión de esfuerzo normal en un paciente de unos 50 años tendría un período de garantía de al menos 9 años, lo que indica que la práctica clínica habitual de estudios más frecuentes es excesiva. Estos interesantes hallazgos deberán incorporarse probablemente en próximas actualizaciones de las guías de angina estable60.
Pronóstico de la gated-SPECT en cardiopatía isquémica crónica en algunos grupos especialesDespués de la revascularización y ante la persistencia o reaparición de la sintomatologíaEn estos pacientes, la prueba de esfuerzo convencional no aporta información importante y la coronariografía puede no ser concluyente por la complejidad de la anatomía coronaria posrevascularización. En los que permanecen asintomáticos no hay beneficio de la SPECT sistemática y sólo estaría indicada una vez transcurrido el«período de garantía», que en estos pacientes es de 5 años tras la revascularización63. Otro aspecto diferente sería documentar la mejoría de la perfusión en áreas de isquemia en reposo después de la cirugía de revascularización64. Adachi et al65 observaron que, en pacientes con infarto previo y revascularizados, la presencia de necrosis sin isquemia predijo la ausencia de necesidad de nueva revascularización a los 100 meses de seguimiento. Por el contrario, el 50% de los pacientes con isquemia requirió una nueva revascularización. Elhendey et al66, con tetrofosmina esfuerzo o dobutamina, encontraron complicaciones graves (muerte, infarto, revascularización) a los 4,5 años de una angioplastia coronaria o una cirugía de revascularización en un 19% de los pacientes con defectos de perfusión reversibles y en un 4% en los pacientes sin ellos, independientemente de la presencia de angina antes de la prueba (que no fue predictiva), lo que mejoraba el pronóstico aportado por los datos clínicos. Además, se recomendaba no diferir más de este tiempo un nuevo estudio en pacientes asintomáticos revascularizados66.
En la isquemia miocárdica silenteEn esta situación, la gated-SPECT es predictiva de complicaciones en voluntarios«sanos»67, si se incluye entre las complicaciones la necesidad de revascularización, y en la isquemia clandestina6,25. Dentro de este grupo estaría la diabetes mellitus, sobre todo insulinodependiente, y con mayor valor en las mujeres68, así como los pacientes con bloqueo de rama izquierda45 y factores de riesgo coronario importantes o síntomas atípicos. Este apartado incluiría también el preoperatorio de cirugía no cardiaca69 (con un valor predictivo negativo del 99%) y los candidatos a trasplante renal, pancreático70 o hepático.
En mujeres de edad avanzada y con síntomas atípicosHa demostrado tener un valor pronóstico especialmente alto62,71.
En pacientes con dolor torácico y con anomalías de la repolarización importantesPor hipertrofia ventricular izquierda en la hipertensión arterial, preexcitación o bajo tratamiento con fármacos como la digoxina.
En el asma bronquial y en pacientes seleccionados para SPECT con dobutaminaLa respuesta del ECG y de la frecuencia cardiaca a la dobutamina tiene valor pronóstico y debe incorporarse a la interpretación de la imagen para maximizar la estratificación de riesgo72.
CONCLUSIONESPor todo lo expuesto, puede concluirse que en el estudio pronóstico de la cardiopatía isquémica crónica la gated-SPECT de perfusión miocárdica es una gran herramienta para el tratamiento de los pacientes, como queda avalado por la amplia evidencia bibliográfica disponible. La objetividad de los datos que aporta permite determinar el tratamiento más adecuado e individualizado en todos los subgrupos de pacientes. La reproducibilidad de la técnica facilita la realización de estudios de seguimiento, incluso desde distintos centros y utilizando distintos protocolos, lo que convierte a esta técnica en una de los mejores métodos para el estudio pronóstico de la enfermedad coronaria.