INTRODUCCIÓN Y OBJETIVOS: La prueba de esfuerzo de bajo riesgo se relaciona con un buen pronóstico en los pacientes con cardiopatía isquémica crónica. Sin embargo, apenas existen estudios que hayan evaluado prospectivamente el pronóstico de los pacientes con angina inestable controlada con tratamiento médico y que realizan una prueba de esfuerzo de bajo riesgo. Nuestro objetivo fue determinar el pronóstico de esta población específica y si existen variables clínicas o derivadas de la ergometría predictoras de eventos.
MÉTODOS: Se diseñó un protocolo de estudio prospectivo, según el cual se evaluaron 175 pacientes con diagnóstico de angina inestable, a los que se realizó una prueba de esfuerzo para la valoración pronóstica antes del alta hospitalaria durante un período de dos años. La población de estudio estaba constituida por los 93 pacientes (un 82% de varones; edad: 60 ± 9 años) que no presentaron criterios de alto riesgo previamente definidos en la prueba de esfuerzo y fueron dados de alta con tratamiento farmacológico.
RESULTADOS: Tras un período de seguimiento medio de 13 ± 6 meses, 30 pacientes (32%) padecieron algún evento: 2 muertes (2%); 6 infarto agudo de miocardio no mortal (6%); 18 angina inestable (19%) y 4 revascularización (4%). En el análisis multivariado, sólo la angina durante la prueba de esfuerzo fue un predictor independiente de eventos ( odds ratio: 2,35; intervalo de confianza del 95%: 1,22-4,50; p = 0,01).
CONCLUSIÓN: Los pacientes con angina inestable que realizan una ergometría de bajo riesgo y son dados de alta con tratamiento médico tienen una incidencia de eventos relativamente elevada durante el primer año. En esta población específica, la presencia de angina durante la ergometría se asocia a una evolución desfavorable.
Palabras clave
Angina inestable
Enfermedad coronaria
Pronóstico
INTRODUCCIÓN
La prueba de esfuerzo (PE) convencional continúa siendo la exploración no invasiva más utilizada para demostrar la presencia de isquemia inducible y, por tanto, para definir el pronóstico de los pacientes con enfermedad coronaria. La mayor parte de los estudios que han demostrado la utilidad pronóstica de la PE se han realizado en poblaciones de pacientes con cardiopatía isquémica crónica estable 1-3 o tras un infarto agudo de miocardio 3.
La información sobre la utilidad de la PE en la valoración del pronóstico de los pacientes con angina inestable (AI) que se ha controlado con tratamiento farmacológico es limitada 4,5. Por ello, para la toma de decisiones clínicas en esta población específica se recomienda considerar criterios de riesgo de la PE que han sido validados exclusivamente en pacientes con cardiopatía isquémica crónica 6,7, no con AI. Los pacientes con una prueba positiva de alto riesgo deben ser remitidos para la realización de coronariografía y valoración de la posibilidad de revascularización, mientras que en aquellos que son capaces de realizar una PE sin evidencia de isquemia severa se acepta, en la mayoría de los casos, una actitud conservadora 6,8,9. Sin embargo, se ha descrito una elevada incidencia de eventos durante el seguimiento a largo plazo de pacientes con AI que han sido controlados con tratamiento farmacológico y que son capaces de realizar una PE convencional sin evidencia de isquemia, en los que, por tanto, se sigue una pauta de tratamiento no invasivo 10. Esta circunstancia sugiere que una PE de bajo riesgo puede no implicar un pronóstico favorable en cierto grupo de pacientes con AI.
Los objetivos de este estudio fueron: a) determinar el pronóstico de los pacientes con AI primaria estabilizada con tratamiento farmacológico en los que se realiza una PE convencional que no demuestra criterios de alto riesgo, y b) determinar si existen variables clínicas o derivadas de la PE que se correlacionen con la presencia de eventos en el seguimiento de estos pacientes. MÉTODOS
Selección de pacientes
Los pacientes fueron seleccionados, según un protocolo de estudio prospectivo, entre todos aquellos ingresados en la Unidad de Cardiología de nuestro hospital, entre enero de 1997 y diciembre de 1998, con el diagnóstico de AI primaria, cuyo estado clínico se había estabilizado con tratamiento farmacológico (al menos 72 h sin nuevos episodios de dolor torácico), a los que se realizó una PE para su valoración pronóstica antes del alta hospitalaria. Dado el objetivo del estudio, no se consideraron los pacientes con alteraciones basales del ECG de reposo asociadas a una respuesta eléctrica no interpretable para isquemia en la PE (bloqueo de rama izquierda, ritmo de marcapasos, preexcitación, descenso del segmento ST >= 1 mm o menor en presencia de tratamiento con digoxina u otros criterios de hipertrofia ventricular izquierda) 3, y se excluyeron los pacientes incapaces de completar el estadio II del protocolo de Bruce en ausencia de isquemia inducible.
Durante el período de estudio se realizó una PE a 183 pacientes con el diagnóstico de AI estabilizada con tratamiento médico. Ocho pacientes (4%) fueron incapaces de completar el estadio II del protocolo de Bruce y la prueba fue negativa, por lo que fueron excluidos.
Definiciones
De acuerdo con la clasificación de Braunwald 11, se consideró AI a aquella de reciente inicio o progresiva; la angina de reposo subaguda, y la angina de reposo aguda. Sólo se incluyeron pacientes con AI primaria, de modo que no se consideraron los pacientes con AI secundaria o angina postinfarto. Tampoco se incluyó a ningún paciente con infarto agudo de miocardio sin onda Q.
Prueba de esfuerzo
La PE se realizó en cinta sin fin siguiendo el protocolo de Bruce 12 estándar, empleando un sistema computarizado de electrocardiografía de esfuerzo comercialmente disponible. En todos los pacientes se mantuvo el tratamiento farmacológico prescrito. Se midió la presión arterial antes del inicio de la prueba y, con posterioridad, cada dos minutos durante el esfuerzo máximo y siempre que se consideró clínicamente indicado. Se obtuvo un ECG de 12 derivaciones antes de iniciar el ejercicio y, posteriormente, a intervalos de 3 minutos durante el ejercicio (al final de cada estadio del protocolo de Bruce), durante el máximo esfuerzo, a intervalos de 1 min durante al menos los primeros 5 min de la fase de recuperación y siempre que se consideró clínicamente indicado. Durante toda la prueba se monitorizaron de forma continua 3 derivaciones del ECG y la derivación con máxima desviación del ST.
Se consideraron criterios de finalización de la prueba: a) el agotamiento de la capacidad física o alcanzar la frecuencia cardíaca máxima prevista según la edad (220 - edad); b) descenso de la presión arterial sistólica por debajo de la basal o respuesta hipertensiva (presión arterial sistólica >= 230 mmHg o diastólica >= 130 mmHg); c) ataxia, mareo o presíncope, disnea intensa, claudicación severa, evidencia de hipoperfusión periférica (cianosis o palidez); d) arritmias ventriculares (extrasístoles ventriculares frecuentes, complejos multiformes o rachas de tres latidos); e) dificultades técnicas en la monitorización del ECG o la presión arterial; f) angina de pecho intensa; g) descenso del ST >= 3 mm, y h) a petición del paciente.
Se consideraron criterios de positividad de la prueba: a) la presencia de angina (prueba positiva clínica), y b) el descenso del segmento ST >= 1 mm, o el ascenso del segmento ST >= 1 mm en derivaciones sin onda Q patológica (diferentes de aVR), medido a 80 ms del punto J (prueba positiva eléctrica). Se admitió la lectura de la desviación del segmento ST efectuada por el sistema computarizado de electrocardiografía de esfuerzo, confirmada por un cardiólogo experto en la técnica.
Se consideraron criterios de alto riesgo de la PE los siguientes: a) respuesta clínica y/o eléctrica positiva con una frecuencia cardíaca < 120 lat/min o durante los 2 primeros estadios del protocolo de Bruce; b) el descenso del ST >= 1 mm que persiste >= 6 min en fase de recuperación o presente en >= 5 derivaciones; c) el descenso del ST >= 2 mm a cualquier nivel de ejercicio; d) la elevación del segmento ST (excepto aVR) en derivaciones sin onda Q; e) el descenso sostenido de la presión arterial sistólica durante el ejercicio progresivo, y f) la presencia de taquicardia ventricular.
Manejo del paciente
A todos los pacientes se les realizó de manera rutinaria un ECG de 12 derivaciones en el momento del ingreso hospitalario, durante e inmediatamente después de cada episodio de dolor torácico, a las 24 h del ingreso y antes de la realización de la PE. También de forma rutinaria se obtuvieron muestras de sangre para la determinación de la creatincinasa plasmática y su isoenzima MB cada 8 h durante las primeras 24 h. Los pacientes recibieron tratamiento con nitratos (tópicos, orales o nitroglicerina intravenosa), calcioantagonistas, betabloqueantes, aspirina o heparina (intravenosa o de bajo peso molecular), a juicio del cardiólogo clínico responsable del paciente. En los pacientes que recibieron heparina intravenosa, el tratamiento se monitorizó mediante la determinación de la actividad parcial de tromboplastina, persiguiendo un valor de 1,5-2,5 veces el control. En todos los casos se realizó la PE tras permanecer >= 72 h sin nuevos episodios de dolor torácico
Se definió prospectivamente la estrategia de manejo definitivo, de modo que los pacientes con una PE de alto riesgo (presencia de alguno de los criterios de alto riesgo) fueron remitidos para coronariografía y valoración de revascularización y los pacientes que completaron una PE de bajo riesgo (ausencia de todos los criterios de alto riesgo) fueron dados de alta con tratamiento médico.
De los 175 pacientes que realizaron la PE, en 79 (45%) resultó de alto riesgo y en 96 (55%) de bajo riesgo. En 78 pacientes con PE de alto riesgo se realizó coronariografía. Ésta no se realizó en ninguno de los 96 pacientes con ergometría de bajo riesgo.
Seguimiento de los pacientes
Los pacientes que realizaron una PE de bajo riesgo fueron evaluados en las consultas ambulatorias de la Unidad de Cardiología de nuestro centro, a los 3 meses tras el alta hospitalaria, y posteriormente, con una periodicidad semestral. En los pacientes que no acudieron a la cita se efectuó el seguimiento mediante entrevista telefónica realizada por personal médico.
Se consideraron eventos en el seguimiento, en orden decreciente de gravedad, la presencia de muerte de origen cardíaco, infarto agudo de miocardio no mortal, ingreso hospitalario por angina inestable y la revascularización por angina de esfuerzo estable de clase funcional III o IV de la Sociedad Cardiovascular Canadiense. Se consideró muerte de origen cardíaco la que sucedió en ausencia de diagnóstico clínico o patológico de una causa extracardíaca. La presencia de infarto agudo de miocardio o de angina inestable se confirmó en todos los casos mediante los informes clínicos hospitalarios correspondientes. En los pacientes con más de un evento sólo se consideró el más grave.
Tres de los 96 pacientes (3%) con PE de bajo riesgo fueron perdidos para el seguimiento, por lo que la población de estudio en este grupo estuvo finalmente confirmada por 93 pacientes.
Variables de estudio
Se registraron prospectivamente las siguientes variables:
1. Clínicas: edad, sexo, hábito tabáquico, hipertensión arterial, hipercolesterolemia, diabetes mellitus, historia anterior de cardiopatía isquémica (angina crónica estable o infarto de miocardio antiguo), revascularización previa (angioplastia coronaria percutánea o cirugía de derivación aortocoronaria), enfermedad vascular arterial periférica, forma de presentación de la angina inestable (reciente inicio/progresiva o de reposo) y presencia de episodios de angina recurrente durante la hospitalización.
2. Electrocardiográficas: presencia de cambios objetivos de la repolarización en el ECG, presencia de ECG preergometría anormal.
3. Ergométricas: duración de la prueba (minutos de ejercicio), doble producto (presión arterial sistólica × frecuencia cardíaca) máximo, porcentaje de la frecuencia cardíaca máxima prevista alcanzado, resultado de la PE (positivo o negativo), respuesta clínica, respuesta eléctrica e índice de Duke. El índice de Duke se calculó según la fórmula:
duración del ejercicio en minutos - (5 × máxima desviación neta del segmento ST durante o después del ejercicio, en mm) - (4 × índice de angina).
El índice de angina se consideró 0 si el paciente no tuvo angina durante la prueba, 1 si el paciente tuvo angina que no limitó el ejercicio, y 2 si la angina fue la causa de detener la prueba 13.
Análisis estadístico
Las variables cuantitativas se expresan como media ± desviación estándar. Las comparaciones univariadas entre grupos de variables continuas se realizaron aplicando el test de la t de Student para muestras no relacionadas o el test U de Mann-Whitney si los datos no se distribuían de forma normal. Las variables cualitativas se representan como porcentajes y su comparación univariada se realizó mediante la prueba de la χ >2 aplicando la corrección de Fisher cuando fue necesario. Se consideró significativa una p < 0,05. Se utilizó un análisis multivariado a través de un modelo de regresión logística múltiple con el método Forward para seleccionar variables independientes predictoras de eventos. Todas las variables se incluyeron en el modelo. Se obtuvieron las odds ratio con intervalo de confianza (IC) del 95% asociadas a las variables incluidas en el modelo. Se emplearon curvas de Kaplan-Meier para ilustrar las diferencias en la supervivencia libre de eventos entre los pacientes con y sin variables significativas en el modelo de regresión. Para comparar las curvas de supervivencia se usó el test log-rank. Todos los cálculos se realizaron con el paquete estadístico SPSS. RESULTADOS
Características clínicas
Las características clínicas de los pacientes se detallan en la tabla 1. Comparados con los pacientes con PE de alto riesgo, los pacientes con ergometría de bajo riesgo presentaban menor edad, menor incidencia de historia previa de cardiopatía isquémica, de angina de reciente inicio o progresiva como forma de presentación clínica y de algún episodio de angina recurrente durante la hospitalización. También fue menor la proporción de pacientes con ergometría de bajo riesgo que presentaron cambios de la repolarización en el ECG o una repolarización anormal en el ECG antes de la prueba de esfuerzo.
Se realizó un ecocardiograma a 78 de los 93 pacientes (84%) de bajo riesgo, y a 75 de los 79 de alto riesgo (95%). En éstos la presencia de disfunción sistólica ventricular izquierda leve o moderada fue mayor (el 27 frente al 11%; p = 0,009). Ningún paciente presentaba disfunción ventricular severa.
Resultados de la prueba de esfuerzo
En la tabla 2 se exponen los resultados de la PE. Como era de esperar, en los pacientes con PE de alto riesgo, la duración del ejercicio, el doble producto máximo, el porcentaje de la frecuencia cardíaca máxima prevista y el índice de Duke fueron significativamente menores que en los pacientes con ergometría de bajo riesgo. En éstos, el número de respuestas clínicas y electrocardiográficas positivas fue significativamente menor.
EVENTOS DURANTE EL SEGUIMIENTO
Los 93 pacientes con PE de bajo riesgo fueron dados de alta con tratamiento médico, sin la realización previa de coronariografía. En el momento del alta hospitalaria se prescribieron nitratos en 63 (67%) pacientes, betabloqueantes en 47 (50%), calcioantagonistas en 50 (54%) y antiagregantes en 83 (89%). El tiempo medio de seguimiento fue de 13 ± 6 meses (rango: 1-26).
Treinta de los 93 (32%) pacientes padecieron algún evento en el seguimiento: muerte en 2 (2%), infarto agudo de miocardio no mortal en 6 (6%), ingreso hospitalario por angina inestable en 18 (19%) y revascularización por la presencia de angina estable severa en 4 (4%).
Predictores de eventos
En la tabla 3 se detallan los resultados de las variables clínicas, electrocardiográficas y ergométricas analizadas en los pacientes que presentaron algún evento en el seguimiento y en los que tuvieron una evolución favorable.
La presencia de angina durante la PE fue más frecuente en los pacientes con eventos (9 pacientes [30%]) que en los que no tuvieron ninguno (4 pacientes [6%]; p = 0,002). Se observó una tendencia estadística a una mayor proporción de pacientes diabéticos (el 33 frente al 16%; p = 0,55) y a un menor índice de Duke (4,3 ± 6 frente a 6,5 ± 5; p = 0,095) en el grupo de pacientes con eventos.
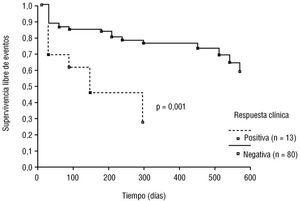
En el análisis de regresión logística, sólo la presencia de angina durante la prueba de esfuerzo fue un predictor independiente de eventos adversos en el seguimiento ( odds ratio: 2,35; IC del 95%: 1,22-4,50; p = 0,01). Los resultados fueron similares cuando se consideraron sólo los pacientes con eventos espontáneos (muerte, infarto de miocardio no mortal y angina inestable). Las curvas de supervivencia de los pacientes con y sin angina durante la PE se observan en la figura 1.
Fig. 1. Curvas de supervivencia libre de eventos según la respuesta clínica en la prueba de esfuerzo.
DISCUSIÓN
El presente estudio fue diseñado para evaluar prospectivamente el pronóstico de los pacientes con AI que realizan una PE de bajo riesgo, según unos criterios definidos con anterioridad, derivados de la población global de pacientes con cardiopatía isquémica crónica 14,15 y aceptados ampliamente en nuestro medio 16. Con el fin de disponer de una población homogénea, sólo se consideraron candidatos a la inclusión en el estudio los pacientes con AI primaria. Antes de la inclusión en el estudio, la decisión de remitir al paciente para la realización de la PE fue exclusivamente adoptada por el cardiólogo responsable del mismo, tal y como se lleva a cabo en la asistencia clínica diaria. Por tanto, salvo la inestabilidad clínica, no se definieron prospectivamente criterios específicos para no efectuar la PE. Sin embargo, ninguno de los pacientes del estudio había sido sometido a revascularización percutánea o quirúrgica durante los 6 meses precedentes, tenía disfunción sistólica ventricular izquierda severa en el ecocardiograma (que se efectuó en el 89% de la población), ni había presentado hipotensión ni signos clínicos o radiológicos de insuficiencia cardíaca aguda. Sin embargo, la decisión de efectuar la PE implicaba la aceptación de una estrategia de manejo previamente definida, según la cual, la presencia de alguno de los criterios de alto riesgo implicaba la realización de coronariografía, y la ausencia de todos los criterios de alto riesgo, el alta hospitalaria con tratamiento médico.
Se han publicado algunos estudios que han evaluado la utilidad pronóstica de la PE en pacientes con AI y su capacidad para añadir información adicional a la proporcionada por la valoración clínica 4,5,17-20. En dichos estudios se han descrito diversas variables clínicas (la diabetes mellitus 4, la angina recurrente durante la hospitalización 4, y los cambios de la repolarización o alteraciones en el ECG de reposo 4,20) y ergométricas (el resultado de la prueba 4,18-20, el doble producto máximo 4,19 y el número de derivaciones con descenso significativo del segmento ST 5) con capacidad de predecir un pronóstico adverso a largo plazo, con una amplia variabilidad en sus resultados.
La heterogeneidad de las poblaciones, la inclusión de pacientes con diversas formas de presentación de la AI, poco sistematizadas en el momento de su realización 11, y las pautas de tratamiento (farmacológico e invasivo), en la mayoría de los casos diferentes a las que se siguen en la actualidad, han podido contribuir a la amplia variabilidad en los resultados. Además, es importante señalar que la mayoría de los estudios que han evaluado la utilidad de la PE en la valoración pronóstica de la AI se han basado en el análisis retrospectivo de poblaciones altamente seleccionadas, lo cual introduce un sesgo crucial a la hora de interpretar sus resultados. Así, por ejemplo, en el estudio de Wilcox et al 4 sobre una población de 296 pacientes con AI, 117 (40%) fueron referidos para revascularización y fueron excluidos del análisis. La población de estudio estuvo finalmente constituido por 107 pacientes a los que se efectuó una PE y fueron dados de alta con tratamiento médico. En 43 (40%) de estos 107 pacientes se realizó, además, coronariografía. En dicho estudio no se especifican los criterios que se siguieron para su indicación, ni si los pacientes remitidos a revascularización habían realizado previamente una PE, ni su resultado.
Tras una extensa revisión de la bibliografía, no hemos encontrado ningún estudio que, como el nuestro, haya evaluado prospectivamente el pronóstico de una población homogénea de pacientes con AI primaria y PE de bajo riesgo, para los que se definió previamente una pauta de tratamiento conservador. La evaluación prospectiva de los pacientes de nuestro estudio con PE de bajo riesgo demostró una baja mortalidad (2%) al año de seguimiento. Estos resultados son similares a los encontrados por otros investigadores en poblaciones similares 5,10,19. Sin embargo, encontramos una incidencia de eventos isquémicos agudos, como infarto agudo de miocardio no mortal (6%) o de nuevo ingreso hospitalario por angina inestable (19%), relativamente elevada. La angina durante la PE fue el único predictor independiente de eventos durante el seguimiento. El valor pronóstico independiente de la respuesta clínica durante la prueba de esfuerzo en pacientes con cardiopatía isquémica crónica ha sido descrito por otros autores 1,21. No obstante, en nuestro estudio, el número de pacientes con respuesta clínica positiva fue reducido (14%) y un 60% de los pacientes con eventos no tuvieron angina durante la prueba. Esta circunstancia probablemente limite la utilidad práctica de la predicción según esta variable.
Las limitaciones para predecir la evolución de estos pacientes deriva, probablemente, de diversas circunstancias. Los pacientes que realizan una PE de bajo riesgo han sido seleccionados con anterioridad y, en ellos, las variables clínicas asociadas clásicamente a un mayor riesgo (como los antecedentes de enfermedad coronaria, la angina recurrente durante la hospitalización o las alteraciones del ECG de reposo) son significativamente menos frecuentes que en los pacientes que realizan una PE de alto riesgo, (tabla 1), y probablemente, que en los que no se les efectúa la prueba. Además, la definición de PE de bajo riesgo implica un resultado de la misma homogéneo que dificulta encontrar subgrupos con diferencias significativas (tabla 2) que permitan discriminar poblaciones de riesgo diferente. Otro aspecto probablemente importante que dificulta la predicción de eventos isquémicos agudos recurrentes es la fisiopatología de los mismos. Los pacientes con síndromes isquémicos inestables tienen una particular susceptibilidad para padecer recurrencias y dificultad para predecirlas, pues en muchos casos son consecuencia de rotura de placas ateroscleróticas, hasta entonces estables e incapaces de provocar isquemia 22.
Sin embargo, a pesar de estas limitaciones, los resultados de nuestro estudio sugieren que es posible que la detección de ciertos marcadores de isquemia (como la angina durante la prueba de esfuerzo) inducible tras la estabilización pueden ser útiles en la predicción de eventos isquémicos recurrentes en estos pacientes. En este sentido, se ha sugerido que otras exploraciones no invasivas, más precisas que la PE para la detección y cuantificación de la isquemia como son los estudios de perfusión miocárdica 23 o la ecocardiografía de estrés 24, son útiles para la predicción del riesgo a largo plazo de los pacientes con AI. Sería interesante conocer en el futuro si estas técnicas podrían ayudar a identificar, dentro de esta población específica de pacientes con prueba de esfuerzo de bajo riesgo, a aquellos con mayor probabilidad de desarrollar eventos isquémicos recurrentes. CONCLUSIÓN
Los pacientes con AI primaria estabilizada con tratamiento farmacológico y con una PE con fines pronósticos de bajo riesgo, tienen una baja mortalidad (2%) durante el primer año tras el alta hospitalaria. Sin embargo, durante este período, uno de cada cuatro pacientes experimenta un evento isquémico espontáneo (infarto agudo de miocardio no mortal o ingreso hospitalario por angina inestable). En esta población específica es difícil predecir la presencia de estos eventos sobre la base de las características clínicas y el resultado de la PE. Sin embargo, la presencia de angina durante la misma se asocia a una evolución desfavorable. Por ello, es posible que otras exploraciones no invasivas capaces de identificar isquemia miocárdica y cuantificar su severidad, mediante marcadores alternativos y más precisos que los que ofrece la prueba de esfuerzo convencional, puedan mejorar la capacidad de predicción de la misma en este grupo de pacientes.
La prueba de esfuerzo (PE) convencional continúa siendo la exploración no invasiva más utilizada para demostrar la presencia de isquemia inducible y, por tanto, para definir el pronóstico de los pacientes con enfermedad coronaria. La mayor parte de los estudios que han demostrado la utilidad pronóstica de la PE se han realizado en poblaciones de pacientes con cardiopatía isquémica crónica estable 1-3 o tras un infarto agudo de miocardio 3.
La información sobre la utilidad de la PE en la valoración del pronóstico de los pacientes con angina inestable (AI) que se ha controlado con tratamiento farmacológico es limitada 4,5. Por ello, para la toma de decisiones clínicas en esta población específica se recomienda considerar criterios de riesgo de la PE que han sido validados exclusivamente en pacientes con cardiopatía isquémica crónica 6,7, no con AI. Los pacientes con una prueba positiva de alto riesgo deben ser remitidos para la realización de coronariografía y valoración de la posibilidad de revascularización, mientras que en aquellos que son capaces de realizar una PE sin evidencia de isquemia severa se acepta, en la mayoría de los casos, una actitud conservadora 6,8,9. Sin embargo, se ha descrito una elevada incidencia de eventos durante el seguimiento a largo plazo de pacientes con AI que han sido controlados con tratamiento farmacológico y que son capaces de realizar una PE convencional sin evidencia de isquemia, en los que, por tanto, se sigue una pauta de tratamiento no invasivo 10. Esta circunstancia sugiere que una PE de bajo riesgo puede no implicar un pronóstico favorable en cierto grupo de pacientes con AI.
Los objetivos de este estudio fueron: a) determinar el pronóstico de los pacientes con AI primaria estabilizada con tratamiento farmacológico en los que se realiza una PE convencional que no demuestra criterios de alto riesgo, y b) determinar si existen variables clínicas o derivadas de la PE que se correlacionen con la presencia de eventos en el seguimiento de estos pacientes. MÉTODOS
Selección de pacientes
Los pacientes fueron seleccionados, según un protocolo de estudio prospectivo, entre todos aquellos ingresados en la Unidad de Cardiología de nuestro hospital, entre enero de 1997 y diciembre de 1998, con el diagnóstico de AI primaria, cuyo estado clínico se había estabilizado con tratamiento farmacológico (al menos 72 h sin nuevos episodios de dolor torácico), a los que se realizó una PE para su valoración pronóstica antes del alta hospitalaria. Dado el objetivo del estudio, no se consideraron los pacientes con alteraciones basales del ECG de reposo asociadas a una respuesta eléctrica no interpretable para isquemia en la PE (bloqueo de rama izquierda, ritmo de marcapasos, preexcitación, descenso del segmento ST >= 1 mm o menor en presencia de tratamiento con digoxina u otros criterios de hipertrofia ventricular izquierda) 3, y se excluyeron los pacientes incapaces de completar el estadio II del protocolo de Bruce en ausencia de isquemia inducible.
Durante el período de estudio se realizó una PE a 183 pacientes con el diagnóstico de AI estabilizada con tratamiento médico. Ocho pacientes (4%) fueron incapaces de completar el estadio II del protocolo de Bruce y la prueba fue negativa, por lo que fueron excluidos.
Definiciones
De acuerdo con la clasificación de Braunwald 11, se consideró AI a aquella de reciente inicio o progresiva; la angina de reposo subaguda, y la angina de reposo aguda. Sólo se incluyeron pacientes con AI primaria, de modo que no se consideraron los pacientes con AI secundaria o angina postinfarto. Tampoco se incluyó a ningún paciente con infarto agudo de miocardio sin onda Q.
Prueba de esfuerzo
La PE se realizó en cinta sin fin siguiendo el protocolo de Bruce 12 estándar, empleando un sistema computarizado de electrocardiografía de esfuerzo comercialmente disponible. En todos los pacientes se mantuvo el tratamiento farmacológico prescrito. Se midió la presión arterial antes del inicio de la prueba y, con posterioridad, cada dos minutos durante el esfuerzo máximo y siempre que se consideró clínicamente indicado. Se obtuvo un ECG de 12 derivaciones antes de iniciar el ejercicio y, posteriormente, a intervalos de 3 minutos durante el ejercicio (al final de cada estadio del protocolo de Bruce), durante el máximo esfuerzo, a intervalos de 1 min durante al menos los primeros 5 min de la fase de recuperación y siempre que se consideró clínicamente indicado. Durante toda la prueba se monitorizaron de forma continua 3 derivaciones del ECG y la derivación con máxima desviación del ST.
Se consideraron criterios de finalización de la prueba: a) el agotamiento de la capacidad física o alcanzar la frecuencia cardíaca máxima prevista según la edad (220 - edad); b) descenso de la presión arterial sistólica por debajo de la basal o respuesta hipertensiva (presión arterial sistólica >= 230 mmHg o diastólica >= 130 mmHg); c) ataxia, mareo o presíncope, disnea intensa, claudicación severa, evidencia de hipoperfusión periférica (cianosis o palidez); d) arritmias ventriculares (extrasístoles ventriculares frecuentes, complejos multiformes o rachas de tres latidos); e) dificultades técnicas en la monitorización del ECG o la presión arterial; f) angina de pecho intensa; g) descenso del ST >= 3 mm, y h) a petición del paciente.
Se consideraron criterios de positividad de la prueba: a) la presencia de angina (prueba positiva clínica), y b) el descenso del segmento ST >= 1 mm, o el ascenso del segmento ST >= 1 mm en derivaciones sin onda Q patológica (diferentes de aVR), medido a 80 ms del punto J (prueba positiva eléctrica). Se admitió la lectura de la desviación del segmento ST efectuada por el sistema computarizado de electrocardiografía de esfuerzo, confirmada por un cardiólogo experto en la técnica.
Se consideraron criterios de alto riesgo de la PE los siguientes: a) respuesta clínica y/o eléctrica positiva con una frecuencia cardíaca < 120 lat/min o durante los 2 primeros estadios del protocolo de Bruce; b) el descenso del ST >= 1 mm que persiste >= 6 min en fase de recuperación o presente en >= 5 derivaciones; c) el descenso del ST >= 2 mm a cualquier nivel de ejercicio; d) la elevación del segmento ST (excepto aVR) en derivaciones sin onda Q; e) el descenso sostenido de la presión arterial sistólica durante el ejercicio progresivo, y f) la presencia de taquicardia ventricular.
Manejo del paciente
A todos los pacientes se les realizó de manera rutinaria un ECG de 12 derivaciones en el momento del ingreso hospitalario, durante e inmediatamente después de cada episodio de dolor torácico, a las 24 h del ingreso y antes de la realización de la PE. También de forma rutinaria se obtuvieron muestras de sangre para la determinación de la creatincinasa plasmática y su isoenzima MB cada 8 h durante las primeras 24 h. Los pacientes recibieron tratamiento con nitratos (tópicos, orales o nitroglicerina intravenosa), calcioantagonistas, betabloqueantes, aspirina o heparina (intravenosa o de bajo peso molecular), a juicio del cardiólogo clínico responsable del paciente. En los pacientes que recibieron heparina intravenosa, el tratamiento se monitorizó mediante la determinación de la actividad parcial de tromboplastina, persiguiendo un valor de 1,5-2,5 veces el control. En todos los casos se realizó la PE tras permanecer >= 72 h sin nuevos episodios de dolor torácico
Se definió prospectivamente la estrategia de manejo definitivo, de modo que los pacientes con una PE de alto riesgo (presencia de alguno de los criterios de alto riesgo) fueron remitidos para coronariografía y valoración de revascularización y los pacientes que completaron una PE de bajo riesgo (ausencia de todos los criterios de alto riesgo) fueron dados de alta con tratamiento médico.
De los 175 pacientes que realizaron la PE, en 79 (45%) resultó de alto riesgo y en 96 (55%) de bajo riesgo. En 78 pacientes con PE de alto riesgo se realizó coronariografía. Ésta no se realizó en ninguno de los 96 pacientes con ergometría de bajo riesgo.
Seguimiento de los pacientes
Los pacientes que realizaron una PE de bajo riesgo fueron evaluados en las consultas ambulatorias de la Unidad de Cardiología de nuestro centro, a los 3 meses tras el alta hospitalaria, y posteriormente, con una periodicidad semestral. En los pacientes que no acudieron a la cita se efectuó el seguimiento mediante entrevista telefónica realizada por personal médico.
Se consideraron eventos en el seguimiento, en orden decreciente de gravedad, la presencia de muerte de origen cardíaco, infarto agudo de miocardio no mortal, ingreso hospitalario por angina inestable y la revascularización por angina de esfuerzo estable de clase funcional III o IV de la Sociedad Cardiovascular Canadiense. Se consideró muerte de origen cardíaco la que sucedió en ausencia de diagnóstico clínico o patológico de una causa extracardíaca. La presencia de infarto agudo de miocardio o de angina inestable se confirmó en todos los casos mediante los informes clínicos hospitalarios correspondientes. En los pacientes con más de un evento sólo se consideró el más grave.
Tres de los 96 pacientes (3%) con PE de bajo riesgo fueron perdidos para el seguimiento, por lo que la población de estudio en este grupo estuvo finalmente confirmada por 93 pacientes.
Variables de estudio
Se registraron prospectivamente las siguientes variables:
1. Clínicas: edad, sexo, hábito tabáquico, hipertensión arterial, hipercolesterolemia, diabetes mellitus, historia anterior de cardiopatía isquémica (angina crónica estable o infarto de miocardio antiguo), revascularización previa (angioplastia coronaria percutánea o cirugía de derivación aortocoronaria), enfermedad vascular arterial periférica, forma de presentación de la angina inestable (reciente inicio/progresiva o de reposo) y presencia de episodios de angina recurrente durante la hospitalización.
2. Electrocardiográficas: presencia de cambios objetivos de la repolarización en el ECG, presencia de ECG preergometría anormal.
3. Ergométricas: duración de la prueba (minutos de ejercicio), doble producto (presión arterial sistólica × frecuencia cardíaca) máximo, porcentaje de la frecuencia cardíaca máxima prevista alcanzado, resultado de la PE (positivo o negativo), respuesta clínica, respuesta eléctrica e índice de Duke. El índice de Duke se calculó según la fórmula:
duración del ejercicio en minutos - (5 × máxima desviación neta del segmento ST durante o después del ejercicio, en mm) - (4 × índice de angina).
El índice de angina se consideró 0 si el paciente no tuvo angina durante la prueba, 1 si el paciente tuvo angina que no limitó el ejercicio, y 2 si la angina fue la causa de detener la prueba 13.
Análisis estadístico
Las variables cuantitativas se expresan como media ± desviación estándar. Las comparaciones univariadas entre grupos de variables continuas se realizaron aplicando el test de la t de Student para muestras no relacionadas o el test U de Mann-Whitney si los datos no se distribuían de forma normal. Las variables cualitativas se representan como porcentajes y su comparación univariada se realizó mediante la prueba de la χ >2 aplicando la corrección de Fisher cuando fue necesario. Se consideró significativa una p < 0,05. Se utilizó un análisis multivariado a través de un modelo de regresión logística múltiple con el método Forward para seleccionar variables independientes predictoras de eventos. Todas las variables se incluyeron en el modelo. Se obtuvieron las odds ratio con intervalo de confianza (IC) del 95% asociadas a las variables incluidas en el modelo. Se emplearon curvas de Kaplan-Meier para ilustrar las diferencias en la supervivencia libre de eventos entre los pacientes con y sin variables significativas en el modelo de regresión. Para comparar las curvas de supervivencia se usó el test log-rank. Todos los cálculos se realizaron con el paquete estadístico SPSS. RESULTADOS
Características clínicas
Las características clínicas de los pacientes se detallan en la tabla 1. Comparados con los pacientes con PE de alto riesgo, los pacientes con ergometría de bajo riesgo presentaban menor edad, menor incidencia de historia previa de cardiopatía isquémica, de angina de reciente inicio o progresiva como forma de presentación clínica y de algún episodio de angina recurrente durante la hospitalización. También fue menor la proporción de pacientes con ergometría de bajo riesgo que presentaron cambios de la repolarización en el ECG o una repolarización anormal en el ECG antes de la prueba de esfuerzo.
Se realizó un ecocardiograma a 78 de los 93 pacientes (84%) de bajo riesgo, y a 75 de los 79 de alto riesgo (95%). En éstos la presencia de disfunción sistólica ventricular izquierda leve o moderada fue mayor (el 27 frente al 11%; p = 0,009). Ningún paciente presentaba disfunción ventricular severa.
Resultados de la prueba de esfuerzo
En la tabla 2 se exponen los resultados de la PE. Como era de esperar, en los pacientes con PE de alto riesgo, la duración del ejercicio, el doble producto máximo, el porcentaje de la frecuencia cardíaca máxima prevista y el índice de Duke fueron significativamente menores que en los pacientes con ergometría de bajo riesgo. En éstos, el número de respuestas clínicas y electrocardiográficas positivas fue significativamente menor.
EVENTOS DURANTE EL SEGUIMIENTO
Los 93 pacientes con PE de bajo riesgo fueron dados de alta con tratamiento médico, sin la realización previa de coronariografía. En el momento del alta hospitalaria se prescribieron nitratos en 63 (67%) pacientes, betabloqueantes en 47 (50%), calcioantagonistas en 50 (54%) y antiagregantes en 83 (89%). El tiempo medio de seguimiento fue de 13 ± 6 meses (rango: 1-26).
Treinta de los 93 (32%) pacientes padecieron algún evento en el seguimiento: muerte en 2 (2%), infarto agudo de miocardio no mortal en 6 (6%), ingreso hospitalario por angina inestable en 18 (19%) y revascularización por la presencia de angina estable severa en 4 (4%).
Predictores de eventos
En la tabla 3 se detallan los resultados de las variables clínicas, electrocardiográficas y ergométricas analizadas en los pacientes que presentaron algún evento en el seguimiento y en los que tuvieron una evolución favorable.
La presencia de angina durante la PE fue más frecuente en los pacientes con eventos (9 pacientes [30%]) que en los que no tuvieron ninguno (4 pacientes [6%]; p = 0,002). Se observó una tendencia estadística a una mayor proporción de pacientes diabéticos (el 33 frente al 16%; p = 0,55) y a un menor índice de Duke (4,3 ± 6 frente a 6,5 ± 5; p = 0,095) en el grupo de pacientes con eventos.
En el análisis de regresión logística, sólo la presencia de angina durante la prueba de esfuerzo fue un predictor independiente de eventos adversos en el seguimiento ( odds ratio: 2,35; IC del 95%: 1,22-4,50; p = 0,01). Los resultados fueron similares cuando se consideraron sólo los pacientes con eventos espontáneos (muerte, infarto de miocardio no mortal y angina inestable). Las curvas de supervivencia de los pacientes con y sin angina durante la PE se observan en la figura 1.
Fig. 1. Curvas de supervivencia libre de eventos según la respuesta clínica en la prueba de esfuerzo.
DISCUSIÓN
El presente estudio fue diseñado para evaluar prospectivamente el pronóstico de los pacientes con AI que realizan una PE de bajo riesgo, según unos criterios definidos con anterioridad, derivados de la población global de pacientes con cardiopatía isquémica crónica 14,15 y aceptados ampliamente en nuestro medio 16. Con el fin de disponer de una población homogénea, sólo se consideraron candidatos a la inclusión en el estudio los pacientes con AI primaria. Antes de la inclusión en el estudio, la decisión de remitir al paciente para la realización de la PE fue exclusivamente adoptada por el cardiólogo responsable del mismo, tal y como se lleva a cabo en la asistencia clínica diaria. Por tanto, salvo la inestabilidad clínica, no se definieron prospectivamente criterios específicos para no efectuar la PE. Sin embargo, ninguno de los pacientes del estudio había sido sometido a revascularización percutánea o quirúrgica durante los 6 meses precedentes, tenía disfunción sistólica ventricular izquierda severa en el ecocardiograma (que se efectuó en el 89% de la población), ni había presentado hipotensión ni signos clínicos o radiológicos de insuficiencia cardíaca aguda. Sin embargo, la decisión de efectuar la PE implicaba la aceptación de una estrategia de manejo previamente definida, según la cual, la presencia de alguno de los criterios de alto riesgo implicaba la realización de coronariografía, y la ausencia de todos los criterios de alto riesgo, el alta hospitalaria con tratamiento médico.
Se han publicado algunos estudios que han evaluado la utilidad pronóstica de la PE en pacientes con AI y su capacidad para añadir información adicional a la proporcionada por la valoración clínica 4,5,17-20. En dichos estudios se han descrito diversas variables clínicas (la diabetes mellitus 4, la angina recurrente durante la hospitalización 4, y los cambios de la repolarización o alteraciones en el ECG de reposo 4,20) y ergométricas (el resultado de la prueba 4,18-20, el doble producto máximo 4,19 y el número de derivaciones con descenso significativo del segmento ST 5) con capacidad de predecir un pronóstico adverso a largo plazo, con una amplia variabilidad en sus resultados.
La heterogeneidad de las poblaciones, la inclusión de pacientes con diversas formas de presentación de la AI, poco sistematizadas en el momento de su realización 11, y las pautas de tratamiento (farmacológico e invasivo), en la mayoría de los casos diferentes a las que se siguen en la actualidad, han podido contribuir a la amplia variabilidad en los resultados. Además, es importante señalar que la mayoría de los estudios que han evaluado la utilidad de la PE en la valoración pronóstica de la AI se han basado en el análisis retrospectivo de poblaciones altamente seleccionadas, lo cual introduce un sesgo crucial a la hora de interpretar sus resultados. Así, por ejemplo, en el estudio de Wilcox et al 4 sobre una población de 296 pacientes con AI, 117 (40%) fueron referidos para revascularización y fueron excluidos del análisis. La población de estudio estuvo finalmente constituido por 107 pacientes a los que se efectuó una PE y fueron dados de alta con tratamiento médico. En 43 (40%) de estos 107 pacientes se realizó, además, coronariografía. En dicho estudio no se especifican los criterios que se siguieron para su indicación, ni si los pacientes remitidos a revascularización habían realizado previamente una PE, ni su resultado.
Tras una extensa revisión de la bibliografía, no hemos encontrado ningún estudio que, como el nuestro, haya evaluado prospectivamente el pronóstico de una población homogénea de pacientes con AI primaria y PE de bajo riesgo, para los que se definió previamente una pauta de tratamiento conservador. La evaluación prospectiva de los pacientes de nuestro estudio con PE de bajo riesgo demostró una baja mortalidad (2%) al año de seguimiento. Estos resultados son similares a los encontrados por otros investigadores en poblaciones similares 5,10,19. Sin embargo, encontramos una incidencia de eventos isquémicos agudos, como infarto agudo de miocardio no mortal (6%) o de nuevo ingreso hospitalario por angina inestable (19%), relativamente elevada. La angina durante la PE fue el único predictor independiente de eventos durante el seguimiento. El valor pronóstico independiente de la respuesta clínica durante la prueba de esfuerzo en pacientes con cardiopatía isquémica crónica ha sido descrito por otros autores 1,21. No obstante, en nuestro estudio, el número de pacientes con respuesta clínica positiva fue reducido (14%) y un 60% de los pacientes con eventos no tuvieron angina durante la prueba. Esta circunstancia probablemente limite la utilidad práctica de la predicción según esta variable.
Las limitaciones para predecir la evolución de estos pacientes deriva, probablemente, de diversas circunstancias. Los pacientes que realizan una PE de bajo riesgo han sido seleccionados con anterioridad y, en ellos, las variables clínicas asociadas clásicamente a un mayor riesgo (como los antecedentes de enfermedad coronaria, la angina recurrente durante la hospitalización o las alteraciones del ECG de reposo) son significativamente menos frecuentes que en los pacientes que realizan una PE de alto riesgo, (tabla 1), y probablemente, que en los que no se les efectúa la prueba. Además, la definición de PE de bajo riesgo implica un resultado de la misma homogéneo que dificulta encontrar subgrupos con diferencias significativas (tabla 2) que permitan discriminar poblaciones de riesgo diferente. Otro aspecto probablemente importante que dificulta la predicción de eventos isquémicos agudos recurrentes es la fisiopatología de los mismos. Los pacientes con síndromes isquémicos inestables tienen una particular susceptibilidad para padecer recurrencias y dificultad para predecirlas, pues en muchos casos son consecuencia de rotura de placas ateroscleróticas, hasta entonces estables e incapaces de provocar isquemia 22.
Sin embargo, a pesar de estas limitaciones, los resultados de nuestro estudio sugieren que es posible que la detección de ciertos marcadores de isquemia (como la angina durante la prueba de esfuerzo) inducible tras la estabilización pueden ser útiles en la predicción de eventos isquémicos recurrentes en estos pacientes. En este sentido, se ha sugerido que otras exploraciones no invasivas, más precisas que la PE para la detección y cuantificación de la isquemia como son los estudios de perfusión miocárdica 23 o la ecocardiografía de estrés 24, son útiles para la predicción del riesgo a largo plazo de los pacientes con AI. Sería interesante conocer en el futuro si estas técnicas podrían ayudar a identificar, dentro de esta población específica de pacientes con prueba de esfuerzo de bajo riesgo, a aquellos con mayor probabilidad de desarrollar eventos isquémicos recurrentes. CONCLUSIÓN
Los pacientes con AI primaria estabilizada con tratamiento farmacológico y con una PE con fines pronósticos de bajo riesgo, tienen una baja mortalidad (2%) durante el primer año tras el alta hospitalaria. Sin embargo, durante este período, uno de cada cuatro pacientes experimenta un evento isquémico espontáneo (infarto agudo de miocardio no mortal o ingreso hospitalario por angina inestable). En esta población específica es difícil predecir la presencia de estos eventos sobre la base de las características clínicas y el resultado de la PE. Sin embargo, la presencia de angina durante la misma se asocia a una evolución desfavorable. Por ello, es posible que otras exploraciones no invasivas capaces de identificar isquemia miocárdica y cuantificar su severidad, mediante marcadores alternativos y más precisos que los que ofrece la prueba de esfuerzo convencional, puedan mejorar la capacidad de predicción de la misma en este grupo de pacientes.
Bibliografía
[1]
Prognostic value of a treadmill exercise score in outpatients with suspected coronary artery disease. N Engl J Med 1991; 325: 849-853.
[2]
Prediction of cardiovascular death by means of clinical and exercise test variables in patients selected for cardiac catheterization. Am Heart J 1993; 125: 1717-1726.
[3]
ACC/AHA Guidelines for Exercise Testing. A report of the American College of Cardiology/ American Heart Association task force on practice guidelines (Committee on exercise testing). J Am Coll Cardiol 1997; 30: 260-315.
[4]
Prognostic significance of a predischarge exercise test in risk stratification after unstable angina pectoris. J Am Coll Cardiol 1991; 18: 677-683.
[5]
Risk stratification by early exercise testing after an episode of unstable coronary artery disease. RISC study group. Int J Cardiol 1993; 39: 131-142.
[6]
Diagnosing and managing unstable angina. Circulation 1994; 90: 613-622.
[7]
Las exploraciones no invasivas en el manejo de los pacientes con cardiopatía isquémica crónica. Recomendaciones para su utilización. Rev Esp Cardiol 1997; 50: 145-156.
[8]
Effects of tissue plasminogen activator and a comparison of early invasive and conservative strategies in unstable angina and non-Q-wave infarction: results of the TIMI IIIB trial. Circulation 1994; 89: 1545-1556.
[9]
Outcomes in patients with acute non-Q-wave myocardial infarction randomly assigned to an invasive as compared with a conservative management strategy. N Engl J Med 1998; 338: 1785-1792.
[10]
Prognosis of medically stabilized unstable angina pectoris with a negative exercise test. Am J Cardiol 1998; 82: 662-665.
[11]
Unstable angina: a classification. Circulation 1989; 80: 410.
[12]
Enhanced risk assessment for primary coronary artery disease events by maximal exercise testing: 10 years' experience of Seattle Heart Watch. J Am Coll Cardiol 1983; 2: 565-573.
[13]
Exercise treadmill score for predicting prognosis in coronary artery disease. Ann Intern Med 1987; 106: 793-800.
[14]
Estratificación no invasiva del riesgo de la angina inestable pasada la fase aguda. Valor de la prueba de esfuerzo y de los tests de estrés farmacológico en la valoración del pronóstico. Rev Esp Cardiol 1999; 52 (Supl 1): 107-116.
[15]
Utilidad de la prueba de esfuerzo y de otros métodos basados en el electrocardiograma en la cardiopatía isquémica crónica. Rev Esp Cardiol 1997; 50: 6-14.
[16]
Indicaciones y técnicas actuales de la prueba de esfuerzo. En: Asín Cardiel E, Cosín Aguilar J, Del Río del Busto A, editores. Normas de actuación clínica en cardiología. Madrid: Sociedad Española de Cardiología, 1996; 384-393.
[17]
Submaximal exercise testing after unstable angina. Am Heart J 1980; 99: 772-778.
[18]
Early exercise testing after stabilization of unstable angina: correlation with coronary angiographic findings and subsequent cardiac events. Am Heart J 1986; 111: 11-18.
[19]
Predictive importance of clinical findings and a predischarge exercise test in patients with suspected unstable coronary artery disease. Am J Cardiol 1987; 59: 208-214.
[20]
The basal electrocardiogram and the exercise stress test in assessing prognosis in patients with unstable angina. Eur Heart J 1998; 9: 441-446.
[21]
Exercise testing provides additional prognostic information in angiographically defined subgroups of patients with coronary artery disease. Circulation 1983; 68: 979-985.
[22]
Unstable angina and non-Q-wave myocardial infarction: Does the clinical diagnosis have therapeutic implications? J Am Coll Cardiol 1999; 33: 107-118.
[23]
Exercise technetium-99m myocardial tomography for the risk stratification of men with medically treated unstable angina pectoris. Am J Cardiol 1995; 76: 236-240.
[24]
Long-term prognostic importance of exercise echocardiography after an episode of unstable angina. Cardiology 1995; 86: 426-431.