La enfermedad de Chagas es una causa frecuente de insuficiencia cardiaca en Latinoamérica, y su pronóstico es peor que el de otras etiologías. La puntuación de supervivencia en la insuficiencia cardiaca (Heart Failure Survival Score) se ha utilizado para evaluar el pronóstico de los pacientes con insuficiencia cardiaca; sin embargo, dicha puntuación no se ha evaluado todavía en pacientes con cardiopatía chagásica.
MétodosSe calculó la puntuación Heart Failure Survival Score en 55 pacientes con disfunción sistólica ventricular izquierda grave debida a enfermedad de Chagas. Se evaluaron las correlaciones entre la Heart Failure Survival Score y las variables derivadas de las ecocardiografías, las pruebas de esfuerzo cardiorrespiratorias, las medidas de la calidad de vida y las pruebas de distancia recorrida en 6 min.
ResultadosSe distribuyó a los pacientes según las clases II-IV de la New York Heart Association; un 89% recibía tratamiento con inhibidores de la enzima de conversión de la angiotensina o antagonistas de los receptores de la angiotensina II; un 62%, con bloqueadores beta; un 86%, con diuréticos y un 74%, con antagonistas de los receptores de aldosterona. La media de la puntuación Heart Failure Survival Score fue de 8,75±0,80. La puntuación mostró buena correlación con las variables derivadas de la prueba cardiorrespiratoria, como la captación de oxígeno máxima (0,662; p<0,01), la captación de oxígeno en el umbral anaeróbico (0,644; p<0,01), la pendiente de eficiencia ventilatoria de dióxido de carbono (–0,417; p<0,01), el pulso de oxígeno (0,375; p<0,01), la pendiente de eficiencia de captación de oxígeno (0,626; p<0,01), la prueba de distancia recorrida en 6 min (0,370; p<0,01), la fracción de eyección ventricular izquierda (0,650; p=0,01) y el diámetro de la aurícula izquierda (–0,377; p<0,01). Se observó también una correlación en el límite de la significación estadística entre la puntuación Heart Failure Survival Score y la calidad de vida (–0,283; p<0,05).
ConclusionesEn pacientes con enfermedad de Chagas que presentaban insuficiencia cardiaca, la puntuación Heart Failure Survival Score mostró buena correlación con las principales variables de las pruebas funcionales pronósticas.
Palabras clave
La insuficiencia cardiaca (IC) es el estadio final de casi todas las enfermedades que afectan al corazón. A pesar de los avances en la prevención primaria y secundaria de la enfermedad cardiaca, la IC sigue siendo una causa prevalente de mortalidad y hospitalización1.
Se han estudiado varios instrumentos para evaluar el pronóstico de la IC. Los más establecidos son las puntuaciones y la prueba de esfuerzo cardiorrespiratoria (PECR). La puntuación Heart Failure Survival Score (HFSS) es una de las más estudiadas y utilizadas en la práctica clínica1, 2, 3. La PECR es la mejor forma de medir la capacidad funcional y la más reproducible. Además, mediante la interpretación de otras variables obtenidas en la misma prueba, puede valorarse también la fisiopatología de los síntomas del paciente. Partiendo del conocimiento de que la IC es un síndrome multifactorial, la HFSS combina datos de diferentes marcadores pronósticos de la IC para determinar mejor el riesgo en esa población específica.
La enfermedad de Chagas es una causa prevalente de IC en Brasil y otros países latinoamericanos4. Los casos importados son cada vez más frecuentes en Norteamérica y Europa. El pronóstico de la IC debida a enfermedad de Chagas parece ser peor que el que se da en otras etiologías5, 6. Recientemente se ha publicado una puntuación específica para la evaluación del pronóstico en la enfermedad de Chagas7.
Aunque la PECR y las variables derivadas de ella (captación de oxígeno [VO2] máxima, pendiente de eficiencia ventilatoria de dióxido de carbono [pendiente VE/VCO2], recuperación de la frecuencia cardiaca en el primer minuto, pendiente de eficiencia de captación de oxígeno [OUES] y pulso de oxígeno) y la prueba de distancia recorrida en 6 min (6MWT) se han estudiado ampliamente en la IC8, 9, 10, 11, 12, 13, no se ha estudiado el rendimiento de la HFSS en la IC debida a enfermedad de Chagas. Por lo tanto, el objetivo de este estudio es evaluar la correlación entre la HFSS, una puntuación más genérica de la IC, y las pruebas pronósticas clásicas de la IC, en una población con IC sintomática y avanzada debida a enfermedad de Chagas.
MétodosPoblación en estudioEstudiamos a 55 pacientes con IC debida a enfermedad de Chagas. Los pacientes debían tener entre 18 y 75 años y una confirmación serológica de la enfermedad de Chagas mediante el empleo de dos métodos diferentes: disfunción ventricular izquierda grave (fracción de eyección < 35%) y síntomas (clases II-IV de la New York Heart Association [NYHA]) después de un periodo de tratamiento farmacológico estable. Formaron la población pacientes consecutivos que en el examen de selección cumplían los criterios citados y para los que se dispuso de todas las pruebas específicas que se indican más adelante antes de la asignación aleatoria a uno de dos protocolos de ensayo distintos que se estaban llevando a cabo en pacientes con IC por enfermedad de Chagas en nuestro centro14. Del total de casos, se seleccionó a 21 pacientes para un ensayo en el que se asignaba aleatoriamente a los pacientes el tratamiento con células madre intracoronarias autólogas o placebo; se seleccionó a los 34 pacientes restantes para un protocolo en el que se asignaba aleatoriamente a los pacientes el uso de pentoxifilina, factor estimulador de colonias de granulocitos o placebo. En ambos protocolos se pretendía determinar la posible mejora de la función ventricular izquierda. No se seleccionó a pacientes con enfermedades pulmonares, valvulopatías cardiacas primarias, lesiones coronarias con obstrucción > 50% o pacientes con mal cumplimiento del tratamiento farmacológico. Como parte de los exámenes de inclusión de ambos protocolos, se realizaron las siguientes pruebas: PECR, análisis de laboratorio, electrocardiogramas, registro Holter de 24 h, 6MWT, evaluación clínica y calidad de vida evaluada con el cuestionario Minnesota Living with Heart Failure Questionnaire (MLHFQ). El protocolo del estudio fue aprobado por un consejo de revisión interno, y todos los pacientes dieron su consentimiento informado antes de la inclusión en el estudio.
Evaluación inicialLa evaluación inicial de estos pacientes incluyó una exploración física realizada a todos los pacientes por el mismo médico. En ese momento se obtuvieron datos clínicos y físicos y se determinó la clase de la NYHA con el empleo de la escala de actividad específica de Goldman que es específica para la IC. Se extrajeron muestras de sangre para los análisis de laboratorio tras 12 h de ayuno. Se obtuvieron electrocardiogramas con los pacientes en decúbito supino tras 5 min de reposo. Un mismo operador realizó las ecocardiografías Doppler color bidimensionales a todos los pacientes, la fracción de eyección se calculó con el método de Simpson, y se determinaron los parámetros de modo M clásicos. A continuación, se programó el registro de electrocardiograma Holter. Los aparatos para el registro se colocaron por la mañana y se retiraron a la mañana siguiente. Se indicó a los pacientes que mantuvieran sus actividades diarias y su medicación habitual durante el periodo de registro. La 6MWT la realizó el mismo médico, utilizando un pulsioxímetro digital, en un pasillo de 30 m de largo; se indicaba al paciente que caminara al ritmo más intenso que pudiera durante 6 min, y se determinaba la distancia recorrida por cada paciente. Los pacientes completaron también el cuestionario MLHFQ15.
Procedimiento de la prueba de esfuerzo cardiorrespiratoriaSe realizaron PECR limitadas por los síntomas, utilizando una cinta sin fin, con analizador de gases respiración a respiración (Cortex MetaLyzer 3B; Cortex Biophysik, Leipzig, Alemania) que se calibró con gas antes de cada prueba. Se utilizó un protocolo de rampa para igualar una duración de 8-12 min para la fase de ejercicio. Se registraron electrocardiogramas en reposo y, al menos, a intervalos de 2 min durante el ejercicio. La monitorización electrocardiográfica se mantuvo durante como mínimo 4 min en la fase de recuperación. La presión arterial se verificó en reposo cada minuto durante toda la prueba. Los datos de ventilación obtenidos respiración a respiración se tabularon a intervalos de 10 s. Se determinó la VO2 máxima y la relación de intercambio mediante los valores máximos alcanzados durante la fase de ejercicio. El umbral anaeróbico se determinó con el método de la pendiente V16. La pendiente VE/VCO2 se calculó mediante la ventilación (VE) y la producción de CO2 (VCO2) desde el inicio del ejercicio hasta el momento del ejercicio máximo, según el modelo de regresión lineal (y=mχ+b, donde m=pendiente). Basándonos también en publicaciones previas, se utilizó un valor de corte > 34 para determinar el resultado peor en esa variable9. Los mismos datos de VE y VO2 en ese mismo intervalo se utilizaron para determinar la OUES utilizando ecuaciones logarítmicas publicadas con anterioridad17. Se determinó la recuperación de la frecuencia cardiaca en el primer minuto mediante la diferencia entre: a) frecuencia cardiaca en el momento de ejercicio máximo, y b) frecuencia cardiaca en el primer minuto de recuperación pasiva. Basándonos en publicaciones previas en poblaciones con IC, utilizamos un valor de corte < 16 lpm como marcador de riesgo11. El pulso de oxígeno se calculó mediante el cociente entre la VO2 máxima y la frecuencia cardiaca máxima y se expresó en ml/lat.
Heart Failure Survival ScoreLa HFSS se calculó según lo indicado en la publicación original, utilizando las variables inherentes de cada paciente obtenidas en la visita inicial y en los exámenes basales3, 7.
HFSS=[(0,0216×frecuencia cardiaca en reposo)+(–0,0255×presión arterial media)+(–0,0464×fracción de eyección)+(–0,047×sodio sérico)+(–0,0546×VO2 máxima)+(0,608×presencia de defecto de la conducción interventricular £)+(0,6931×presencia de enfermedad coronaria £)].
£ presente=1 o ausente=0
Análisis estadísticoLos datos se expresaron en forma de media±desviación estándar. Se utilizaron coeficientes de correlación de Pearson para valorar la asociación entre las variables. La población de pacientes se dividió en dos grupos en función de la VO2 máxima (VO2 máxima=12ml/kg/min y VO2 máxima > 12ml/kg/min). Las guías especificas para la IC utilizan este valor como punto de corte de la VO2 máxima indicativo de un peor pronóstico en los pacientes tratados con bloqueadores beta2. Se compararon los valores de HFSS, los resultados de las variables de la PECR, las variables del electrocardiograma, las puntuaciones del MLHFQ y los resultados de la 6MWT en los dos grupos. Se utilizó la prueba de la χ2 para las variables discretas y la prueba de la t de Student para datos no apareados para las variables continuas. La significación estadística se determinó con un valor de p<0,05.
ResultadosCaracterísticas basalesEn la Tabla 1 se presentan las características demográficas, clínicas y de laboratorio de la población. La mayoría de los pacientes eran varones (69%). Además, el 89% de los pacientes recibían tratamiento con inhibidores de la enzima de conversión de la angiotensina o antagonistas de los receptores de la angiotensina II, y un 62% tomaba bloqueadores beta. La media del valor de la HFSS fue 8,75±0,8. De entre las diversas variables de esta puntuación, los valores medios de sodio, presión arterial, fracción de eyección y VO2 máxima fueron los siguientes: 138 mEq/l, 78mmHg, 27,6% y 17,3ml/kg/min, respectivamente. Había un defecto de la conducción intraventricular o un ritmo de marcapasos en 47 pacientes (85%). Ningún paciente presentaba enfermedad coronaria. La media de la distancia recorrida en la 6MWT fue < 400 m. La media del valor obtenido en el MLHFQ fue 38.
Tabla 1. Características basales y medicaciones
| Población total, n | 55 |
| Sexo masculino, n (%) | 38 (69) |
| Edad (años) | 52±9 |
| Clase NYHA, n (%) | |
| I | 0 |
| II | 41 (74) |
| III | 12 (22) |
| IV | 2 (4) |
| Ritmo, n (%) | |
| Sinusal | 40 (73) |
| Fibrilación auricular | 6 (11) |
| Marcapasos | 9 (16) |
| Datos clínicos | |
| Presión sistólica (mmHg) | 104±16 |
| Presión arterial media (mmHg) | 78±13 |
| Frecuencia cardiaca (lpm) | 68±8 |
| IMC | 24±3 |
| Medicación (% que la toma) | |
| IECA | 60 |
| ARA-II | 29 |
| Bloqueadores beta | 62 |
| Diuréticos | 86 |
| Digital | 69 |
| Inhibidor de aldosterona | 74 |
| Datos de laboratorio | |
| Hemoglobina (g/dl) | 14±1 |
| Hematocrito (%) | 42±4 |
| Sodio (mEq/l) | 138±4 |
| Potasio (mEq/l) | 4,5±0,4 |
| Urea (mg/dl) | 46±20 |
| Creatinina (mg/dl) | 1,2±0,3 |
| Puntuación MLHFQ | 38±18 |
| Distancia recorrida en 6 min (m) | 399±102 |
| Duración del QRS (min) | 132±21 |
| BRIH o BRDH o marcapasos (%) | 85 |
| Taquicardia ventricular detectada en Holter (%) | 78 |
| QRS de bajo voltaje (%) | 11 |
| HFSS | 8,75±0,80 (7,05-10,69) |
| Puntuación de Chagas | 13±2 (8-20) |
ARA-II: antagonistas de los receptores de la angiotensina II; BRDH: bloqueo de rama derecha del haz; BRIH: bloqueo de rama izquierda del haz; HFSS: Heart Failure Survival Score; IECA: inhibidor de la enzima de conversión de la angiotensina; IMC: índice de masa corporal; MLHFQ: Minnesota Living with Heart Failure Questionnaire; NYHA: New York Heart Association.
Los datos se expresan en forma de media±desviación estándar (intervalo) o porcentaje, salvo que se indique otra cosa.
Los datos de la ecocardiografía se presentan en la Tabla 2. La media de la fracción de eyección del 27,6% y la media del diámetro de la aurícula izquierda de 44 mm caracterizan a un grupo de pacientes con una disfunción cardiaca grave y una sobrecarga de volumen.
Tabla 2. Valores medios ecocardiográficos en la población total (n=55)
| Variables | Valores medios |
| Fracción de eyección (%) | 27,6±6,6 |
| Diámetro AI (mm) | 44±7 |
| Diámetro telesistólico VI (mm) | 60±9 |
| Diámetro telediastólico VI (mm) | 68±8,7 |
AI: auricular izquierda; VI: ventrículo izquierdo.
Los datos se expresan en forma de media±desviación estándar.
Los datos de PECR se presentan en la Tabla 3. La media de la relación de intercambio fue de 1,08, lo cual es compatible con un ejercicio máximo desde el punto de vista metabólico (relación de intercambio > 1,05). La media de VO2 máxima fue 17,3ml/kg/min, lo cual corresponde a una clasificación de Weber et al18 media de II/IV. La media de la pendiente de VE/VCO2 fue 36 (> 34). La media del porcentaje del pulso de O2 fue del 74%. Es importante señalar que el 61% de los pacientes presentaban una recuperación de la frecuencia cardiaca atenuada, que era < 16 lpm.
Tabla 3. Características generales de las variables de la prueba de esfuerzo cardiorrespiratoria (n=55)
| Variables | Valor |
| VO2 (ml/kg/min) | 17,3±6,2 |
| VO2 absoluta (l/min) | 1,09±0,47 |
| RER | 1,08±0,17 |
| Pendiente de VE/VCO2 | 36±10,6 |
| OUES (l/min) | 0,66±0,27 |
| Pulso de O2 máximo (ml/lat) | 9,3±3,5 |
| Pulso de O2 máximo alcanzado (%) | 74±20 |
| VO2 en el umbral anaeróbico (ml/kg/min) | 11,6±3,4 |
| Recuperación de FC < 16 lpm (%) | 61 |
FC: frecuencia cardiaca; OUES: pendiente de eficiencia de captación de oxígeno; pendiente de VE/VCO2: pendiente de eficiencia ventilatoria de dióxido de carbono; RER: relación de intercambio; VO2: captación de oxígeno máxima.
Los datos se expresan en forma de media±desviación estándar o porcentaje.
En la Tabla 4 se muestran las correlaciones entre la puntuación HFSS y las variables pronósticas de la IC y los correspondientes coeficientes de regresión beta y alfa. La HFSS se asoció a las variables de la PECR (VO2 máxima, VO2 en el umbral anaeróbico, pendiente VE/VCO2 [Figura], OUES y pulso de O2, 6MWT, fracción de eyección, diámetro de aurícula izquierda y puntuación del MLHFQ). En la Tabla 5 se presenta la comparación dentro de cada grupo en cuanto a la VO2 máxima > 12ml/kg/min o VO2 máxima ≤ 12ml/kg/min. Hubo una diferencia significativa entre los grupos en la HFSS, las variables de la PECR, la determinación de la calidad de vida y los resultados de la 6MWT.
Tabla 4. Correlaciones entre variables pronósticas y Heart Failure Survival Score
| Variable | HFSS (correlación de Pearson) | Coeficientes de regresión | |
| α | β (IC95%) | ||
| VO2 (ml/kg/min) | 0,662 a | 7,2 | 0,09 (0,06-0,11) |
| VO2 en el umbral anaeróbico (ml/kg/min) | 0,644 a | 7,0 | 0,15 (0,10-0,20) |
| Pendiente de VE/VCO2 | –0,417 a | 9,9 | –0,03 (–0,05 a –0,01) |
| Pulso de O2 | 0,375 a | 7,9 | 0,08 (0,03-0,14) |
| OUES (l/min) | 0,626 a | 7,5 | 1,8 (1,1-2,4) |
| 6MWT (m) | 0,370 a | 7,6 | 0,003 (0,001-0,005) |
| Fracción de eyección (%) | 0,650 a | 6,5 | 0,08 (0,05-0,1) |
| Diámetro AI (mm) | –0,377 a | 10,7 | –0,04 (–0,07 a –0,10) |
| CdV | –0,283 b | 9,2 | –0,01 (–0,02 a 0) |
6MWT: prueba de distancia recorrida en 6 min; AI: aurícula izquierda; CdV: calidad de vida; HFSS: Heart Failure Survival Score; IC95%: intervalo del confianza del 95%; OUES: pendiente de eficiencia de captación de oxígeno; pendiente de VE/VCO2: pendiente de eficiencia ventilatoria de dióxido de carbono; VO2: captación de oxígeno máxima.
a p<0,01.
b p<0,05.
Tabla 5. Comparación de los grupos en cuanto a la captación de oxígeno máxima
| Variable | VO2 ≤ 12 ml/kg/min (n=9) | VO2 > 12 ml/kg/min (n=46) | p |
| Pendiente VE/VCO2 | 45,3±13 | 34,2±9 | 0,003 |
| RER | 0,94±0,16 | 1,10±0,16 | 0,011 |
| Pulso de O2 (ml/lat) | 6,7±2,6 | 9,9±3,4 | 0,012 |
| VO2 en el umbral anaeróbico (ml/kg/min) | 7,4±1,8 | 12,5±3 | < 0,001 |
| OUES | 0,45±0,23 | 0,71±0,26 | 0,008 |
| Fracción de eyección (%) | 25±4,5 | 28±6,9 | 0,191 |
| 6MWT (m) | 279±66 | 415±96 | 0,002 |
| CdV | 55±13 | 35±17 | 0,002 |
| HFSS | 7,82±0,45 | 8,93±0,73 | 0,001 |
6MWT: prueba de distancia recorrida en 6 min; CdV: calidad de vida; HFSS: Heart Failure Survival Score; OUES: pendiente de eficiencia de captación de oxígeno; pendiente de VE/VCO2: pendiente de eficiencia ventilatoria de dióxido de carbono; RER: relación de intercambio; VO2: captación de oxígeno máxima.
Los datos se expresan en forma de media±desviación estándar.
Nuestro estudio se centró en el análisis de la puntuación HFSS en pacientes con IC y enfermedad de Chagas. Es importante señalar que describimos las correlaciones entre la HFSS y otras variables pronósticas de la IC en una población específica de pacientes con IC por enfermedad de Chagas y disfunción sistólica grave. Nuestra cohorte reflejaba un grupo de pacientes con IC por enfermedad de Chagas sintomáticos graves, con una fracción de eyección media del 27,6% y una media de VO2 máxima de 17,3ml/kg/min. Observamos que la HFSS presentaba una clara asociación con las principales variables pronósticas de la PECR, el electrocardiograma, la 6MWT y el cuestionario. Al estratificar a los pacientes con el empleo de un valor de corte ≤ 12 o > 12ml/kg/min para la VO2 máxima, pudimos poner de manifiesto que los pacientes del grupo con valores inferiores a esa cifra tenían una puntuación de la HFSS significativamente menor.
La HFSS se ha utilizado desde el momento de su publicación para determinar el pronóstico de la IC y ha sido validada en cohortes de pacientes con independencia del sexo, la raza y el uso de bloqueadores beta19, 20, 21. Es también un instrumento aceptado para la toma de decisiones respecto al trasplante de corazón. A pesar de su amplio uso y su divulgación, esta puntuación no ha sido probada todavía en una población con IC por enfermedad de Chagas. Aunque ya existe una puntuación de la IC específica para la enfermedad de Chagas, que incluye todas las formas de cardiopatía chagásica (formas indeterminada, arrítmica y dilatada), no hay una puntuación específica para los pacientes con enfermedad de Chagas que presentan síntomas de IC. Además, dado que la HFSS es una puntuación aceptada ya para otras etiologías, si también puede utilizarse en la IC debida a la enfermedad de Chagas, es posible que facilite el tratamiento de estos pacientes en las clínicas de IC, que generalmente tratan a pacientes con IC de diferentes etiologías.
La población del estudio corresponde a un grupo de los pacientes que se encuentran en los estadios C y D de la IC, según la guía de la American Heart Association1. La mayor parte de los pacientes se encontraban en las clases II y III de la NYHA; esto concuerda con la media de VO2 máxima de 17,3ml/kg/min, que es compatible con una media de clase II/IV en la clasificación de Weber et al18. En estudios previos se ha estratificado el riesgo con el empleo de la HFSS y se han clasificado los grupos como de riesgo alto, medio y bajo con el uso de los siguientes valores de corte: < 7,20, 7,20-8,09 y > 8,093. La media de HFSS de nuestra población fue de 8,75, lo cual corresponde a un grupo de riesgo bajo. Con el uso de valores de corte para la VO2 máxima (< 10, 10-14 y > 14ml/kg/min) según lo determinado por Mancini et al8, el grupo sería un grupo de riesgo bajo, con una estratificación del riesgo similar mediante la VO2 y la HFSS en ese grupo de pacientes con enfermedad de Chagas. Por otra parte, Mady et al22 observaron una tasa de supervivencia de tan sólo un 66% a 1 año en una población con IC por enfermedad de Chagas, con una media de VO2 máxima de 18ml/kg/min. Esto contrasta con la tasa de supervivencia del 94% observada por Mancini et al8 en un grupo general de pacientes con IC con una VO2 máxima > 14ml/kg/min.
Koelling et al21, que analizaron a un grupo de 500 pacientes ambulatorios con IC en la era actual de tratamiento de la IC, con una media de VO2 máxima de 15,7ml/kg/min y una media de la fracción de eyección del 21%, observaron una media de HFSS de 8,01. En comparación con los pacientes del estudio de Koelling et al, los de nuestro análisis tenían mayor prevalencia de defectos de la conducción intraventricular (el 85 frente al 25%). Es de destacar que en el estudio de Koelling et al el 56% de los pacientes presentaban una cardiopatía isquémica, lo cual puede asociarse a una peor HFSS. En estudios previos se ha demostrado que el pronóstico de la cardiopatía de Chagas es peor que el de otras etiologías, incluida la isquémica6, 23. La media de la frecuencia cardiaca en nuestros pacientes fue de 68 lpm, lo cual es inferior a la media de 81 lpm del estudio de Koelling et al, a pesar de que el porcentaje de uso de bloqueadores beta fuera similar (el 62% en nuestra población frente al 59% en la población de Koelling et al). Dadas las características específicas inherentes a la etiología chagásica que están relacionadas, por ejemplo, con el pronóstico y con la frecuencia cardiaca, los valores de corte de la HFSS en este trastorno pueden diferir de los de la población general con IC.
Hemos demostrado que la HFSS, en pacientes con enfermedad de Chagas e IC, se asocia a la capacidad funcional principal y a las variables respiratorias de la PECR, así como a la 6MWT, la fracción de eyección y la calidad de vida. Dado que la VO2 máxima forma parte ya del cálculo de la HFSS, la asociación entre estas variables y las dependientes de la VO2 máxima era previsible. Lo mismo ocurre con la fracción de eyección ventricular izquierda. En los últimos años, múltiples estudios han evidenciado la importancia pronóstica de la pendiente VE/VCO2 en la IC9, 11. Esta variable tiene una significación pronóstica independiente e incluso superior a la de la VO2 máxima. Hay una correlación lineal entre VE y VCO2 durante el ejercicio, ya que el incremento del espacio muerto derivado de la congestión pulmonar conduce a una elevación de VE, que da lugar, a su vez, a un valor más alto de la relación. La significación pronóstica de esta variable se mantiene incluso en presencia de un esfuerzo submáximo. Pudimos demostrar una asociación entre la HFSS y la pendiente VE/VCO2 (Figura). Es importante señalar que, para el cálculo de la HFSS, fueron necesarios datos de variables obtenidas a partir de diferentes pruebas; para el cálculo de la pendiente VE/VCO2, todos los datos proceden de una única PECR. Para el desarrollo de cualquier puntuación en una determinada enfermedad, es necesario disponer de un buen conocimiento de las variables y de su asociación con los resultados clínicos. No siempre se dispone con facilidad de todas las variables en una primera visita, para poder calcular una determinada puntuación. En consecuencia, el conocimiento de las variables individuales, así como de sus correlaciones con puntuaciones bien validadas, es importante y podría facilitar la toma de decisiones, sobre todo si continúa sin disponerse de las variables utilizadas para el cálculo de las puntuaciones en las visitas iniciales.
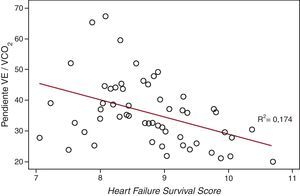
Figura. Gráfico de dispersión de puntos de las correlaciones entre la puntuación Heart Failure Survival Score y la pendiente de eficiencia ventilatoria de dióxido de carbono (pendiente VE/VCO2).
La mortalidad no es el único resultado clínico importante en la IC. La calidad de vida adquiere también un papel importante y relevante. Algunos tratamientos prolongan la vida sin aumentar la calidad de esta. Los investigadores han estudiado la forma en que la calidad de vida está relacionada con las variables funcionales24, 25, 26 y han llegado a conclusiones diversas. No se ha estudiado todavía la relación entre la HFSS y la calidad de vida. En nuestra población, pudimos demostrar una correlación débil pero estadísticamente significativa entre la calidad de vida (evaluada con el MLHFQ) y la HFSS.
Las guías existentes aceptan un valor de VO2 máxima ≤ 12ml/kg/min como criterio para indicar el trasplante de corazón en pacientes con IC sintomáticos que reciben una medicación basada en la evidencia optimizada, incluidos los bloqueadores beta2. En nuestro estudio, basándonos en el valor de VO2 máxima, dividimos a la población en dos grupos de mejor y peor pronóstico, y observamos que las variables funcionales y la calidad de vida diferían en los grupos de la misma manera en que difería la HFSS en cuanto a la significación estadística de la comparación. La media de la HFSS en el grupo con una VO2 máxima ≤ 12ml/kg/min fue de 7,82, lo cual corresponde a una HFSS de riesgo intermedio. La media de distancia recorrida en la 6MWT y el valor de la pendiente VE/VCO2 en el grupo de ≤ 12ml/kg/min (279 m y 45,3, respectivamente) correspondieron a un riesgo alto (< 300 m)13 y a una clase respiratoria IV en la valoración de la pendiente VE/VCO2 (pendiente VE/VCO2 > 44)11.
LimitacionesNuestro estudio tiene ciertas limitaciones. En primer lugar, el tamaño muestral es pequeño. En segundo lugar, el estudio se llevó a cabo en un solo centro. En tercer lugar, no obtuvimos datos sobre la función ventricular derecha, que se ha demostrado que tiene utilidad para la predicción de la capacidad funcional en los pacientes chagásicos27; así pues, no se pudo evaluar las posibles correlaciones entre la HFSS y la función ventricular derecha en esta población. Por último, no disponemos de datos de resultados clínicos que permitan evaluar la correlación entre las variables cardiorrespiratorias o ecocardiográficas y la evolución clínica.
ConclusionesEn los pacientes con enfermedad de Chagas e IC, la puntuación HFSS mostró buena correlación con las principales variables pronósticas de las pruebas funcionales, pero tuvo una correlación débil con la calidad de vida. Tal como se esperaba, los pacientes con valores de clase funcional inferiores presentaron una HFSS más baja. La HFSS podría ser un instrumento útil para la evaluación pronóstica en la IC debida a enfermedad de Chagas. Serán necesarios estudios longitudinales con un seguimiento clínico para determinar mejor los valores de corte de la HFSS para la toma de decisiones en esta población específica.
FinanciaciónEste estudio se financió en su totalidad por el Ministerio de Salud de Brasil, la Fundación de Apoyo a la Investigación del estado de Bahía y el Instituto Brasileño de Investigación Clínica de São Paulo, Brasil.
Conflicto de interesesNinguno.
Recibido 20 Octubre 2011
Aceptado 22 Diciembre 2011
Autor para correspondencia: Duke Clinical Research Institute, Box 3850, 2400 Pratt Street, Room 0311, Terrace Level, Durham, NC 27705, Estados Unidos. renato.lopes@duke.edu