Este artículo presenta las características y los resultados del trasplante cardiaco en España desde que empezó su actividad en mayo de 1984.
MétodosSe realiza un análisis descriptivo de las características de receptores, donantes, procedimiento quirúrgico y resultados de los trasplantes cardiacos realizados en España hasta el 31 de diciembre de 2012.
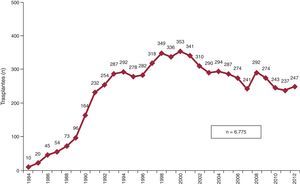
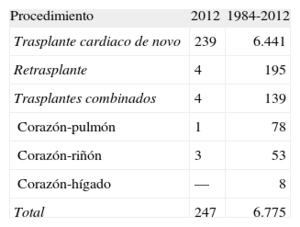
ResultadosDurante 2012 se han realizado 247 procedimientos, con lo que en la serie histórica constan 6.775 trasplantes. En los últimos años, se observa un empeoramiento del perfil clínico tanto de los receptores (el 34% mayores de 60 años, el 22% con insuficiencia renal grave, el 17% con diabetes mellitus insulinodependiente, el 29% con cirugía cardiaca previa y el 16% con ventilación mecánica), como de los donantes (el 38% mayores de 45 años y el 26% con discordancia de peso >20%) y del procedimiento (el 29% con tiempo de isquemia >4 h y el 36% en procedimientos urgentes). La supervivencia a 1, 5, 10 y 15 años ha sido del 78, el 67, el 53 y el 38% respectivamente. Estas cifras permanecen estables desde 1995.
ConclusionesLa actividad del trasplante cardiaco en España permanece estable en los últimos años, con alrededor de 250 procedimientos al año. A pesar del claro empeoramiento en las características de donantes, receptores y tiempos quirúrgicos, se mantienen unos resultados en mortalidad comparables a los de nuestro entorno.
Palabras clave
Desde 1991, el Registro Español de Trasplante Cardiaco (RETC) viene publicando la descripción de las características clínicas y quirúrgicas y los resultados generales de los procedimientos de trasplante cardiaco que se realizan en España (anexo)1–23. El presente artículo describe dichos datos, que incluyen a los pacientes trasplantados hasta el 31 de diciembre de 2012. La mayor fortaleza del RETC es que incluye prácticamente todos los procedimientos de trasplante cardiaco realizados en todos los hospitales de nuestro país desde mayo de 1984, independientemente de sus características y resultados. Además, la recogida de datos se realiza prospectivamente de acuerdo con una base de datos común, consensuada por todos los grupos.
MÉTODOSPacientes y centrosDe los 19 centros que han aportado datos al RETC, actualmente permanecen activos 18 (tabla 1). El número de procedimientos realizados anualmente se resume en la figura 1. Hay que destacar que, de la serie total, el RETC no dispone de información de 14 pacientes, motivo por el que los datos de este trabajo se refieren a un total de 6.761 pacientes. Los tipos de procedimientos realizados en 2012 y en la serie total se resumen en la tabla 2.
Centros participantes (por orden de realización del primer trasplante) en el Registro Español de Trasplante Cardiaco (1984-2012)
| 1. | Hospital de la Santa Creu i Sant Pau, Barcelona |
| 2. | Clínica Universitaria de Navarra, Pamplona |
| 3. | Clínica Puerta de Hierro, Majadahonda |
| 4. | Hospital Marqués de Valdecilla, Santander |
| 5. | Hospital Reina Sofía, Córdoba |
| 6. | Hospital Universitario y Politécnico La Fe, Valencia |
| 7. | Hospital Gregorio Marañón, Madrid |
| 8. | Fundación Jiménez Díaz, Madrid* |
| 9. | Hospital Virgen del Rocío, Sevilla |
| 10. | Hospital 12 de Octubre, Madrid |
| 11. | Hospital Universitario de A Coruña, A Coruña |
| 12. | Hospital de Bellvitge, L’Hospitalet de Llobregat |
| 13. | Hospital La Paz, Madrid |
| 14. | Hospital Central de Asturias, Oviedo |
| 15. | Hospital Clínic, Barcelona |
| 16. | Hospital Virgen de la Arrixaca, El Palmar |
| 17. | Hospital Miguel Servet, Zaragoza |
| 18. | Hospital Clínico, Valladolid |
| 19. | Hospital Vall d’Hebron, Barcelona |
La base de datos consta de 175 variables clínicas, preestablecidas de manera consensuada por todos los grupos, que recogen datos de receptor, donante, técnica quirúrgica, inmunosupresión y seguimiento. La principal novedad de este año es la puesta en marcha de una herramienta en la web que permite la introducción directa de los datos y su actualización online. El soporte de la base de datos es un archivo de Microsoft Excel. Este procedimiento sustituye al anterior, en el que cada centro enviaba los datos al director del registro en formato de Microsoft Access mediante correo electrónico. El mantenimiento de la base de datos, el control de calidad y el análisis estadístico están contratados con una CRO (contract research organisation) externa: actualmente ODDS, SL.
La aprobación por el comité ético, la auditoría y el registro en el Ministerio de Sanidad, Servicios Sociales e Igualdad se han realizado según lo dispuesto en la Ley Orgánica de Protección de Datos 15/1999.
Análisis estadísticoLas variables se presentan como media±desviación estándar y porcentaje. Los resultados se categorizan por el año del trasplante, dividiendo la muestra total en seis grupos de 5 años (excepto el último, de 2009-2012, que solo incluye cuatro). Las curvas de supervivencia se han calculado mediante el test de Kaplan-Meier y la comparación entre ellas, con el método de log rank test. Los análisis, a no ser que se indique lo contrario, se refieren a toda la serie, incluidos retrasplantes y trasplantes combinados. Se ha considerado diferencia significativa si p<0,05.
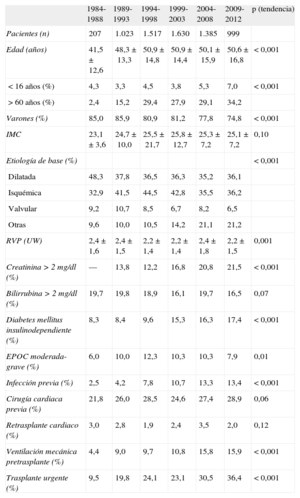
RESULTADOSCaracterísticas de los receptoresEn 2012, la edad de los receptores era de 52±15 años y el 82% eran varones, con diagnósticos basales mayoritarios de miocardiopatía isquémica (30,9%) y dilatada idiopática (24,8%). Las características de los pacientes trasplantados se resumen en la tabla 3 y se muestran por cuatrienios. En el último periodo, destaca que más de un tercio de los receptores eran mayores de 60 años y el porcentaje de mujeres supera el 25%. Se constata asimismo un incremento en condiciones de riesgo, como son disfunción renal, diabetes mellitus, infección en los 15 días previos al trasplante y necesidad de ventilación mecánica previa al trasplante. El porcentaje de procedimientos urgentes ha ido creciendo hasta llegar al 36% actual. El retrasplante, en cambio, ha permanecido estable en alrededor del 3%.
Características del receptor en el Registro Español de Trasplante Cardiaco (1984-2012)
| 1984-1988 | 1989-1993 | 1994-1998 | 1999-2003 | 2004-2008 | 2009-2012 | p (tendencia) | |
| Pacientes (n) | 207 | 1.023 | 1.517 | 1.630 | 1.385 | 999 | |
| Edad (años) | 41,5±12,6 | 48,3±13,3 | 50,9±14,8 | 50,9±14,4 | 50,1±15,9 | 50,6±16,8 | <0,001 |
| <16 años (%) | 4,3 | 3,3 | 4,5 | 3,8 | 5,3 | 7,0 | <0,001 |
| >60 años (%) | 2,4 | 15,2 | 29,4 | 27,9 | 29,1 | 34,2 | |
| Varones (%) | 85,0 | 85,9 | 80,9 | 81,2 | 77,8 | 74,8 | <0,001 |
| IMC | 23,1±3,6 | 24,7±10,0 | 25,5±21,7 | 25,8±12,7 | 25,3±7,2 | 25,1±7,2 | 0,10 |
| Etiología de base (%) | <0,001 | ||||||
| Dilatada | 48,3 | 37,8 | 36,5 | 36,3 | 35,2 | 36,1 | |
| Isquémica | 32,9 | 41,5 | 44,5 | 42,8 | 35,5 | 36,2 | |
| Valvular | 9,2 | 10,7 | 8,5 | 6,7 | 8,2 | 6,5 | |
| Otras | 9,6 | 10,0 | 10,5 | 14,2 | 21,1 | 21,2 | |
| RVP (UW) | 2,4±1,6 | 2,4±1,5 | 2,2±1,4 | 2,2±1,4 | 2,4±1,8 | 2,2±1,5 | 0,001 |
| Creatinina >2 mg/dl (%) | — | 13,8 | 12,2 | 16,8 | 20,8 | 21,5 | <0,001 |
| Bilirrubina >2 mg/dl (%) | 19,7 | 19,8 | 18,9 | 16,1 | 19,7 | 16,5 | 0,07 |
| Diabetes mellitus insulinodependiente (%) | 8,3 | 8,4 | 9,6 | 15,3 | 16,3 | 17,4 | <0,001 |
| EPOC moderada-grave (%) | 6,0 | 10,0 | 12,3 | 10,3 | 10,3 | 7,9 | 0,01 |
| Infección previa (%) | 2,5 | 4,2 | 7,8 | 10,7 | 13,3 | 13,4 | <0,001 |
| Cirugía cardiaca previa (%) | 21,8 | 26,0 | 28,5 | 24,6 | 27,4 | 28,9 | 0,06 |
| Retrasplante cardiaco (%) | 3,0 | 2,8 | 1,9 | 2,4 | 3,5 | 2,0 | 0,12 |
| Ventilación mecánica pretrasplante (%) | 4,4 | 9,0 | 9,7 | 10,8 | 15,8 | 15,9 | <0,001 |
| Trasplante urgente (%) | 9,5 | 19,8 | 24,1 | 23,1 | 30,5 | 36,4 | <0,001 |
EPOC: enfermedad pulmonar obstructiva crónica; IMC: índice de masa corporal; RVP: resistencias vasculares pulmonares.
Salvo otra indicación, los datos expresan media ± desviación estándar.
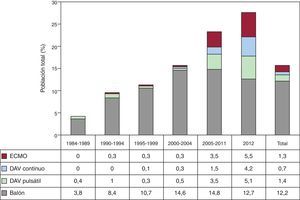
Desde 2004 se aprecia un aumento constante en el uso de soporte circulatorio mecánico más allá del tradicional balón intraaórtico de contrapulsación. En 2012 se ha utilizado oxigenación con membrana extraorpórea en el 5,5%, dispositivos de asistencia ventricular continua en el 4,2% y pulsátil en el 5,1%. Por lo tanto, en este último año, el uso de estos dispositivos (14,8%) ha superado al de balón de contrapulsación como método único de asistencia (12,7%). La distribución de los procedimientos de asistencia ventricular por periodos se muestra en la figura 2.
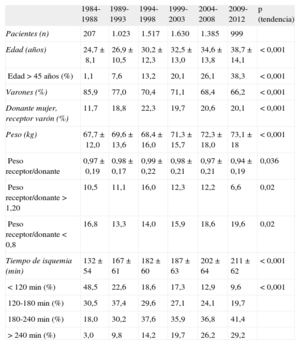
Características de los donantes y tiempo de isquemiaEn 2012, la media de edad de los donantes fue 39,7±13,4 años (el 41,3% mayores de 45 años), y el 71,0% eran varones. En el 19,5% de los casos, el peso del donante era un 20% mayor que el del receptor, y lo contrario sucedía en el 8,7%. En el 19,5% de los casos, un varón recibió el injerto de una donante.
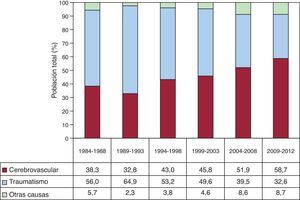
Las características de los donantes se resumen en la tabla 4 y las causas de muerte del donante, en la figura 3. En los periodos descritos se aprecia un incremento de los accidentes cerebrovasculares como principal causa de muerte, en contraposición a los traumatismos craneoencefálicos.
Características del donante y tiempo de isquemia en el Registro Español de Trasplante Cardiaco (1984-2012)
| 1984-1988 | 1989-1993 | 1994-1998 | 1999-2003 | 2004-2008 | 2009-2012 | p (tendencia) | |
| Pacientes (n) | 207 | 1.023 | 1.517 | 1.630 | 1.385 | 999 | |
| Edad (años) | 24,7±8,1 | 26,9±10,5 | 30,2±12,3 | 32,5±13,0 | 34,6±13,8 | 38,7±14,1 | <0,001 |
| Edad >45 años (%) | 1,1 | 7,6 | 13,2 | 20,1 | 26,1 | 38,3 | <0,001 |
| Varones (%) | 85,9 | 77,0 | 70,4 | 71,1 | 68,4 | 66,2 | <0,001 |
| Donante mujer, receptor varón (%) | 11,7 | 18,8 | 22,3 | 19,7 | 20,6 | 20,1 | <0,001 |
| Peso (kg) | 67,7±12,0 | 69,6±13,6 | 68,4±16,0 | 71,3±15,7 | 72,3±18,0 | 73,1±18 | <0,001 |
| Peso receptor/donante | 0,97±0,19 | 0,98±0,17 | 0,99±0,22 | 0,98±0,21 | 0,97±0,21 | 0,94±0,19 | 0,036 |
| Peso receptor/donante >1,20 | 10,5 | 11,1 | 16,0 | 12,3 | 12,2 | 6,6 | 0,02 |
| Peso receptor/donante <0,8 | 16,8 | 13,3 | 14,0 | 15,9 | 18,6 | 19,6 | 0,02 |
| Tiempo de isquemia (min) | 132±54 | 167±61 | 182±60 | 187±63 | 202±64 | 211±62 | <0,001 |
| <120min (%) | 48,5 | 22,6 | 18,6 | 17,3 | 12,9 | 9,6 | <0,001 |
| 120-180min (%) | 30,5 | 37,4 | 29,6 | 27,1 | 24,1 | 19,7 | |
| 180-240min (%) | 18,0 | 30,2 | 37,6 | 35,9 | 36,8 | 41,4 | |
| >240min (%) | 3,0 | 9,8 | 14,2 | 19,7 | 26,2 | 29,2 |
Salvo otra indicación, los datos expresan media ± desviación estándar.
El tiempo de isquemia se ha ido incrementando en la serie temporal, de tal manera que en el periodo 2009-2012 excede en casi 1.30 h el tiempo en el periodo inicial 1984-1988. En el periodo más reciente, casi un tercio de los procedimientos tienen un tiempo de isquemia >4 h (tabla 4).
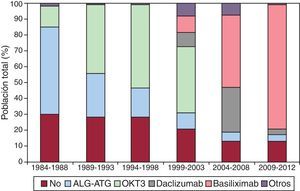
InmunosupresiónEn 2012, el 87,3% de los receptores recibieron algún tratamiento inmunosupresor de inducción, en su inmensa mayoría (85,2%) basiliximab. En la figura 4 se aprecia que la inducción ha ido incrementándose hasta su uso casi generalizado actual. En la época más reciente, se induce a más del 80% de los pacientes con inhibidores de la interleucina 2 (basiliximab o daclizumab, fundamentalmente el primero).
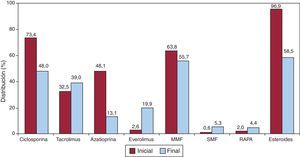
En 2012, la inmunosupresión de inicio se realizó mayoritariamente con tacrolimus (75,9%) como inhibidor de la calcineurina, micofenolato mofetilo (94,9%) como antiproliferativo y esteroides (96,4%). En la figura 5 se resumen los fármacos usados en la inmunosupresión inicial y al final del seguimiento en toda la serie. En un seguimiento promedio de 6,7 años, el 58% de los pacientes continuaban en tratamiento con corticoides. Como se puede apreciar, el uso de tacrolimus tiende a igualarse con el de ciclosporina, la azatioprina mantiene un uso apenas testimonial y, llamativamente, casi un cuarto de los pacientes están en tratamiento con inhibidores de la m-TOR (everolimus o sirolimus) en el último seguimiento.
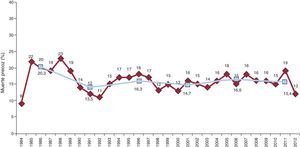
SupervivenciaEn la figura 6 se resume la evolución de la mortalidad quirúrgica (primeros 30 días tras la cirugía) por años y por quinquenios. En 2012 fue del 12%, ligeramente inferior a la de la cohorte histórica, que oscila, con leves variaciones, entre el 15 y el 16%.
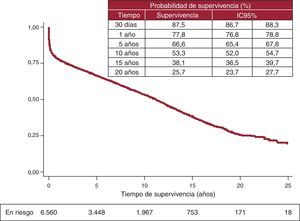
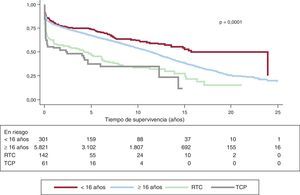
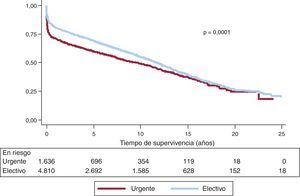
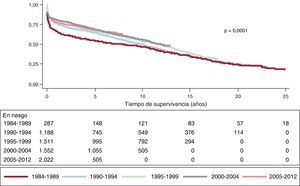
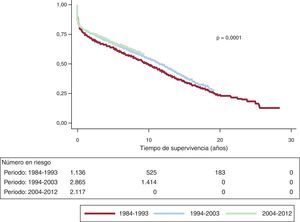
La supervivencia actuarial en el conjunto de la serie al mes y a 1, 5, 10, 15 y 20 años se resume en la figura 7. Esto supone una mortalidad anual promedio de un 2-3% aproximadamente, con una mediana de supervivencia de 11,2 años. Hubo diferencias significativas por edad y tipo de procedimiento. Así, la supervivencia fue significativamente peor para los pacientes retrasplantados y los trasplantes cardiopulmonares respecto a los primeros trasplantes, tanto en la edad adulta como en receptores de menos de 16 años (fig. 8). De igual manera, se detectan diferencias significativas entre trasplantes urgentes y electivos (fig. 9) y según el periodo en el que se realiza el procedimiento (fig. 10). De esta figura se puede inferir que los resultados mejoraron ostensiblemente a partir de 1994, fundamentalmente a expensas de una mejora de la supervivencia al primer año, que pasó del 73% en el periodo anterior a 1994 al 78% después (fig. 11).
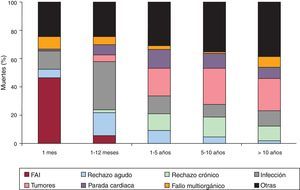
Las causas de fallecimiento cambian según el periodo postrasplante que se considere (fig. 12). En el primer mes postrasplante, casi el 50% de los fallecimientos se producen por fallo primario del injerto. Después del primer mes y hasta cumplir el primer año, el rechazo agudo y, sobre todo, las infecciones son la principal causa de muerte. Después del primer año, la causa mayoritaria son los tumores y las distintas manifestaciones de la enfermedad vascular del injerto (rechazo crónico, muerte súbita).
DISCUSIÓNEl RETC cuenta ya casi un cuarto de siglo de vida y ha sufrido un aumento de volumen, consecuencia del aumento del número de centros trasplantadores y de la acumulación de los procedimientos realizados, y sobre todo de la complejidad. La gran fortaleza del RETC es haber conseguido el registro de todos los trasplantes cardiacos realizados en España desde el primer procedimiento en 1984 y haberse adaptado a los cambios en el procedimiento y el conocimiento de este con el correr del tiempo. En última instancia, el esfuerzo continuo de todos los programas españoles ha hecho posible implementar este año el uso de una aplicación online que permite la actualización en tiempo real de los datos del RETC. Esto constituirá indudablemente un instrumento muy importante para mejorar la calidad y la productividad del RETC. La puesta en común de manera estandarizada de datos prospectivamente consensuados resulta un instrumento de investigación y sobre todo clínico de primera magnitud. Esto es particularmente cierto en casos como el del trasplante cardiaco en España, un procedimiento de implantación dispersa (actualmente hay programas en 18 centros) y, en consecuencia, con bajo volumen por centro. Parece obvio que solo el análisis conjunto de los datos puede garantizar un mínimo de consistencia en los hallazgos.
En 2012 se han realizado 247 trasplantes, un número que está en línea con los realizados en los últimos años. El descenso del número de trasplantes que se evidencia después de las cifras máximas de finales de los años noventa es un fenómeno común al ámbito europeo24. Probablemente las causas sean multifactoriales y complejas. Sin duda incluyen la escasez de donantes óptimos, principalmente provenientes de los accidentes de tráfico, y la mejora del pronóstico de las cardiopatías más frecuentes, secundaria a la madurez de los tratamientos farmacológicos e instrumentales, que tomaron carta de naturaleza en la década inmediatamente anterior y retrasan la necesidad de trasplante.
El análisis de las tendencias temporales de las características del trasplante puede arrojar luz sobre los cambios en la práctica clínica a lo largo del tiempo. En primer lugar, nuestros datos muestran un progresivo empeoramiento del perfil clínico del receptor. En los últimos 5-10 años ha aumentado el porcentaje de pacientes añosos, con peor función renal, más diabetes mellitus insulinodependiente y en ventilación mecánica. Todos estos son factores de reconocida incidencia en el pronóstico a corto y largo plazo24. Asimismo, van aumentando los procedimientos realizados con carácter de urgencia, que llegan casi al 40% en los últimos 4 años. Solo se puede especular sobre las causas de estas tendencias. Por una parte, el aumento de la experiencia de los programas puede llevar a asumir mayores riesgos derivados de la inclusión de pacientes con peor perfil clínico. Por otra, el drástico avance en el tratamiento médico e instrumental de las cardiopatías en las últimas dos décadas ha posibilitado un pronóstico similar al del trasplante hasta estadios funcionales relativamente avanzados25, lo que aconseja en términos generales retrasar la inclusión de los pacientes en lista de espera y la realización del trasplante.
De manera similar, es posible detectar una progresiva ampliación de los criterios de donación, como parece derivarse del significativo aumento en la media de edad de los donantes y el porcentaje de donantes añosos (> 45 años) así como de los donantes fallecidos por accidente cerebrovascular, con frecuencia asociado a mayor incidencia de arteriosclerosis. Probablemente esta tendencia refleje la lucha de los programas contra la creciente escasez de donación considerada óptima.
La misma tendencia descrita para el perfil del receptor y el donante se observa para el procedimiento quirúrgico, como parece indicar la prolongación progresiva en el tiempo de isquemia. Es llamativo que en los últimos 4 años se trasplantara hasta a un 29% de los pacientes con tiempos de isquemia >4 h, tiempo que se considera el límite para asegurar la adecuada viabilidad del injerto. Hasta la fecha, es difícil achacar estos retrasos al deterioro progresivo en las condiciones logísticas del procedimiento, al menos en general. Detrás de ello podría estar la cada vez mayor disposición a aceptar órganos de referencias lejanas, sobre todo en el contexto del trasplante urgente, y la incidencia que pudiera tener la realización de trasplantes en pacientes portadores de mecanismos de soporte circulatorio a medio-largo plazo, que en ocasiones conllevan un procedimiento quirúrgico menos predecible.
A pesar de todo lo anterior, los resultados generales en mortalidad después de transcurrido el primer decenio de actividad (1984-1994), que podríamos calificar como fundacional, se mantienen relativamente estables y pueden compararse favorablemente con los publicados en el registro internacional24. No obstante, en general la mortalidad quirúrgica se ha mantenido relativamente elevada, lo que constituye un objetivo claro de mejora. Habrá que ver si en los próximos años se confirma una tendencia positiva en dicha mortalidad como la que parece observarse en 2012.
Probablemente, la novedad más llamativa en los últimos 5 años sea el uso cada vez mayor de dispositivos de soporte circulatorio antes del trasplante, que ya en 2012 han superado en porcentaje al tradicional balón de contrapulsación intraaórtico. España se ha incorporado muy tarde al uso de estos dispositivos respecto a otros países, muy probablemente por razones logísticas en gran parte, pero no siempre, derivadas de limitaciones económicas. Todavía es pronto para evaluar el impacto de estos dispositivos tanto en el reclutamiento de posibles receptores de trasplante como en las condiciones en que llegue el receptor al procedimiento y, por lo tanto, el pronóstico. La implementación de estas complejas técnicas tiene que superar una curva de aprendizaje relacionada con, primero, la adecuada selección de los pacientes subsidiarios de estas técnicas; segundo, su manejo en estas particulares circunstancias clínicas, y tercero, el establecimiento del momento idóneo para realizar el trasplante después de su implantación. Es esperable que el esfuerzo individual y la puesta en común del conocimiento generado en los distintos centros a través del soporte del RETC conlleve una mejora en los resultados los próximos años. Además, es previsible que la mayor utilización del uso del soporte circulatorio conlleve cambios en los criterios de selección para el trasplante de urgencia, un aspecto en continua evolución y cambio que tiene profundas repercusiones en la política de asignación de injertos.
También se detectan cambios temporales en la inmunosupresión. Actualmente se ha generalizado la inducción, fundamentalmente con el uso de inhibidores de la interleucina 2 y particularmente basiliximab. Estos son potentes inductores que permiten retrasar la introducción de los inhibidores de la calcineurina, una práctica cada vez más extendida en el contexto de la insuficiencia renal peritrasplante. A esto se une una excelente tolerabilidad clínica, en contraposición con fármacos ya obsoletos como el OKT3. Actualmente la inmunosupresión de inicio sigue basándose en la triple terapia tradicional, si bien se observa un cambio definitivo en los inhibidores de la calcineurina hacia el tacrolimus y en los antiproliferativos hacia el micofenolato mofetilo, en detrimento de la ciclosporina y la azatioprina, respectivamente. Por otra parte, el uso de inhibidores de la m-TOR (sirolimus y, sobre todo, everolimus) ha aumentado hasta alcanzar actualmente en total al 23% de los pacientes, lo que se enmarca en la cada vez más frecuente individualización de la inmunosupresión con objeto de preservar la función renal y prevenir la enfermedad vascular del injerto y las neoplasias postrasplante.
CONCLUSIONESEl trasplante cardiaco es actualmente una técnica terapéutica bien establecida para pacientes seleccionados con insuficiencia cardiaca en estadios avanzados y no candidatos a otros tratamientos. A pesar de que el contexto clínico en el que se utiliza ha ido progresando hacia entornos cada vez más complejos, los resultados siguen manteniéndose dentro de los estándares internacionales, aunque hay aspectos potencialmente mejorables, como la mortalidad perioperatoria y la adecuación de la inmunosupresión y el cuidado a largo plazo para la prevención de las principales causas de mortalidad, como neoplasias, enfermedad vascular del injerto, infecciones e insuficiencia renal. En los próximos años habrá que continuar con el esfuerzo por incorporar de manera efectiva y eficiente la utilización preoperatoria y postoperatoria de dispositivos de soporte circulatorio en el manejo habitual de los pacientes susceptibles de trasplante cardiaco.
FINANCIACIÓNEl RETC está parcialmente financiado por una beca no condicionada de Novartis.
CONFLICTO DE INTERESESF. González-Vílchez: remuneración por desarrollo de ponencias: Astellas, Novartis, Roche, Pfizer. Gastos de viaje, alojamiento o asistencia a reuniones: Roche, Astellas, Novartis.
Agradecemos el soporte estadístico realizado por ODDS, SL.
| Clínica Universitaria Puerta de Hierro, Majadahonda, Madrid | Javier Segovia-Cubero, Inés Sayado y Luis Alonso-Pulpón |
| Hospital Universitario y Politécnico La Fe, Valencia | Luis Martínez-Dolz, Ignacio Sánchez-Lázaro y Mónica Cebrián |
| Hospital Universitario de A Coruña, A Coruña | Maria J. Paniagua-Martín, Raquel Marzoa-Rivas y Eduardo Barge-Caballero |
| Hospital Universitario Reina Sofía, Córdoba | Amador López-Granados y Juan Carlos Castillo-Dieguez |
| Hospital Universitario Marqués de Valdecilla, Santander | Manuel Cobo-Belaustegui, Miguel Llano-Cardenal, Jose A. Vázquez de Prada |
| Hospital Gregorio Marañón (adultos), Madrid | Jesús Palomo, Adolfo Villa, Juan Fernández-Yáñez, Iago Sousa y Pablo Díez |
| Hospital Universitario 12 de Octubre, Madrid | Maria J. Ruiz, Pilar Escribano, Miguel A. Gómez, Marta Paradina |
| Hospital de la Santa Creu i Sant Pau, Barcelona | Vicenç Brosa, Sonia Mirabet, Laura López y Josep Padró |
| Hospital Universitario Virgen del Rocío, Sevilla | Jose Manuel Sobrino, Alejandro Adsuar |
| Hospital Universitario de Bellvitge, L’Hospitalet de Llobregat, Barcelona | Josep Roca-Elías, José González-Costello, Joel Salazar-Mendiguchía |
| Clínica Universitaria de Navarra, Pamplona | Beltrán Levy, Rafael Hernández |
| Hospital Clínic Universitari, Barcelona | Monserrat Cardona, Marta Farrero, M. Ángeles Castel |
| Hospital Universitario Central de Asturias, Oviedo | Beatriz Díez de Molina |
| Hospital Universitario Gregorio Marañón (niños), Madrid | Constancio Medrano |
| Hospital Universitario Virgen de la Arrixaca, El Palmar, Murcia | Iris Garrido |
| Hospital Universitario Miguel Servet, Zaragoza | María L. Sanz-Julvé, Ana Portolés |
| Hospital Clínico Universitario, Valladolid | Javier López-Díaz, Amada Recio |
| Hospital Universitario La Paz, Madrid | Daniel Borches, Luz Polo, Carlos Labrandero, Lucía Deiros |
| Hospital Universitario Vall d’Hebron, Barcelona | Ferrán Gran, Raúl Abella |
Colaboradores: Gregorio Rábago, Félix Pérez-Villa, José L. Lambert, Manuela Camino, Domingo Pascual, María T. Blasco, Luis de la Fuente, Luis García-Guereta y Dimpna C. Albert.