Se describen los resultados en España de la segunda encuesta de la Sociedad Europea de Cardiología sobre terapia de resincronización cardiaca (CRT-Survey II) y se comparan con los de los demás países participantes.
MétodosPacientes a los que se implantó un dispositivo de terapia de resincronización cardiaca entre octubre de 2015 y diciembre de 2016 en 36 centros participantes. Se recogieron datos sobre las características basales de los pacientes y del implante, y un seguimiento a corto plazo hasta el alta hospitalaria.
ResultadosLa tasa de éxito del implante fue del 95,9%. La mediana [intervalo intercuartílico] de implantes anuales/centro en España fue significativamente menor que en los demás países participantes: 30 [21-50] frente a 55 [33-100] implantes/año (p=0,00003). En los centros españoles hubo una menor proporción de pacientes de edad ≥ 75 años (el 27,9 frente al 32,4%; p=0,0071), una mayor proporción de pacientes en clase funcional II de la New York Heart Association (el 46,9 frente al 36,9%; p <0,00001) y un mayor porcentaje de pacientes con criterios electrocardiográficos de bloqueo de rama izquierda (el 82,9 frente al 74,6%; p <0,00001). La media de la estancia hospitalaria fue menor en los centros españoles (5,8±8,5 frente a 6,4±11,6; p <0,00001) y una mayor proporción de pacientes recibieron un cable de ventrículo izquierdo cuadripolar (el 74 frente al 56%; p <0,00001) y fueron seguidos a distancia (el 55,8 frente al 27,7%; p <0,00001).
ConclusionesLa encuesta CRT-Survey II muestra que en España hay una menor proporción de pacientes de 75 o más años que reciben un dispositivo de terapia de resincronización cardiaca, una mayor proporción de pacientes en clase funcional II de la New York Heart Association, con bloqueo completo de la rama izquierda del haz de His y con seguimiento a distancia, con estancias hospitalarias significativamente menores.
Palabras clave
Se ha demostrado que la terapia de resincronización cardiaca (TRC) reduce la morbimortalidad de los pacientes con insuficiencia cardiaca sintomática, fracción de eyección reducida y QRS ancho adecuadamente seleccionados1–7. Por este motivo, las guías de práctica clínica tanto europeas como de otros países recogen las indicaciones de esta terapia basándose en una evidencia sólida y otorgándoles niveles altos de recomendación8–11.
La evidencia científica disponible sobre la TRC proviene tanto de ensayos clínicos aleatorizados como de estudios observacionales y registros. Los ensayos clínicos aleatorizados han sido diseñados para dar respuesta a preguntas concretas, adecuadamente preespecificadas en su protocolo, y cuentan con unos criterios de inclusión y exclusión estrictos. Esto hace que los resultados de dichos estudios puedan ser aplicables únicamente a la población específicamente incluida en el estudio. Por el contrario, los datos provenientes de registros y encuestas reflejan la realidad de la práctica clínica diaria y ofrecen una visión real sobre el uso y el beneficio de una determinada medicación o dispositivo12.
Los resultados de la primera edición de la encuesta de la Sociedad Europea de Cardiología (ESC) sobre terapia de resincronización cardiaca (CRT-Survey I), realizada entre 2008-2009 en 13 países miembros de la ESC, mostraron que la TRC se estaba aplicando a un espectro de población muy amplio, que no estaba adecuadamente representado en los ensayos clínicos aleatorizados publicados hasta ese momento13. Esta población escasamente representada en los grandes ensayos clínicos incluía a pacientes de edad> 75 años, pacientes con QRS estrecho, pacientes con fibrilación auricular y pacientes en los que se realizaba un procedimiento de upgrade desde un marcapasos convencional o desde un desfibrilador automático implantable. Además de esto, la CRT-Survey I mostró una amplia variedad regional y nacional en cuanto a las prácticas habituales de implante de TRC. Desde la publicación de esta primera encuesta, se han introducido importantes novedades en las guías ESC de práctica clínica en lo concerniente a la TRC tanto por la Heart Failure Association(HFA) como por la European Heart Rhythm Association (EHRA)8,9. Con estos antecedentes, ambas asociaciones decidieron llevar a cabo una segunda edición de la ESC-CRT-Survey. El objetivo es proporcionar una visión sobre la práctica clínica contemporánea que sea útil para pacientes, médicos, gestores, industria farmacéutica y fabricantes de dispositivos. Se presentan los resultados en España de la CRT-Survey II y se comparan con los obtenidos en los otros países participantes.
MÉTODOSDiseño de la encuesta y Comité CientíficoLa encuesta se ha diseñado como una iniciativa conjunta de la HFA y la EHRA14. El diseño de la CRT-Survey II así como el contenido detallado del cuaderno de recogida de datos electrónico se han publicado previamente14.
Cada país participante miembro de la ESC estuvo representado por un coordinador nacional nombrado por el presidente de la correspondiente sociedad nacional de cardiología. El coordinador nacional se encargó de obtener la aprobación en el comité ético en caso necesario, reclutar a los centros participantes y distribuir la información del comité científico a todos los participantes. En el caso de España, se invitó a un total de 54 hospitales, de los que finalmente 36 participaron activamente en la encuesta e incluyeron al menos a 1 paciente.
Población del estudio y periodo de inclusión de pacientesEn el estudio se incluyó a cualquier paciente de los 36 hospitales españoles participantes seleccionado para implante de un dispositivo, ya fuera TRC con marcapasos o con desfibrilador. Se incluyó a los pacientes tanto si el implante fue exitoso como si no, y se incluyeron tanto primoimplantes como procedimientos de upgrading desde un marcapasos previo o un desfibrilador automático implantable previo. Se excluyeron del estudio tanto los recambios de generador como las revisiones quirúrgicas de dispositivos previamente implantados, ya que la encuesta se diseñó para incluir los implantes de nuevos dispositivos de TRC.
Inicialmente se planificó que la inclusión de pacientes en el estudio tuviera una duración de 9 meses, y se incluyó al primer paciente el 1 de octubre de 2015. Posteriormente, el Comité Científico decidió prolongar el periodo de inclusión 6 meses más hasta el 31 de diciembre de 2016, con el objetivo de ampliar la muestra para aumentar la representatividad y así posibilitar las comparaciones entre los diferentes países participantes.
Cuestionario sobre el centro hospitalarioCada uno de los centros participantes tuvo que completar un cuestionario sobre las características del centro, como información sobre el tamaño del hospital (número de camas), el tipo de centro (público/privado/universitario), la población de referencia, el grado de especialización del operador, las infraestructuras y el protocolo habitual de actuación respecto al implante de dispositivos de TRC14.
Cuaderno de recogida de datos electrónicoSe solicitó a los centros participantes que incluyeran a pacientes que iban a recibir un dispositivo de TRC y que completaran un cuaderno de recogida de datos electrónico para cada uno de ellos. El cuaderno de recogida de datos electrónico recoge información sobre las características del paciente, pruebas complementarias realizadas, indicación de la TRC, procedimiento de implante y un seguimiento a corto plazo que incluía eventos adversos y complicaciones hasta el alta hospitalaria14. No se registraron datos sobre seguimiento a más largo plazo. En todo momento se aseguró el anonimato de los pacientes participantes. El protocolo del estudio fue aprobado por el Comité de Ensayos Clínicos del Hospital Universitari i Politècnic La Fe de Valencia.
Recopilación y tratamiento de los datosEl cuaderno de recogida de datos electrónico, el tratamiento de los datos y el análisis estadístico fueron realizados por el Institut für Herzinfarktforschung15. El control operativo diario de la marcha de la encuesta se realizó en el Stavanger University Hospital, University of Bergen, Noruega.
Los datos de las variables continuas se presentan como mediana [intervalo intercuartílico]. Las variables discretas se presentan en forma de porcentaje. La comparación de los datos obtenidos por los centros españoles respecto al resto de los centros participantes se realizó utilizando el test de la t de Student para las variabales continuas y el test de la χ2 para las variables discretas. Se consideró significativo un valor de p ≤ 0,05.
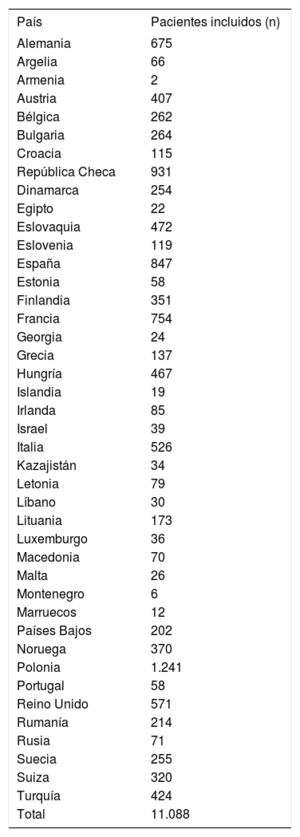
RESULTADOSLa encuesta CRT-Survey II incluyó a un total de 11.088 pacientes de 42 países pertenecientes a la ESC (tabla 1). En España, se incluyó en total a 847 pacientes de los 36 hospitales participantes (tabla 2). Se realizó una estimación de la representatividad de la encuesta utilizando los datos sobre implantes en cada país, recogidos en el libro blanco de la EHRA. De este modo, en total, la encuesta recogió al 20,1% de todos los implantes de TRC esperables en España durante el periodo de inclusión establecido.
Países participantes y número de pacientes incluidos
| País | Pacientes incluidos (n) |
|---|---|
| Alemania | 675 |
| Argelia | 66 |
| Armenia | 2 |
| Austria | 407 |
| Bélgica | 262 |
| Bulgaria | 264 |
| Croacia | 115 |
| República Checa | 931 |
| Dinamarca | 254 |
| Egipto | 22 |
| Eslovaquia | 472 |
| Eslovenia | 119 |
| España | 847 |
| Estonia | 58 |
| Finlandia | 351 |
| Francia | 754 |
| Georgia | 24 |
| Grecia | 137 |
| Hungría | 467 |
| Islandia | 19 |
| Irlanda | 85 |
| Israel | 39 |
| Italia | 526 |
| Kazajistán | 34 |
| Letonia | 79 |
| Líbano | 30 |
| Lituania | 173 |
| Luxemburgo | 36 |
| Macedonia | 70 |
| Malta | 26 |
| Montenegro | 6 |
| Marruecos | 12 |
| Países Bajos | 202 |
| Noruega | 370 |
| Polonia | 1.241 |
| Portugal | 58 |
| Reino Unido | 571 |
| Rumanía | 214 |
| Rusia | 71 |
| Suecia | 255 |
| Suiza | 320 |
| Turquía | 424 |
| Total | 11.088 |
Centros españoles participantes en la CRT-Survey II y número de pacientes incluidos por centro
| Hospital | Pacientes incluidos, n |
|---|---|
| Hospital General Universitario de Albacete | 27 |
| Hospital General de Alicante | 34 |
| Hospital de San Juan de Alicante | 33 |
| Hospital Araba | 24 |
| Hospital Universitario Central de Asturias | 30 |
| Hospital Germans Trias i Pujol, Badalona | 48 |
| Hospital Clínic de Barcelona | 6 |
| Hospital Vall d’Hebron, Barcelona | 40 |
| Hospital de Basurto, Bilbao | 8 |
| Hospital General Universitario de Castellón | 63 |
| Hospital Reina Sofía, Córdoba | 22 |
| Hospital Universitario de Getafe | 15 |
| Hospital Virgen de las Nieves, Granada | 3 |
| Hospital General Universitario de Guadalajara | 9 |
| Hospital Insular de Gran Canaria | 17 |
| Complejo Hospitalario de León | 8 |
| Hospital Arnau Vilanova de Lleida | 27 |
| Hospital Clínico de Madrid | 10 |
| Hospital 12 Octubre, Madrid | 53 |
| Hospital Universitario Gregorio Marañón, Madrid | 20 |
| Hospital La Paz, Madrid | 1 |
| Hospital Puerta Hierro, Madrid | 10 |
| Hospital Son Espases, Mallorca | 20 |
| Hospital Costa del Sol, Marbella | 17 |
| Hospital Clínico Universitario Virgen de la Arrixaca, Murcia | 43 |
| Hospital Morales Meseguer, Murcia | 5 |
| Hospital Reina Sofía, Murcia | 15 |
| Hospital Universitario de Salamanca | 22 |
| Complejo Hospitalario de Santiago de Compostela | 31 |
| Hospital Ntra. Sra. de Valme, Sevilla | 7 |
| Hospital Virgen del Rocío, Sevilla | 32 |
| Hospital Nuestra Señora del Prado, Talavera de la Reina | 1 |
| Hospital Joan XXIII de Tarragona | 6 |
| Hospital Clínico Universitario de Valencia | 31 |
| Hospital Dr. Peset, Valencia | 24 |
| Hospital Universitari i Politècnic La Fe, Valencia | 85 |
| Total | 847 |
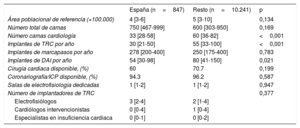
La mediana de implantes anuales de TRC reportada por los 36 centros españoles fue de 30 [21-50], cifra significativamente inferior a la mediana de 55 [33-100] reportada por el conjunto de los demás países participantes (p <0,001) (tabla 3). La mayoría de los centros españoles participantes eran hospitales universitarios (94,3%), mientras que en los otros países había una amplia representación de hospitales docentes no universitarios (25,9%) y hospitales privados (8,8%).
Características de los hospitales participantes
| España (n=847) | Resto (n=10.241) | p | |
|---|---|---|---|
| Área poblacional de referencia (×100.000) | 4 [3-6] | 5 [3-10] | 0,134 |
| Número total de camas | 750 [467-999] | 600 [303-950] | 0,169 |
| Número camas cardiología | 33 [28-58] | 60 [36-82] | <0,001 |
| Implantes de TRC por año | 30 [21-50] | 55 [33-100] | <0,001 |
| Implantes de marcapasos por año | 278 [200-400] | 250 [175-400] | 0,783 |
| Implantes de DAI por año | 54 [30-98] | 80 [41-150] | 0,021 |
| Cirugía cardiaca disponible, (%) | 60 | 70.7 | 0,199 |
| Coronariografía/ICP disponible, (%) | 94.3 | 96.2 | 0,587 |
| Salas de electrofisiología dedicadas | 1 [1-2] | 1 [1-2] | 0,947 |
| Número de implantadores de TRC | 0,377 | ||
| Electrofisiólogos | 3 [2-4] | 2 [1-4] | |
| Cardiólogos intervencionistas | 0 [0-4] | 1 [0-4] | |
| Especialistas en insuficiencia cardiaca | 0 [0-1] | 0 [0-2] | |
DAI: desfibrilador automático implantable; ICP: intervención coronaria percutánea; TRC: terapia de resincronización cardiaca.
Salvo otra indicación, los valores expresan mediana [intervalo intercuartílico].
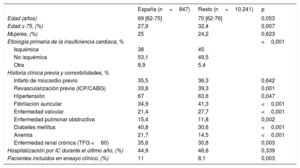
La mediana de edad de los pacientes incluidos en España era 69 [62-75] años, similar a la del resto (70 [62-76] años) (tabla 4). Hubo una menor proporción de pacientes de edad ≥ 75 años en los centros españoles (27,9%) que en el resto (32,4%; p=0,007). La proporción de implantes en varones y mujeres fue muy similar, el 75 y el 25% en centros españoles frente al 75,8 y el 24,2% en el resto. Los implantes en España se realizaron mediante un ingreso programado en una menor proporción que en el resto de los países (el 68,8 frente al 77,6%; p <0,001). Sin embargo, en España el número de pacientes incluidos en ensayos clínicos fue mayor (el 11,0 frente al 8,1%; p=0,003). En España, la etiología de la cardiopatía que motivó el implante difirió significativamente respecto al resto, con una menor proporción de pacientes con miocardiopatía dilatada isquémica (el 38 frente al 45%) y una mayor proporción de pacientes con miocardiopatía dilatada no isquémica (MCDNI) (el 53,1 frente al 49,5%) o con otras etiologías de la insuficiencia cardiaca (el 8,9 frente al 5,4%; p <0,001).
Características demográficas de los pacientes
| España (n=847) | Resto (n=10.241) | p | |
|---|---|---|---|
| Edad (años) | 69 [62-75] | 70 [62-76] | 0,053 |
| Edad ≥ 75, (%) | 27,9 | 32,4 | 0,007 |
| Mujeres, (%) | 25 | 24,2 | 0,623 |
| Etiología primaria de la insuficiencia cardiaca, % | <0,001 | ||
| Isquémica | 38 | 45 | |
| No isquémica | 53,1 | 49,5 | |
| Otra | 8,9 | 5,4 | |
| Historia clínica previa y comorbilidades, % | |||
| Infarto de miocardio previo | 35,5 | 36,3 | 0,642 |
| Revascularización previa (ICP/CABG) | 33,8 | 39,3 | 0,001 |
| Hipertensión | 67 | 63,6 | 0,047 |
| Fibrilación auricular | 34,9 | 41,3 | <0,001 |
| Enfermedad valvular | 21,4 | 27,7 | <0,001 |
| Enfermedad pulmonar obstructiva | 15,4 | 11,8 | 0,002 |
| Diabetes mellitus | 40,8 | 30,6 | <0,001 |
| Anemia | 21,7 | 14,5 | <0,001 |
| Enfermedad renal crónica (TFG <60) | 35,6 | 30,8 | 0,003 |
| Hospitalización por IC durante el último año, (%) | 44,9 | 46,6 | 0,339 |
| Pacientes incluidos en ensayo clínico, (%) | 11 | 8,1 | 0,003 |
CABG: cirugía de revascularización aortocoronaria; IC: insuficiencia cardiaca; ICP: intervención coronaria percutáneo; TFG: tasa de filtrado glomerular.
Los valores expresan porcentaje o mediana [intervalo intercuartílico].
Además, una menor proporción de pacientes tenía antecedentes de fibrilación auricular (el 34,9 frente al 41,3%; p <0,001) y enfermedad valvular (el 21,4 frente al 27,7%; p <0,001) (tabla 4). Sin embargo, los pacientes incluidos en los centros españoles tenían con mayor frecuencia otras comorbilidades, como enfermedad pulmonar obstructiva crónica, diabetes mellitus, anemia o enfermedad renal. El 26,1% del total de implantes realizados corresponde a procedimientos de upgrading en pacientes que ya llevaban implantado otro dispositivo.
Valoración clínica previa al implanteLa mayoría de los pacientes se encontraban en clase funcional II de la New York Heart Association (46,9%) o III (47,5%) (tabla 5). A diferencia del resto de los países participantes en la encuesta, una mayor proporción de pacientes se encontraba en clase II (el 46,9 frente al 36,9%; p <0,001) y la de pacientes en clase funcional IV fue testimonial (el 0,7 frente al 4,8%; p <0,001).
Evaluación clínica previa al implante
| España (n=847) | Resto (n=10.241) | p | |
|---|---|---|---|
| Clase funcional de la NYHA, (%) | <0,001 | ||
| I | 4,9 | 3,3 | |
| II | 46,9 | 36,9 | |
| III | 47,5 | 55,1 | |
| IV | 0,7 | 4,8 | |
| IMC | 28 [25-31] | 27 [25-31] | 0,167 |
| Presión arterial sistólica (mmHg) | 122 [110-135] | 122 [110-137] | 0,154 |
| Presión arterial diastólica (mmHg) | 70 [61-79] | 72 [67-80] | <0,001 |
| Parámetros analíticos (más reciente) | |||
| BNP (pg/ml) | 619 [205-1.105] | 420 [149-1.115] | 0,257 |
| NT-proBNP (pg/ml) | 2.469 [978-5.250] | 2.400 [1.070-5.523] | 0,667 |
| Creatinina sérica (mg/dl) | 1 [1-2] | 1 [1-1] | 0,309 |
| Hb (g/dl) | 13 [12-14] | 13 [12-15] | <0,001 |
| ECG antes del implante | |||
| Frecuencia cardiaca (lpm) | 70 [60-79] | 70 [61-80] | <0,001 |
| Ritmo auricular (%) | 0,023 | ||
| Sinusal | 72,6 | 68,9 | |
| Fibrilación auricular | 23,1 | 25,9 | |
| Ritmo auricular estimulado | 2,2 | 2,9 | |
| Otros | 2,2 | 2,4 | |
| Intervalo PR (ms) | 180 [160-210] | 180 [160-210] | 0,877 |
| Bloqueo AV II/III (%) | 22,9 | 18,6 | 0,002 |
| Dependiente de marcapasos, (%) | 15,8 | 13,9 | 0,128 |
| Morfología del QRS, (%) | <0,001 | ||
| Bloqueo de rama izquierda | 81,7 | 72 | |
| Bloqueo de rama derecha | 8,9 | 6,4 | |
| Otros | 9,4 | 21,6 | |
| Duración del QRS (ms) | 160 [145-174] | 160 [140-174] | 0,020 |
| <120ms, (%) | 3,7 | 7,8 | |
| 120-129ms, (%) | 4 | 5,4 | |
| 130-149ms, (%) | 19,3 | 18,6 | |
| 150-179ms, (%) | 51,3 | 46,7 | |
| > 180ms, (%) | 21,7 | 21,5 | |
| Indicación clínica para la TRC (%) | |||
| IC con QRS ancho | 55 | 60,4 | 0,002 |
| IC o disfunción del VI e indicación de DAI | 50.2 | 47,7 | 0,152 |
| Indicación de MP y alto porcentaje de estimulación del VD esperado | 24,8 | 22,7 | 0,166 |
| Evidencia de asincronía mecánica | 8,4 | 11,8 | 0,002 |
| Otras | 2,5 | 4,6 | 0,004 |
| FEVI (%) | 29 [24-34] | 29 [23-34] | 0,145 |
| FEVI <25%, % | 26,9 | 27,6 | |
| FEVI 25-35%, % | 59,2 | 59,5 | |
| FEVI> 35%, % | 13,9 | 12,9 | |
| DTDVI (mm) | 62 [57-68] | 63 [58-69] | 0,002 |
| Insuficiencia mitral (%) | 0,478 | ||
| Ligera | 44 | 46,7 | |
| Moderada | 25,3 | 26,6 | |
| Grave | 8 | 6,8 | |
| Ninguna | 22,7 | 20 | |
BNP: péptido natriurético cerebral; ECG: electrocardiograma; DAI: desfibrilador automático implantable; DTDVI: diámetro telediastólico del ventrículo izquierdo; FEVI: fracción de eyección del ventrículo izquierdo; Hb: hemoglobina; IC: insuficiencia cardiaca; IMC: índice de masa corporal; MP: marcapasos; NT-proBNP: fracción aminoterminal del propéptido natriurético cerebral; NYHA: New York Heart Association; TRC: terapia de resincronización cardiaca; VD: ventrículo derecho; VI: ventrículo izquierdo.
Los valores expresan porcentaje o mediana [intervalo intercuartílico].
El 72,6% de los pacientes se encontraban en ritmo sinusal en el momento del implante, con una proporción de pacientes en fibrilación auricular ligeramente inferior (23,1%) que en el resto de los países, aunque sin llegar a la significación estadística (el 23,1 frente al 25,9%; p=0,078). La duración media del QRS fue de 159±24ms. El 73% de los pacientes tenían un QRS ≥ 150ms y el 19,3% tenía un QRS de 130-150ms, cifras comparables a las del resto de los países. Destaca que, entre los pacientes incluidos en España, había una mayor proporción de bloqueo completo de la rama izquierda del haz de His (BCRIHH) (el 81,7 frente al 72%; p <0,001) y bloqueo completo de la rama derecha del haz de His (BCRDHH) (el 8,9 frente al 6,4%; p=0,005) respecto al resto de los países (tabla 5).
Un 23,3% de los pacientes incluidos en España tenían una fracción de eyección del ventrículo izquierdo (FEVI) ≥ 35% y un 33% tenía una insuficiencia mitral al menos moderada. La indicación más frecuente de implante de TRC fue la presencia de insuficiencia cardiaca y QRS ancho (el 55% de los pacientes). Tenían insuficiencia cardiaca, disfunción grave del ventrículo izquierdo (VI) e indicación de desfibrilador automático implantable el 50% de los pacientes. En el 24,8% de los casos, el único motivo para el implante fue la necesidad de estimulación y la previsión de un alto porcentaje de estimulación.
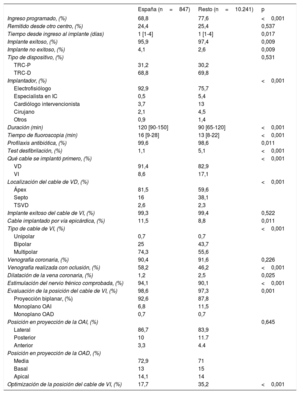
Parámetros relativos al implanteLa tasa total de éxito del implante fue del 95,9% (tabla 6). A diferencia de lo registrado en los demás países, en España los implantes fueron realizados mayoritariamente por electrofisiólogos (el 92,9 frente al 75,7%; p <0,001). La cifra de intentos de implante no exitosos fue significativamente mayor en España (el 4,1 frente al 2,6%; p=0,009). Las proporciones de TRC con desfibrilador y TRC con marcapasos fueron del 68,8 y el 31,2%, comparables a las de los demás países. En los pacientes con miocardiopatía dilatada isquémica, se implantó una mayor proporción de dispositivos TRC con desfibrilador que de TRC con marcapasos (el 80,1 y el 19,9%) que en los pacientes con MCDNI (el 64,7 y el 35,3%) (p <0,001). En el grupo de pacientes cuya indicación de la TRC fue la necesidad de estimulación o una previsión de un alto porcentaje de estimulación ventricular, se implantó una mayor proporción de dispositivos de TRC con marcapasos que de TRC con desfibrilador (el 58,5 frente al 41,5%). La mediana de duración del implante reportada en España fue significativamente mayor que la media (120 [90-150] frente a 90 [65-120] min; p <0,001). El 11,4% de los cables de VI se implantaron en el epicardio por vía quirúrgica. Se utilizaron cables de VI multipolares en el 74,2% de los casos, porcentaje muy superior al registrado en el resto de los países. En el 86,7% de los casos, la posición del cable de VI fue lateral y en el 72,9%, en segmentos medios del VI. La tasa de complicaciones periprocedimiento fue del 7,2%, significativamente mayor que el 5,4% reportado como media del resto de los países participantes (p=0,028) (tabla 7).
Parámetros relativos al implante
| España (n=847) | Resto (n=10.241) | p | |
|---|---|---|---|
| Ingreso programado, (%) | 68,8 | 77,6 | <0,001 |
| Remitido desde otro centro, (%) | 24,4 | 25,4 | 0,537 |
| Tiempo desde ingreso al implante (días) | 1 [1-4] | 1 [1-4] | 0,017 |
| Implante exitoso, (%) | 95,9 | 97,4 | 0,009 |
| Implante no exitoso, (%) | 4,1 | 2,6 | 0,009 |
| Tipo de dispositivo, (%) | 0,531 | ||
| TRC-P | 31,2 | 30,2 | |
| TRC-D | 68,8 | 69,8 | |
| Implantador, (%) | <0,001 | ||
| Electrofisiólogo | 92,9 | 75,7 | |
| Especialista en IC | 0,5 | 5,4 | |
| Cardiólogo intervencionista | 3,7 | 13 | |
| Cirujano | 2,1 | 4,5 | |
| Otros | 0,9 | 1,4 | |
| Duración (min) | 120 [90-150] | 90 [65-120] | <0,001 |
| Tiempo de fluoroscopia (min) | 16 [9-28] | 13 [8-22] | <0,001 |
| Profilaxis antibiótica, (%) | 99,6 | 98,6 | 0,011 |
| Test desfibrilación, (%) | 1,1 | 5,1 | <0,001 |
| Qué cable se implantó primero, (%) | <0,001 | ||
| VD | 91,4 | 82,9 | |
| VI | 8,6 | 17,1 | |
| Localización del cable de VD, (%) | <0,001 | ||
| Ápex | 81,5 | 59,6 | |
| Septo | 16 | 38,1 | |
| TSVD | 2,6 | 2,3 | |
| Implante exitoso del cable de VI, (%) | 99,3 | 99,4 | 0,522 |
| Cable implantado por vía epicárdica, (%) | 11,5 | 8,8 | 0,011 |
| Tipo de cable de VI, (%) | <0,001 | ||
| Unipolar | 0,7 | 0,7 | |
| Bipolar | 25 | 43,7 | |
| Multipolar | 74,3 | 55,6 | |
| Venografía coronaria, (%) | 90,4 | 91,6 | 0,226 |
| Venografía realizada con oclusión, (%) | 58,2 | 46,2 | <0,001 |
| Dilatación de la vena coronaria, (%) | 1,2 | 2,5 | 0,025 |
| Estimulación del nervio frénico comprobada, (%) | 94,1 | 90,1 | <0,001 |
| Evaluación de la posición del cable de VI, (%) | 98,6 | 97,3 | 0,001 |
| Proyección biplanar, (%) | 92,6 | 87,8 | |
| Monoplano OAI | 6,8 | 11,5 | |
| Monoplano OAD | 0,7 | 0,7 | |
| Posición en proyección de la OAI, (%) | 0,645 | ||
| Lateral | 86,7 | 83,9 | |
| Posterior | 10 | 11.7 | |
| Anterior | 3,3 | 4.4 | |
| Posición en proyección de la OAD, (%) | |||
| Media | 72,9 | 71 | |
| Basal | 13 | 15 | |
| Apical | 14,1 | 14 | |
| Optimización de la posición del cable de VI, (%) | 17,7 | 35,2 | <0,001 |
OAD: oblicua anterior derecha; OAI: oblicua anterior izquierda; TRC-D: terapia de resinconización cardiaca con desfibrilador automático implantable; TRC-P: terapia de resincronización cardiaca con marcapasos; VD: ventrículo derecho; VI: ventrículo izquierdo; TSVD: tracto de salida del ventrículo derecho.
Salvo otra indicación, los valores expresan mediana [intervalo intercuartílico].
Complicaciones relacionadas con el procedimiento y hasta el alta hospitalaria
| España (n=847) | Resto (n=10.241) | p | |
|---|---|---|---|
| Complicaciones periprocedimiento, (%) | 7,2 | 5,4 | 0,028 |
| Muerte, (%) | 0,1 | 0,1 | 0,604 |
| Sangrado, (%) | 0,9 | 1 | 0,927 |
| Requiere intervención | 0 | 0,4 | 0,088 |
| Hematoma de bolsillo | 0,9 | 0,8 | 0,536 |
| Neumotórax, (%) | 0,5 | 1 | 0,103 |
| Hemotórax, (%) | 0,1 | 0,1 | 0,694 |
| Disección del seno coronario, (%) | 3,7 | 1,8 | <0,001 |
| Taponamiento cardiaco, (%) | 0,3 | 0,2 | 0,539 |
| Otras, (%) | 1,9 | 1,5 | 0,407 |
| Eventos adversos mayores durante la hospitalización, (%) | 3,5 | 4,9 | 0,082 |
| Infarto miocardio | 0 | 0,1 | 0,417 |
| Ictus | 0 | 0,1 | 0,482 |
| Infección sistema | 0,4 | 0,6 | 0,446 |
| Empeoramiento de la insuficiencia cardiaca | 1,1 | 0,7 | 0,187 |
| Empeoramiento de la función renal | 1,5 | 0,9 | 0,127 |
| Arritmias | 0,5 | 1,2 | 0,054 |
| Otras | 0,9 | 2 | 0,019 |
| Complicaciones que precisaron intervención, (%) | 2,4 | 4.2 | 0,009 |
| Estimulación frénica | 1 | 1,1 | 0,647 |
| Dislocación del cable | 0,7 | 1,8 | 0,021 |
| Ventrículo derecho | 0,1 | 5,3 | 0,437 |
| Ventrículo izquierdo | 0,5 | 0,9 | 0,480 |
| Aurícula derecha | 0,1 | 0,3 | 0,872 |
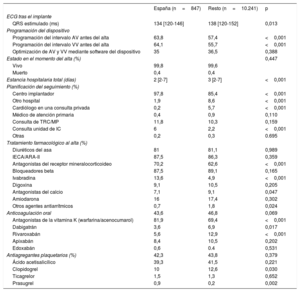
La mediana de estancia hospitalaria para el implante fue significativamente menor en España que en el resto de los países: 2 [2-7] frente a 3 [2-7] días (p <0,001) (tabla 8). La tasa de eventos adversos mayores ocurridos durante la hospitalización fue del 3,5%, incluida una tasa de mortalidad del 0,4%. Para la mayoría de los pacientes se reprogramaron los intervalos AV y VV antes del alta hospitalaria, en un 35% de los casos utilizando el software específico del dispositivo. En el 98% de los casos el seguimiento tras el implante se realizó en el mismo centro implantador. El 55,8% de los pacientes recibieron monitorización a distancia, cifra significativamente mayor que en el resto de los países (27,7%; p <0,001).
Parámetros tras el implante
| España (n=847) | Resto (n=10.241) | p | |
|---|---|---|---|
| ECG tras el implante | |||
| QRS estimulado (ms) | 134 [120-146] | 138 [120-152] | 0,013 |
| Programación del dispositivo | |||
| Programación del intervalo AV antes del alta | 63,8 | 57,4 | <0,001 |
| Programación del intervalo VV antes del alta | 64,1 | 55,7 | <0,001 |
| Optimización de AV y VV mediante software del dispositivo | 35 | 36,5 | 0,388 |
| Estado en el momento del alta (%) | 0,447 | ||
| Vivo | 99,8 | 99,6 | |
| Muerto | 0,4 | 0,4 | |
| Estancia hospitalaria total (días) | 2 [2-7] | 3 [2-7] | <0,001 |
| Planificación del seguimiento (%) | |||
| Centro implantador | 97,8 | 85,4 | <0,001 |
| Otro hospital | 1,9 | 8,6 | <0,001 |
| Cardiólogo en una consulta privada | 0,2 | 5,7 | <0,001 |
| Médico de atención primaria | 0,4 | 0,9 | 0,110 |
| Consulta de TRC/MP | 11,8 | 10,3 | 0,159 |
| Consulta unidad de IC | 6 | 2,2 | <0,001 |
| Otras | 0,2 | 0,3 | 0.695 |
| Tratamiento farmacológico al alta (%) | |||
| Diuréticos del asa | 81 | 81,1 | 0,989 |
| IECA/ARA-II | 87,5 | 86,3 | 0,359 |
| Antagonistas del receptor mineralocorticoideo | 70,2 | 62,6 | <0,001 |
| Bloqueadores beta | 87,5 | 89,1 | 0,165 |
| Ivabradina | 13,6 | 4,9 | <0,001 |
| Digoxina | 9,1 | 10,5 | 0,205 |
| Antagonistas del calcio | 7,1 | 9,1 | 0,047 |
| Amiodarona | 16 | 17,4 | 0,302 |
| Otros agentes antiarrítmicos | 0,7 | 1,8 | 0,024 |
| Anticoagulación oral | 43,6 | 46,8 | 0,069 |
| Antagonistas de la vitamina K (warfarina/acenocumarol) | 81,9 | 69,4 | <0,001 |
| Dabigatrán | 3,6 | 6,9 | 0,017 |
| Rivaroxabán | 5,6 | 12,9 | <0,001 |
| Apixabán | 8,4 | 10,5 | 0,202 |
| Edoxabán | 0,6 | 0.4 | 0,531 |
| Antiagregantes plaquetarios (%) | 42,3 | 43,8 | 0,379 |
| Ácido acetisalicílico | 39,3 | 41,5 | 0,221 |
| Clopidogrel | 10 | 12,6 | 0,030 |
| Ticagrelor | 1,5 | 1,3 | 0,652 |
| Prasugrel | 0,9 | 0,2 | 0,002 |
ARA-II: antagonistas del receptor de la angiotensina II; AV: auriculoventricular; IC: insuficiencia cardiaca; IECA: inhibidores de la enzima de conversión de la angiotensina; MP: marcapasos; TRC: terapia de resincronización cardiaca; VV: interventricular.
Los datos en España de la CRT-Survey II ofrecen una foto fija del tipo de pacientes que están recibiendo realmente un dispositivo de TRC en España, más allá del perfil de pacientes incluidos en los grandes ensayos clínicos o lo que recomiendan las guías de práctica clínica.
Los resultados muestran que, tal y como indican los datos publicados por Eucomed, la EHRA y los registros nacionales de marcapasos y desfibriladores automáticos implantables16–19, la tasa de implantes de dispositivos de TRC en los hospitales españoles se encuentra muy por debajo de la media de implantes de los hospitales de los países del entorno. Respecto al perfil de los pacientes a los que se implanta un TRC, la mediana de edad se encuentra en torno a los 70 años, la proporción de pacientes a los que se implanta el dispositivo por encima de los 75 años se encuentra por debajo del 30%, a diferencia de lo que ocurre en los demás países, y solo 1 de cada 4 implantes se realiza en mujeres. La etiología predominante para el implante del TRC es la MCDNI, al igual que ocurre en el resto de los países. Sin embargo, destaca que las diferencias entre la proporción de pacientes con MCDNI y miocardiopatía dilatada isquémica en España sean significativamente mayores a favor de la MCDNI en comparación con el resto de los países. Esto podría explicarse por el hecho de que, al tener una menor tasa total de implantes, estos se seleccionen al máximo y, por lo tanto, se favorezcan más los implantes en los subgrupos que mayor beneficio han mostrado con la TRC, como es el caso de los pacientes con MCDNI20. En consonancia con este argumento, la inmensa mayoría de los pacientes que recibieron un dispositivo de TRC en hospitales españoles se encontraban en clase funcional II-III, mientras que los pacientes en clase funcional IV fueron testimoniales (0,7%).
Por otra parte, la selección de los pacientes en función de la morfología y la anchura del QRS puede considerarse como adecuada a las guías8,9, ya que hasta un 83% de los pacientes incluidos en centros españoles tenían un BCRIHH en el electrocardiograma basal, cifra significativamente superior a la del resto de los países participantes. Del mismo modo, en lo que a la anchura del QRS se refiere, el 73% de los pacientes tenían un QRS ≥ 150ms y únicamente el 7,7% tenía QRS <130ms. En ambos casos, las cifras registradas en España son significativamente superiores a las del resto de los países participantes en la encuesta, lo que indica una tendencia a una mejor selección de los candidatos a TRC. Sin embargo, se siguen realizando implantes en pacientes con BCRDHH (hasta el 8,8%), a pesar de que los datos publicados indican falta de eficacia de la TRC en este subgrupo de pacientes21. Asimismo hasta un 14% de los pacientes incluidos en España tenían una FEVI> 35%, aunque es muy probable que gran parte de este porcentaje corresponda a pacientes con indicación de estimulación permanente cuya FEVI reducida llevó al implante de un cable de estimulación en el VI. Es llamativo que solo un 25% de los implantes se realicen en mujeres ya que, como es sabido, un mayor porcentaje de mujeres con insuficiencia cardiaca y FEVI reducida tienen BCRIHH y, además, pueden mostrar mayor beneficio de la TRC con QRS menos anchos que los varones22,23.
En cuanto a aspectos meramente técnicos del implante, la tasa total de éxito del implante del dispositivo es muy alta (96,3%), como también lo es la tasa de éxito del implante del cable de VI (99,3%). Destaca que hasta el 11,4% de los cables se implantaron en el epicardio, aunque en la encuesta no se recogía información sobre los motivos para el implante epicárdico. Se trata de un gran porcentaje en el que probablemente no solo se haya incluido a pacientes con fracaso previo de la vía transvenosa, sino también a otros pacientes con indicación para la TRC a los que se había implantado un cable de VI durante una cirugía cardiaca concomitante. Otra de las informaciones novedosas que aporta la encuesta es la generalizada utilización de cables cuadripolares, que ya suponen prácticamente un 75% del total de los cables de VI implantados en centros españoles, tasa muy superior a la registrada en el resto de los centros participantes. Sin embargo, la encuesta no recogía información sobre si los generadores implantados tenían capacidad de estimulación multipunto ni si esta se activó en el implante.
También resulta destacable que la tasa de complicaciones periprocedimiento fue significativamente superior en los centros españoles que en el resto. No obstante, si se analizan pormenorizadamente las causas de dichas complicaciones, se observa que la diferencia se basa en una mayor tasa de disecciones del seno coronario (el 50% de todas las complicaciones periprocedimiento en centros españoles frente al 32,6% en los demás países). En general, la disección del seno coronario es una complicación que no suele conllevar repercusiones graves para el paciente y ni siquiera impide el implante del cable de VI en la mayoría de los casos24. Por el contrario, la tasa del resto de complicaciones fue comparable a la de los demás países, y destaca una tasa significativamente menor de neumotórax en nuestros centros (el 0,46 frente al 1,06%; p=0,011). La tasa de mortalidad periprocedimiento es muy baja (el 0,11% en centros españoles) y otras complicaciones graves, como el taponamiento cardiaco, ocurrieron únicamente en el 0,23% de los casos. En otras grandes series publicadas, como el registro estadounidense, con más de 439.000 pacientes que recibieron un dispositivo de TRC estando ingresados, la tasa de complicaciones periprocedimiento se encuentra constantemente en torno al 7% reportado en España25.
LimitacionesLa principal limitación del estudio es su naturaleza observacional en forma de encuesta, que únicamente recoge los datos preestablecidos desde el momento del implante hasta el momento del alta hospitalaria. Por lo tanto, la ausencia de seguimiento de los pacientes limita la validez de los datos de complicaciones y morbimortalidad aportados, ya que podrían estar infraestimados debido a la ausencia de seguimiento. Además, el hecho de que solo se haya incluido un 20,1% del total de implantes esperados en el periodo de inclusión establecido hace que los datos obtenidos puedan no ser reflejo de la realidad en España. Sería deseable la realización de encuestas más amplias para confirmar estos hallazgos.
CONCLUSIONESLos resultados en España de CRT-Survey II permiten obtener una foto fija acerca de la utilización de esta terapia en España. Los resultados muestran que la tasa de éxito del implante es alta (96,3%). En los centros españoles se registra una menor proporción de pacientes de edad ≥ 75 años y una mayor proporción de pacientes en clase II, con BCRIHH y seguimiento a distancia, con estancias hospitalarias significativamente menores.
FINANCIACIÓNEste trabajo ha recibido financiación de: EHFA, HFA, Biotronik, Boston Scientific, Medtronic; Sorin, St. Jude Medical, Abbott, Bayer, Bristol-Myers-Squibb y Servier.
CONFLICTO DE INTERESESK. Dickstein ha recibido durante la realización del presente trabajo becas de la HFA, Biotronik, Boston Scientific, Medtronic, Sorin, St. Jude Medical, Abbott, Bayer, Bristol-Myers-Squibb, Servier y la EHRA. C. Normand ha recibido durante la realización del presente trabajo becas de la HFA, Biotronik, Boston Scientific, Medtronic, Sorin, St. Jude Medical, Abbott, Bayer, Bristol-Myers-Squibb, Servier y la EHRA. C. Linde ha recibido becas de investigación de Astra a través del Karolinska Institutet Stockholm (Suecia), y honorarios por ponencias de Vifor, Novartis, Medtronic y Abbot sin relación alguna con el presente manuscrito. Los demás autores no reportan ningún conflicto de intereses.
- –
La TRC disminuye la morbimortalidad de los pacientes con insuficiencia cardiaca, disfunción del ventrículo izquierdo, QRS ancho y tratamiento farmacológico óptimo.
- –
Las guías de práctica clínica han establecido las indicaciones fundamentales para la TRC basándose en los resultados de grandes ensayos clínicos aleatorizados.
- –
La encuesta CRT-Survey II ha permitido realizar una «foto fija» sobre el estado actual de la utilización de la TRC en Europa.
- –
Se trata de datos que reflejan la práctica clínica real, a diferencia de los obtenidos de los grandes ensayos aleatorizados.
- –
Los resultados en España permiten conocer a qué tipo de pacientes se está implantando un dispositivo de TRC, cómo se realizan esos implantes y qué resultados a corto plazo se obtienen.
- –
Además, la encuesta ha permitido comparar los resultados en España con los de los demás países participantes en la CRT-Survey II.
Los autores desean agradecer la ayuda prestada por Tessa Baak, coordinadora de operaciones de la encuesta CRT-Survey II, en la recopilación de datos y en la preparación del manuscrito. Asimismo, se agradece la ayuda del Institut für Herzinfarktforschung por la ayuda prestada en el tratamiento de los datos y el análisis estadístico.