Tanto la diabetes mellitus como la enfermedad renal crónica aumentan el riesgo de fibrilación auricular. A su vez, la concomitancia de diabetes mellitus y enfermedad renal crónica incrementa de manera sinérgica el riesgo tromboembólico asociado con la fibrilación auricular, lo que pone al paciente en esta situación en especial riesgo y obliga a no fijar nuestra actuación solo en la reducción del riesgo embólico, sino a buscar una protección general. Aunque todos los anticoagulantes orales reducen eficazmente el riesgo de ictus en el paciente diabético con fibrilación auricular, hay datos que indican que el rivaroxabán podría disminuir además la mortalidad cardiovascular en esta población, ofreciendo una protección adicional. Por otra parte, se ha descrito un empeoramiento de la función renal con el empleo de los antagonistas de la vitamina K (nefropatía por warfarina). En consecuencia, sería deseable que el tratamiento anticoagulante no solo disminuyera el riesgo de complicaciones tromboembólicas, sino que además no se asociara con este deterioro de la función renal. En este sentido, parece que algunos anticoagulantes orales de acción directa, como el dabigatrán y el rivaroxabán, tendrían un menor riesgo de eventos renales adversos en comparación con warfarina.
Palabras clave
La diabetes mellitus (DM) es actualmente una auténtica epidemia. Si en España el estudio Di@bet.es estimó una prevalencia del 14%, esta cifra se incrementará en cerca del 50% en los próximos 25 años, como consecuencia del envejecimiento de la población y los cambios en el estilo de vida (más sedentarismo, obesidad, etc.)1,2.
La DM aumenta de manera importante el riesgo de complicaciones de origen cardiovascular (CV), principalmente cardiopatía isquémica, ictus, insuficiencia cardiaca, enfermedad arterial periférica y muerte CV3. Así, en el estudio REACH, tras 4 años de seguimiento, los pacien-tes con DM tuvieron más riesgo de muerte de causa CV, infarto de miocardio no mortal o ictus no mortal que los no diabéticos (el 16,5 frente al 13,1%)4. Además, el riesgo de muerte por cualquier causa también se incrementa en los pacientes con DM (el 14,3 frente al 9,9%)4. Esto se debe a que la hiperglucemia afecta negativamente, entre otros, a la función vascular, el perfil lipídico y la coagulación5.
Del mismo modo, la DM aumenta significativamente el riesgo de fibrilación auricular (FA). En el estudio de Framingham, la DM incre-mentó en 1,4 veces en varones y 1,6 veces en mujeres la probabilidad de sufrir esta arritmia6. Más recientemente, en un metanálisis7 se observó que la DM aumentaba el riesgo de FA en un 40%; tras ajustar por diferentes factores, este incremento significativo seguía siendo del 24%. En la misma línea, en un estudio realizado en Estados Unidos8, se observó que al alta hospitalaria la incidencia de FA fue mayor en los diabéticos que en los no diabéticos (el 14,9 frente al 10,3%; p < 0,0001 ). También se ha visto que la DM incrementa el riesgo de hospitalización por FA9, de tal manera que en un estudio realizado en España, la inci-dencia de ingresos por FA fue 3,24 y 4,27 veces mayor en varones y mujeres con DM2 que en los pacientes sin DM10. Cabe señalar además que el riesgo de FA no es el mismo en todos los diabéticos, se han indi-cado como predictores de mayor riesgo de FA tanto el pobre control glucémico como la mayor duración de la DM11-13. Por otra parte, la DM es la principal causa de insuficiencia renal, y la enfermedad renal dia-bética es un factor independiente de ateroesclerosis, lo que hace a esta población especialmente sensible a la aparición de enfermedad CV, muerte CV y FA14,15. Por este motivo, el objetivo de tratamiento en estos pacientes no se debería limitar a la prevención de las complicaciones tromboembólicas, sino dirigirse también a la prevención de todas las complicaciones CV en su conjunto, con especial énfasis en evitar un deterioro precoz de la función renal.
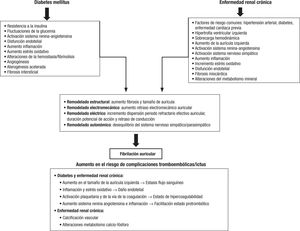
Se han descrito múltiples factores que tratan de explicar la interre-lación entre la FA y la DM, como la resistencia a la insulina, el estrés oxidativo, la inflamación, etc., y que en último término se van a tradu-cir en un aumento de la fibrosis y el tamaño de la aurícula (remode-lado estructural), un incremento en el retraso electromecánico auricular, un remodelado eléctrico y un desequilibrio del sistema ner-vioso autónomo, lo que finalmente va a aumentar el riesgo de FA (Figura 1)16-23.
Aunque la FA aumente en general hasta en 5 veces el riesgo de ictus en la población general, la presencia concomitante de DM se asocia de manera independiente con un incremento adicional de ese riesgo del 2-3,5%16. En consecuencia, la prevención del ictus mediante una adecuada anticoagulación es de especial relevancia en la pobla-ción diabética con FA24.
Relevancia de la enfermedad renal crónica en la fibrilación auricular no valvularExiste una estrecha interrelación entre la enfermedad renal cró-nica (ERC) y la FA. De hecho, la FA supone la arritmia más frecuente en esta población25-27. La prevalencia de FA es mucho mayor en los pacientes con ERC, que de media alcanza el 7-18% de ellos frente al 3% de la población general, y es aún mayor conforme aumenta la edad de los pacientes (un 12-25% a edad > 70 años)25-29. Además, se ha visto un incremento de la FA en pacientes con ERC. Por ejemplo, se ha obser-vado que en Estados Unidos, entre los pacientes tratados con hemo-diálisis, el número de sujetos con FA ha aumentado en 6,6 veces entre 1992 y 200630. Son múltiples los mecanismos por los cuales la ERC aumenta el riesgo de FA, algunos comunes a otras enfermedades como la DM o la hipertensión arterial, que frecuentemente se presen-tan de manera concomitante, pero otros son más específicos de la ERC, como las alteraciones del metabolismo óseo-mineral o la sobre-carga hemodinámica (Figura 1)25,31-33. Por otra parte, los dicumarínicos se han asociado con mayor progresión de la rigidez aórtica medida mediante velocidad de onda de pulso en pacientes en hemodiálisis comparados con pacientes que no recibían dicho tratamiento34. Como consecuencia del incremento de la rigidez aórtica, con su efecto en el flujo cerebral, aumenta el riesgo de ictus, sobrecarga sistólica y ERC y disminuye la perfusión coronaria en diástole, que asimismo incre-menta el riesgo de cardiopatía isquémica35.
Los pacientes con ERC que contraen FA tienen un mayor riesgo de deterioro de la función renal, así como de complicaciones CV y muerte27,36,37. Los pacientes con FA y ERC tienen un riesgo incremen-tado de ictus, aunque la ERC no se incluye como factor de riesgo en la escala CHA2DS2-VASc24. De hecho, varios autores han propuesto que la insuficiencia renal debería ser incluida como una variable dentro de las escalas de estratificación de riesgo tromboembólico en el paciente con FA38,39. Por otra parte, la ERC incrementa el riesgo de hemorragias debido a la disfunción plaquetaria inducida por la uremia especial-mente en estadios avanzados de enfermedad renal, y está incluida en las escalas de estratificación de riesgo de hemorragia24.
Este aumento en el riesgo de ictus en los pacientes con ERC se debe a varias causas, muchas comunes a otras afecciones como la DM (aumento de tamaño de la aurícula izquierda, lo que facilita la estasis sanguínea, el aumento del estado inflamatorio y el estrés oxidativo, lo que incrementa el daño endotelial, y el incremento en el estado de hipercoagulabilidad y protrombótico), pero también participan otras más características de la ERC, como la calcificación vascular o las alte-raciones del metabolismo calciofosfórico (Figura 1)25,40,41. Por otra parte, también se ha observado que la proteinuria, conocido marcador de daño renal y predictor de riesgo CV, aumenta tanto el riesgo de ictus como el de complicaciones CV y muerte en sujetos con FA, lo que nuevamente supone un factor de riesgo añadido para esta población que, al igual que la diabética, está en especial riesgo cardioembólico en presencia de FA42,43.
Anticoagulación y mortalidad cardiovascular del paciente diabético con fibrilación auricular no valvularEstá demostrado que la anticoagulación reduce el riesgo de ictus de los pacientes diabéticos con FA. Así, en Estados Unidos se ha observado que, entre 1992 y 2010, la tasa de ictus isquémicos en pacientes diabéticos con FA se redujo en un 71%, en paralelo con un aumento en la prescripción de warfarina del 28 al 62%44. Sin embargo, un gran número de pacientes con indicación de anticoagu-lación no la reciben, en parte por las limitaciones asociadas con el tratamiento con antagonistas de la vitamina K (AVK), que obligan a un control periódico de la anticoagulación y frecuentes cambios de dosis45,46. Además, el mal control de muchos pacientes con AVK debería acompañarse de un rápido cambio a un anticoagulante oral de acción directa (ACOD), que muchas veces no se realiza por las dificultades en la detección del mal control y las barreras a la pres-cripción en España47,48.
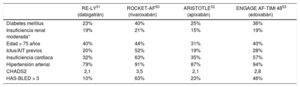
En general y en comparación con warfarina, los ACOD se han demostrado igual de eficaces para la prevención del ictus, pero con un mejor perfil de seguridad, sobre todo por un menor riesgo de hemo-rragias intracraneales y mortales49. En los ensayos clínicos fundamen-tales con los ACOD, se incluyó a un elevado número de pacientes con DM, que varió desde algo más del 20% en los estudios RE-LY y ARIS-TOTLE al 40% en el estudio ROCKET-AF (tabla 1)50-53. De hecho, en los sujetos con DM, el CHADS2 medio en el estudio ROCKET-AF fue de 3,7, frente a 2,9 en el ARISTOTLE y 3,0 en el RE-LY54-56.
Características basales de los pacientes incluidos en los ensayos clínicos fundamentales
| RE-LY51 (dabigatrán) | ROCKET-AF50 (rivaroxabán) | ARISTOTLE52 (apixabán) | ENGAGE AF-TIMI 4853 (edoxabán) | |
|---|---|---|---|---|
| Diabetes mellitus | 23% | 40% | 25% | 36% |
| Insuficiencia renal moderada* | 19% | 21% | 15% | 19% |
| Edad > 75 años | 40% | 44% | 31% | 40% |
| Ictus/AIT previos | 20% | 52% | 19% | 28% |
| Insuficiencia cardiaca | 32% | 63% | 35% | 57% |
| Hipertensión arterial | 79% | 91% | 87% | 94% |
| CHADS2 | 2,1 | 3,5 | 2,1 | 2,8 |
| HAS-BLED > 3 | 10% | 63% | 23% | 46% |
AIT: accidente isquémico transitorio.
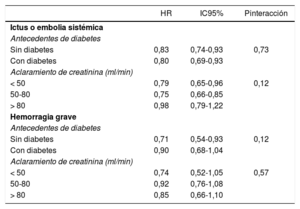
En su conjunto los estudios con ACOD en la población diabética, en comparación con warfarina, asociaron estos fármacos con una reduc-ción significativa del 20% en el riesgo de ictus o embolia sistémica, con tendencia a un menor riesgo de hemorragias mayores. Estos beneficios coincidieron con los de la población total (tabla 2)49. Al analizar cada ensayo clínico individualmente, la eficacia (reducción de ictus o embolia sistémica) fue independiente de la presencia de DM.
Eficacia y seguridad de los anticoagulantes orales de acción directa frente a warfarina en un metanálisis de los ensayos clínicos fundamentales, de acuerdo con la presencia de diabetes mellitus y la función renal
| HR | IC95% | Pinteracción | |
|---|---|---|---|
| Ictus o embolia sistémica | |||
| Antecedentes de diabetes | |||
| Sin diabetes | 0,83 | 0,74-0,93 | 0,73 |
| Con diabetes | 0,80 | 0,69-0,93 | |
| Aclaramiento de creatinina (ml/min) | |||
| < 50 | 0,79 | 0,65-0,96 | 0,12 |
| 50-80 | 0,75 | 0,66-0,85 | |
| > 80 | 0,98 | 0,79-1,22 | |
| Hemorragia grave | |||
| Antecedentes de diabetes | |||
| Sin diabetes | 0,71 | 0,54-0,93 | 0,12 |
| Con diabetes | 0,90 | 0,68-1,04 | |
| Aclaramiento de creatinina (ml/min) | |||
| < 50 | 0,74 | 0,52-1,05 | 0,57 |
| 50-80 | 0,92 | 0,76-1,08 | |
| > 80 | 0,85 | 0,66-1,10 | |
Tabla elaborada con datos de Ruff et al49. HR: hazard ratio; IC95%: intervalo de confianza del 95%.
En el estudio ROCKET-AF, los pacientes diabéticos presentaron un mayor riesgo tromboembólico que los no diabéticos (CHADS2 de 3,7 frente a 3,3). Sin embargo, los resultados tanto en eficacia como en seguridad fueron acordes con los de la población total, excepto en la mortalidad CV, ya que hubo una reducción significativa del 20% en los pacientes tratados con rivaroxabán frente a warfarina, aunque estos resultados hay que considerarlos meramente exploratorios e inter-pretarlos con cautela por las limitaciones inherentes a los análisis de subgrupos55. Este beneficio apreciado con el rivaroxabán indica la hipótesis de que podría existir un comportamiento diferencial con respecto a otros ACOD en la población diabética, que habría que con-firmar en estudios específicos57.
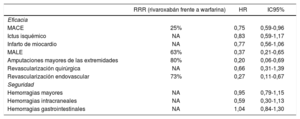
En los últimos años se han publicado datos de la práctica clínica con rivaroxabán en sujetos con DM y FA con resultados acordes con los del ensayo clínico principal en cuanto al riesgo de ictus y de hemo-rragias en comparación con warfarina. Además, han mostrado una reducción significativa del 25% en los eventos adversos cardiovascu-lares mayores (MACE), del 63% en los eventos adversos mayores de las extremidades (MALE), del 17% en el riesgo de lesión renal aguda, y del 18% en el riesgo de enfermedad renal terminal o necesidad de diálisis (tabla 3 ytabla 4)58-60.
Efectividad y seguridad del rivaroxabán frente a la warfarina en prevención de MACE y MALE en pacientes con fibrilación auricular no valvular y diabetes mellitus tipo 2 en un estudio no aleatorizado de la práctica clínica
| RRR (rivaroxabán frente a warfarina) | HR | IC95% | |
|---|---|---|---|
| Eficacia | |||
| MACE | 25% | 0,75 | 0,59-0,96 |
| Ictus isquémico | NA | 0,83 | 0,59-1,17 |
| Infarto de miocardio | NA | 0,77 | 0,56-1,06 |
| MALE | 63% | 0,37 | 0,21-0,65 |
| Amputaciones mayores de las extremidades | 80% | 0,20 | 0,06-0,69 |
| Revascularización quirúrgica | NA | 0,66 | 0,31-1,39 |
| Revascularización endovascular | 73% | 0,27 | 0,11-0,67 |
| Seguridad | |||
| Hemorragias mayores | NA | 0,95 | 0,79-1,15 |
| Hemorragias intracraneales | NA | 0,59 | 0,30-1,13 |
| Hemorragias gastrointestinales | NA | 1,04 | 0,84-1,30 |
Tabla elaborada con datos de Baker et al60. HR: hazard ratio; IC95%: intervalo de confianza del 95%; MACE: eventos adversos cardiovasculares mayores; MALE: eventos adversos mayores de las extremidades; NA: no aplicable.
Consecuencias renales del rivaroxabán frente a la warfarina en pacientes con fibrilación auricular no valvular y diabetes mellitus en un estudio no aleatorizado de la práctica clínica
| Tasa de eventos/100 personas-año | HR | IC95% | ||
|---|---|---|---|---|
| Rivaroxabán (n = 10.017) | Warfarina (n = 11.665) | |||
| Lesión renal aguda | 7,70 | 13,45 | 0,83 | 0,74-0,92 |
| Progresión a enfermedad renal crónica en estadio 5 o necesidad de hemodiálisis | 3,74 | 6,03 | 0,82 | 0,70-0,96 |
Tabla elaborada con datos de Hernández et al59. HR: hazard ratio; IC95%: intervalo de confianza del 95%.
Varios estudios han demostrado que la anticoagulación de los pacientes con ERC es beneficiosa. Así, en los pacientes con ERC en estadio 3 incluidos en los estudios de fase III SPAF (Stroke Prevention in Atrial Fibrillation), el uso de warfarina se asoció con una reducción significativa del 76% en el riesgo de ictus isquémico o embolia sisté- mica, y sin diferencias en el riesgo de hemorragia mayor en compara-ción con el ácido acetilsalicílico61. En otro estudio que incluyó a pacientes con ERC no dializados y CHA2DS2-VASc > 2, la warfarina redujo significativamente en un 29% el riesgo de ictus y hemorragias mortales y la muerte por cualquier causa en un 36%62.
Sin embargo, el tratamiento con AVK se asocia con importantes limitaciones en los pacientes con ERC. Además de las limitaciones habituales (estrecha ventana terapéutica, respuesta variable a la anticoagulación, múltiples interacciones, etc.), en el paciente con ERC existen algunas limitaciones adicionales (mayor riesgo de ictus en pacientes en hemodiálisis, nefropatía por warfarina, mayor difi-cultad para lograr un adecuado control de la anticoagulación, aumento en el riesgo de calcificación vascular, efectos secundarios y hemorragias), que no solo podrían hacer más difícil su empleo en esta población, sino incluso empeorar la evolución de la enfermedad renal de base25.
En este contexto, la evidencia disponible plantea ventajas de los ACOD sobre los AVK. En los ensayos clínicos fundamentales, se incluyó a un 20% de pacientes con insuficiencia renal moderada (tabla 1)50-53. En su conjunto, el beneficio de los ACOD frente a la warfarina en cuanto al riesgo de ictus o embolia sistémica y de hemorragias mayo-res fue independiente de la función renal (tabla 2)49. Al analizar cada ensayo clínico individualmene, y teniendo en cuenta que se trata de datos obtenidos de análisis de subgrupos, es importante destacar que tanto los eventos tromboembólicos como las complicaciones hemo-rrágicas fueron más frecuentes en los pacientes con ERC que en aque-llos con función renal normal62-66. En el estudio RE-LY, los resultados en los pacientes con ERC concuerdan con los del ensayo clínico gene-ral. Sin embargo, en el análisis de subgrupos hubo un menor riesgo de hemorragias mayores con el dabigatrán en los que tenían un aclara-miento de creatinina ≥ 80 ml/min63. Por otro lado, tanto en el estudio ROCKET-AF como en el ARISTOTLE, la eficacia y la seguridad del riva-roxabán y el apixabán frente a warfarina concuerdan con los resulta-dos generales independientemente de la función renal64,65. Final-mente, aunque en el estudio ENGAGE AF-TIMI 48 la seguridad y el beneficio clínico neto fueron independientes de la función renal, el análisis exploratorio mostró un aparente descenso en la eficacia rela-tiva del edoxabán en comparación con la warfarina en la reducción de las complicaciones tromboembólicas en la banda alta de aclaramiento de creatinina (> 95 ml/min). Sin embargo, a causa de los menores índices de hemorragia mayor, el beneficio clínico neto fue más favora-ble con dosis altas de edoxabán en todo el espectro del aclaramiento de creatinina66.
También hay evidencia de la práctica clínica real de la utilidad de los ACOD en los pacientes con ERC. En un análisis retrospectivo de bases de datos de 39.872 pacientes tratados con rivaroxabán (3.572 con insuficiencia renal) y 48.637 con warfarina (8.230 con insuficien-cia renal), los pacientes con insuficiencia renal tratados con este ACOD mostraron una reducción significativa del 45% en el riesgo de ictus isquémico, en ausencia de incremento del riesgo de hemorragias mayores67.
En el ROCKET-AF se analizó específicamente qué es lo que ocurría con los pacientes que presentaban un deterioro de la función renal durante el seguimiento del estudio, pacientes estos con un mayor riesgo de muerte CV, y para los que se observó, en comparación con warfarina, una reducción significativa del ictus o la embolia sistémica (1,54 frente a 3,25 eventos/100 pacientes-años; HR = 0,50; IC95%, 0,27-0,93) en los tratados con rivaroxabán68.
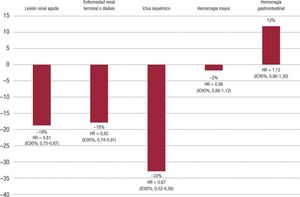
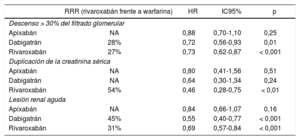
De todos es sabido que los pacientes presentan un deterioro de la función renal asociado al envejecimiento, un deterioro progresivo que es mayor en sujetos con ciertas comorbilidades, como la FA y la DM. Los AVK pueden contribuir al daño estructural renal y al deterioro de la función renal, sobre todo en pacientes con mal control de la anti-coagulación, lo que ha dado pie a hablar de la «nefropatía por warfa-rina o por AVK»25. En el estudio de Yao et al.69 se estudió el efecto de los diferentes ACOD en comparación con warfarina en el descenso en el filtrado glomerular, la duplicación de la creatinina sérica y la lesión renal aguda, analizando los datos obtenidos de una base de datos nor-teamericana de prescripción en la práctica clínica. Aunque los pacien-tes con warfarina y apixabán tenían más edad, un CHA2DS2-VASc mayor y un filtrado glomerular menor que los pacientes con rivaroxa-bán y dabigatrán, las poblaciones se emparejaron mediante propen-sity score. Mientras que el apixabán mostró un efecto similar al de la warfarina, el dabigatrán y el rivaroxabán mostraron un efecto benefi-cioso renal en comparación con los AVK (tabla 5)69. Este beneficio del rivaroxabán en comparación con la warfarina en las complicaciones renales también se ha observado en otro estudio en práctica clínica no aleatorizado, con reducciones significativas en el riesgo de lesión renal aguda y enfermedad renal terminal o diálisis (Figura 2)70.
Efectividad y seguridad de los ACOD frente a la warfarina en el deterioro de la función renal de pacientes con fibrilación auricular no valvular diabéticos y no diabéticos en un estudio no aleatorizado de la práctica clínica
| RRR (rivaroxabán frente a warfarina) | HR | IC95% | p | |
|---|---|---|---|---|
| Descenso > 30% del filtrado glomerular | ||||
| Apixabán | NA | 0,88 | 0,70-1,10 | 0,25 |
| Dabigatrán | 28% | 0,72 | 0,56-0,93 | 0,01 |
| Rivaroxabán | 27% | 0,73 | 0,62-0,87 | < 0,001 |
| Duplicación de la creatinina sérica | ||||
| Apixabán | NA | 0,80 | 0,41-1,56 | 0,51 |
| Dabigatrán | NA | 0,64 | 0,30-1,34 | 0,24 |
| Rivaroxabán | 54% | 0,46 | 0,28-0,75 | < 0,01 |
| Lesión renal aguda | ||||
| Apixabán | NA | 0,84 | 0,66-1,07 | 0,16 |
| Dabigatrán | 45% | 0,55 | 0,40-0,77 | < 0,001 |
| Rivaroxabán | 31% | 0,69 | 0,57-0,84 | < 0,001 |
Tabla elaborada con datos de Yao et al69. ACOD: anticoagulantes orales de acción directa;
HR: hazard ratio; IC95%: intervalo de confianza del 95%; NA: no aplicable;
RRR: reducción relativa del riesgo.
Impacto del rivaroxabán en la función renal, la eficacia y la seguridad en pacientes con fibrilación auricular en un estudio no aleatorizado de la práctica clínica. Tabla elaborada con datos de Coleman et al70. HR: hazard ratio; IC95%: intervalo de confianza del 95%.
La DM y la ERC son 2 enfermedades muy frecuentes en nuestro medio, con una prevalencia creciente, y cuya asociación con la FA, por múltiples mecanismos, es evidente. Las 3 entidades, además de su no poco frecuente concomitancia, tienen un efecto sinérgico a la hora de determinar el riesgo cardioembólico total individual. No solo es que haya un mayor riesgo de FA, sino que además el riesgo de ictus se encuentra marcadamente elevado cuando coexisten estas entidades, por lo que la anticoagulación es prioritaria para prevenir el riesgo de complicaciones tromboembólicas. Ahora bien, tanto en el paciente con DM como con ERC, no solo es importante la prevención del ictus con el tratamiento anticoagulante, sino que habría que buscar benefi-cios adicionales más allá de la prevención de las complicaciones tromboembólicas para optimizar el abordaje de estos pacientes y ase-gurar una protección integral, máxime cuando algunas estrategias anticoagulantes pueden deteriorar la función renal.
En las últimas guías de DM tanto nacionales como internacionales se propone que el abordaje del diabético se debe realizar de manera integral, no solo buscando el control metabólico (HbA1c), sino sobre todo utilizando los tratamientos con demostrado beneficio en cuanto a la reducción de los eventos CV71. En este contexto conceptual, la anti-coagulación se hace prioritaria para disminuir el riesgo de complicacio-nes tromboembólicas24, y en este sentido, la guía europea recomienda el uso de los ACOD para la anticoagulación de pacientes con FA y DM con un grado de recomendación máxima (I A)71. Todos los anticoagu-lantes se han demostrado útiles en la prevención de las complicaciones tromboembólicas. Ahora bien, con las limitaciones de los estudios ana-lizados, la reducción del 20% en el riesgo de muerte CV observada en el análisis de subgrupos del ROCKET-AF, así como el descenso de MACE observado en algunos estudios de práctica clínica indican un beneficio adicional, si bien son necesarios más estudios para confirmar estos datos. Es importante ser prudentes en la interpretación de los datos observacionales y, a menos que los ensayos clínicos prospectivos con-firmen estos hallazgos, la potencial reducción del riesgo renal obser-vada con algunos ACOD continúa siendo especulativa55,57,60.
La ERC aumenta el riesgo tanto de ictus como de hemorragias en el paciente con FA. Aunque los AVK reducen eficazmente el riesgo de ictus en los sujetos con FA, tienen numerosas limitaciones que dificul-tan su uso en la práctica clínica, y especialmente la nefropatía por warfarina, que implica un mayor deterioro de la función renal que el correspondiente a la edad o las comorbilidades de los pacientes25. En cualquier caso, la disminución de la función renal es común entre los pacientes con FA tratados con cualquier anticoagulante oral. Los ACOD, particularmente el dabigatrán y el rivaroxabán, pueden estar asociados con menores riesgos de eventos renales adversos en com-paración con la warfarina69.
Ahora bien, a pesar de las ventajas que los ACOD ofrecen frente a los AVK, uno de los problemas que se plantean con los primeros es la dosificación inadecuada, principalmente la infradosificación, lo que se traduce en una menor protección para la prevención de los ictus69,72. Es evidente que la dosificación de los ACOD se debería realizar de acuerdo con la ficha técnica de cada uno de ellos y aplicar las dosis menores solo en los casos indicados24, y no según la percepción del riesgo hemorrágico, ya que, como indican los resultados del estudio PREFER in AF, el riesgo de hemorragia depende más de determinadas características del paciente que del hecho de estar anticoagulado73.
ConclusionesExiste una estrecha sinergia entre la DM y la ERC con el riesgo de FA no valvular y fenómenos tromboembólicos relacionados con estas 3 entidades, de tal manera que, si bien los pacientes con FA tienen un riesgo incrementado de ictus, este aumenta todavía más cuando coe-xisten tanto con la DM como con la ERC. No solo es importante redu-cir el riesgo de ictus en el paciente con FA no valvular, sino que es necesario buscar una protección integral del paciente. En el caso de la DM, reduciendo el riesgo de complicaciones CV, en particular la muerte CV, y en el caso de la ERC, manteniendo su eficacia y su segu-ridad. Todos los anticoagulantes se han demostrado útiles en la pre-vención de las complicaciones tromboembólicas. Sin embargo, la reducción del 20% en el riesgo de muerte CV observada en el análisis de subgrupos del ROCKET-AF en la población diabética, así como el menor riesgo de complicaciones renales en comparación con warfa-rina indican un beneficio adicional, que es necesario confirmar en estudios específicos.
AgradecimientosContent Ed Net (Madrid) proporcionó asistencia editorial en la redacción de este manuscrito, con financiación de Bayer Hispania.
Conflicto de interesesJ.M. Cepeda ha recibido honorarios por asesoría o ponencias de Bayer, Daiichi-Sankyo y BMS-Pfizer. V.I. Arrarte ha recibido honora-rios en los últimos años por formación de laboratorios: Bayer, Daiichi-Sankyo, Pfizer, Bristol-Myers Squibb y Boehringer Ingelheim. L. Facila Rubio ha recibido honorarios por asesoría y ponencias de Bayer, Daiichi-Sankyo, BMS-Pfizer y Boehringer Ingelheim. V. Giner Galvañ ha recibido honorarios por actividades formativas y becas para asistencia a diversas reuniones científicas por parte de diversos laborato-rios, entre ellos Abbott, Takeda, Bayer y otros. J.L. Górriz ha recibido honorarios por realizar ponencias: Bayer Hispania, Daiichi Sankyo, Boehringer Ingelheim, Pfizer. J. Trujillo declara no tener conflictos de intereses.