Full English text available from: www.revespcardiol.org/en
El infarto agudo de miocardio con elevación del segmento ST (IAMCEST) es consecuencia de la oclusión brusca de una arteria coronaria epicárdica. La aplicación rápida de una intervención coronaria percutánea (ICP) primaria ha pasado a ser el tratamiento de elección para los pacientes afectados. La reperfusión mecánica con implantación de stents liberadores de fármacos (SLF) o farmacoactivos se ha asociado a una mejora de la seguridad y la eficacia en comparación con la angioplastia con balón sola o el implante de stents metálicos sin recubrimiento (SMSR)1.
STENTS LIBERADORES DE FÁRMACOS DE PRIMERA GENERACIÓNEl stent liberador de paclitaxel (SLP) Taxus® (Boston Scientific; Boston, Massachusetts, Estados Unidos) y el stent liberador de sirolimus (SLS) Cypher® (Cordis Corporation; New Jersey, Estados Unidos) fueron los primeros SLF de primera generación que se emplearon en la práctica clínica. Posteriormente, multitud de datos clínicos han mostrado la eficacia superior de los SLF de primera generación respecto a los SMSR. Un metanálisis en red, con una comparación combinada de los diversos tratamientos, en el que se incluyeron datos de 38 ensayos que emplearon SMSR, SLP y SLS describió menos riesgo de necesidad de nueva revascularización (revascularización de lesión diana) a los 4 años de seguimiento con ambos SLF que con los SMSR, y no hubo diferencias en la mortalidad. Se observaron unos riesgos comparables de trombosis del stent (TS) definitiva (0 días-4 años); sin embargo, la TS definitiva tardía (> 30 días) aumentó con el uso de SLP en comparación con los SMSR o los SLS. Además, los SLS fueron los stents que se asociaron a un riesgo más bajo de infarto de miocardio (IM) (razón de riesgos [HR] = 0,83; intervalo de confianza del 95% [IC95%], 0,71-1,00; p=0,045 frente a los SLP).2 En la misma línea, un metanálisis de 16 ensayos de comparación de los SLS con los SLP mostró resultados favorables a los primeros, con una reducción significativa del riesgo de reintervención y de TS, así como una tendencia a mayor riesgo de IM con los SLP3.
STENTS LIBERADORES DE FÁRMACOS DE NUEVA GENERACIÓNMientras tanto, se introdujeron los SLF de nueva generación, caracterizados por una mejora de las plataformas metálicas, el uso de polímeros más biocompatibles y la incorporación de nuevos fármacos antiproliferativos. Los SLS y los SLP utilizaban plataformas de acero inoxidable, con unos struts relativamente gruesos, mientras que los nuevos SLF utilizan aleaciones de cobalto-cromo (CoCr) o de platino-cromo. Estas últimas permitieron diseñar plataformas metálicas con struts finos, que aportan más aplicabilidad, visibilidad y adaptabilidad, un menor contenido de níquel y molibdeno y una reendotelización más rápida. Se utilizaron polímeros novedosos, específicamente diseñados para mejorar la biocompatibilidad, puesto que los polímeros de los SLF de primera generación se asociaban a un retraso en las reacciones de cicatrización e inflamatorias. Los SLF de nueva generación aprobados por la Food and Drug Administration incluyen el stent liberador de everolimus (SLE) de CoCr (SLE-CoCr) Xience V® (Abbott Vascular; California, Estados Unidos) y el stent liberador de zotarolimus Endeavor Resolute® (Medtronic; Minnesota, Estados Unidos), entre otros.
Hoy hay más de 40 plataformas en diferentes fases de desarrollo que se están utilizando en todo el mundo. Las innovaciones consecutivas incluyen la superioridad demostrada de los struts más finos, la incorporación de polímeros biodegradables como portadores de los fármacos, la liberación de fármacos exenta de polímeros que utilizan superficies microporosas o nanoporosas como portadoras, la liberación exclusivamente abluminal del fármaco para evitar efectos tóxicos endoteliales, los SLF duales que combinan propiedades antiproliferativas y procicatrizantes e incluso los armazones completamente bioabsorbibles4. La evidencia clínica basada en ensayos aleatorizados ha puesto de manifiesto que los SLE-CoCr y los stents liberadores de zotarolimus Endeavor Resolute® han alcanzado unos excelentes resultados de seguridad y eficacia, tanto a corto como a largo plazo. Los SLE-CoCr son los que se han asociado a la tasa de TS más baja, incluso en comparación con los SMSR5.
COMPARACIONES ENTRE STENTS LIBERADORES DE PACLITAXEL Y LIBERADORES DE EVEROLIMUSLos ensayos clínicos del proyecto SPIRIT, así como el ensayo COMPARE con inclusión de todos los pacientes consecutivos, han aportado un amplio conjunto de evidencias para la comparación de los SLP con los SLE-CoCr. Los resultados de los ensayos individuales, los análisis de subgrupos de poblaciones específicas y los datos de registro disponibles se resumen en la tabla. En un análisis combinado de datos de pacientes de los ensayos SPIRIT II, III, IV y COMPARE, con un total de 6.789 pacientes, el tratamiento con SLE fue un potente factor independiente predictivo de la ausencia de IM, revascularizaciones y eventos cardiovasculares adversos mayores a los 2 años27. Además, un metanálisis del seguimiento a 3 años de los ensayos SPIRIT puso de manifiesto que los SLE, en comparación con los SLP, reducían significativamente la mortalidad por todas las causas (el 3,2 frente al 5,1%; p=0,003) y el riesgo de TS definitiva o probable (el 0,7 frente al 1,7%; p=0,003)28.
Comparación de los stents liberadores de paclitaxel de primera generación con los stents liberadores de everolimus de nueva generación
| A. ECA (SLE frente a SLP) | SPIRIT II6 | SPIRIT III7 | SPIRIT IV8 | SPIRIT V9 | COMPARE10 | EXECUTIVE11 | PROMISE12 |
| Características de la población | Lesiones de novo, pacientes no complejos | Lesiones de novo, pacientes no complejos | Lesiones de novo, pacientes no complejos | Pacientes diabéticos | Estudio de todos los pacientes tratados | EC multivaso | Lesiones de novo, pacientes no complejos |
| Pacientes, n | 223 frente a 77 | 669 frente a 333 | 2.458 frente a 1.229 | 261 frente a 115 | 897 frente a 903 | 103 frente a 97 | 425 frente a 425 |
| Seguimiento angiográfico (meses) | 6 | 8 | — | 9 | — | 9 | — |
| Pérdida luminal tardía en el stent (mm) | 0,11 frente a 0,36a | 0,16 frente a 0,30a | — | 0,19 frente a 0,39a | — | 0,05 frente a 0,24a | — |
| Reestenosis en el stent, % | 1,3 frente a 3,5 | 2,3 frente a 5,7 | — | 3,1 frente a 6,1 | — | — | — |
| Seguimiento clínico más largo (meses) | 60 | 60 | 36 | 24 | 36 | — | 24 |
| MACEb | 8,0 frente a 18,1a | 13,7 frente a 20,2a | — | 11,2 frente a 12,5 | 9,3 frente a 14,5a | 11,1 frente a 16,5 | 2,5 frente a 5,6a |
| Muerte (cardiaca) | 1,5 frente a 7,3a | 5,9 frente a 10,1a,c | 3,2 frente a 5,1a | 0,5 frente a 2,9 | 4,9 frente a 5,1 | 1,0 frente a 1,1 | 1,2 frente a 1,5c |
| Infarto de miocardio | — | 4,4 frente a 6,3 | 3,0 frente a 4,6a | 2,8 frente a 8,7a,d | 5,2 frente a 9,9a | 1,0 frente a 3,3 | 0,2 frente a 0,8 |
| Revascularización de lesión diana | 4,7 frente a 9,4e | 8,6 frente a 12,1e | 6,2 frente a 7,8e | 8,4 frente a 3,8e | 3,7 frente a 7,6a,e | 6,1 frente a 7,7e | 1,2 frente a 3,5a |
| Trombosis de stent definitiva/probable | 0,9 frente a 2,8 | 1,4 frente a 1,6 | 0,6 frente a 1,6a | 0,0 frente a 1,9 | 1,4 frente a 4,9a | — | 0,7 frente a 0,3 |
| B. Análisis de subgrupos de ECA (SLE frente a SLP) | SPIRIT II y III13 | SPIRIT II y III14 | SPIRIT III15 | SPIRIT III y IV16 | SPIRIT IV17 | SPIRIT IV18 | COMPARE19 |
| Características de la población | Vasos pequeños (< 2,765 mm) | Mujeres | Pacientes ancianos (≥ 65 años) | EC multivaso | Pacientes diabéticos | Ramas laterales enjauladas | IAMCEST/IAMSEST |
| Pacientes, n | 376 frente a 165 | 177 frente a 80 | 293 frente a 141 | 511 frente a 274 | 786 frente a 399 | 963 frente a 463 | 434 frente a 429 |
| Seguimiento angiográfico (meses) | 6 y 8 | 6 y 8 | 8 | — | — | — | — |
| Pérdida luminal tardía en el stent (mm) | 0,15 frente a 0,30a | 0,09 frente a 0,29a | 0,15 frente a 0,45a | — | — | — | — |
| Reestenosis en el stent, % | 2,3 frente a 5,7 | 3,1 frente a 7,4 | 2,7 frente a 12,7a | — | — | — | — |
| Seguimiento clínico más largo (meses) | 12 | 24 | 36 | 12 | 12 | 24 | 24 |
| MACEb | 5,2 frente a 10,7a | 8,5 frente a 16,4a | 7,9 frente a 15,4a | 6,2 frente a 12,5a | 6,4 frente a 7,1 | 6,6 frente a 12,2a | 9,2 frente a 16,1a |
| Muerte (cardiaca) | 0,8 frente a 0,6 | 0,8 frente a 0,8 | 1,4 frente a 3,0 | 0,8 frente a 1,1 | 0,9 frente a 0,3 | 1,0 frente a 1,4 | 3,0 frente a 3,0 |
| Infarto de miocardio | 1,9 frente a 5,0 | 2,7 frente a 7,0a | 3,2 frente a 4,6 | 2,2 frente a 6,1a,d | 2,6 frente a 3,7 | 2,0 frente a 5,4a,d | 4,2 frente a 8,2a |
| Revascularización de lesión diana | 3,0 frente a 6,3 | 6,2 frente a 9,4 | 4,0 frente a 7,7 | 4,2 frente a 8,0a | 4,2 frente a 4,7 | 4,1 frente a 7,9a,e | 3,0 frente a 6,5a |
| Trombosis de stent definitiva/probable | 0,3 frente a 1,9 | 1,2 frente a 0,8 | 1,4 frente a 0,0 | 1,2 frente a 2,7 | 0,8 frente a 1,33 | 1,1 frente a 6,3a | 1,4 frente a 4,7a |
| C. Datos de registros (SLE frente a SLP) | Taniwaki et al20 | ESTROFA-LM21 | FLM Taxus y LEMAX22 | Valenti et al23 | Simsek et al24 | GHOST25 | ESTROFA-IM26 |
| Características de la población | Injertos de vena safena | Principal izquierda | Principal izquierda | Oclusiones totales crónicas | Pacientes diabéticos | Pacientes consecutivosf | IAMCEST |
| Pacientes, n | 127 frente a 58 | 355 frente a 415 | 172 frente a 172 | 112 frente a 146 | 804 frente a 547 | 287 frente a 287 | 350 frente a 350 |
| Seguimiento clínico más largo (meses) | 48 | 36 | 24 | 9 | 36 | 24 | 24 |
| MACEb | 58,7 frente a 45,6 | 18,0 frente a 16,4 | 7,6 frente a 17,4a | 8,9 frente a 22,6a | 18,0 frente a 20,6 | 13,0 frente a 19,0 | 14,9 frente a 11,5a |
| Muerte (cardiaca) | 15,3 frente a 21,8 | — | 2,3 frente a 6,4 | 0,9 frente a 2,1 | 12,0 frente a 9,6 | 7,0 frente a 9,1 | 9,2 frente a 9,0c |
| Infarto de miocardio | 9,1 frente a 1,8 | — | 4,1 frente a 9,9a,d | 0,0 frente a 2,1 | 3,1 frente a 7,4 | 5,6 frente a 7,3 | — |
| Revascularización de lesión diana | 25,8 frente a 12,6 | 6,0 frente a 4,0 | 4,1 frente a 6,4 | 8,0 frente a 20,5a,g | 5,6 frente a 11,5a | 4,2 frente a 8,4a,g | 4,6 frente a 2,9 |
| Trombosis de stent definitiva/probable | 10,1 frente a 5,7 | — | 0,6 frente a 1,2 | — | 6,8 frente a 10,2 | 1,1 frente a 3,8a | 4,3 frente a 1,4a |
EC: enfermedad coronaria; ECA: ensayos controlados y aleatorizados; IAMCEST: infarto agudo de miocardio con elevación del segmento ST; IAMSEST: infarto agudo de miocardio sin elevación del segmento ST; MACE: eventos cardiovasculares adversos mayores; SLE: stents liberadores de everolimus; SLP: stent liberador de paclitaxel.
El análisis de ciertos subgrupos importantes (vasos pequeños, mujeres, ancianos, enfermedad de múltiples vasos, etc.) ha corroborado la superioridad de los SLE respecto a los SLP, con la notable excepción de los pacientes diabéticos, en los que el SLP produjo unos resultados clínicos similares.
ESTUDIOS DE LA CICATRIZACIÓN VASCULAR Y DE AUTOPSIAEl deterioro de la cicatrización arterial se caracteriza por una reendotelización incompleta, un engrosamiento mínimo de la neoíntima y la persistencia de fibrina, y es un sustrato importante para la trombosis tardía de los SLF29. Las técnicas de imagen intravasculares permiten la identificación de los struts no cubiertos, la mala aposición adquirida tardía, el remodelado positivo y las protuberancias coronarias. En comparación con los SLE, los SLP han mostrado una mayor frecuencia de struts no cubiertos y con mala aposición (el 5,2 frente al 2,3% y el 5,7 frente al 2,1%; p<0,001) en los estudios de tomografía de coherencia óptica realizados a los 6 meses30. En otro estudio llevado a cabo 1 año después del implante simultáneo de SLP y SLE en 30 pacientes, los SLP se asociaron de manera significativa a un porcentaje superior de struts con mala aposición y no cubiertos (el 62 frente al 15%; p<0,001) y a un área de mala aposición proximal mayor (0,6±0,3 frente a 0,25±0,2mm2; p=0,001)31.
En esta misma línea, Otsuka et al describieron una frecuencia superior de TS tardía y muy tardía (el 26 frente al 4%; p<0,001), un porcentaje más alto de struts no cubiertos (el 18,7 frente al 2,6%; p<0,001) y mayores puntuaciones de inflamación y de depósito de fibrina con los SLP en comparación con los SLE, en casos de autopsia con un tiempo tras el implante > 30 días y<3 años32. Tiene interés señalar que un informe reciente, en el que se compararon dos dispositivos con la misma plataforma y el mismo polímero biodegradable pero con fármacos diferentes (everolimus o paclitaxel) en un modelo porcino, muestra menos endotelización (un 40±4% frente al 100%) y mayor puntuación de inflamación a los 28 días (2,1±0,3 frente a 1,0), así como una menor inhibición de la hiperplasia de neoíntima a los 90 días con paclitaxel33.
STENTS LIBERADORES DE PACLITAXEL FRENTE A LIBERADORES DE EVEROLIMUS EN PACIENTES CON INFARTO AGUDO DE MIOCARDIO CON ELEVACIÓN DEL SEGMENTO STEn un artículo publicado en Revista Española de Cardiología, de la Torre Hernández et al presentan los resultados de un estudio de registro multicéntrico retrospectivo en el que se comparó, en pacientes con IAMCEST tratados con ICP primaria, el implante de SLP o SLE. Además, los autores presentan un análisis estratificado según el uso de trombectomía26. Se utilizó la igualación por propensity score con objeto de introducir una corrección respecto a las diferencias existentes en las características basales en una cohorte de 1.042 pacientes, con lo que se obtuvieron dos grupos de 350 pacientes con unas características basales, angiográficas y de la intervención similares.
Los análisis retrospectivos tienen el inconveniente de que, mientras se intenta reducir el sesgo de selección (es decir, la elección del stent por el operador), adquieren mayor importancia otras limitaciones como la falta de criterios de evaluación clínica e hipótesis definidas prospectivamente y las diferencias temporales; además, los posibles factores de confusión desconocidos limitan siempre la interpretación de las comparaciones realizadas con igualación por propensity score. Para los fines de este estudio, 16 centros debían aportar dos cohortes diferentes y consecutivas de 30 pacientes, una de ellas tratada entre 2005 y 2007 y la otra, entre 2006 y 2009. En estos pacientes, todas las lesiones debían haberse tratado con el mismo tipo de stent (SLP o SLE) en el contexto de una ICP primaria, y se excluyó a los pacientes que estaban en shock cardiogénico.
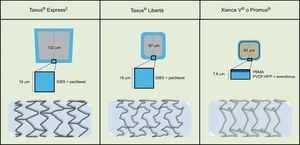
Al stent Taxus® se le ha asignado la marca CE (Conformité Européenne) para tres plataformas, Taxus® Express2 (enero de 2003), Taxus® Liberté (septiembre de 2005) y Taxus® Element (mayo de 2010). En el marco del presente estudio se utilizaron las dos primeras. En el ensayo TAXUS ATLAS, se asignó aleatoriamente a 1.862 pacientes al Taxus® Liberté o el Taxus® Express2, y en los primeros se alcanzó un resultado de no inferioridad, con ausencia de diferencias significativas en cuanto a eficacia y seguridad34. El SLE Xience V® (enero de 2006) y el SLE Promus® (octubre de 2006) son el mismo stent comercializado bajo marcas y nombres diferentes (figura).
Comparación esquemática del stent de primera generación liberador de paclitaxel Taxus® y el stent de nueva generación liberador de everolimus Xience V® o Promus®. SIBS: poliestireno-b-isobutileno-b-estireno; PBMA: poli-n-butil metacrilato; PVDF-HFP: copolímero de fluoruro de vinilideno y hexafluoropropileno.
No resultó extraño que los SLP se asociaran a una incidencia superior de muerte, IM o revascularización de lesión diana a los 2 años (el 14,9 frente al 11,5%; p=0,04) y de la TS definitiva o probable (el 4,3 frente al 1,4%; p=0,01) en comparación con los SLE. No se observaron diferencias significativas en cuanto a la incidencia de mortalidad por cualquier causa (el 9,2 frente al 9,0%; p=0,51). Se han descrito resultados similares en un análisis post-hoc del ensayo COMPARE, con la inclusión de 864 pacientes con IAMCEST y 411 pacientes con infarto agudo de miocardio sin elevación del segmento ST, en el que se observó una reducción significativa del objetivo principal combinado de muerte por cualquier causa, IM y revascularización del vaso diana (el 9,2 frente al 16,1%; p=0,002), así como de la TS definitiva o probable (el 1,4 frente al 4,7%; p=0,005) empleando los SLE en comparación con los SLP a los 2 años19. Es de destacar que el ensayo HORIZONS-AMI, en el que se incluyó a un total de 3.006 pacientes en la asignación aleatoria a SLP o SMSR (3:1), demostró que con los primeros se reduce significativamente la tasa de revascularización de la lesión diana a causa de isquemia a los 12 meses (un efecto beneficioso que se mantuvo durante 3 años), sin que hubiera aumento alguno del objetivo combinado de seguridad formado por muerte, reinfarto, ictus y TS35.
La única comparación directa entre los SLE-CoCr y los SLF de primera generación en pacientes con síndrome coronario agudo (el 96% con IAMCEST) es la derivada del ensayo XAMI36, en el que se asignó aleatoriamente (2:1) a 625 pacientes a SLE-CoCr o SLS. Las características basales de esta población revelan un riesgo ligeramente inferior en comparación con la población del presente análisis, con menor frecuencia de factores de riesgo, ICP previa o IM de cara anterior. El objetivo principal combinado de muerte cardiaca, IM y revascularización de vaso diana fue comparable en los dos grupos (el 5,3 frente al 4,0%; p=0,10), sin que hubiera diferencias en la TS a 1 año (el 1,2 frente al 2,7%; p=0,21). En un metanálisis en red exhaustivo, que incluía 22 ensayos en los que se utilizaron SMSR, stents de primera generación y de nueva generación autorizados por la Food and Drug Administration, Palmerini et al37 describieron un menor riesgo de muerte o IM con los SLE-CoCr que con los SLP para los pacientes con IAMCEST (HR=0,73; IC95%, 0,54-0,98), así como menos riesgo de TS definitiva o probable (HR=0,32; IC95%, 0,12-0,71). Además, los SLE-CoCr se asociaron al perfil de seguridad y eficacia más favorable de entre todos los dispositivos, incluidos los SMSR37.
INTERACCIÓN ENTRE LA PLATAFORMA DEL STENT Y LA ASPIRACIÓN DEL TROMBOLa aspiración del trombo en el contexto de una ICP primaria por un IAMCEST sigue siendo objeto de controversia. En el ensayo TASTE (Thrombus Aspiration in ST-Elevation Myocardial Infarction in Scandinavia), el mayor estudio publicado hasta ahora de comparación entre trombectomía por aspiración e ICP primaria en pacientes con IAMCEST, no se pudo demostrar una diferencia de mortalidad por cualquier causa, reinfarto o revascularización de lesión diana a los 30 días. Sin embargo, se observó una tendencia a la reducción de las TS (HR=0,47; IC95%, 0,20-1,02; p=0,06)38. En un metanálisis actualizado que incluye a 11.321 pacientes de 20 ensayos controlados y aleatorizados, entre los que se encuentra el ensayo TASTE, Kumbhani et al han descrito recientemente una reducción significativa de la mortalidad tardía (6–12 meses) y menores tasas de IM (riesgo relativo=0,64; IC95%, 0,44-0,92; p=0,017) y TS (riesgo relativo=0,54; IC95%, 0,32-0,91; p=0,021)39. De la Torre Hernández et al han observado un mayor efecto beneficioso con SLE que con SLP en cuanto a la incidencia de TS cuando no se aplica la aspiración del trombo. En otras palabras, el uso de SLP se asoció a las tasas más altas de TS cuando no se realiza trombectomía. El proyecto ESTROFA (Estudio ESpañol sobre TROmbosis de stents FArmacoactivos) ha hecho aportaciones de interés en el campo de la cardiología intervencionista. En 2008, el primer informe, sobre 23.500 pacientes incluidos prospectivamente en el estudio, mostró una incidencia acumulada de TS tras el uso de SLF de primera generación de un 2% a los 3 años, sin que hubiera diferencias entre los SLP y los SLS40. Dos años más tarde, un segundo informe sobre 4.768 pacientes tratados con SLE-CoCr o stent liberador de zotarolimus indicó una incidencia acumulada de TS definitiva o probable a los 2 años del 1,7% con ambos dispositivos, pero con una tasa de TS superior en los pacientes con enfermedad de la bifurcación tratados con stent liberador de zotarolimus (HR=4,0; IC95%, 1,1-13,0; p=0,03)41. Más recientemente, el registro SCAAR, con la inclusión de 61.351 pacientes no seleccionados, tratados con SMSR, SLF de primera generación o de nueva generación, puso de manifiesto que los SLF de nueva generación se asocian a un riesgo de TS definitiva significativamente inferior que los SMSR (HR=0,38; IC95%, 0,28-0,52) y los SLF de primera generación (HR=0,57; IC95%, 0,41-0,79)42.
En resumen, los SLP de primera generación se han sustituido en gran parte por los SLF de nueva generación, que tienen un perfil de seguridad y eficacia más favorable, lo que parece ser de especial importancia en los pacientes con IAMCEST a los que se aplica una ICP primaria.
FINANCIACIÓNE. Spitzer ha recibido una beca de investigación de la EAPCI (European Association of Percutaneous Cardiovascular Interventions) de la European Society of Cardiology y una subvención de investigación de la Sociedad Española de Cardiología.
CONFLICTO DE INTERESESS. Windecker ha tenido contratos de investigación con la institución de Biotronik y St. Jude Medical.