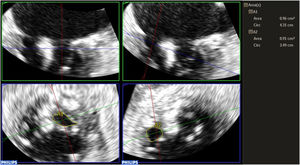
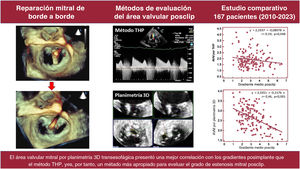
La reparación mitral percutánea de borde a borde es una técnica con poca evidencia acerca del método más preciso para medir el área valvular mitral (AVM) posprocedimiento. Nuestro objetivo fue evaluar el mejor método en este contexto y su correlación con el gradiente medio transvalvular.
MétodosSe realizó un registro de pacientes sometidos a reparación mitral percutánea, y se analizaron los diferentes métodos de medición de AVM y su correlación con el gradiente medio.
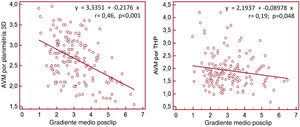
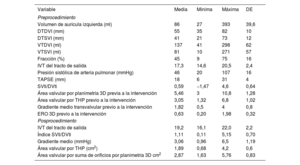
ResultadosSe incluyó a 167 pacientes, con una edad media de 76 años (± 10,3); el 54% eran varones y el 46% mujeres; con etiología degenerativa (45%), funcional (39%) y mixta (16%). Las medidas de AVM posclip fueron 1,89±0,60 cm2 mediante tiempo de hemipresión (THP) y 2,87±0,83 cm2 mediante planimetría 3D, y el gradiente medio promedio fue de 3±1,19mmHg. El AVM mediante planimetría 3D presentó una mejor correlación con el gradiente medio (r=0,46, p<0,001) que el AVM obtenida por THP (r=0,19, p=0,048), así como una mayor concordancia interobservador que la obtenida por el THP (coeficiente de correlación intraclase de 0,90 frente al 0,81%, y coeficiente de variación de 9,6 frente al 19,7%, respectivamente).
ConclusionesNuestro estudio muestra que el THP infraestima significativamente el AVM posimplante de clip mitral comparado con la medición directa mediante planimetría 3D transesofágica, y que este último método presenta una mejor correlación con los gradientes posimplante y una menor variabilidad interobservador, lo que sugiere que es un método más apropiado para evaluar la estenosis mitral en este contexto.
Palabras clave
Identifíquese
¿Aún no es suscriptor de la revista?
Comprar el acceso al artículo
Comprando el artículo el pdf del mismo podrá ser descargado
Precio: 19,34 €
Teléfono para incidencias
De lunes a viernes de 9h a 18h (GMT+1) excepto los meses de julio y agosto que será de 9 a 15h