La angioplastia primaria está reconocida como la mejor estrategia de reperfusión en el infarto agudo de miocardio con elevación del segmento ST. Como procedimiento comprende una serie de posibilidades técnicas y farmacológicas que influyen en diferente medida en sus resultados. El uso de los inhibidores de la glucoproteína IIb/IIIa está en continua discusión, con diferentes metaanálisis y estudios que siguen ofreciendo información acerca de los beneficios en los procedimientos intervencionistas y otros en los que no se aprecia tal efecto. El abciximab es el fármaco del que se dispone de más evidencia en la actualidad. La vía de acceso radial en el intervencionismo para disminuir el riesgo hemorrágico tiene como contrapartida aumentar los tiempos de procedimiento. Se analizan los dispositivos para prevenir la embolización y cómo, tras varios estudios sin demostrar mejoría en los parámetros clínicos, en la actualidad se está demostrando la efectividad de algunos de ellos. Por último, se analiza el manejo actual del shock cardiogénico, cómo se ha conseguido disminuir la mortalidad a base de reperfusión coronaria como medida más eficaz y la evidencia actual sobre el uso de los diferentes tratamientos para estabilizar al paciente.
Palabras clave
En la actualidad, tanto las sociedades norteamericanas como la europea de cardiología1,2 recomiendan, dentro de unos estándares de tiempo y calidad del centro asistencial, la reperfusión mecánica como el tratamiento de reperfusión de elección en el infarto agudo de miocardio con elevación del segmento ST (IAMCEST). De ésta existen diferentes tipos según el momento y las condiciones en que se realice; así, la intervención coronaria percutánea primaria (ICPp) es la que se aplica en los IAMCEST de menos de 12h desde el inicio de los síntomas con persistencia de las alteraciones en el ECG, y se realiza sin ninguna medicación fibrinolítica administrada previa o concomitantemente al procedimiento. En los centros con alto volumen de ICP, los resultados en cuanto a reducción de la mortalidad y consecución de flujo coronario óptimo son mejores y su efectividad, comparada con la fibrinolisis, muestra mayor reperfusión, menores tasas de reoclusión, mejor función ventricular y mejor pronóstico a largo plazo. En las guías europeas1, la ICPp tiene una indicación de clase I, nivel de evidencia A, y debe realizarse en general en menos de 2h desde el primer contacto médico, y si el infarto agudo de miocardio (IAM) es de menos de 2h, en menos de 90min (grado I, nivel de evidencia B si el infarto es extenso y el riesgo de sangrado es bajo). La AHA/ACC2 recomienda la ICPp en el IAM de menos de 3h si se puede realizar en menos de 60min y la recomienda para realizarlo lo antes posible si la duración de los síntomas es mayor de 3h, con un grado de evidencia IB en las guías de 2004, mientras que en la actualización de 20073 sólo se refiere a intentar realizar la ICP en los primeros 90min desde el contacto médico.
La ICP de rescate es la que se realiza cuando el fibrinolítico no ha conseguido reperfundir la arteria. En este punto se debe aclarar en qué momento se decide que el fármaco no ha realizado su función; uno de los criterios más aceptados es la resolución de < 50% del ST, en las derivaciones en que más asciende, a los 90min de iniciado el tratamiento, con o sin persistencia del dolor. Aquí aparece una de las dificultades para crear una pauta de actuación basada en la evidencia, ya que no hay unanimidad a la hora de definir la reperfusión, sobre todo en lo referente al tiempo, ya que hay quien valora la reperfusión a los 60min y la resolución del ST entre el 50 y el 75%. Varios estudios aleatorizados la han comparado con el tratamiento conservador; en el REACT4, la disminución en las tasas de reinfarto son tan importantes que el objetivo combinado de muerte, reinfarto, accidente cerebrovascular e insuficiencia cardiaca severa es favorable a la ICP de rescate respecto al tratamiento conservador o a la refibrinolisis. Varios metaanálisis5,6 posteriores muestran los beneficios de la angioplastia de rescate, con una tendencia a disminuir la mortalidad y descenso significativo de los ingresos por reinfarto e insuficiencia cardiaca pese a que hay mayor número de accidentes cerebrovasculares isquémicos y hemorragias menores.
La tercera opción de intervencionismo en el IAMCEST es la ICP facilitada, que es aquella en la que se administran fármacos para intentar la reperfusión mientras el paciente espera, bien por traslado, bien por retrasos en el mismo centro, a que le realicen una ICP. Varias estrategias con fibrinolíticos, combinados o no con inhibidores de la glucoproteína IIb/IIIa, han sido probadas en diferentes estudios y ninguna ha dado resultado respecto a la ICPp sola.
En todos los casos de ICP en el IAM existen diferentes opciones, bien con dispositivos, bien con fármacos, que buscan un mejor resultado inmediato en el procedimiento y, de ser posible, trasladarlo a medio-largo plazo.
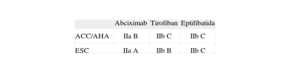
TRATAMIENTO ANTITROMBÓTICO PERIPROCEDIMIENTOInhibidores de la glucoproteína IIb/IIIaEl uso de estos fármacos antes de la ICP primaria tiene la finalidad de realizar el procedimiento en las mejores condiciones locales posibles, referidas a la arteria ocluida y a la antiagregación plaquetaria. Frecuentemente, este uso está considerado facilitación de la ICP pero, ateniéndonos estrictamente a su definición, no la incluiríamos ya que la finalidad no es intentar abrir la arteria; además, en muchas ocasiones se aplica en el mismo laboratorio de hemodinámica, antes o durante el procedimiento. De todos modos, su uso, aunque bastante generalizado, sigue puesto en duda, pues hay tanto estudios que los apoyan como otros que no muestran beneficio. Las guías de práctica clínica exponen su recomendación según el fármaco y la sociedad que las escribe, tal como se aprecia en la tabla 1.
Recomendaciones de las sociedades científicas sobre el uso de los diferentes inhibidores de la glucoproteína IIb/IIIa en la angioplastia primaria, sin especificar el momento de administración y sin considerar su uso como angioplastia facilitada
| Abciximab | Tirofiban | Eptifibatida | |
| ACC/AHA | IIa B | IIb C | IIb C |
| ESC | IIa A | IIb B | IIb C |
El estudio Admiral7 fue el que sentó la indicación del uso del abciximab en el IAMCEST tratado con ICPp. Además de su uso, se analizó a los pacientes en función del momento en que se administraba el fármaco, y la mayor parte se aplicó en el laboratorio de hemodinámica (73 frente a 26), y en los pacientes de fuera de esta localización se apreció significativamente menos tiempo de isquemia. A los 30 días el objetivo primero (MACE) era significativamente menor en los pacientes a los que el abciximab se administraba en la ambulancia o la sala de urgencias, y las diferencias a los 6 meses todavía eran mayores.
Diferentes estudios han mantenido esta práctica basada en la mayor permeabilidad del vaso en el momento de la ICP cuando se administra el fármaco, la mejoría en el flujo microvascular en el área del infarto, la disminución del tamaño de éste al aumentar la efectividad de las estrategias de reperfusión, la mejoría de la función ventricular y la disminución de eventos trombóticos adversos8. Diferentes metaanálisis han confirmado esta efectividad correlacionándola con eventos clínicos; en el realizado por Montalescot et al9, la administración de abciximab redujo en un 37% el riesgo relativo de muerte o reinfarto en un seguimiento a 3 años y la muerte en un 31%, aunque en contrapartida aumentaba ligeramente las hemorragias mayores en un 0,6% de forma absoluta. En el subgrupo de diabéticos, las reducciones son mayores, con un 47,5% menos riesgo relativo de muerte o reinfarto. Otro metaanálisis, publicado por De Luca et al10, muestra unos resultados similares con disminución significativa de los reinfartos a los 30 días y de la mortalidad a largo plazo. La publicación del estudio FINESSE11 en 2008 demostró que entre las diferentes opciones de tratamiento para facilitar la ICP, en el caso de la administración previa de abciximab, no se encontró ninguna ventaja con la ICPp sola, por lo que el uso de este tipo de fármacos está en entredicho pese a que en la práctica diaria se continúa usándolo por la evidencia de los estudios previamente nombrados y, en particular, en los pacientes con alto riesgo.
Respecto a los otros fármacos inhibidores de la glucoproteína IIb/IIIa, las llamadas moléculas pequeñas, tanto el tirofiban como la eptifibatida tienen interés debido a la reversibilidad más precoz de su acción antiagregante y el menor coste. Ambos presentan menor número de estudios en la ICPp y en ellos han demostrado un efecto similar al del abciximab en cuanto a beneficios en el procedimiento cuando se los compara con placebo12,13. Debido al menor número de pacientes en sus estudios, varios metaanálisis los han comparado con el abciximab, y ambos fármacos consiguen un efecto similar respecto al primero en beneficios clínicos14,15.
Otros antiagregantes plaquetariosLas novedades más importantes están en la familia de las tienopiridinas, en especial el clopidogrel, al menos mientras no se comercialice de forma general el prasugrel. La dosis de carga es el elemento más destacable como punto que comentar de este fármaco, una vez demostrado en el estudio PCI-CLARITY16 que 300mg como dosis de carga antes de la ICP disminuye los eventos trombóticos a los 30 días en un 10-20%. Estudios recientes con dosis de carga mayores han demostrado que el efecto antiagregante es mayor y se alcanza más rapidamente con 600mg que con 30017. Esto ha servido de base para probar nuevas estrategias en la ICPp; en el estudio BRAVE 318 se comparó la administración de abciximab tras una dosis de carga de 600mg en pacientes a los que se realizaba ICPp, y el fármaco intravenoso no ofreció beneficio adicional en términos de reducción del tamaño del infarto sobre el pretratamiento con clopidogrel, pero entre las limitaciones del estudio están que los pacientes no tenían alto riesgo y que carecía de la suficiente potencia estadística para demostrar diferencias clínicas; además, en el grupo del abciximab se produjeron menos trombosis del stent.
Inhibidores directos de la trombinaEl único disponible es la bivalirudina, que en las guías europeas tiene una recomendación de uso IIa B. En los estudios en que se la ha comparado con la heparina no fraccionada y los inhibidores de la glucoproteína IIb/IIIa, ha salido beneficiada por el menor número de hemorragias. En el estudio HORIZONS19 se aleatorizó a los pacientes con IAMCEST a las mismas medicaciones antes citadas e implante de stent recubierto de paclitaxel o convencional. A los 30 días los fallecimientos en el grupo de la bivalirudina fueron significativamente menos, tanto los de causa cardiaca como los no cardiacos, gracias a que disminuye la aparición de hemorragias. La incidencia de trombosis del stent fue significativamente mayor a las 24h en el grupo de la bivalirudina y no hubo diferencias a los 30 días.
VÍA DE ACCESO EN LA ICP PRIMARIALa vía de acceso es la principal pero no la más grave fuente de complicaciones hemorrágicas en el IAMCEST tratado con ICPp. Los pacientes ingresados por esta causa presentan un riesgo hemorrágico de por sí elevado debido a la edad, las comorbilidades como la insuficiencia renal y la suma de medicaciones antiagregantes y anticoagulantes. Los sangrados importantes pueden desencadenar una espiral de complicaciones que, en ocasiones, puede llevar a un aumento de los eventos isquémicos periprocedimiento. Para frenar la hemorragia se suspenden los fármacos antiagregantes y antitrombóticos, y las transfusiones que se requieren en ocasiones agregan nuevos factores de coagulación y plaquetas activadas que inducen trombosis. Por todo esto, la vía de acceso, aunque en muchas ocasiones no suficientemente reconocida, tiene gran importancia en el intervencionismo coronario. El acceso radial presenta menor número de complicaciones graves, tanto trombóticas como hemorrágicas, que el convencional femoral, pero penaliza con mayor duración del procedimiento y mayor dosis de radiación para el operador. Existen pocos estudios aleatorizados que comparen ambas vías en el IAM; uno de ellos, el FERIA20, realizado en España, incluyó a 439 pacientes, con 218 en el grupo femoral, y los resultados fueron que el procedimiento es más corto con el acceso femoral (9,5 ± 4,6 frente a 11,7 ± 5,8min), así como el tiempo hasta el inflado del primer balón (18 ± 8 frente a 21 ± 11min), de forma significativa. En el número de complicaciones y la tasa de éxito no hay diferencias, y sí las hay a favor de la vía radial en el coste del procedimiento incluido el ingreso. Otro estudio español, de Díaz de la Llera et al21, no encuentra diferencias entre una y otra vía de acceso. Esta vía de acceso en el IAM debería reservarse a operadores con amplia experiencia en su uso, ya que no sabemos hasta qué punto se puede penalizar el retraso en abrir la arteria respecto a disminuir las complicaciones hemorrágicas.
ELECCIÓN DEL TIPO DE STENT EN EL IAMCESTDurante 2007 se vivió la polémica sobre la seguridad en el uso de los stents farmacoactivos (SFA) cuando eran empleados en indicaciones off label, entre las que se encuentra el IAMCEST. Varios estudios publicados en esas fechas demostraron la efectividad en prevenir la reestenosis, sin aumentar el número de trombosis del stent, si bien eran estudios que carecían de seguimientos largos y tenían diferentes diseños22–25. En el registro ESTROFA, realizado en España, sobre la trombosis de los SFA en la práctica real, el IAMCEST es predictor independiente de trombosis tanto aguda como subaguda y tardía26. En la línea de los resultados del mundo real también está el estudio SORT OUT II, realizado en Dinamarca27, en el que se aleatorizó a pacientes con diferentes indicaciones (entre ellas IAMCEST) a implante de SFA con rapamicina o paclitaxel; el total de pacientes incluidos fue 368, de los que 194 recibieron stent con rapamicina. Los objetivos eran clínicos, y el primario era un combinado de muerte de origen cardiaco, infarto, TLR y TVR y el secundario, todos los anteriores por separado además de la trombosis del stent, según la definición de la Academic Research Consortium. No se encontraron diferencias significativas entre los dos grupos de pacientes tratados en el ojetivo primario ni en ninguno de los secundarios.
El estudio MISSION28 comparó el stent no farmacoactivo (SNFA) con el SFA recubierto de rapamicina, buscando como objetivo primario la pérdida luminal tardía (LL) en la angiografía de control a los 9 meses del implante y como objetivo secundario la mala aposición tardía, muerte, reinfarto, TLR, TVF, trombosis del stent y éxito del procedimiento. De los 310 pacientes reclutados, 158 fueron asignados al SFA; 131 (82,9%) de ellos completaron el seguimiento, y en el grupo del SNFA, el 81,6%. La LL fue significativamente menor en el grupo SFA (0,12 ± 0,43 frente a 0,68 ± 0,57; p < 0,001) tanto dentro del stent como en los bordes. La mala aposición del stent se dio significativamente más con el SFA (37,5%) a pesar del buen resultado angiográfico inicial conseguido, estando la mayor parte localizada en el cuerpo del stent, y aumentó de un 18,3% inmediatamente después del implante a un 25% en el seguimiento. En el SNFA la mala aposición se presentó en el 12,5% de los casos y cambió de un 11,3% en el implante a un 5% en el seguimiento. Los mecanismos que pueden explicarla pasan por subexpansión inicial del stent al no valorar el tamaño real del vaso debido a vasoconstricción por la situación adrenérgica del IAM, disolución del trombo entre la pared del vaso y el stent y remodelado positivo debido al fármaco. A pesar de estos datos, no hubo diferencias en la trombosis del stent y sí menos necesidad de nuevas revascularizaciones a largo plazo en el SC.
En el estudio MULTISTRATEGY29 se aleatorizó a los pacientes a cuatro grupos: abciximab con SNFA, abciximab con SFA recubierto de sirolimus, tirofiban con SNFA y tirofiban con SFA con sirolimus, con el objetivo primario de valorar la no inferioridad del tirofiban respecto al abciximab en la resolución del ST en los 90min después de la intervención y saber si el SFA es superior al SNFA en el objetivo combinado de muerte, reinfarto y TVR en los 8 meses siguientes. Respecto a la comparación entre los fármacos, se demostró la no inferioridad del tirofiban, y en cuanto a los stents, el SFA fue significativamente superior en el objetivo combinado (el 7,8 frente al 14,5%; p = 0,004) a expensas de disminuir la necesidad de nuevas revascularizaciones del 10,2 al 3,2%. No se encontraron diferencias en la aparición de trombosis del stent a pesar de que el tiempo recomendado para la doble antiagregación era de al menos 3 meses y el 60% de los pacientes la cumplió durante menos de 8 meses.
En resumen, los SFA mantienen la eficacia para la que fueron diseñados al reducir la reestenosis y la necesidad de nuevas revascularizaciones a largo plazo de forma significativa respecto al SNFA. Con las pautas de antiagregación actuales, no parece que en la trombosis del stent haya diferencias entre los dos grupos de stents, si bien seguimos careciendo de estudios de seguimiento a más largo plazo.
OTROS DISPOSITIVOS DE AYUDA EN LA ICP PRIMARIALa ICP primaria, a pesar de su efectividad, tiene una serie de aspectos, además de los ya comentados, que están en discusión, como son la prevención de la embolización distal, bien mediante dispositivos que aspiran parte del trombo, bien sistemas de protección tanto proximal como distal que previenen la distribución de este material en el lecho distal a la lesión causal. Obtener conclusiones de la evidencia científica publicada con estos dispositivos es complicado, ya que los diferentes estudios no siempre coinciden en valorar los mismos objetivos, que en muchas ocasiones no son clínicos; además, los dispositivos son técnicamente diferentes, por lo que compararlos puede ser complicado en ocasiones, pese a que su uso tenga un sentido lógico, ya que aspirar el trombo y/o evitar su dispersión es uno de los objetivos del procedimiento.
El arsenal de materiales disponibles para realizar la trombectomía es variado; los dispositivos más usados son los de aspiración, por su sencillez de manejo y su coste, que suelen consistir en un catéter hidrófilo al que se conecta una jeringa que realiza el vacío, se avanza hasta la zona del trombo y se inicia la recogida de éste. Los más conocidos son el Pronto® (Vascular Solutions Inc.), el Diver® (Invatec Inc.) y el Export® (Medtronic Inc.). Los dispositivos de fragmentación y aspiración son más complejos y la aspiración la suele realizar un dispositivo mecánico que fractura el coágulo y lo aspira. El más conocido es el X-Sizer (EV3 Inc.). Existe una tercera variedad, que es la llamada trombectomía reolítica, que consiste en un catéter que, a través de unas microcorrientes de suero salino de alto flujo en la zona del trombo, es capaz de fragmentarlo y aspirarlo por el efecto Bernoulli; el representante de esta categoría es el Angiojet® (Possis Medical Inc.). Por último, de los sistemas de protección existen dos clases, los de tipo filtro —que suele ser una cesta de malla muy fina que se ubica distal a la lesión y se queda con el trombo de tamaño mayor que la malla— y las de balón de oclusión, que puede ser proximal o distal, según donde se infle, y evita que el flujo sanguíneo arrastre el material trombótico. Tras el procedimiento, se aspira el detrito que queda libre.
Respecto a la aspiración manual, el estudio TAPAS30 ha sido de los más importantes. Se aleatorizó a 1.071 pacientes a ICP previa trombectomía de aspiración manual con el catéter Export® o ICP sin este dispositivo. Aunque el objetivo primario no era clínico, sino el blush miocárdico, sí lo eran algunos de los objetivos secundarios, entre los que se encontraba el análisis a los 30 días de muerte, reinfarto, necesidad de nueva revascularización y el combinado de los tres. El objetivo combinado y la muerte fueron significativamente menos en el grupo de trombectomía, pero relacionados con el miocardial blush y la resolución del ST, lo cual confirma la correlación entre estos parámetros y los clínicos.
Para corroborar datos como éste, el metaanálisis de De Luca et al31, en el que se analizan nueve estudios aleatorizados (incluido el TAPAS) con 1.209 pacientes tratados con trombectomía y 1.208 con tratamiento médico, se valoró como objetivo primario la mortalidad a los 30 días y como secundarios, los objetivos angiográficos, y los resultados fueron significativos a favor de la trombectomía en todos ellos, como se aprecia en la tabla 2.
Influencia de la realización de trombectomía manual en la angioplastia primaria en diferentes parámetros angiográficos y en la mortalidad a 30 días, según el metaanálisis de De Luca et al30
| Trombectomía manual (%) | Sin trombectomía (%) | p | |
| TIMI 3 tras ICP | 87,2 | 81,2 | < 0,0001 |
| MBG 3 tras ICP | 52,1 | 31,7 | < 0,0001 |
| Embolización distal | 7,9 | 19,5 | < 0,0001 |
| Mortalidad a 30 días | 1,7 | 3,1 | 0,04 |
MBG 3 tras ICP: perfusión miocárdica normal; la tinción del miocardio con contraste tras el intervencionismo es igual que en el territorio de una arteria sin lesión significativa; TIMI 3 tras ICP: perfusión coronaria completa tras el intervencionismo coronario percutáneo; la llegada de contraste al lecho distal a la lesión no se ve afectada, y se rellena y se lava igual que en un vaso sin lesión.
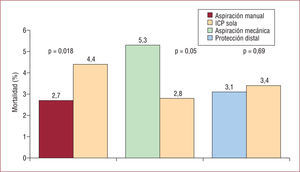
El metaanálisis de Bavry et al32 analiza 30 estudios con 6.415 pacientes con los diferentes tipos de dispositivos en comparación con la ICP sola. Los resultados obtenidos (fig. 1) muestran que la aspiración manual reduce la mortalidad, y hace necesario tratar a 59 pacientes para salvar 1 vida; la aspiración mecánica la empeora respecto a no hacerla y la protección distal no tiene efecto en la mortalidad. El peor resultado de la trombectomía mecánica en el metaanálisis se debe a los resultados del estudio AiMI33, realizado con el dispositivo AngioJet®, para lo cual los investigadores no encontraron explicación. También se encontró que todos los dispositivos en general tendían a producir más embolias cerebrales, probablemente debido a la fragmentación del trombo o la embolización aérea. Se puede concluir respecto a estos dispositivos que el punto más importante es la selección adecuada del paciente. El IAMCEST sucede sobre una placa rota en la que la cantidad de trombo varía de forma muy importante, y en aquellos en que es mayor, el resultado de la trombectomía es mejor; de todos modos, ningún dispositivo previene de forma completa la embolización y en los pacientes con bajo riesgo hoy es difícil obtener diferencias en la mortalidad.
Incidencia de mortalidad en el seguimiento según las diferentes técnicas de trombectomía empleadas comparadas con la angioplastia primaria sola según el metaanálisis de Bavry et al32. ICP: intervención coronaria percutánea.
El shock cardiogénico (SC) es la manifestación clínica más severa de la enfermedad cardiaca asociada a IAMCEST. Se define con una serie de parámetros clínicos que se manifiestan como hipoperfusión de órganos vitales (frialdad de la piel, disminución del nivel de conciencia, oliguria, etc.) y hemodinámicas, como la hipotensión persistente con presión arterial sistólica (PAS) < 80 o 90mmHg, presión arterial media 30mmHg menor que la basal o un índice cardiaco < 1,8l/min/m2 sin medidas de soporte o < 2 o 2,2l/min/m2 con medidas de soporte manteniendo unas presiones de llenado del ventrículo izquierdo (VI) ≥ 18mmHg o ≥ 10-15mmHg del ventrículo derecho (VD). La causa más frecuente es el IAM masivo y otras causas menos frecuentes son: complicaciones mecánicas del IAM, IAM de ventrículo derecho, miopericarditis aguda, síndrome de tako-tsubo, insuficiencia valvular aguda, estenosis mitral o aórtica críticas, taponamiento cardiaco y tromboembolia pulmonar masiva. La incidencia en el IAM ha pasado de estar en un 20% de los infartos al 7% en la actualidad, y actualmente la mortalidad está en un 50-60%, sin cambios en los últimos años. La incidencia según la etiología y la mortalidad se expresan en la tabla 3. Como el IAMCEST masivo es la causa más frecuente, analizaremos las medidas terapéuticas para este tipo de shock, ya que en las demás complicaciones del infarto el tratamiento es básicamente quirúrgico. En el manejo inicial del SC las evaluaciones hemodinámica, angiográfica y ecocardiográfica deben realizarse con premura, ya que la instauración de medidas que cambian el pronóstico dependen de estas técnicas. Aunque clásicamente se entendía el SC como un problema puramente mecánico de fallo de bomba, en la actualidad sabemos que la hipoperfusión da lugar a que se liberen catecolaminas y diferentes mediadores bioquímicos que intentan mantener la perfusión y aumentar la contractilidad; así, la liberación de vasopresina y angiotensina II aumenta la perfusión coronaria y periférica a expensas de aumentar la poscarga, lo que conlleva empeoramiento de la función ventricular. Sin embargo, no todos los pacientes reaccionan igual; en algunos se comportan inicialmente como un shock séptico con resistencias vasculares sistémicas muy bajas. Es la entidad conocida como SIRS (systemic inflammatory response syndrome), que es más común cuanto mayor es la duración del shock, y en él participan mediadores como la interleucina 6 y el factor de necrosis tumoral alfa, que tienen efectos cardioinhibidores, el complemento o el óxido nítrico producido en exceso que conduce a la hipotensión. Todos estos parámetros hemodinámicos generan un círculo vicioso que es necesario cortar34 lo antes posible para revertir el proceso.
Distribución de las diferentes etiologías del shock cardiogénico y mortalidad hospitalaria
| IVI | IVD | CIV tras IAM | IM | Rotura de pared libre | Otras | Total | |
| Incidencia (%) | 78,5 | 2,8 | 3,9 | 6,9 | 1,4 | 6,7 | 100 |
| Mortalidad (%) | 59,2 | 55 | 87,5 | 55 | 55 | 65,3 | 60 |
CIV: comunicación interventricular; IAM: infarto agudo de miocardio; IM: insuficiencia mitral; IVD: insuficiencia del ventrículo derecho; IVI: insuficiencia del ventrículo izquierdo.
Se debe mantener una buena oxigenación y, en general, considerar que el umbral para la intubación no debe ser muy alto, ya que con la ventilación mecánica se disminuye el trabajo respiratorio y se puede actuar sobre la precarga y la poscarga. Los antiagregantes y anticoagulantes que se administran en el IAMCEST también están indicados en el SC; la única duda puede ser el clopidogrel, por la necesidad hipotética de enviar al paciente a cirugía.
El uso de inotrópicos y agentes vasopresores, aunque mejora los parámetros hemodinámicos, no se ha demostrado que aumente la supervivencia hospitalaria de forma significativa y, además, cuando se usan a dosis altas están asociados a peor supervivencia35; sin embargo, siguen siendo las medidas que utilizar mientras no se implanta el balón intraaórtico de contrapulsación (BIACP) o se realiza la revascularización. Dopamina y dobutamina son los fármacos más usados y en ocasiones también los vasodilatadores con la intención de disminuir la poscarga y las presiones de llenado del VI, pero suelen asociarse a hipotensión y empeoran la situación hemodinámica al empeorar la perfusión coronaria. En los casos en que el SC se manifiesta como SIRS, puede ser necesario el uso de noradrenalina —que, además de propiedades vasoconstrictoras, también las tiene inotrópicas— para mantener la perfusión coronaria, sobre todo cuando la presión arterial diastólica es < 50-60mmHg.
Balón intraaórtico de contrapulsaciónEste dispositivo, desde su inicio en 1968, siempre ha estado ligado al SC como una de las piezas clave para su manejo. Su uso hace que la perfusión coronaria aumente y disminuye la poscarga, y todo esto hace que mejore la función ventricular, por lo que se ha convertido en una de las primeras medidas que tomar cuando se diagnostica el SC por insuficiencia ventricular izquierda o alguna de las complicaciones mecánicas del IAMCEST. Las guías del ACC/AHA lo recomiendan como clase IB2 en el SC y las europeas como IC1. Sin embargo, no todos los pacientes reaccionan al uso del balón intraaórtico de contrapulsación (BIACP) con mejoría, y esto es un predictor de mal pronóstico36. Además, no hay evidencia científica de que su uso obtenga beneficio; en un metaanálisis37 reciente se ha encontrado que mejora los datos de mortalidad en el SC cuando se usa en el IAMCEST trombolisado, y no ha demostrado beneficio en la ICPp, aunque los autores reconocen que el análisis tiene limitaciones por lo heterogéneo de los estudios incluidos, pero que es un desafío a las recomendaciones de las guías de práctica clínica.
Las complicaciones del uso de este dispositivo han disminuido en la actualidad al mejorar sus características, y en las grandes series las complicaciones mayores están en un 2,8%; el sexo femenino, la talla baja y la enfermedad vascular periférica son las variables relacionadas con ellas. Entre los problemas que pueden aparecer, se encuentran isquemia de la extremidad, laceraciones de la arteria femoral, disección aórtica, infecciones, hemolisis, trombocitopenia y embolia periférica.
Medidas de reperfusiónLa reperfusión precoz es la medida que ha demostrado salvar más vidas en el SC y está más claro cuando se refiere a la ICP o la revascularización quirúrgica, pero no en el caso de la fibrinolisis, ya que la hipotensión y la vasoconstricción impiden la entrada adecuada del fármaco en la arteria ocluida y disminuyen su efectividad38, por lo que sólo está indicada si no hay otra opción de revascularización y el SC está en sus primeras 3h. El estudio SHOCK39, que tiene una parte de aleatorización con 302 pacientes y otra de registro con 1.190, encontró en la primera que, aunque no hubo diferencias en la mortalidad a los 30 días entre el grupo de revascularización (el 64% ICP y el 36% cirugía) con el grupo de estabilización médica, a los 6 meses y a 1 año los revascularizados tenían significativamente mejor supervivencia, y estos datos también se hallaron en el registro. El estudio SMASH40, con menor número de pacientes, encontró resultados similares. Si está claro que se debe revascularizar, también lo está que se debe realizarlo lo antes posible y las primeras 6-8h desde el inicio del SC es cuando se obtiene mayor beneficio39,41, aunque se aprecia mejoría en la supervivencia si se realiza en las primeras 48h tras el infarto y en las primeras 18h tras el inicio del SC. Respecto al tipo de revascularización, tanto la cirugía como la ICP presentan buenos resultados y son similares, pero la primera presenta más retraso en su realización, hasta 2,7h en el estudio SHOCK42,43. En caso de afección de un vaso, parece claro que la ICP es la primera opción de tratamiento, pero en los pacientes con enfermedad multivaso, que pueden ser hasta el 80%, está menos clara cuál es la mejor alternativa; por eso las guías de la ACC/AHA recomiendan cirugía si la afección es difusa, y en caso de ICP, diferir el tratamiento de la arteria no causal para un segundo tiempo2.
El uso de los inhibidores de la glucoproteína IIb/IIIa en el SC se limita tan sólo al abciximab, que es el que en diferentes estudios observacionales y en uno aleatorizado se ha demostrado que mejora el pronóstico de los pacientes tratados con ICP7,44.
Otro punto importante en el manejo del SC es la edad de los pacientes, ya que desde el primer análisis realizado en el estudio SHOCK se apreció que los pacientes mayores de 75 años tenían peor pronóstico cuando eran revascularizados45, pero en subanálisis posteriores se apreció que si el paciente, a pesar de la edad, presentaba buenas condiciones, mejoraba la supervivencia. Así, las guías de la ACC/AHA recogen para los pacientes mayores de 75 años con SC la revascularización precoz como clase I; para los de 75 o más años es IIa si el estado funcional previo es bueno2.
Dispositivos de asistencia ventricular izquierdaDiferentes dispositivos se han desarrollado para conseguir que el paciente en SC mantenga la perfusión de los órganos y se libere el corazón de los mecanismos que, inicialmente al menos, lo sobrecargan, para permitir su recuperación o servir de puente a la espera de un trasplante. Existen varios en el mercado, unos de implante quirúrgico, como el TandemHeart (Cardiac Assist, Inc.; Pittsburg, Pennsylvania, Estados Unidos), y otros percutáneos, como el Impella (Abiomed, Inc., Danvers, Massachusetts, Estados Unidos). Entre la poca evidencia existente, en algún estudio46 se ha apreciado que la mejora de parámetros hemodinámicos no siempre se acompaña de mejor supervivencia tras la revascularización quirúrgica, por lo que se requieren más estudios para aclarar sus indicaciones.
Infarto de ventrículo derechoEl infarto de ventrículo derecho puede manifestarse de diferente gradación y ser tanto causa como contribuyente al SC. Determina una situación de bajo gasto cardiaco limitando el llenado del VI por la incapacidad de bombear sangre hacia el lecho pulmonar, y/o por la interdependencia ventricular, esto es, el desplazamiento del septo interventricular hacia la cavidad izquierda debido a la dilatación del VD. Tradicionalmente se ha manejado con aumento de las presiones de llenado derechas para mantener el gasto cardiaco, pero esto puede hacer que, por el desplazamiento del septo, disminuya el llenado izquierdo, de modo que, con presiones telediastólicas derechas de 10-15mmHg, se consigue un llenado óptimo, y en caso de que no se aprecie mejoría, estaría indicado agregar inotrópicos. La disminución de la resistencia pulmonar con óxido nítrico inhalado puede ser una alternativa cuando fallan otras medidas. La revascularización precoz en estos pacientes también es la medida más eficaz para mejorar la supervivencia.
CONCLUSIONESEn la realización de una angioplastia primaria entran diferentes aspectos que influyen en su resultado final; el uso de los inhibidores de la glucoproteína IIb/IIIa fuera de la estrategia de la angioplastia facilitada mejora los resultados del intervencionismo. La dosis de carga de clopidogrel de 300mg ya está aceptada como parte del tratamiento estándar del IAM y la de 600mg aporta el mismo efecto de forma más precoz. La bivalirudina es una alternativa en los pacientes con alto riesgo hemorrágico en los que está planeado usar heparina con inhibidores de la glucoproteína IIb/IIIa. La vía de acceso radial disminuye las complicaciones hemorrágicas en un ambiente propicio para que éstas aparezcan y penaliza por el tiempo del procedimiento, por lo que se debe realizar en centros con gran experiencia en este acceso. Las técnicas de trombectomía de aspiración manual son las únicas con demostrada mejora de la supervivencia en el seguimiento de los pacientes tratados. El shock cardiogénico sigue siendo un reto para la cardiología y la disminución de su mortalidad se basa en intentar una revascularización lo más precoz y completa posible, ya que hasta ahora los diferentes dispositivos de asistencia ventricular carecen de estudios adecuados para demostrar su efectividad.