La combinación de una gran variedad de fármacos antitrombóticos disponibles y la falta de consenso sobre el régimen óptimo para un paciente determinado han dado lugar a una larga lista de posibilidades. Además del riesgo de eventos isquémicos recurrentes, existen otros factores importantes que se debe tener en cuenta antes del intervencionismo coronario percutáneo (en caso de que sea necesario), como el riesgo de sangrado, el momento y la dosis de clopidogrel o heparina de bajo peso molecular, la función renal o si el paciente tiene historia de reacciones adversas a fármacos, como trombocitopenia inducida por heparina. Se presentan dos casos clínicos con la intención de subrayar las medidas que se debe considerar al iniciar un tratamiento antitrombótico determinado.
Palabras clave
ácido acetilsalicílico.
coronaria derecha.
circunfleja.
descendente anterior.
electrocardiograma.
fibrilación auricular.
fracción de eyección.
hipertensión arterial.
intervencionismo coronario percutáneo.
primera obtusa marginal.
presión arterial.
síndrome coronario agudo.
tronco coronario izquierdo.
ventrículo izquierdo.
Varón de 80 años diagnosticado de hipertensión arterial (HTA) e hipercolesterolemia, con buenos controles crónicos, que 3 años antes había ingresado por ictus cardioembólico en el contexto de fibrilación auricular (FA), que dejó como secuela una ligera hemiparesia izquierda residual, estaba en tratamiento crónico con diltiazem, acenocumarol, atorvastatina, ramipril y omeprazol. Situación basal con buena calidad de vida para su edad, sin angina ni edemas y en clase funcional II de la escala de la New York Heart Association (NYHA).
El paciente acudió al servicio de urgencias tras tener heces negras y malolientes desde hacía 1 semana. Además refería episodios de dolor torácico mal definido en reposo, sin irradiación y de minutos de duración en los últimos 3 días.
A la inspección destacaba marcada palidez mucocutánea, con regular estado general. A la exploración física, tendencia a la hipotensión (90/60 mmHg) y taquicardia (110 lpm). No presentaba ingurgitación yugular y a la auscultación estaba arrítmico, con soplo sistólico eyectivo II/VI en foco aórtico y segundo ruido conservado, sin otros signos de insuficiencia cardiaca. El abdomen no era doloroso a la palpación, sin masas ni visceromegalias, y extremidades sin edemas y con pulsos conservados. Se realizó tacto rectal, que confirmó la presencia de melenas.
Se realizó electrocardiograma (ECG), que muestra una FA con respuesta ventricular media a unos 110-120 lpm y con descenso del segmento ST horizontal de 3 mm en precordiales izquierdas (V4-V6). En la analítica destacan: creatinina, 1,47 mg/dl; urea, 62 mg/dl; hemoglobina, 7,5 mg/dl, y hematocrito, 21% con un volumen corpuscular medio bajo. La coagulación mostraba un INR = 3,1 y los marcadores de isquemia miocárdica seriados alcanzaron un pico de creatincinasa (CK) a las 24 h de 386 U/l; CK-MB, 55,5 ng/ml, y troponina T, 0,46 ng/ml. La radiografía de tórax no muestra cardiomegalia ni infiltrados pulmonares.
Con todo lo anterior, el paciente quedó ingresado con los diagnósticos de anemia aguda por hemorragia digestiva alta, infarto sin elevación del ST secundario a la anemia y taquicardización e insuficiencia renal no conocida (aclaramiento de creatinina por MDMR, 48 ml/min).
Dado el alto riesgo hemorrágico del paciente, junto con la presencia de sangrado activo, se revirtió el tratamiento anticoagulante con vitamina K y se transfundieron 2 concentrados de hematíes, sin iniciar tratamiento antiagregante.
El paciente subió a planta, donde persistía la anemización progresiva por sangrados digestivos recurrentes, que requirieron nuevas transfusiones. Se realizó una gastroscopia urgente, con la que no se encontró afección que justificara el sangrado, por lo que se indicó un estudio del tubo digestivo con cápsula endoscópica. Tras el análisis de las imágenes, se objetivaron varias lesiones de pequeño tamaño y aspecto angiodisplásico en yeyuno distal, algunas de las cuales presentaban signos de sangrado activo. Todas estas lesiones eran accesibles con enteroscopia de doble balón, por lo que 2 días después se procedió a su electrocauterización; el resultado final fue satisfactorio.
Una vez tratado el problema hemorrágico, se solicitó una ecocardiografía de estrés con dobutamina con interés pronóstico. En reposo, se comprobó una acinesia inferior del ventrículo izquierdo (VI) con hipocinesia septoapical y lateral, con fracción de eyección (FE) en reposo del 40%. Con dosis bajas de dobutamina, mejoró la contractilidad de casi todos los segmentos basales y medios, quedando sólo acinético parte del ápex. Al presentar una salva de taquicardia ventricular no sostenida de 15 latidos y dada la extensión de las alteraciones de la contractilidad segmentaria, se decidió suspender la prueba con el diagnóstico de sospecha de enfermedad multivaso, con viabilidad en amplio territorio inferoposterolateral y septal.
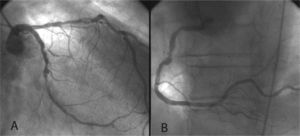
Ante el resultado de la prueba, que indicaba alto riesgo, se procedió a realizar una coronariografía. Mediante acceso por vía femoral, se observaba un tronco de la arteria coronaria izquierda (TCI) sin lesiones, arteria descendente anterior (DA) difusamente enferma y calcificada con lesiones severas en tercio proximal y distal, circunfleja (CX) difusamente enferma y severamente calcificada con lesión severa en rama primera obtusa marginal (OM1) y coronaria derecha (CD) severamente calcificada con lesiones significativas en tercio medio (fig. 1). Tras el diagnóstico de enfermedad severa de tres vasos con disfunción sistólica moderada del VI, se planteó la posibilidad de revascularización quirúrgica. Sin embargo, el paciente rechazó la cirugía, por lo que finalmente se decidió revascularizar de forma percutánea a pesar del alto riesgo del procedimiento. Este resultó muy complejo, con necesidad de aterectomía rotacional y el implante de 9 stents (5 convencionales y 4 farmacoactivos por el alto riesgo de reestenosis de las lesiones) en DA, CX y CD, con buen resultado angiográfico final.
Tras el intervencionismo, el paciente se mantenía hemodinámicamente estable, sin nuevos episodios de sangrado, con hemoglobina estable (12 g/dl) y sin empeoramiento franco de la función renal (creatinina, 1,5 mg/dl). Tras 19 días de ingreso y tras valorar los riesgos trombótico, embólico y hemorrágico, el tratamiento antitrombótico previo al alta era clopidogrel 75 mg/día y acenocumarol. Tras 1 año de seguimiento, sigue asintomático desde el punto de vista cardiológico, en clase funcional I-II de la NYHA y con algún sangrado digestivo ocasional que ha precisado puntualmente alguna transfusión de hemoderivados.
CASO 2Varón de 44 años fue remitido a nuestro servicio para realización de angioplastia primaria. Entre sus antecedentes destacan hipercolesterolemia en tratamiento dietético y colitis ulcerosa en tratamiento con mesalazina y azatioprina. Además, antecedentes familiares de cardiopatía isquémica (padre con infarto a los 48 años). Sin antecedentes de angina; clase funcional NYHA I.
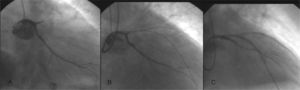
El paciente refería dolor torácico con cortejo vegetativo acompañante que había comenzado 3 h antes. Acudió a su hospital de referencia, donde se encontraba estable hemodinámicamente y con una exploración física anodina. Se realizó un ECG, que muestra una elevación del segmento ST de 1 mm en cara anterolateral, motivo por el que lo remitieron para realización de angioplastia primaria. Antes del traslado, se le administraron 300 mg de clopidogrel, 300 mg de ácido acetilsalicílico (AAS) y 80 mg subcutáneos de enoxaparina. A su llegada a nuestra unidad (40 min después) persistía sintomático y con cifras de presión arterial (PA) sistólica > 120 mmHg. Por acceso femoral derecho, se objetivó una oclusión trombótica de la DA proximal hasta la primera diagonal (fig. 2A). Tras pasar sendas guías a dichas ramas y dilatar con balón, se produjo una trombosis del catéter que abarcaba el TCI y el origen de las arterias DA y CX (fig. 2B). En ese momento el paciente se desestabilizó hemodinámicamente y precisó intubación orotraqueal y ventilación mecánica, así como colocación de balón de contrapulsación y perfusión de dobutamina. Se administraron 10.000 U de heparina sódica intracoronaria y un bolo intracoronario de abciximab ajustado por peso. Finalmente se consiguió dilatar las arterias y se implantaron 3 stents recubiertos (2 en tercio proximal de DA y 1 en tercio proximal de CX). El resultado angiográfico final fue bueno, sin restos de trombo y con flujo TIMI III (fig. 2C).
A: coronariografía que muestra oclusión trombótica en tercio proximal de arteria descendente anterior. B: trombosis del catéter con extensión del trombo hacia el tronco coronario izquierdo y origen de la arteria circunfleja. C: buen resultado angiográfico final tras implante de stents en las arterias descendente anterior y circunfleja.
El paciente pasó a la unidad coronaria en situación hemodinámica Killip IV. En las primeras 24 h sufrió un episodio de epistaxis profusa con caída de hematocrito (21%) que requirió la colocación de un taponamiento nasal anterior y la transfusión de 2 concentrados de hematíes. La evolución posterior fue buena y en las primeras 48 h se retiraron los fármacos vasoactivos, así como el balón de contrapulsación. El quinto día se consiguió retirar la sedación y extubar al paciente sin complicaciones. Los marcadores de isquemia miocárdica alcanzaron un pico de CK de 2.916 U/l; CK-MB, 293,8 ng/ml y troponina T, 4,37 ng/ml, y la ecocardiografía mostraba una hipocinesia septoapical y lateroapical del VI con una FE del 45%. Finalmente, tras 7 días de ingreso en la unidad coronaria pasó a planta de cardiología en tratamiento con AAS, clopidogrel, ramipril, carvedilol, atorvastatina y su tratamiento crónico para la colitis ulcerosa.
Una vez en planta, comenzó con episodios de dolor abdominal difuso sin signos de irritación peritoneal y con rectorragias. Se produjo una caída progresiva del hematocrito sin hipotensión que requirió la transfusión de otros 2 concentrados de hematíes. Lo valoró el digestólogo de guardia, que definió el cuadro como un brote de colitis ulcerosa, por lo que inició tratamiento intravenoso con metilprednisolona, que consiguió controlar los síntomas del paciente. En ningún momento se suspendió el tratamiento antitrombótico, dada la estabilidad hemodinámica del paciente y la buena respuesta al tratamiento esteroideo. Sin embargo, al décimo día de ingreso hospitalario, apareció de nuevo el dolor torácico opresivo y sudoración profusa. A la exploración física se encontraba taquicárdico (110 lpm), con una PA de 150/90 mmHg, y a la auscultación cardiopulmonar, rítmico con crepitantes bibasales. El ECG muestra de nuevo una elevación del ST en cara anterolateral, por lo que se volvió a indicar una coronariografía urgente. Por acceso femoral derecho, se objetivó una trombosis de los stents del tercio proximal de la arteria DA. Se consiguió recanalizar el vaso y, tras aspirar con dispositivo de trombectomía y dilatar con balón, se implantó stent convencional y se logró flujo TIMI III. A pesar de todo, en la siguiente inyección se observó de nuevo una trombosis del catéter. Esta afecta proximalmente hasta el TCI, y se resolvió con implante de nuevo stent recubierto tras la administración de 10.000 U de heparina sódica y un bolo de abciximab intracoronarios. En esta ocasión el paciente mantuvo la PA y pasó a la unidad coronaria en situación Killip II. Se inició tratamiento diurético intravenoso sin necesidad de fármacos vasoactivos, y tras 48 h, pasó a planta de cardiología. Una vez allí, la evolución posterior fue favorable, sin nuevos episodios de dolor torácico ni de hemorragia. Se realizó ecocardiografía de control, que muestra una FE del VI del 50%, a expensas de una hipocinesia apical. Finalmente, tras 19 días de ingreso hospitalario, se decidió el alta con tratamiento antitrombótico de AAS 150 mg/día y clopidogrel 75 mg/día. Seis meses después, el paciente seguía asintomático desde el punto de vista cardiológico y digestivo. Se realizó coronariografía de control, que muestra permeabilidad de los stents, sin nuevas lesiones significativas.
DISCUSIÓNEl tratamiento antitrombótico es la piedra angular en el manejo de los síndromes coronarios agudos (SCA). La gran variedad de fármacos anticoagulantes y antiplaquetarios disponibles hace que el proceso de elección en ocasiones sea complejo. La decisión sobre la elección del régimen antitrombótico, por lo tanto, debe ser individualizado, teniendo en consideración tanto el riesgo de eventos isquémicos recurrentes como el riesgo de complicaciones hemorrágicas.
Los pacientes con FA que presentan un SCA constituyen un grupo especial. Así, en los sujetos con FA de moderado-alto riesgo de ictus que necesitan tratamiento crónico con anticoagulantes orales, se debe ser incluso más cuidadoso al elegir la estrategia antitrombótica óptima, ya que, además, habrá que prevenir la aparición de complicaciones embólicas y un mayor riesgo de complicaciones hemorrágicas que conlleva el tratamiento antitrombótico combinado. Nuestro caso 1 es un ejemplo de ello. Se trata de un paciente con alto riesgo embólico, debido a los antecedentes de ictus cardioembólico previo, HTA y edad mayor de 75 años (score CHADS2 de 4), que presenta un SCA en el contexto de una hemorragia digestiva. Tras el diagnóstico de la disfunción ventricular de etiología isquémica, se optó por la revascularización percutánea, dada la negativa del paciente a la cirugía.
Estudios previos han demostrado un menor riesgo de complicaciones vasculares y hemorrágicas relacionadas con el sitio de punción mediante el acceso radial frente al femoral1,2. Además, en pacientes anticoagulados con warfarina, el acceso femoral es un predictor independiente de complicaciones en el sitio de punción3, por lo que debería considerarse la vía radial para el tratamiento de estos pacientes.
En nuestro caso, dada la complejidad de la anatomía coronaria, se procedió al acceso femoral. En pacientes anticoagulados con dicumarínicos la adición de doble antiagregación («triple terapia») parece ser la mejor opción para evitar la trombosis del stent y la tromboembolia. La combinación de warfarina y clopidogrel puede ser una alternativa en pacientes con alto riesgo de sangrado y/o bajo riesgo de trombosis del stent4, aunque la evidencia actual es limitada. En casos de muy alto riesgo de sangrado, el stent farmacoactivo debería evitarse5 y hay que valorar como opciones terapéuticas la angioplastia simple con balón o el implante de stents metálicos con el objetivo de disminuir el tiempo necesario de triple terapia (tabla 1)6.
Estrategias antitrombóticas recomendadas tras el intervencionismo coronario percutáneo en pacientes con fibrilación auricular de moderado-alto riesgo tromboembólico (en los que la anticoagulación oral es necesaria)
| Riesgo hemorrágico | Contexto clínico | Tipo de stent | Recomendaciones |
| Bajo o intermedio | Electivo | Metálico | 1 mes: triple terapia de warfarina (INR 2-2,5) + AAS ≤ 100 mg/día + clopidogrel 75 mg/día. Indefinidamente, warfarina (INR 2-3) sola |
| Electivo | Farmacoactivo | 3 (grupo -olimus) a 6 (paclitaxel) meses: triple terapia de warfarina (INR 2-2,5) + AAS ≤ 100 mg/día + clopidogrel 75 mg/día. Hasta los 12 meses: combinación de warfarina (INR 2-2,5) + clopidogrel 75 mg/día (o AAS ≤ 100 mg/día)a. Indefinidamente, warfarina (INR 2-3) sola | |
| SCA | Metálico/farmacoactivo | 6 meses: triple terapia de warfarina (INR 2-2,5) + AAS ≤ 100 mg/ día + clopidogrel 75 mg/día. Hasta los 12 meses, combinación de warfarina (INR 2-2,5) + clopidogrel 75 mg/día (o AAS ≤ 100 mg/día)a. Indefinidamente, warfarina (INR 2-3) sola | |
| Alto | Electivo | Metálicob | 2-4 semanas: triple terapia de warfarina (INR 2-2,5) + AAS ≤ 100 mg/día + clopidogrel 75 mg/día. Indefinidamente, warfarina (INR 2-3) sola |
| SCA | Metálicob | 4 semanas: triple terapia de warfarina (INR 2-2,5) + AAS ≤ 100 mg/ día + clopidogrel 75 mg/día. Hasta los 12 meses, combinación de warfarina (INR 2-2,5) + clopidogrel 75 mg/día (o AAS ≤ 100 mg/día)a. Indefinidamente, warfarina (INR 2-3) sola |
SCA: síndrome coronario agudo.
Modificado con permiso de Lip GY et al6.
Por otra parte, el riesgo hemorrágico de nuestro paciente es alto, pues posee varios de los factores de riesgo asociados a complicaciones hemorrágicas en pacientes con SCA sometidos a intervencionismo coronario percutáneo (ICP), como son la edad mayor de 75 años, insuficiencia renal, antecedentes de sangrado, anemia o la necesidad de tratamiento concomitante de fármacos anticoagulantes y antiagregantes7,8. A pesar de que en estos pacientes es deseable evitar el uso de stents farmacoactivos, finalmente fueron los implantados debido a la complejidad de la anatomía coronaria y el alto riesgo de reestenosis (vasos difusamente enfermos con lesiones largas).
Una vez aquí, nos encontramos con un paciente con alto riesgo embólico (CHADS2 de 4), alto riesgo hemorrágico y alto riesgo trombótico (enfermedad de tres vasos grave con implante de 9 stents, 4 de ellos farmacoactivos), por lo que la elección del régimen antitrombótico resultaba realmente compleja. Finalmente se optó por acenocumarol y clopidogrel. Sin embargo, esta estrategia resulta escasa en la protección del alto riesgo trombótico del paciente, por lo que la triple terapia (acenocumarol para mantener INR en 2-2,5, AAS 100 mg/día y clopidogrel 75 mg/día) durante al menos 6 meses sería la opción deseable, para continuar hasta completar el año con acenocumarol y un fármaco antiplaquetario6.
Por otro lado, en nuestro caso 2, presentamos a un paciente con dos episodios de trombosis del catéter durante el ICP y una trombosis subaguda del stent. Vamos a analizar brevemente el tratamiento antitrombótico administrado, así como las posibles alternativas terapéuticas.
En primer lugar comentaremos el uso de la enoxaparina en el seno del ICP primario. En nuestro caso se administró una dosis de 1 mg/kg por vía subcutánea unos 50 min antes del procedimiento. Estudios previos han mostrado que el uso de enoxaparina subcutánea como única terapia anticoagulante en este contexto se asocia a un mayor riesgo de trombosis del catéter. Esto se debe a que no se alcanzan niveles suficientes de actividad anti-Xa. Probablemente el mayor tono simpático, la vasoconstricción subcutánea, el gasto cardiaco disminuido o la inflamación durante el infarto con elevación del segmento ST puedan atenuar la absorción del fármaco por esta vía9,10.
Las estrategias que combinan la administración subcutánea con un bolo intravenoso de enoxaparina (0,3-0,5 mg/kg) o con dosis reducidas de heparina no fraccionada (50 U/kg) parecen mostrar mayor seguridad11,12. Recientemente se han presentado los resultados del estudio ATOLL (Acute STEMI Treated with primary angioplasty and intravenous enoxaparin Or UFH to Lower ischemic and bleeding events at short-and Long-term follow-up). Se trata de un ensayo aleatorizado que compara la estrategia de enoxaparina intravenosa (0,5 mg/kg) frente a heparina no fraccionada en pacientes con infarto con elevación del ST que se someten a ICP primario. Aunque no demostró superioridad en el objetivo primario, de nuevo parece confirmarse que el uso de enoxaparina intravenosa es una estrategia segura13.
Otro punto que tener en cuenta es el momento y la dosis de clopidogrel antes del ICP. En nuestro caso 2, se administraron 300 mg apenas unos 50 min antes del ICP. Estudios previos han demos trado que dosis mayores de clopidogrel (600 mg) consiguen una mayor y más precoz inhibición de la agregación plaquetaria14, por lo que las guías actuales recomiendan la administración, si es posible, de una dosis de carga de 600 mg tan pronto como se pueda, para seguir posteriormente con una dosis de 75 mg/día15.
En ningún momento se interrumpió el tratamiento antiagregante en nuestro paciente, ya que el episodio hemorrágico digestivo se atribuyó directamente a un brote de la enfermedad inflamatoria intestinal, que cedió tras la administración de esteroides. Sin embargo, a los 10 días del ICP primario, se produjo una trombosis subaguda de los stents implantados. Además de los factores relacionados con el procedimiento, como la posible infraexpansión de los stents, una hipotética resistencia al tratamiento con clopidogrel pudo influir en el desencadante trombótico. Como ya se ha comentado en el apartado correspondiente de esta monografía, existe una gran variabilidad individual en la respuesta al clopidogrel, en la que están implicados factores genéticos, celulares y clínicos16.
En la actualidad no hay evidencia suficiente para recomendar la monitorización de la función plaquetaria sistemática ni aun ocasional durante el tratamiento con fármacos antiagregantes, ya que un cambio terapéutico derivado de ella no conduce a ninguna ventaja clínica relevante17. En este escenario, el prasugrel, también de la familia de las tienopiridinas, se presenta como una nueva opción terapéutica. Además de ser un fármaco atractivo en el ICP primario por su mayor potencia antiagregante y su mayor rapidez de acción, el prasugrel es especialmente útil en los pacientes que presentan recurrencia de eventos trombóticos a pesar de estar en tratamiento con clopidogrel18.
CONCLUSIONESLa selección del régimen antitrombótico apropiado para los pacientes con SCA puede ser una tarea compleja. A pesar de los grandes avances en el tratamiento antitrombótico, existen situaciones de alto riesgo como consecuencia de las interacciones entre las comorbilidades de los pacientes, las combinaciones de fármacos y sus vías de administración o la variedad del entorno de atención. Por todo ello, se hace necesario el desarrollo de escalas de beneficio-riesgo combinadas útiles en la práctica clínica diaria que permitan individualizar la estrategia terapéutica óptima para cada caso concreto.
CONFLICTO DE INTERESESLos autores declaran no tener ningún conflicto de intereses.