Como consecuencia de la creciente prevalencia de los factores de riesgo cardiovascular, la enfermedad coronaria (EC) se ha convertido en la principal causa mundial de muerte de personas de 60 o más años. Se calcula que la carga mundial de EC alcanzará en 2020 los 82 millones de años de vida ajustados por discapacidad1.
Se ha observado un sustancial descenso lineal de las tasas de cirugía de revascularización aortoconaria durante las últimas 2 décadas. Este declive se ha acompañado del correspondiente aumento de los procedimientos de revascularización coronaria percutánea, de tal modo que la mayoría de las lesiones de la arteria coronaria que precisan intervención se suelen tratar mediante implante de stent2. En este sentido, se prevé que el número total de procedimientos de intervención coronaria percutánea (ICP) que se realizarán en Europa aumente a una tasa anual del 3,5% en los próximos 5 años. En cuanto a las previsiones del mercado internacional respecto a los stents intracoronarios, se prevé un crecimiento del 2,9% entre 2016 y 20203.
La trombosis del stent (TS) es una complicación de la ICP poco frecuente con una inhibición eficaz de la reactivación plaquetaria mediante ácido acetilsalicílico y un inhibidor del receptor plaquetario P2Y124. Sin embargo, preocupa la tasa de eventos graves asociados con la TS: como resultado, casi todos los pacientes sufren un infarto de miocardio (IM) y fallece 1/4 pacientes con TS. Además, el tratamiento de la TS exige una nueva revascularización coronaria urgente, aunque la reperfusión óptima se logra únicamente en 2/3 pacientes. A pesar de que el riesgo de un episodio de TS recurrente es alto (incidencia a 5 años, 24%)5, los pacientes con TS precoz son los que se encuentran expuestos a un mayor riesgo de muerte.
Debido al aumento de la población de pacientes con stent implantado, la TS contribuye al porcentaje creciente de pacientes con un IM con elevación del segmento ST. Un estudio que incluyó a todos los pacientes tratados con stents intracoronarios demostró que más del 60% de los pacientes reingresados por IM con elevación del segmento ST en el transcurso del seguimiento a 5 tenía TS definitiva6.
Teniendo en cuenta todos estos factores y la tendencia actual hacia una estructura demográfica que envejece, la demanda de revascularización percutánea se consolida y la cuestión de la TS y su prevención cobra más importancia.
PREVENCIÓNIdentificación de los factores de riesgoDiversos factores se han asociado con el riesgo de TS, y se clasifican en relacionados con el perfil del paciente, con las características del procedimiento y con la eficacia del tratamiento antiplaquetario (tabla 1). Se ha confirmado que el riesgo trombótico es más alto para los pacientes cuando concurren el síndrome coronario agudo (SCA) como indicación para la ICP y diabetes mellitus, nefropatía crónica, tabaquismo, fracción de eyección del ventrículo izquierdo reducida y otras enfermedades protrombóticas concomitantes, como el cáncer o la trombocitopatía. El tipo de lesión y los factores relacionados con el procedimiento también influyen en la resistencia vascular en los stents. Además, el riesgo de TS aumenta ante todo procedimiento intervencionista que se lleve a cabo en EC difusa y en presencia de microangiopatía, y sobre todo cuando implique lesiones con complejidad anatómica, presencia de un trombo, lesiones ostiales/bifurcadas y en los casos con resultados deficientes (p. ej., insuficiente expansión del stent, infradimensionamiento del stent, disección residual o struts fracturados).
Factores que influyen en la trombosis del stent
| Relacionados con el paciente | Síndrome coronario agudo |
| Tabaquismo habitual | |
| Diabetes mellitus insulinodependiente | |
| Nefropatía crónica | |
| Adhesión al tratamiento antiagregante | |
| Relacionados con el procedimiento | Características de la lesión |
| Tipo de stent | |
| Diámetro del stent | |
| Longitud total del stent | |
| Resultados del procedimiento | |
| Relacionados con el tratamiento combinado de antiagregantes plaquetarios | Ineficacia |
Desde el inicio del uso del stent como estrategia terapéutica de la EC, se considera inadmisible una actuación terapéutica que no prevenga el riesgo de TS mediante una correcta inhibición de la actividad plaquetaria. Así, se debe mantener el tratamiento antiagregante plaquetario doble (TAPD) durante al menos 6 meses tras una ICP en el caso de la EC estable y al menos durante 12 meses tras el implante de stent por SCA7. Una suspensión del TAPD más temprana de lo recomendado, motivada especialmente por el incumplimiento terapéutico del paciente, se ha asociado con un incremento del riesgo de TS8.
Por todo lo anterior, es especialmente importante tomar en consideración tanto el poder predictivo de estos factores como su frecuencia de aparición, ya que los factores predictivos menos potentes se tornan más significativos si se producen con cierta frecuencia. Un análisis de 153.350 pacientes y 2.495 casos de TS demostró que uno de los predictores de TS más habitual y frecuente es la interrupción precoz del tratamiento antiagregante, junto con la extensión de la EC y el número/longitud de los stents9. Así, los factores que se asocian con la TS difieren según el momento de su aparición, sobre todo en las ocurridas antes de 30 días tras la ICP (TS aguda o subaguda), puesto que los factores más potentes están directamente relacionados con el procedimiento de implante del stent.
Escala de predicción de riesgo de TSLa naturaleza multifactorial de la TS facilita la predicción del riesgo de que se produzca. En este sentido, se aconseja estimar el riesgo de TS al término del procedimiento y, a partir de entonces, utilizar la estimación como referencia para controlar los factores de riesgo clínicos e individualizar el tratamiento antitrombótico combinado.
Los análisis de 2 amplios ensayos clínicos aleatorizados que abarcaban toda la esfera del SCA dieron lugar al desarrollo y la validación de una escala de riesgo que engloba 10 variables de fácil evaluación10. Esta escala de riesgo no solo predice la aparición de TS durante el primer año, sino también las complicaciones muy tardías de la TS.
Técnicas de imagen para evitar la TSLas técnicas de imagen intracoronaria, es decir, la ecografía intravascular y la tomografía de coherencia óptica, ayudan a comprender los mecanismos patogénicos de la TS. Esta técnica se emplea en la práctica clínica principalmente para mejorar la colocación del stent y, de este modo, reducir los eventos adversos asociados con el implante de stent, como la TS. El uso de las técnicas de imagen intravascular para guiar la ICP disminuye en más del 50% el riesgo de TS11, aunque cabe prever que la mayor utilidad terapéutica de las técnicas de imagen periprotésica redunde en las lesiones complejas de alto riesgo. El segundo instrumento de prevención de la TS mediante técnicas de imagen intracoronaria es la identificación de factores de riesgo relacionados con el mecanismo patogénico de la TS tras el implante.
Tecnología endoprotésicaLos últimos avances de la tecnología endoprotésica y las mejoras realizadas en la liberación de fármacos y el diseño de los stents han propiciado una mayor reducción de la tasa de TS2.
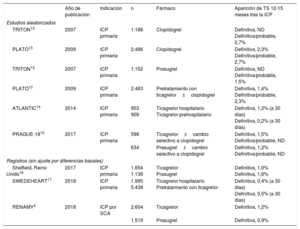
ANTITROMBÓTICOSEl refuerzo del TAPD, al incorporar inhibidores potentes del receptor plaquetario P2Y12 en combinacion con ácido acetilsalicílico, disminuye de manera significativa la incidencia de TS tras la ICP por SCA (tabla 2). Además de ello, para los pacientes con EC estable pero con alto riesgo de TS, se considera igualmente la opción de pautar prasugrel o ticagrelor tras el implante de stent. Con el objeto de identificar a los pacientes con TS de riesgo alto, se suelen emplear escalas validadas, como la SYNTAX, o específicas para la predicción de TS. En el caso de los pacientes que ya han sufrido una TS, es obligado adaptar el TAPD de manera individualizada a una inhibición más intensiva de la reactivación plaquetaria.
Incidencia de la trombosis del stent
| Año de publicación | Indicación | n | Fármaco | Aparición de TS 12-15 meses tras la ICP | |
|---|---|---|---|---|---|
| Estudios aleatorizados | |||||
| TRITON12 | 2007 | ICP primaria | 1.188 | Clopidogrel | Definitiva, ND Definitiva/probable, 2,7% |
| PLATO13 | 2009 | ICP primaria | 2.486 | Clopidogrel | Definitiva, 2,3% Definitiva/probable, 2,7% |
| TRITON12 | 2007 | ICP primaria | 1.152 | Prasugrel | Definitiva, ND Definitiva/probable, 1,5% |
| PLATO13 | 2009 | ICP primaria | 2.463 | Pretratamiento con ticagrelor±clopidogrel | Definitiva, 1,4% Definitiva/probable, 2,3% |
| ATLANTIC14 | 2014 | ICP primaria | 953 909 | Ticagrelor hospitalario Ticagrelor prehospitalario | Definitiva, 1,2% (a 30 días) Definitiva, 0,2% (a 30 días) |
| PRAGUE-1815 | 2017 | ICP primaria | 596 | Ticagrelor±cambio selectivo a clopidogrel | Definitiva, 1,5% Definitiva/probable, ND |
| 634 | Prasugrel±cambio selectivo a clopidogrel | Definitiva, 1,2% Definitiva/probable, ND | |||
| Registros (sin ajuste por diferencias basales) | |||||
| Sheffield, Reino Unido16 | 2017 | ICP primaria | 1.654 1.136 | Ticagrelor Prasugrel | Definitiva, 1,0% Definitiva, 1,6% |
| SWEDEHEART17 | 2018 | ICP primaria | 1.995 5.438 | Ticagrelor hospitalario Pretratamiento con ticagrelor | Definitiva, 0,4% (a 30 días) Definitiva, 0,5% (a 30 días) |
| RENAMY4 | 2018 | ICP por SCA | 2.604 | Ticagrelor | Definitiva, 1,2% |
| 1.519 | Prasugrel | Definitiva, 0,9% | |||
ICP: intervención coronaria percutánea; SCA: síndrome coronario agudo; TS: trombosis del stent.
El inicio prehospitalario de ticagrelor para los pacientes con infarto agudo de miocardio con elevación del segmento ST (IAMCEST) y una estrategia terapéutica de ICP primaria ayudan a reducir la incidencia de la TS precoz (tabla 2).
En tratamiento triple con ácido acetilsalicílico, clopidogrel y dosis bajas de un anticoagulante oral directo redujo de manera significativa el riesgo de TS18. En los pacientes con stent y SCA tratados con TAPD, la toma de rivaroxabán 2,5 mg 2 veces al día se asoció con una reducción de las TS y la mortalidad. El beneficio del rivaroxabán se constató precozmente y se mantuvo. Otro estudio en un contexto semejante con el anticoagulante oral apixabán, que se suspendió anticipadamente, demostró una reducción similar de la TS. Por su parte, los inhibidores del factor Xa interfieren en la cascada de la coagulación inhibiendo la generación de trombina al tiempo que inhiben la agregación de plaquetas, ya que la trombina es un potente estimulador de la reactivación plaquetaria. Sin embargo, los beneficios obtenidos en la reducción de la TS se ven contrarrestados, al menos en parte, por el aumento del riesgo de hemorragias mayores. Así pues, el tratamiento triple se reserva únicamente para los pacientes con alto riesgo de TS y bajo riesgo hemorrágico.
La adherencia al TAPD, que incluye el cumplimiento de la duración recomendada, es la medida preventiva más asequible y, en general, la más eficaz contra la TS9. El abandono prematuro del TAPD debido al incumplimiento terapéutico del paciente, en especial durante la fase temprana tras el implante del stent, aumenta el riesgo de TS y mortalidad8,19. Aparte de acortar la duración del TAPD, no ajustarse a las recomendaciones de las guías de práctica clínica sobre el uso de inhibidores del receptor plaquetario P2Y12 más recientes se considera también incumplimiento del tratamiento antiagregante plaquetario recomendado (en ausencia de un riesgo hemorrágico alto). La adherencia del paciente al tratamiento inhibidor del receptor plaquetario P2Y12 disminuyó tras la introducción de medicamentos más modernos y costosos. El prasugrel y el ticagrelor, cuyo alto precio implica un mayor desembolso para el paciente, contribuyen significativamente a unas menores tasas de cumplimiento terapéutico respecto al clopidogrel20. De esta manera, una reducción escalonada y selectiva del clopidogrel para los pacientes con bajo riesgo isquémico es una oportunidad real de garantizar la continuidad del TAPD. El copago por el paciente actualmente forma parte de la estrategia personalizada del TAPD tras una ICP por SCA21.
RELEVANCIA DE OTROS MEDICAMENTOSEl tratamiento intensivo con estatinas previene el retardo de los procesos de reparación vascular y la inflamación vascular crónica, que son factores predisponentes a la TS muy tardía tras el implante de stents farmacoactivos. Los beneficios de las estatinas se deben no solo a su capacidad de reducir el colesterol unido a lipoproteínas de baja densidad, sino también de mejorar la función endotelial, disminuir la inflamación vascular y reducir la adhesión plaquetaria y la formación de trombos.
CONCLUSIONESLa TS es una complicación grave aunque relativamente infrecuente. Sin embargo, debido a la creciente población de pacientes con stent implantado, este acontecimiento merece cierta atención. La estrategia terapéutica más importante de abordaje de la TS tras una ICP por SCA es su prevención. En lo que respecta a su etiopatogenia multifactorial, los esfuerzos puestos en la prevención de la TS se dirigen a mejorar la expansión del stent, emplear stents de última generación y potenciar la adherencia a un tratamiento antiagregante plaquetario eficaz.
CONFLICTO DE INTERESESZ. Motovska ha recibido de AstraZeneca honorarios por conferencias, sin relación con el trabajo aquí presentado. También es miembro de los comités asesores de AstraZeneca, Bayer y Boehringer Ingelheim.