La endocarditis infecciosa (EI) continúa siendo una enfermedad con una elevada morbimortalidad. Actualmente, la ecocardiografía transesofágica (ETE) es la técnica de imagen de referencia para su diagnóstico y el de sus complicaciones, pero se han publicado series que muestran resultados destacables con la tomografía computarizada con multidetectores (TCMD) en la evaluación prequirúrgica de la EI1–3. Las nuevas guías europeas4 refuerzan su realización tanto ante la sospecha diagnóstica de EI como en casos confirmados para la evaluación de complicaciones, ampliando la definición de complicaciones paravalvulares por TCMD como criterio mayor diagnóstico. La Sociedad Europea de Cardiología5 recomienda la evaluación preoperatoria de la enfermedad coronaria previa a la cirugía en pacientes seleccionados; sin embargo, en el contexto de la EI, la realización de coronariografía invasiva supone un riesgo embólico no despreciable.
Diseñamos un estudio prospectivo cuyo objetivo fue evaluar la utilidad de la TCMD en la EI. Se incluyeron 27 pacientes consecutivos que cumplían criterios diagnósticos de EI posible (41%) o definitiva (59%) según los criterios modificados de Duke4. Se utilizó un equipo de 64 detectores (espesor/incremento de corte 0,6/0,3mm, sincronismo cardiaco, field of view ampliado al abdomen superior) y 80ml de contraste intravenoso (350mg/ml, 5,5ml/s).
Los resultados se compararon con los hallazgos de la ETE y la cirugía en los pacientes intervenidos (tabla). Se incluyeron cinco (18,5%) EI sobre dispositivo (tres sobre el electrodo y dos sobre el catéter central) y 22 valvulares (57% sobre la válvula nativa, 29% en bioprótesis y 14% en válvulas mecánicas).
Características clínicas, tipo de endocarditis, existencia de vegetación, complicaciones y anatomía coronaria
| Caso | Sexo, edad (años) | Probabilidad de EI | Cardiopatía/ condición predisponente | Visualización vegetación en ETE | Visualización vegetación en TCMD | Complicación diagnosticada en ETE | Complicación diagnosticada en TCMD | Coronarias en TCMD | Hallazgos extracardiacos en TCMD |
|---|---|---|---|---|---|---|---|---|---|
| 1 | M, 74 | Posible | Prótesis mitral y aórtica mecánicas | No | No | Absceso periaórtico Sospecha fístula | Seudoaneurisma Descarta fístula | Sin lesiones | Aneurisma micótico en arteria mesentérica superior |
| 2 | V, 81 | Posible | No | No | No | No | No | Enfermedad de dos vasos | Trombo mural en aorta ascendente |
| 3 | V, 62 | Definitiva | No | Sí (aórtica nativa) | No | No | No | No valorables Calcificación intensa | Embolias en bazo y psoas |
| 4 | V, 76 | Definitiva | Prótesis aórtica biológica+CDAC | Sí (aórtica biológica) | Sí | Absceso UMA | No | Enfermedad de un vaso Bypass permeables | |
| 5 | V, 41 | Definitiva | No Adicto a drogas por vía parenteral | Sí (tricúspide nativa) | No | No | No | Sin lesiones | Infartos pulmonares |
| 6 | M, 82 | Posible | Prótesis aórtica biológica+CDAC | Sí (mitral nativa) | No | No | No | No valorables Calcificación intensa | |
| 7 | V, 65 | Definitiva | CDAC | Sí (aórtica nativa) | Sí | No | Perforación velo | Enfermedad de tres vasos Bypass permeables | Derrame pleural bilateral |
| 8 | V, 59 | Definitiva | Prótesis aórtica mecánica | Sí (aórtica mecánica) | No | No | No | Sin lesiones | Derrame pleural |
| 9 | M, 80 | Posible | DAI-TRC | Sí (electrodo) | No | No | No | No valorables Calcificación intensa | |
| 10 | V, 30 | Posible | DAI | Sí (electrodo) | Sí | No | No | Sin lesiones | |
| 11 | M, 66 | Definitiva | Prótesis aórtica mecánica y marcapasos | Sí (electrodo) | No | No | No | Sin lesiones | |
| 12 | V, 68 | Definitiva | No | Sí (mitral y aórtica nativas) | Sí | Perforación velo aórtico Rotura cuerda mitral | Rotura cuerda mitral | Sin lesiones | Infarto esplénico Derrame pleural |
| 13 | V, 48 | Posible | Tubo protésico aórtico | No | No | No | Valoración tubo aórtico | No sincronismo | Hematoma periaórtico |
| 14 | M, 51 | Posible | Catéter central | Sí (catéter) | Sí | No | No | No valorables por fallo del contraste | Trombosis de vena subclavia |
| 15 | V, 84 | Posible | Catéter central | Sí (catéter) | No | No | No | Enfermedad de tres vasos | Consolidación pulmonar Trombosis yugular |
| 16 | V, 60 | Definitiva | No | Sí (mitral nativa) | Sí | No | No | Coronaria derecha y circunfleja no valorables | Infarto esplénico |
| 17 | M, 57 | Definitiva | Miocardiopatía hipertrófica obstructiva | Sí (mitral nativa) | Sí | Absceso UMA | Absceso UMA | Sin lesiones | |
| 18 | V, 70 | Definitiva | Prótesis aórtica biológica | Sí (aórtica biológica y mitral nativa) | Sí | Absceso UMA Desinserción protésica | Absceso UMA Desinserción protésica | Sin lesiones | Aneurisma de aorta ascendente Derrame pleural |
| 19 | V, 76 | Definitiva | Prótesis aórtica biológica+CDAC | Sí (aórtica biológica) | Sí | Absceso UMA | Absceso UMA | Enfermedad TCI+tres vasos Bypass permeables | Infarto esplénico Derrame pleural |
| 20 | M, 79 | Definitiva | Prótesis aórtica biológica | Sí (UMA) | Sí | Absceso UMA | Absceso UMA | Sin lesiones | |
| 21 | V, 32 | Definitiva | Comunicación interventricular subaórtica | Sí (aórtica nativa) | Sí | No | No | Sin lesiones | Infarto esplénico |
| 22 | V, 60 | Definitiva | No | Sí (mitral nativa) | No | Engrosamiento UMA | No | Sin lesiones | Infarto esplénico |
| 23 | M, 23 | Definitiva | Tetralogía de Fallot Conducto ventrículo derecho-arteria pulmonar | Sí (pulmonar biológica) | Sí | No | No | Sin lesiones Evaluación conducto ventrículo derecho-arteria pulmonar | Tromboembolia pulmonar |
| 24 | V, 39 | Posible | Válvula aórtica bicúspide | Sí (aórtica nativa) | Sí | No | No | Sin lesiones | Enfisema paraseptal |
| 25 | V, 78 | Definitiva | Prótesis aórtica biológica | Sí (mitral nativa) | Sí | No | No | Sin lesiones | Derrame pleural |
| 26 | V, 81 | Definitiva | Prótesis aórtica biológica | No | No | Absceso periaórtico | Absceso periaórtico que infiltra UMA y engloba TCI, ADA y ACx | ADA no valorable por calcificación Resto sin lesiones | Infarto esplénico Derrame pleural |
| 27 | V, 59 | Definitiva | Prótesis aórtica mecánica | Sí (raíz aórtica) | Sí | Absceso periaórtico | Seudoaneurisma de seno de Valsalva | Sin lesiones |
ACx: arteria circunfleja; ADA: arteria descendente anterior; CDAC: cirugía de derivación aortocoronaria; DAI: desfibrilador automático implantable; EI: endocarditis infecciosa; ETE: ecocardiografía transesofágica; M: mujer; TCI: tronco coronario izquierdo; TCMD: tomografía computarizada con multidetectores; TRC: terapia de resincronización cardiaca; UMA: unión mitroaórtica; V: varón.
Entre los hallazgos de la TCMD destacan:
- -
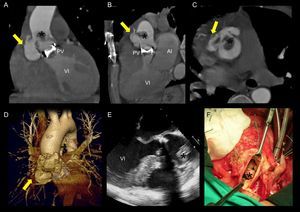
Descartó la fístula aórtica a tronco pulmonar sospechada en la ETE y evaluó adecuadamente dos sospechas de abscesos periaórticos, que se revelaron como seudoaneurismas (figura), todas ellas sobre prótesis aórtica mecánica.
Figura.Endocarditis sobre prótesis aórtica mecánica con seudoaneurisma en la raíz aórtica. La tomografía computarizada con multidetectores identificó un seudoaneurisma en el seno de Valsalva derecho (flecha amarilla) en los plano coronal (A), sagital (B) y axial (C), y en la reconstrucción tridimensional (D), junto con una gran vegetación anclada en la aorta ascendente proximal (*). En la ecocardiografía transesofágica (E) se visualizó la vegetación, pero no se detectó el seudoaneurisma. Estos hallazgos fueron confirmados durante la cirugía (F). AI: aurícula izquierda; PV: prótesis valvular aórtica mecánica; VI: ventrículo izquierdo.
(0.42MB). - -
Evaluó un tubo protésico supracoronario, y definió adecuadamente un gran hematoma peritubo, sin fugas ni complicaciones endocardíticas; un tubo de ventrículo derecho a arteria pulmonar, y permitió la determinación exacta del diámetro de la aorta ascendente en un caso que finalmente requirió un implante de tubo valvulado.
- -
Se diagnosticaron cuatro de los seis abscesos de la unión mitroaórtica visualizados en la ETE y confirmados en la cirugía. Uno de ellos, de gran tamaño, no pudo ser bien evaluado mediante ecocardiografía, y la tomografía permitió definir adecuadamente su extensión, que alcanzaba la ventana aortopulmonar y englobaba el origen de las arterias coronarias.
- -
En el 77% de los pacientes se evaluaron las arterias coronarias nativas o los bypass.
- -
En todos los pacientes reoperados se determinó la distancia del ápex del ventrículo derecho o del bypass al esternón.
- -
En el 70% de los pacientes se describieron hallazgos extracardiacos, lo cual es de especial importancia por constituir criterios menores los fenómenos embólicos arteriales periféricos (26%), los infartos pulmonares (7,4%) y los aneurismas micóticos (3,7%).
- -
En cuanto a las vegetaciones, en la TCMD se observaron 12 de las 17 sobre válvulas (tanto nativas como protésicas) diagnosticadas por ETE y tres de las cinco sobre dispositivo, sin detectar fundamentalmente las filiformes e hipermóviles.
La utilización de la TCMD en la EI, reforzada en las nuevas guías4, no ha sido evaluada hasta ahora en nuestro país. Con este trabajo, basado en una amplia serie, pretendemos destacar varias conclusiones:
- -
En la EI valvular, la TCMD es clave en la visualización de la pared aórtica, habitualmente valorada de manera incompleta con ecocardiografía y, en muchas ocasiones, afectada en forma de fístulas, seudoaneurismas y abscesos. La mayor ventaja se advierte en la EI sobre prótesis aórtica mecánica, con más frecuencia relacionada con estas complicaciones y cuya valoración por ETE resulta especialmente compleja por la presencia de sombras acústicas.
- -
Además, permite evaluar la anatomía coronaria y estimar la distancia del ápex de ventrículo derecho o del bypass coronario al esternón en pacientes con cirugía previa, sin olvidar la utilidad en la EI derecha al diagnosticar embolias pulmonares.
- -
Sin embargo, en nuestra experiencia, la información aportada por la TCMD es menos relevante tanto en la evaluación de vegetaciones (principalmente las filiformes) como en la EI sobre dispositivo, dado que estas últimas no suelen presentar complicaciones locales ni requerir cirugía mayor, por lo que es innecesaria la evaluación de la anatomía coronaria.
Actualmente, con el desarrollo de múltiples modalidades de imagen, es responsabilidad del cardiólogo conocer las ventajas de cada una de ellas para ofrecer la mayor rentabilidad diagnóstica. Consideramos que la TCMD es, sin duda, una técnica de imagen complementaria a la ETE en el tratamiento de la EI.