Palabras clave
Se han descrito diversos factores que influyen en el mantenimiento del ritmo sinusal (RS) a largo plazo tras una cardioversión eléctrica (CE) por una fibrilación auricular (FA) persistente, y el uso de fármacos antiarrítmicos es uno de los factores más relacionados1-10.
Sin embargo, hay pocos datos sobre cuáles son los predictores de mantenimiento del RS a largo plazo en pacientes sin cardiopatía estructural, así como del beneficio de los fármacos antiarrítmicos profilácticos en este tipo de pacientes.
El estudio REVERSE (REgistro sobre la cardio-VERSión en España) se realizó con el objetivo de conocer la práctica clínica de la cardioversión en la fibrilación auricular, ya que no existían registros multicéntricos específicos suficientemente amplios que describieran su uso en la asistencia habitual.
El objetivo del presente análisis fue conocer en la práctica clínica el uso y la utilidad del tratamiento antiarrítmico en el mantenimiento del RS en el primer año tras una CE exitosa por una FA persistente en pacientes sin cardiopatía estructural.
MÉTODOS
El registro REVERSE11 incluyó prospectivamente a todos los pacientes con FA persistente remitidos a CE electiva en 96 hospitales españoles entre el 1 de febrero y el 30 de junio de 2004; se realizó 1 año de seguimiento clínico y electrocardiográfico de los pacientes sin cardiopatía estructural. Se seleccionó una muestra de hospitales de cada comunidad proporcional a su peso demográfico. La selección de estos hospitales también era representativa de todos los niveles asistenciales hospitalarios. Los criterios de inclusión fueron: a) edad ≥ 18 años; b) FA de al menos 7 días de duración, y c) sin causas precipitantes (hipertiroidismo, fiebre, pericarditis, etc.). El registro incluyó a 1.515 pacientes, de los que 1.355 fueron sometidos a CE, que fue efectiva en 1.175 (87%)12. De éstos, en 528 (45%) se consideró que no tenían cardiopatía estructural y se realizó un seguimiento a 1 año. Este grupo es el que se estudia en el presente análisis. Se registraron datos referentes a las características clínicas, los tratamientos, características de la FA, la CE y el ecocardiograma. Se requería un ecocardiograma realizado en los 6 meses previos a la CE. Se consideró que tenía cardiopatía estructural cuando el paciente presentaba alguna de las siguientes anomalías: valvulopatía de grado moderado o importante o estenosis mitral de cualquier grado; infarto de miocardio; miocardiopatía; cardiopatía hipertensiva (hipertensión arterial y grosor de pared posterior o septo > 13 mm); disfunción sistólica (FE < 50%). Se consideró FA aislada cuando el paciente era menor de 60 años y no tenía enfermedad pulmonar, hipertensión ni hipertrofia ventricular izquierda13. No se recomendó ningún tratamiento o manejo específico. Los controles se realizaron 1, 3, 6 y 12 meses después. Se controló al 98% de los pacientes al mes, el 98% a los 3 meses, el 97% a los 6 meses y el 97% a los 12 meses. El 94% completó todos los controles.
Las variables cualitativas se compararon mediante el test de la c2 y las variables cuantitativas, utilizando la prueba de la t de Student. Se realizaron curvas de Kaplan-Meier para describir el efecto del tratamiento antiarrítmico en la recurrencia de FA persistente (duración ≥ 7 días) durante el primer año y se valoraron las diferencias entre los grupos mediante comparación de rangos logarítmicos. Se creó un modelo de análisis multivariable de riesgos relativos de Cox para valorar si la ausencia de tratamiento antiarrítmico se relacionaba con la recurrencia de FA persistente. Se evaluó, según correspondiera, la linealidad y la proporcionalidad de las variables introducidas en el modelo. Se incluyeron en el análisis el peso, la edad, el sexo, la hipertensión arterial, la dilatación auricular izquierda (≥50 mm), el tratamiento antiarrítmico al alta, el tratamiento con IECA o ARA-II y la duración de la FA > 1 año. Se analizó si había interacción entre las variables del modelo.
Se consideró que las diferencias eran estadísticamente significativas si p £ 0,05. Todos los análisis se realizaron con el paquete estadístico SPSS 14.0.
RESULTADOS
Las características clínicas de los 528 pacientes estudiados se resumen en la tabla 1. El 80% de los pacientes recibió tratamiento antiarrítmico profiláctico al alta, y el fármaco más utilizado fue la amiodarona (el 68% de los pacientes tratados) (tabla 2). El 42% fue tratado con IECA o ARA-II. Ninguna variable (duración de la FA, cardioversión previa, sexo, edad, FA aislada) se relacionó con un mayor uso de antiarrítmicos. Durante el seguimiento se observó una elevada proporción de tratamiento antiarrítmico mantenido en los pacientes que seguían en RS en cada control (el 80% al mes, el 89% a los 3 meses, el 88% a los 6 meses y el 95% a los 12 meses), pues se mantuvo el tratamiento antiarrítmico más allá de los 12 meses al 59% de los pacientes que siguieron en RS en todos los controles.
En el control al año, 260 (51%) pacientes se encontraban en RS. De ellos, 191 (37%) se mantuvieron en RS en todos los controles y sin episodios de FA persistente identificados. La mayoría de las recurrencias (64%) ocurrieron en el primer mes tras la CE. De los 337 pacientes con recidiva de FA persistente durante el seguimiento, 41 (12%) revirtieron a RS con fármacos antiarrítmicos y 89 (26%) fueron sometidos a una nueva CE durante el año de seguimiento, mientras que 25 (7%) fueron tratados con métodos no farmacológicos (ablación y/o implantación de marcapasos).
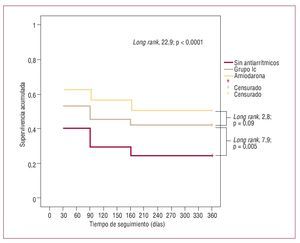
La tabla 3 describe el efecto del tratamiento antiarrítmico entre cada control en la prevención de recidivas de FA en los pacientes que seguían en RS. El tratamiento antiarrítmico se relacionó con una proporción significativamente menor de recidivas de FA persistente entre al alta y el tercer mes; entre el tercer y el sexto mes hubo una tendencia a favor del tratamiento antiarrítmico. Hubo tendencia a que se cambiara con más frecuencia el tratamiento antiarrítmico cuando el paciente era tratado al alta con flecainida o propafenona (grupo Ic de Vaughan-Williams) que cuando era tratado con amiodarona (el 14% con grupo Ic frente al 8% con amiodarona; p = 0,07). El principal motivo fue la ineficacia del tratamiento (el 13% con grupo Ic y el 5% con amiodarona) seguido por la aparición de efectos secundarios (el 3% con amiodarona y el 0,9% con grupo Ic). La figura 1 muestra la curva de Kaplan-Meier de recurrencia de FA persistente durante el primer año en función del tratamiento antiarrítmico al alta (amiodarona, grupo Ic o sin tratamiento); se observan diferencias significativas entre los tres grupos (long rank test, 22,9; p < 0,0001). El grupo tratado con amiodarona tenía la menor proporción de recidivas. Cuando se analizaron las diferencias entre el grupo tratado con amiodarona y el grupo tratado con antiarrítmicos del grupo Ic había una tendencia a la significación en la superioridad de amiodarona (long rank test, 2,8; p = 0,09). Por otra parte, en el grupo tratado con antiarrítmicos del grupo Ic se registraron menos recidivas que en el grupo de no tratados (long rank test, 7,9; p = 0,005). Se realizó un análisis multivariable mediante regresión de Cox en el que la ausencia de tratamiento antiarrítmico al alta (hazard ratio [HR] = 1,59; p = 0,001) y el peso (HR por cada kilo = 1,01; p = 0,04) eran factores independientes relacionados con la recurrencia de FA persistente durante el primer año, ajustado por la edad, sexo, hipertensión, presencia de dilatación auricular izquierda (≥ 50 mm), tratamiento con IECA o ARA-II y duración de la FA > 1 año. No se detectó interacción significativa entre las variables del modelo.
Fig. 1. Curva de Kaplan-Meier de recurrencia de fibrilación auricular persistente durante el primer año en función del tratamiento antiarrítmico al alta.
DISCUSIÓN
En este estudio hemos observado que en la práctica clínica habitual en España, tras una cardioversión eléctrica exitosa la mayoría de pacientes sin cardiopatía estructural son tratados al alta con antiarrítmicos, especialmente amiodarona, tratamiento que se mantiene en más de la mitad de los pacientes que al año continúan en RS. El tratamiento antiarrítmico al alta fue el factor pronóstico más importante de los implicados en el mantenimiento del RS durante el primer año, y muestra su máxima utilidad en los primeros 3-6 meses tras la CE. Hubo una tendencia a la superioridad de la amiodarona respecto a los otros antiarrítmicos.
Aunque se han publicado muchos estudios que analizan la utilidad del tratamiento antiarrítmico tras CE, ninguno se centra específicamente en pacientes con FA persistente y sin cardiopatía estructural. En esos estudios, el uso de fármacos antiarrítmicos se describe de forma constante como predictor de mantenimiento del RS3-10. Aunque con diferentes fármacos antiarrítmicos, como el sotalol, la flecainida y la propafenona, se ha demostrado utilidad, la amiodarona probablemente sea el más estudiado y del que se ha demostrado mejores resultados6-10. El SAFE-T8, que incluyó a 665 pacientes, es el estudio más amplio publicado hasta la fecha en el que se compara el beneficio de los antiarrítmicos antes y tras CE por FA persistente. La amiodarona mostró ser superior a sotalol —y éste, superior a placebo— en el mantenimiento del RS a largo plazo. En el registro REVERSE constatamos que la amiodarona es el fármaco más utilizado tras CE en España y parece que es superior a los demás antiarrítmicos en pacientes sin cardiopatía estructural. Un aspecto en el que no existe consenso en la literatura es la duración del tratamiento antiarrítmico tras CE. Se han publicado recientemente algunos estudios en que se describe el beneficio de mantener durante 3-6 meses el tratamiento con amiodarona. En el SAFE-T el tratamiento mostró su beneficio cuando se mantuvo a largo plazo (1-4 años) tras la CE. En el registro REVERSE observamos que en España es frecuente mantener el tratamiento antiarrítmico a largo plazo en pacientes sin cardiopatía, y lo continúa más de la mitad de los pacientes que seguían en RS al año. Por otra parte, se deduce que el tratamiento antiarrítmico en la prevención de recurrencias de FA persistente en estos pacientes es especialmente útil en los primeros 3 meses y puede ser eficaz en los primeros 6 meses tras la CE.
Hay algunas diferencias entre el uso de antiarrítmicos profilácticos en la práctica clínica en España y las recomendaciones recogidas en la reciente actualización de la guía de práctica clínica sobre la FA de ESC/AHA/ACC14. En la guía se propone como opcional el uso de antiarrítmicos al alta de la CE, pues se considera más útil en pacientes con cardiopatía y se propone su uso en pacientes con CE previa o recurrencias precoces. Hemos observado que en España el uso de antiarrítmicos tras la CE es la práctica habitual, independientemente de que haya cardiopatía o CE previas. En cuanto al fármaco a utilizar, aunque en la guía en el apartado de tratamiento pericardioversión no se hace una referencia explícita al tipo de antiarrítmico, en el apartado de tratamiento farmacológico para el mantenimiento del RS en la mayoría de los casos se considera que la amiodarona es fármaco de segunda elección, especialmente cuando no haya cardiopatía estructural. En nuestro estudio hemos constatado que el fármaco más utilizado es la amiodarona, que parece ser superior a los demás antiarrítmicos en la disminución de recurrencias de FA persistente, a pesar de ser pacientes sin cardiopatía estructural. En cuanto a la duración del tratamiento, en la guía se aconseja no mantener un tratamiento antiarrítmico prolongado tras la CE, mientras que hemos observado que en España se lo mantiene al año en la mitad de pacientes que siguen en RS, aunque la máxima utilidad se observó en los primeros 3-6 meses tras la CE.
La tasa de mantenimiento del RS durante el primer año (37%) es similar a la de estudios previos en que se incluye a pacientes con y sin cardiopatía. Además del uso de fármacos antiarrítmicos, en nuestro estudio la probabilidad de tener recurrencias de FA también se relacionaba con el peso, variable que no había sido descrita previamente como predictora de recidivas, probablemente porque en muchos de los estudios previos no se había incluido en los análisis. Este efecto puede deberse a una dosis de fármaco antiarrítmico relativamente inferior en pacientes con peso elevado o al propio efecto de la obesidad y de la comorbilidad añadida.
El hecho de que no se haya identificado otros predictores de recidiva no invalida la utilidad de otros predictores descritos previamente en otras poblaciones. Debemos situar estos resultados en el contexto de un grupo de pacientes sin cardiopatía estructural y en la influencia de estudios anteriores en la selección de los pacientes candidatos a CE11. En nuestro estudio, la proporción de pacientes con FA de larga duración y con grandes tamaños de la aurícula izquierda era muy escasa, por lo que estas variables difícilmente podían tener significación estadística en la predicción de recurrencias de FA persistente.
También destacamos que no es infrecuente la realización de una segunda CE dentro del primer año y la escasa utilización de tratamientos no farmacológicos (marcapasos o ablación). Aunque en la guía de la ESC/AHA/ACC se juzga como poco útiles posteriores intentos de CE excepto en pacientes muy sintomáticos, algo más de una cuarta parte de los pacientes con recurrencias recibieron una nueva CE. Se puede deducir que no es infrecuente el uso de la estrategia de control del ritmo y que un porcentaje no despreciable de pacientes tienen FA de difícil control sintomático. Aunque tras los estudios AFFIRM y RACE la estrategia de control del ritmo parece haber perdido popularidad, no hay evidencia de que sus conclusiones sean extrapolables a una población sin cardiopatía estructural, dada la elevada proporción de pacientes con cardiopatía que incluían (alrededor del 80%).
CONCLUSIONES
En la práctica clínica habitual, tras una cardioversión eléctrica efectiva por FA persistente en pacientes sin cardiopatía estructural, la gran mayoría recibe fármacos antiarrítmicos, sobre todo amiodarona. En esta población el uso de fármacos antiarrítmicos, especialmente amiodarona, es el principal factor relacionado con el mantenimiento del ritmo sinusal 1 año después.
ABREVIATURAS
CE: cardioversión eléctrica.
FA: fibrilación auricular.
RS: ritmo sinusal.
Full English text available from: www.revespcardiol.org
El registro REVERSE fue financiado por 3M farmacéutica y cuenta con el aval de la Sección de Arritmias de la Sociedad Española de Cardiología. Correspondencia: Dr. J.M. Alegret.
Hospital Universitari de Sant Joan de Reus. Sant Joan, s/n. 43201 Reus. Tarragona. España.
Correo electrónico: txalegret@hotmail.com
Recibido el 13 de diciembre de 2007.
Aceptado para su publicación el 22 de julio de 2008.